Aldehydy i ketony to organiczne związki chemiczne zawierające grupę karbonylową.... Pokaż więcej
Aldehydy i ketony: teoria i reakcje






Budowa i nazewnictwo aldehydów
Aldehydy zawierają grupę aldehydową na końcu łańcucha węglowego. Ich ogólny wzór to R-C\O\H, gdzie R to grupa alkilowa. Tworzą szereg homologiczny zaczynający się od metanalu (HCHO) poprzez etanal (CH₃CHO), propanal (CH₃CH₂CHO) i kolejne.
Nazewnictwo aldehydów jest proste - do nazwy alkanu dodajemy końcówkę "-al". Ważne jest też, że aldehydy wykazują izomerię, np. butanal (CH₃CH₂CH₂CHO) i 2-metylopropanol mają ten sam wzór sumaryczny, ale inną budowę.
Aldehydy otrzymuje się głównie przez utlenianie alkoholi I-rzędowych. W reakcji tej alkohol reaguje z tlenkiem miedzi(II) w podwyższonej temperaturze, tworząc aldehyd, miedź metaliczną i wodę.
💡 Zapamiętaj: Grupa aldehydowa zawsze znajduje się na końcu łańcucha węglowego, co wpływa na jej reaktywność. Dzięki temu aldehydy ulegają charakterystycznym reakcjom addycji i polimeryzacji.

Właściwości chemiczne aldehydów
Aldehydy charakteryzują się dużą reaktywnością chemiczną ze względu na obecność grupy karbonylowej. Najważniejsze reakcje to redukcja i utlenianie. Podczas redukcji (np. z wodorem w obecności niklu jako katalizatora) aldehydy przekształcają się w alkohole I-rzędowe.
Szczególnie ważne są reakcje utleniania, które pozwalają na identyfikację aldehydów. Próba Trommera z wodorotlenkiem miedzi(II) oraz próba Tollensa z amoniakalnym roztworem tlenku srebra to podstawowe testy na obecność aldehydów. W obu przypadkach powstaje kwas karboksylowy, a odczynnik ulega redukcji.
W miarę wydłużania łańcucha węglowego maleje polarność aldehydów, a tym samym ich rozpuszczalność w wodzie. Najprostsze aldehydy, jak formaldehyd (HCHO) i acetaldehyd (CH₃CHO), są dobrze rozpuszczalne w wodzie.
⚠️ Uwaga: Formaldehyd w roztworze wodnym tworzy formalinę , która jest szeroko stosowana jako środek konserwujący i dezynfekujący.
Reakcje polimeryzacji aldehydów
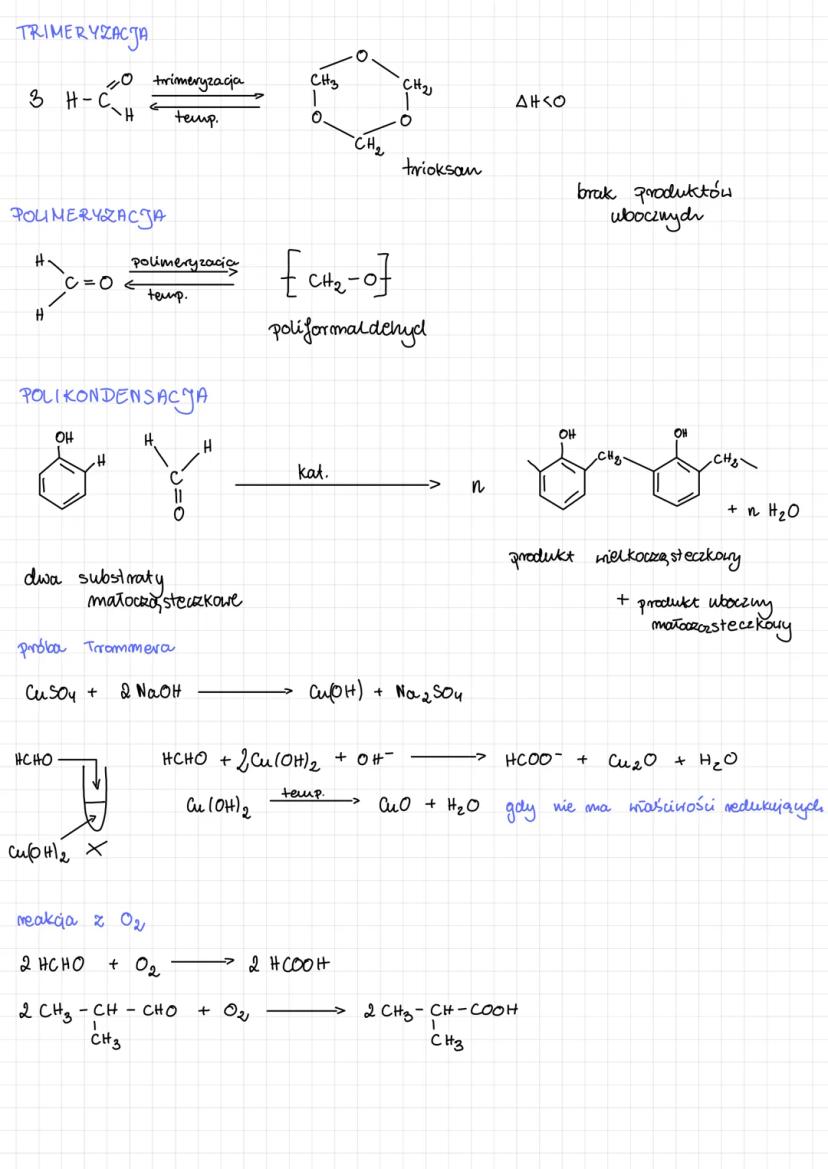
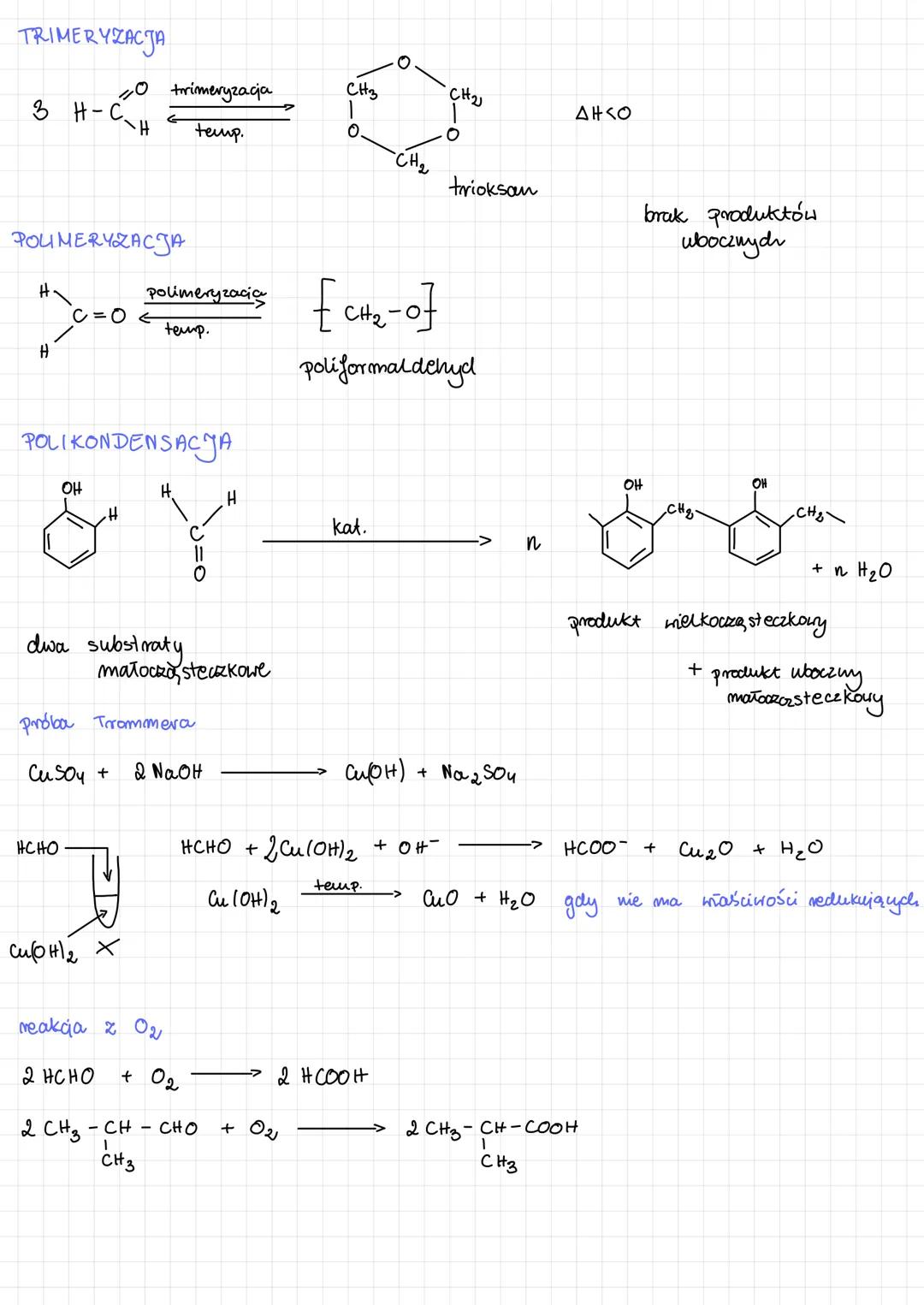
Aldehydy mogą ulegać ciekawym reakcjom tworzenia większych struktur. Jedną z nich jest trimeryzacja, gdzie trzy cząsteczki aldehydu łączą się w pierścień. Przykładowo, formaldehyd może tworzyć trioksan - cykliczną strukturę o wzorze (CH₂O)₃.
W procesie polimeryzacji formaldehyd tworzy poliformaldehyd, długi łańcuch jednostek -CH₂O-. Ta reakcja zachodzi w odpowiedniej temperaturze i prowadzi do powstania materiałów polimerowych o cennych właściwościach.
Aldehydy mogą również uczestniczyć w reakcjach polikondensacji, gdzie dwa różne substraty reagują ze sobą, tworząc produkt wielkocząsteczkowy i małocząsteczkowy produkt uboczny (najczęściej wodę). Te reakcje są kluczowe w produkcji wielu tworzyw sztucznych.
💡 Pamiętaj: Aldehydy mają właściwości redukujące, co można zaobserwować w próbie Trommera. Gdy dodamy aldehyd do roztworu Cu(OH)₂, kompleks ulega redukcji do Cu₂O (ceglastego osadu), co potwierdza obecność grupy aldehydowej.
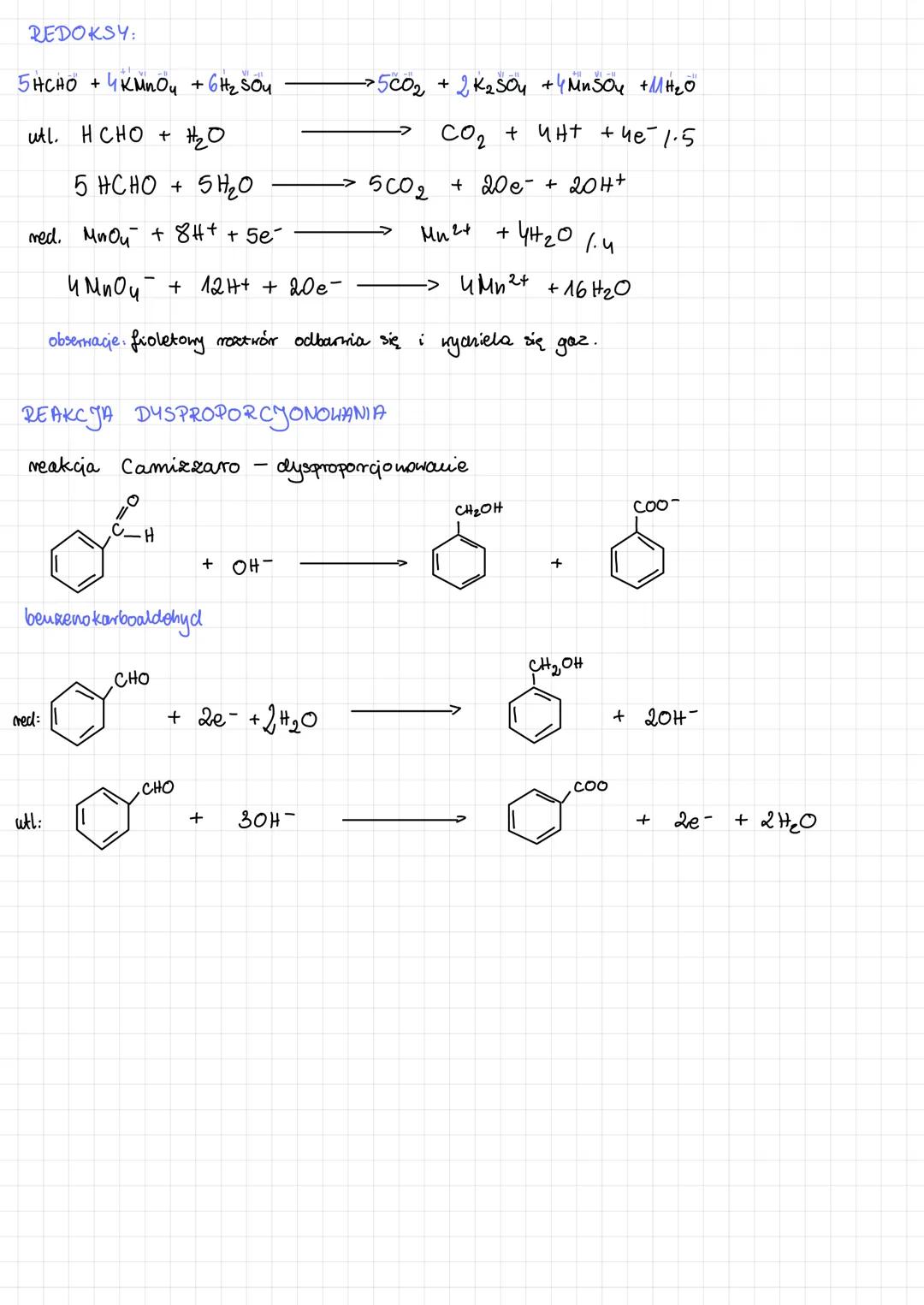
Reakcje redoks aldehydów
Aldehydy łatwo ulegają reakcjom utleniania i redukcji. W reakcjach z silnymi utleniaczami, jak nadmanganian potasu (KMnO₄), aldehydy są utleniane do kwasów karboksylowych lub nawet całkowicie do CO₂ i H₂O, w zależności od warunków.
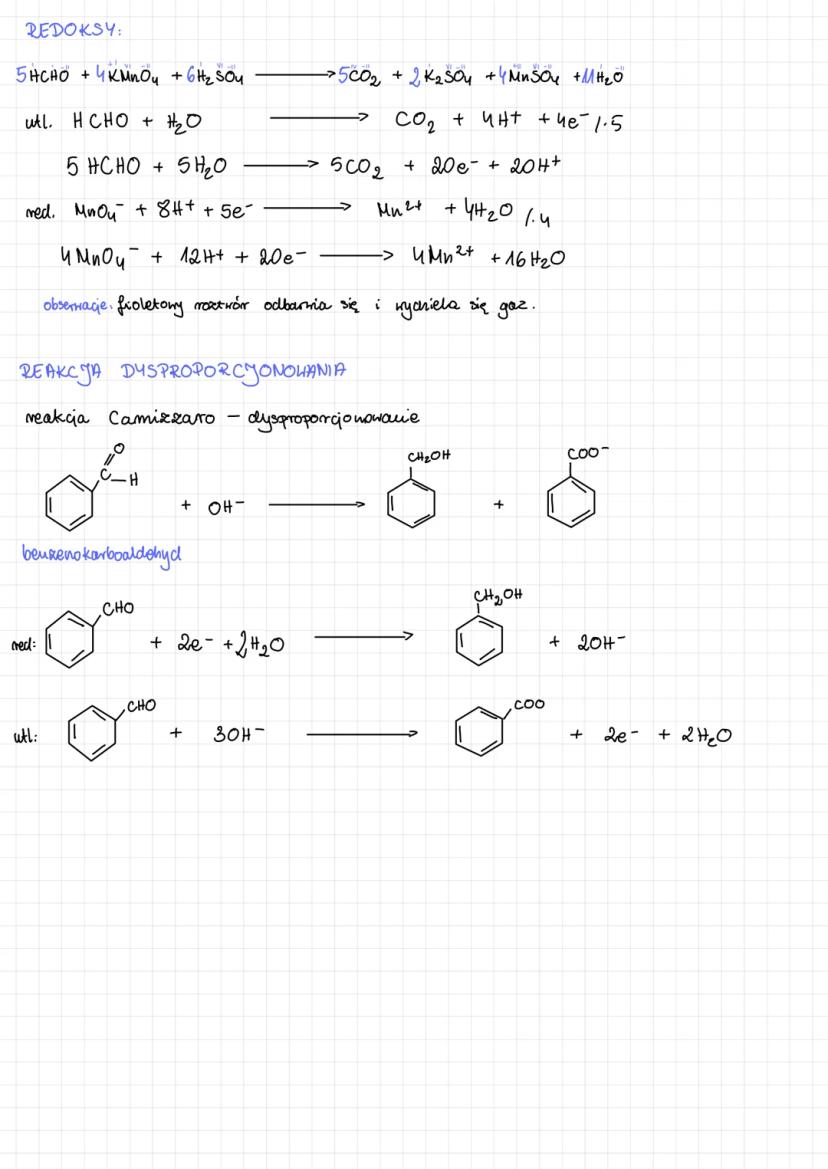
Przykładowa reakcja z nadmanganianem potasu w środowisku kwasowym: 5HCHO + 4KMnO₄ + 6H₂SO₄ → 5CO₂ + 2K₂SO₄ + 4MnSO₄ + 11H₂O
Podczas tej reakcji można zaobserwować odbarwienie fioletowego roztworu KMnO₄ i wydzielanie się gazu (CO₂). To potwierdza, że aldehydy są dobrymi reduktorami.
Ciekawym przypadkiem jest reakcja dysproporcjonowania (reakcja Cannizzaro), w której część cząsteczek aldehydu ulega utlenieniu, a część redukcji. Ta reakcja zachodzi szczególnie łatwo w przypadku aldehydów aromatycznych, jak benzenokarboaldehyd.
🔍 Praktyczna wskazówka: Reakcje redoks aldehydów wykorzystuje się nie tylko w analityce chemicznej do wykrywania tych związków, ale też w syntezie organicznej do otrzymywania różnych pochodnych.

Ćwiczenia z nomenklatury i reakcji aldehydów
Nazewnictwo aldehydów wymaga znajomości podstawowych zasad - grupa aldehydowa znajduje się na końcu łańcucha i otrzymuje najniższy możliwy numer. Przykłady: metanal, 2-metylopropanal, but-2-enal, 3-metylobutanal, cykloheksankarboaldehyd.
Rysowanie wzorów strukturalnych to kolejna ważna umiejętność. Na przykład 2-metylopentanal to CH₃-CH₂-CH₂-CH(CH₃)-CHO, a 2,4-dimetylopentanal to CH₃-CH(CH₃)-CH₂-CH(CH₃)-CHO.
Znajomość reakcji aldehydów pozwala rozwiązywać zadania dotyczące ich przemian. Oto typowe przykłady:
- Utlenianie alkoholi: CH₃OH + CuO → HCHO + Cu + H₂O
- Próba Tollensa: CH₃CHO + Ag₂O → CH₃COOH + 2Ag↓
- Próba Trommera: CH₃CH₂CHO + 2Cu(OH)₂ → CH₃CH₂COOH + Cu₂O + 2H₂O
💡 Zapamiętaj: Próby Tollensa i Trommera pozwalają wykryć grupę aldehydową w związkach organicznych. Positive wynik tych prób (wytrącenie srebra lub powstanie czerwonego osadu Cu₂O) jednoznacznie wskazuje na obecność aldehydu.

Ketony - budowa i nazewnictwo
Ketony, podobnie jak aldehydy, zawierają grupę karbonylową , ale umiejscowioną między dwoma atomami węgla. Ogólny wzór ketonu to R-CO-R', gdzie R i R' to grupy alkilowe lub arylowe.
W nazewnictwie systematycznym ketony otrzymują końcówkę "-on", a pozycję grupy karbonylowej oznacza się liczbą. Przykłady: butan-2-on (CH₃COCH₂CH₃), 3-etylopentan-2-on (CH₃COCH(C₂H₅)CH₂CH₃), cykloheksanon.
Ketony mogą mieć w swojej strukturze także inne grupy funkcyjne lub wiązania nienasycone, np. pent-4-en-2-on czy 4-bromopentan-2-on (CH₃COCH₂CH(Br)CH₃).
🔑 Kluczowa różnica: Grupa karbonylowa w ketonach znajduje się między atomami węgla , natomiast w aldehydach na końcu łańcucha . Ta różnica w budowie ma ogromny wpływ na właściwości chemiczne tych związków.

Porównanie właściwości aldehydów i ketonów
Aldehydy i ketony mają podobną grupę funkcyjną (karbonylową), ale różnice w jej położeniu wpływają na ich reaktywność. Grupa karbonylowa w obu przypadkach ma budowę płaską (hybrydyzacja sp²), co wpływa na ich właściwości.
Aldehydy są bardziej reaktywne niż ketony, szczególnie w reakcjach utleniania. Podczas gdy aldehydy łatwo utleniają się do kwasów karboksylowych, ketony są bardziej odporne na utlenianie. Dlatego próby Tollensa i Trommera dają pozytywne wyniki tylko dla aldehydów.
Oba typy związków mogą powstawać w reakcji hydratacji alkinów. Na przykład:
- HC≡CH + H₂O → CH₃CHO (aldehyd)
- CH₃C≡CH₃ + H₂O → CH₃COCH₃ (keton)
Wraz ze wzrostem długości łańcucha węglowego zmieniają się właściwości fizyczne aldehydów i ketonów: stan skupienia, rozpuszczalność w wodzie oraz temperatury topnienia i wrzenia.
💡 Ciekawostka: Grupa karbonylowa zarówno w aldehydach, jak i ketonach ma płaską strukturę ze względu na hybrydyzację sp² atomu węgla. To wpływa na geometrię całej cząsteczki i jej właściwości.
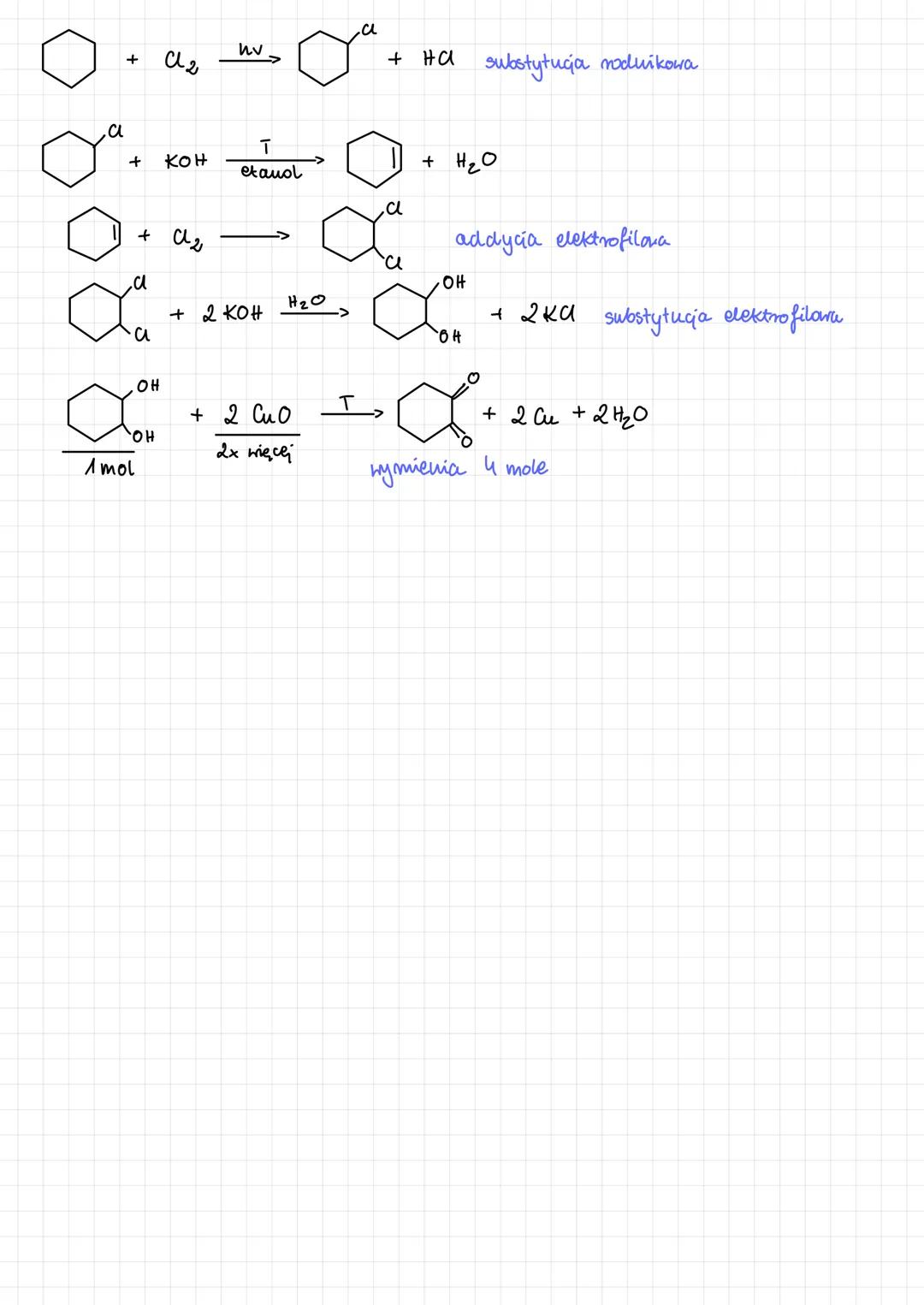
Reakcje charakterystyczne
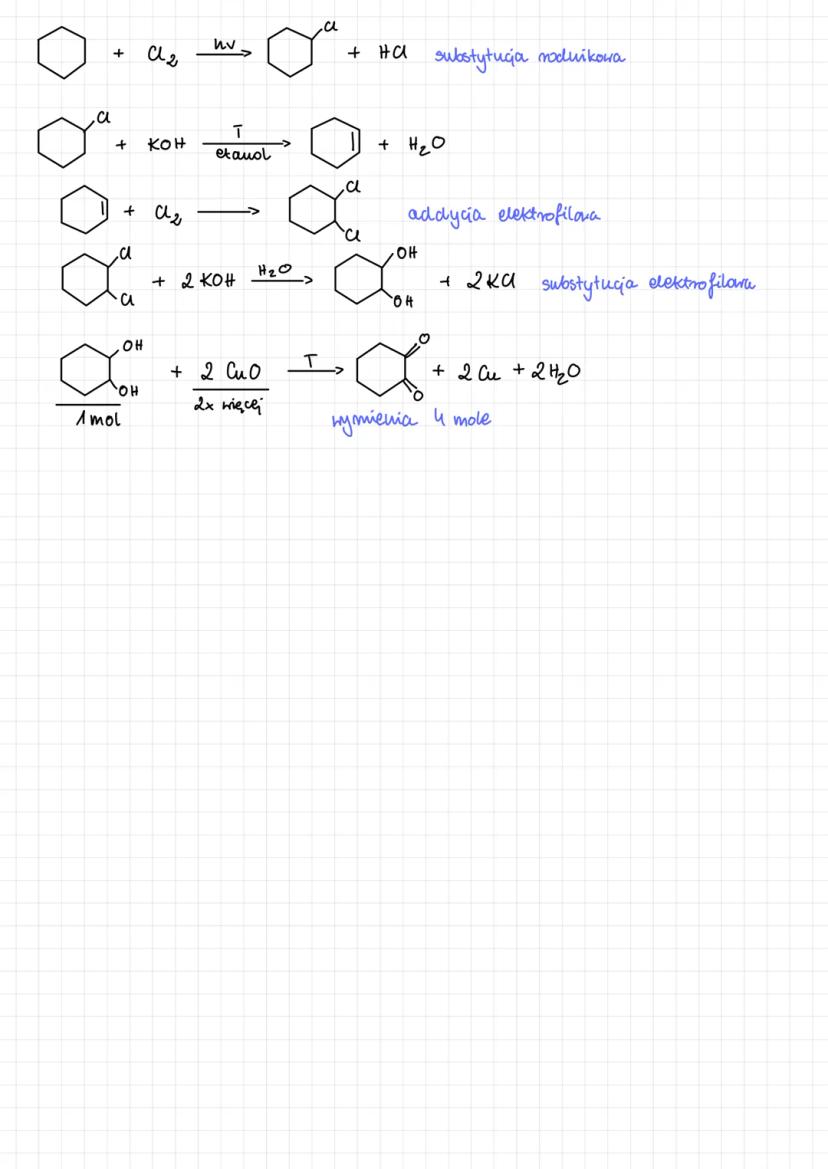
Aldehydy i ketony wykazują zróżnicowaną reaktywność w różnych typach reakcji. W reakcjach z chlorem w obecności światła (hv) zachodzi substytucja rodnikowa prowadząca do powstania produktu chlorowanego i HCl.
W środowisku zasadowym (KOH) w podwyższonej temperaturze mogą zachodzić reakcje eliminacji, natomiast addycja elektrofilowa jest typowa dla reakcji z halogenami, jak Cl₂.
Alkohole pierwszorzędowe mogą być utleniane tlenkiem miedzi(II) do aldehydów: ROH + CuO → RCHO + Cu + H₂O. Reakcja ta wymaga podwyższonej temperatury i jest ważną metodą otrzymywania aldehydów.
⚗️ Laboratoryjnie: Przy planowaniu syntezy pamiętaj, że do otrzymania 4 moli aldehydu potrzebujesz 4 mole alkoholu i 8 moli CuO (dwukrotnie więcej utleniacza). Dbałość o proporcje reagentów jest kluczowa dla wysokiej wydajności.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Aldehydy
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Aldehydy i ketony: teoria i reakcje
Aldehydy i ketony to organiczne związki chemiczne zawierające grupę karbonylową. Różnią się miejscem występowania tej grupy - w aldehydach znajduje się na końcu łańcucha, a w ketonach w środku. Te związki odgrywają ważną rolę w chemii organicznej i mają liczne... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa i nazewnictwo aldehydów
Aldehydy zawierają grupę aldehydową na końcu łańcucha węglowego. Ich ogólny wzór to R-C\O\H, gdzie R to grupa alkilowa. Tworzą szereg homologiczny zaczynający się od metanalu (HCHO) poprzez etanal (CH₃CHO), propanal (CH₃CH₂CHO) i kolejne.
Nazewnictwo aldehydów jest proste - do nazwy alkanu dodajemy końcówkę "-al". Ważne jest też, że aldehydy wykazują izomerię, np. butanal (CH₃CH₂CH₂CHO) i 2-metylopropanol mają ten sam wzór sumaryczny, ale inną budowę.
Aldehydy otrzymuje się głównie przez utlenianie alkoholi I-rzędowych. W reakcji tej alkohol reaguje z tlenkiem miedzi(II) w podwyższonej temperaturze, tworząc aldehyd, miedź metaliczną i wodę.
💡 Zapamiętaj: Grupa aldehydowa zawsze znajduje się na końcu łańcucha węglowego, co wpływa na jej reaktywność. Dzięki temu aldehydy ulegają charakterystycznym reakcjom addycji i polimeryzacji.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości chemiczne aldehydów
Aldehydy charakteryzują się dużą reaktywnością chemiczną ze względu na obecność grupy karbonylowej. Najważniejsze reakcje to redukcja i utlenianie. Podczas redukcji (np. z wodorem w obecności niklu jako katalizatora) aldehydy przekształcają się w alkohole I-rzędowe.
Szczególnie ważne są reakcje utleniania, które pozwalają na identyfikację aldehydów. Próba Trommera z wodorotlenkiem miedzi(II) oraz próba Tollensa z amoniakalnym roztworem tlenku srebra to podstawowe testy na obecność aldehydów. W obu przypadkach powstaje kwas karboksylowy, a odczynnik ulega redukcji.
W miarę wydłużania łańcucha węglowego maleje polarność aldehydów, a tym samym ich rozpuszczalność w wodzie. Najprostsze aldehydy, jak formaldehyd (HCHO) i acetaldehyd (CH₃CHO), są dobrze rozpuszczalne w wodzie.
⚠️ Uwaga: Formaldehyd w roztworze wodnym tworzy formalinę , która jest szeroko stosowana jako środek konserwujący i dezynfekujący.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje polimeryzacji aldehydów
Aldehydy mogą ulegać ciekawym reakcjom tworzenia większych struktur. Jedną z nich jest trimeryzacja, gdzie trzy cząsteczki aldehydu łączą się w pierścień. Przykładowo, formaldehyd może tworzyć trioksan - cykliczną strukturę o wzorze (CH₂O)₃.
W procesie polimeryzacji formaldehyd tworzy poliformaldehyd, długi łańcuch jednostek -CH₂O-. Ta reakcja zachodzi w odpowiedniej temperaturze i prowadzi do powstania materiałów polimerowych o cennych właściwościach.
Aldehydy mogą również uczestniczyć w reakcjach polikondensacji, gdzie dwa różne substraty reagują ze sobą, tworząc produkt wielkocząsteczkowy i małocząsteczkowy produkt uboczny (najczęściej wodę). Te reakcje są kluczowe w produkcji wielu tworzyw sztucznych.
💡 Pamiętaj: Aldehydy mają właściwości redukujące, co można zaobserwować w próbie Trommera. Gdy dodamy aldehyd do roztworu Cu(OH)₂, kompleks ulega redukcji do Cu₂O (ceglastego osadu), co potwierdza obecność grupy aldehydowej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje redoks aldehydów
Aldehydy łatwo ulegają reakcjom utleniania i redukcji. W reakcjach z silnymi utleniaczami, jak nadmanganian potasu (KMnO₄), aldehydy są utleniane do kwasów karboksylowych lub nawet całkowicie do CO₂ i H₂O, w zależności od warunków.
Przykładowa reakcja z nadmanganianem potasu w środowisku kwasowym: 5HCHO + 4KMnO₄ + 6H₂SO₄ → 5CO₂ + 2K₂SO₄ + 4MnSO₄ + 11H₂O
Podczas tej reakcji można zaobserwować odbarwienie fioletowego roztworu KMnO₄ i wydzielanie się gazu (CO₂). To potwierdza, że aldehydy są dobrymi reduktorami.
Ciekawym przypadkiem jest reakcja dysproporcjonowania (reakcja Cannizzaro), w której część cząsteczek aldehydu ulega utlenieniu, a część redukcji. Ta reakcja zachodzi szczególnie łatwo w przypadku aldehydów aromatycznych, jak benzenokarboaldehyd.
🔍 Praktyczna wskazówka: Reakcje redoks aldehydów wykorzystuje się nie tylko w analityce chemicznej do wykrywania tych związków, ale też w syntezie organicznej do otrzymywania różnych pochodnych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Ćwiczenia z nomenklatury i reakcji aldehydów
Nazewnictwo aldehydów wymaga znajomości podstawowych zasad - grupa aldehydowa znajduje się na końcu łańcucha i otrzymuje najniższy możliwy numer. Przykłady: metanal, 2-metylopropanal, but-2-enal, 3-metylobutanal, cykloheksankarboaldehyd.
Rysowanie wzorów strukturalnych to kolejna ważna umiejętność. Na przykład 2-metylopentanal to CH₃-CH₂-CH₂-CH(CH₃)-CHO, a 2,4-dimetylopentanal to CH₃-CH(CH₃)-CH₂-CH(CH₃)-CHO.
Znajomość reakcji aldehydów pozwala rozwiązywać zadania dotyczące ich przemian. Oto typowe przykłady:
- Utlenianie alkoholi: CH₃OH + CuO → HCHO + Cu + H₂O
- Próba Tollensa: CH₃CHO + Ag₂O → CH₃COOH + 2Ag↓
- Próba Trommera: CH₃CH₂CHO + 2Cu(OH)₂ → CH₃CH₂COOH + Cu₂O + 2H₂O
💡 Zapamiętaj: Próby Tollensa i Trommera pozwalają wykryć grupę aldehydową w związkach organicznych. Positive wynik tych prób (wytrącenie srebra lub powstanie czerwonego osadu Cu₂O) jednoznacznie wskazuje na obecność aldehydu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Ketony - budowa i nazewnictwo
Ketony, podobnie jak aldehydy, zawierają grupę karbonylową , ale umiejscowioną między dwoma atomami węgla. Ogólny wzór ketonu to R-CO-R', gdzie R i R' to grupy alkilowe lub arylowe.
W nazewnictwie systematycznym ketony otrzymują końcówkę "-on", a pozycję grupy karbonylowej oznacza się liczbą. Przykłady: butan-2-on (CH₃COCH₂CH₃), 3-etylopentan-2-on (CH₃COCH(C₂H₅)CH₂CH₃), cykloheksanon.
Ketony mogą mieć w swojej strukturze także inne grupy funkcyjne lub wiązania nienasycone, np. pent-4-en-2-on czy 4-bromopentan-2-on (CH₃COCH₂CH(Br)CH₃).
🔑 Kluczowa różnica: Grupa karbonylowa w ketonach znajduje się między atomami węgla , natomiast w aldehydach na końcu łańcucha . Ta różnica w budowie ma ogromny wpływ na właściwości chemiczne tych związków.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Porównanie właściwości aldehydów i ketonów
Aldehydy i ketony mają podobną grupę funkcyjną (karbonylową), ale różnice w jej położeniu wpływają na ich reaktywność. Grupa karbonylowa w obu przypadkach ma budowę płaską (hybrydyzacja sp²), co wpływa na ich właściwości.
Aldehydy są bardziej reaktywne niż ketony, szczególnie w reakcjach utleniania. Podczas gdy aldehydy łatwo utleniają się do kwasów karboksylowych, ketony są bardziej odporne na utlenianie. Dlatego próby Tollensa i Trommera dają pozytywne wyniki tylko dla aldehydów.
Oba typy związków mogą powstawać w reakcji hydratacji alkinów. Na przykład:
- HC≡CH + H₂O → CH₃CHO (aldehyd)
- CH₃C≡CH₃ + H₂O → CH₃COCH₃ (keton)
Wraz ze wzrostem długości łańcucha węglowego zmieniają się właściwości fizyczne aldehydów i ketonów: stan skupienia, rozpuszczalność w wodzie oraz temperatury topnienia i wrzenia.
💡 Ciekawostka: Grupa karbonylowa zarówno w aldehydach, jak i ketonach ma płaską strukturę ze względu na hybrydyzację sp² atomu węgla. To wpływa na geometrię całej cząsteczki i jej właściwości.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje charakterystyczne
Aldehydy i ketony wykazują zróżnicowaną reaktywność w różnych typach reakcji. W reakcjach z chlorem w obecności światła (hv) zachodzi substytucja rodnikowa prowadząca do powstania produktu chlorowanego i HCl.
W środowisku zasadowym (KOH) w podwyższonej temperaturze mogą zachodzić reakcje eliminacji, natomiast addycja elektrofilowa jest typowa dla reakcji z halogenami, jak Cl₂.
Alkohole pierwszorzędowe mogą być utleniane tlenkiem miedzi(II) do aldehydów: ROH + CuO → RCHO + Cu + H₂O. Reakcja ta wymaga podwyższonej temperatury i jest ważną metodą otrzymywania aldehydów.
⚗️ Laboratoryjnie: Przy planowaniu syntezy pamiętaj, że do otrzymania 4 moli aldehydu potrzebujesz 4 mole alkoholu i 8 moli CuO (dwukrotnie więcej utleniacza). Dbałość o proporcje reagentów jest kluczowa dla wysokiej wydajności.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Aldehydy
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.