Chemia organiczna to fascynująca dziedzina, a alkohole i fenole to... Pokaż więcej
Alkohole i Fenole: Podstawy do Matury





Alkohole - budowa i nazewnictwo
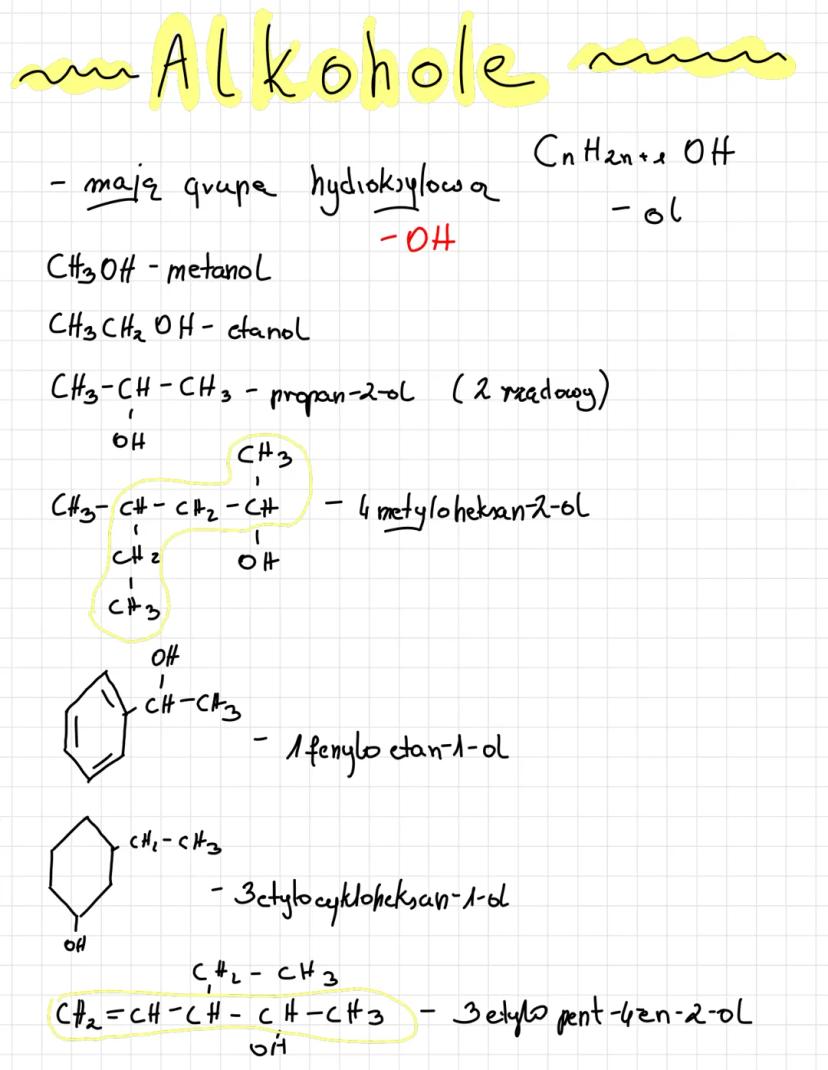
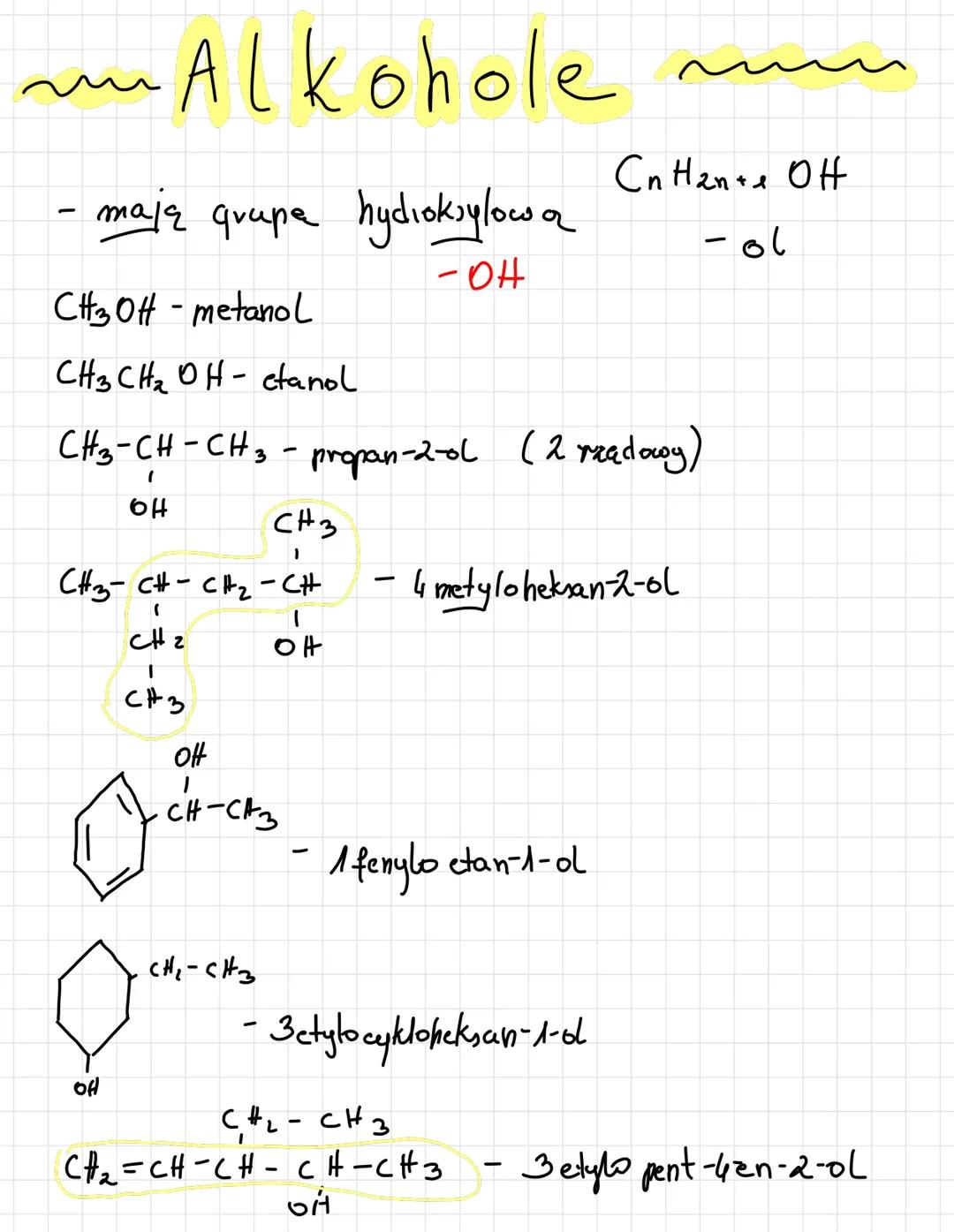
Alkohole to związki organiczne posiadające grupę hydroksylową -OH przyłączoną do węglowodoru. Ich ogólny wzór to CnH2n+1OH. Podstawowe alkohole to metanol (CH3OH) i etanol (CH3CH2OH).
W nazewnictwie alkoholi końcówka "-ol" wskazuje na obecność grupy hydroksylowej. Numer przed nazwą określa pozycję grupy -OH w łańcuchu, np. propan-2-ol to alkohol z grupą -OH przy drugim atomie węgla.
Alkohole możemy klasyfikować jako pierwszo-, drugo- lub trzeciorzędowe, w zależności od tego, ile grup węglowodorowych jest przyłączonych do atomu węgla z grupą -OH. Na przykład propan-2-ol jest alkoholem drugorzędowym.
💡 Szybka wskazówka: Przy tworzeniu nazw alkoholi najpierw zidentyfikuj główny łańcuch, potem numeruj go tak, by grupa -OH miała jak najniższy numer, a następnie dodaj przedrostki dla podstawników z numerami ich pozycji.

Otrzymywanie alkoholi
Metanol można uzyskać kilkoma metodami. Jedną z nich jest synteza z tlenku węgla i wodoru: CO + 2H₂ → CH₃OH (z użyciem katalizatora). Inną metodą jest reakcja substytucji nukleofilowej: CH₃Br + NaOH → CH₃OH + NaBr.
Etanol produkuje się głównie przez fermentację alkoholową cukrów: C₆H₁₂O₆ → 2CH₃CH₂OH + 2CO₂. Ta reakcja zachodzi dzięki enzymom obecnym w drożdżach. Etanol można też otrzymać poprzez hydrolizę zasadową chloropochodnych: CH₃CH₂Cl + KOH → CH₃CH₂OH + KCl.
Zarówno metanol jak i etanol mają charakterystyczne właściwości fizyczne. Są bezbarwnymi cieczami o charakterystycznym zapachu i smaku. Mieszają się z wodą w każdym stosunku, co czyni je doskonałymi rozpuszczalnikami. Temperatura wrzenia metanolu to około 68°C, a etanolu około 78°C.
🧪 Warto wiedzieć: Fermentacja alkoholowa zachodzi tylko do stężenia około 15% etanolu, ponieważ przy wyższych stężeniach enzymy drożdży ulegają denaturacji i proces się zatrzymuje.
Reakcje utleniania alkoholi
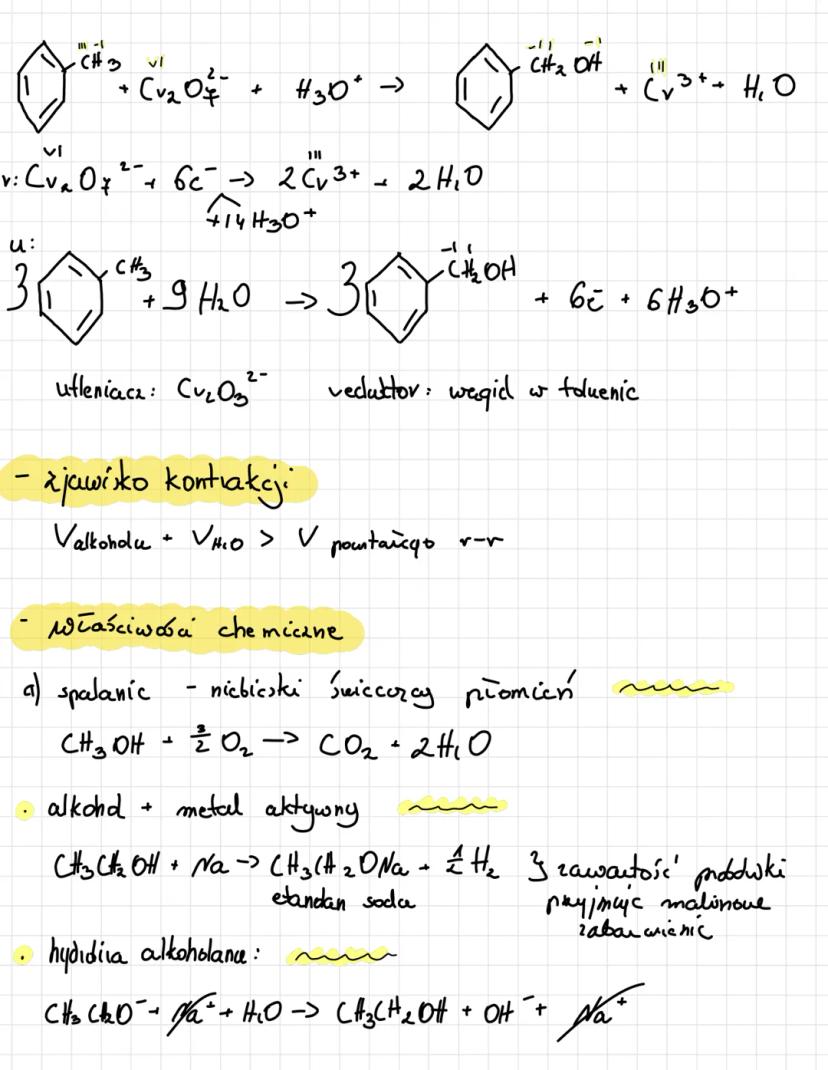
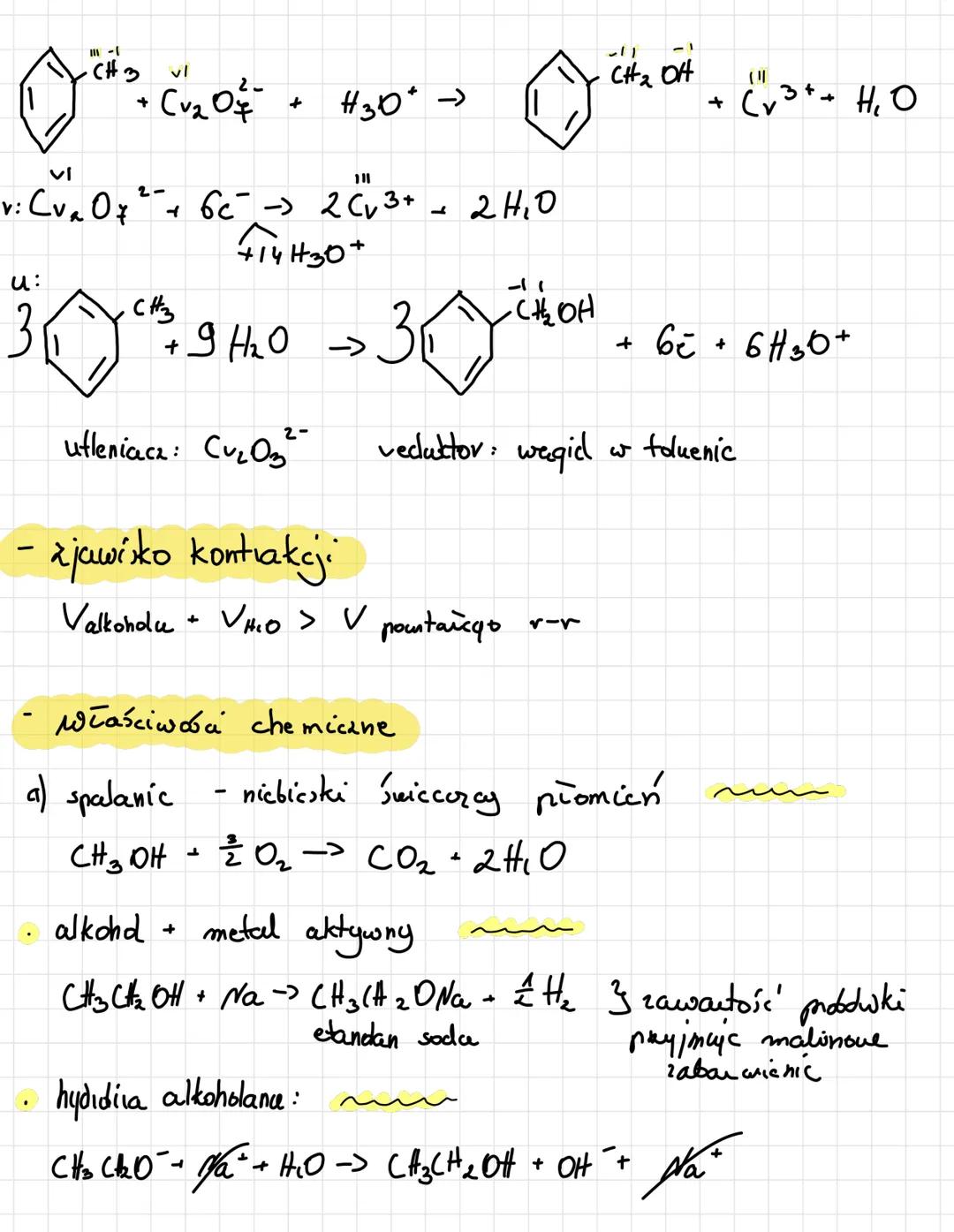
Alkohole ulegają utlenianiu w obecności silnych utleniaczy. Przykładem takiej reakcji jest utlenianie etanolu za pomocą jonów miedzi(II): 3CH₃CH₂OH + 2Cu²⁺ + 8OH⁻ → 3CH₃CHO + 2Cu₂O + 6H₂O. W tej reakcji etanol (utleniacz) przechodzi w aldehyd octowy.
Przy mieszaniu alkoholu z wodą występuje zjawisko kontrakcji objętości - objętość mieszaniny jest mniejsza niż suma objętości składników. To efekt tworzenia wiązań wodorowych między cząsteczkami.
Spalanie alkoholi zachodzi z wydzieleniem znacznej ilości energii. Metanol spala się według równania: CH₃OH + 3/2O₂ → CO₂ + 2H₂O, dając charakterystyczny niebieski płomień.
🔥 Uwaga! Metanol jest silnie toksyczny - nawet mała ilość może powodować ślepotę lub śmierć. W przeciwieństwie do niego, etanol jest mniej toksyczny, ale nadal niebezpieczny w większych ilościach.

Reakcje alkoholi z metalami i związki polihydroksylowe
Alkohole reagują z metalami aktywnymi (jak sód czy potas), wydzielając wodór. Na przykład: CH₃OH + K → CH₃OK + ½H₂. Produktami są alkoholany (np. metanolan potasu) i wodór.
W reakcji z halogenowodorami (np. HBr) tworzą się halogenki alkilowe: CH₃CH₂OH + HBr → CH₃CH₂Br + H₂O. To ważna reakcja w syntezie organicznej, pozwalająca na dalsze przekształcenia.
Alkohole polihydroksylowe to związki zawierające więcej niż jedną grupę -OH. Najważniejsze to glikol i glicerol . Glicerol to gęsta, oleista ciecz, dobrze rozpuszczalna w wodzie.
💧 Ciekawostka: Glicerol jest szeroko stosowany w kosmetykach jako środek nawilżający, a glikol jako składnik płynów do chłodnic samochodowych ze względu na niską temperaturę krzepnięcia.

Otrzymywanie glikolu i glicerolu
Glikol etylenowy można uzyskać w reakcji utleniania etylenu z użyciem katalizatora: CH₂=CH₂ + O₂ → CH₂-CH₂. Produkt pośredni (tlenek etylenu) następnie hydrolizuje się do glikolu: HOCH₂-CH₂OH.
Glicerol otrzymuje się z propenu w kilku etapach. Najpierw propenowi dodaje się chlor: CH₂=CH-CH₃ + Cl₂ → CH₂=CH-CH₂Cl + HCl. Następnie produkt poddaje się reakcji z wodorotlenkiem sodu i utlenia: CH₂=CH-CH₂Cl + NaOH → CH₂=CH-CH₂OH + NaCl. Ostatecznie utlenia się do glicerolu: CH₂=CH-CH₂OH + H₂O₂ → CH₂-CH-CH₂(OH)₃.
Te procesy są kluczowe w przemyśle chemicznym, gdzie glikole i glicerol znajdują zastosowanie w produkcji polimerów, kosmetyków i wielu innych produktów codziennego użytku.
🏭 Zastosowanie w praktyce: Glikol etylenowy jest głównym składnikiem płynów przeciw zamarzaniu, a glicerol znajdziesz w większości kremów nawilżających i mydłach, gdzie pełni rolę substancji zmiękczającej skórę.
Fenole - wprowadzenie i właściwości
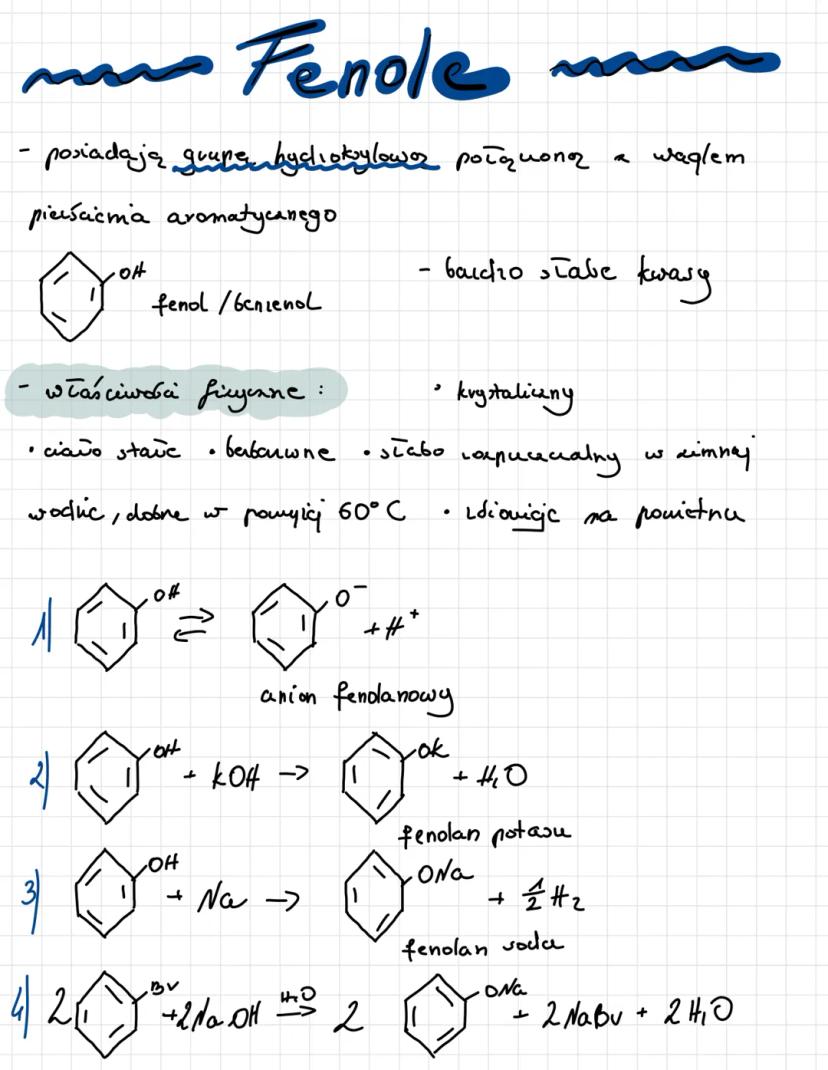
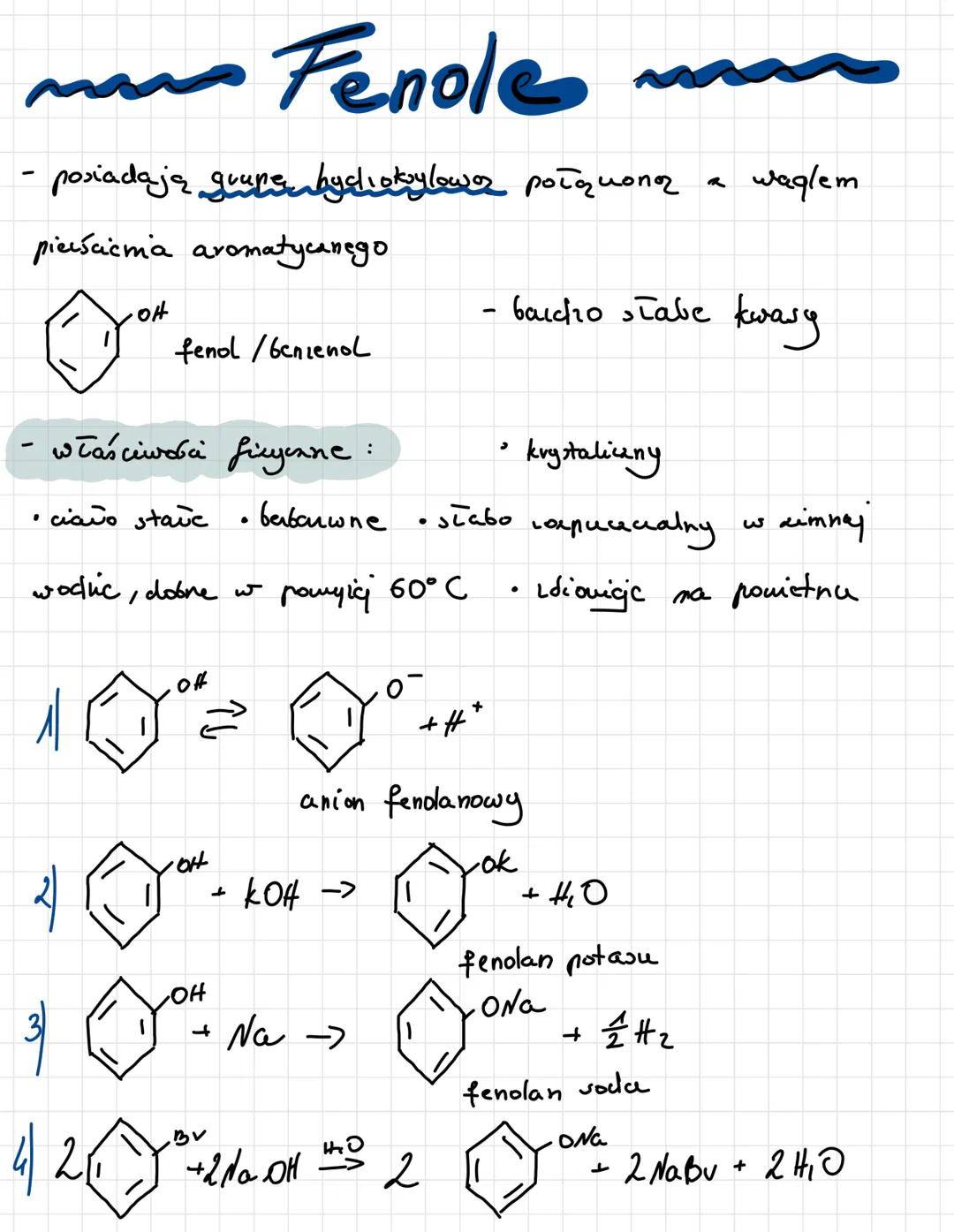
Fenole to związki zawierające grupę hydroksylową -OH połączoną bezpośrednio z pierścieniem aromatycznym. Najprostszym przykładem jest fenol (hydroksybenzen).
W przeciwieństwie do alkoholi, fenole są bardzo słabymi kwasami. Oznacza to, że mogą oddawać proton z grupy -OH, tworząc anion fenolanowy: C₆H₅OH ⇄ C₆H₅O⁻ + H⁺.
Fenol jest ciałem stałym o charakterystycznych właściwościach fizycznych. Jest bezbarwny, krystaliczny i słabo rozpuszczalny w zimnej wodzie (lepiej w wodzie powyżej 60°C). Jest lotny i ma charakterystyczny zapach.
🧪 Ciekawostka laboratoryjna: Fenol reaguje z metalami alkalicznymi (np. sód, potas) tworząc fenolany: C₆H₅OH + Na → C₆H₅ONa + ½H₂. Fenolany są znacznie bardziej rozpuszczalne w wodzie niż same fenole.
Reakcje fenoli
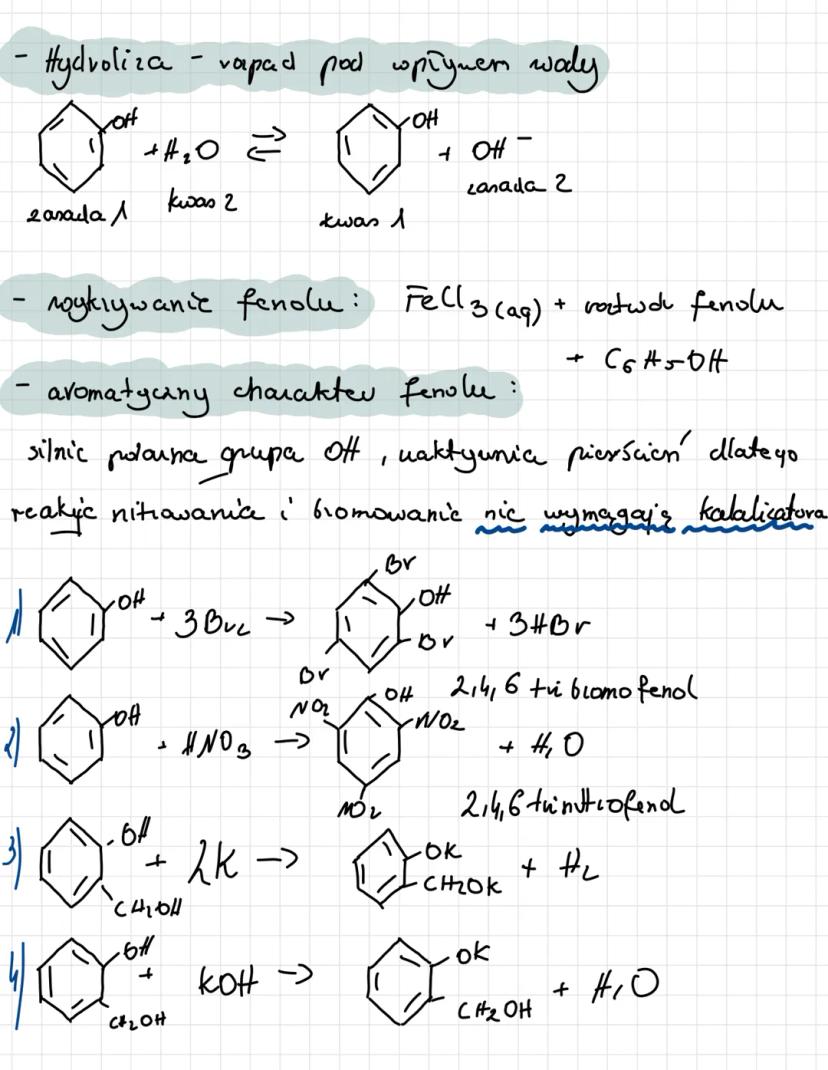
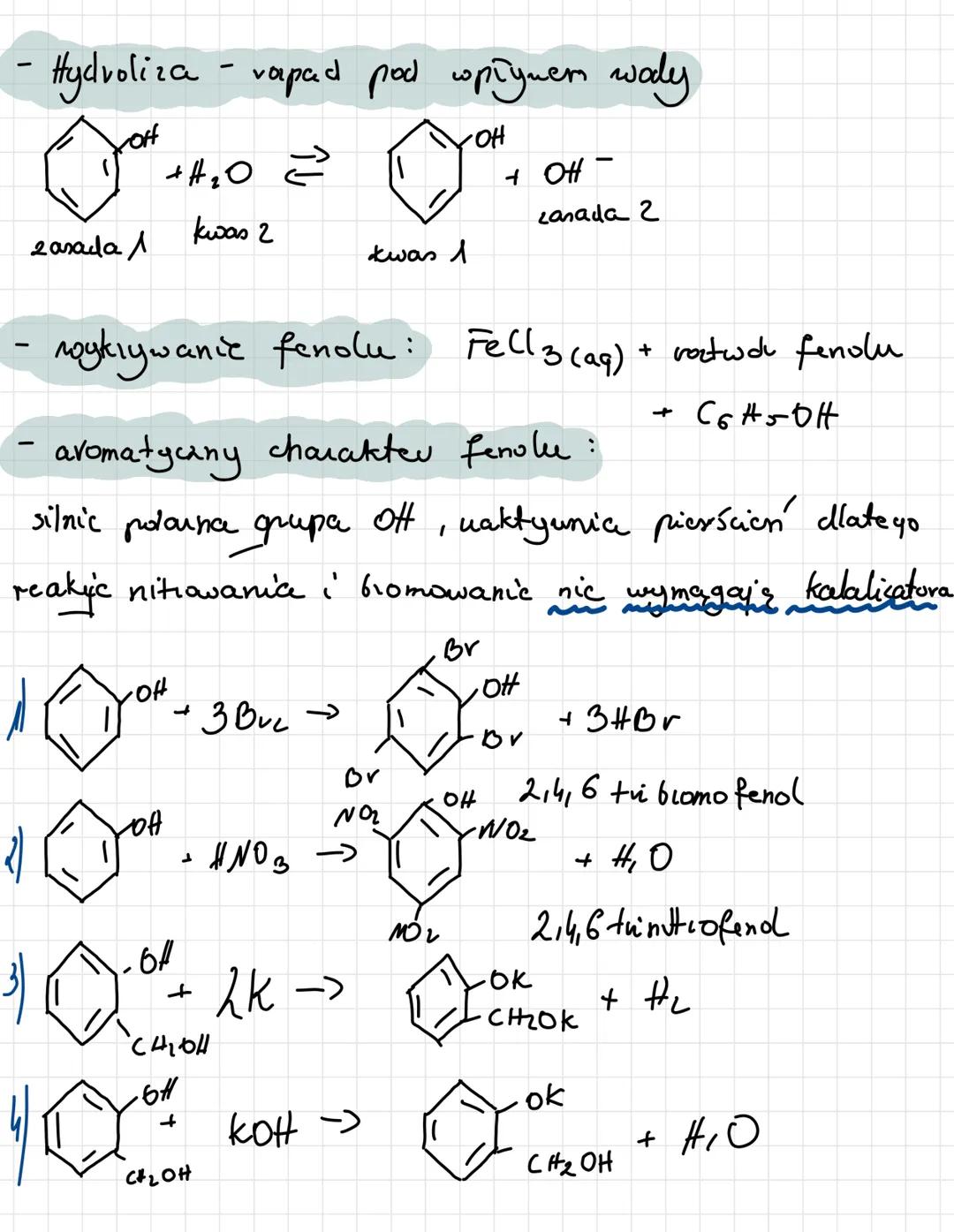
Fenole ulegają hydrolizie - rozpadowi pod wpływem wody: C₆H₅ONa + H₂O → C₆H₅OH + NaOH. W tej reakcji powstaje fenol i wodorotlenek sodu.
Obecność fenolu można wykryć za pomocą chlorku żelaza(III), który daje charakterystyczne zabarwienie z roztworami fenoli. To ważna reakcja analityczna.
Cechą charakterystyczną fenoli jest ich aromatyczny charakter z silnie polarną grupą -OH. Ta grupa aktywuje pierścień aromatyczny, co sprawia, że reakcje nitrowania i bromowania zachodzą bez katalizatora. Na przykład, fenol reaguje z bromem tworząc 2,4,6-tribromofenol: C₆H₅OH + 3Br₂ → C₆H₂Br₃OH + 3HBr.
⚗️ Praktyczna wskazówka: Fenole są znacznie bardziej reaktywne niż zwykłe węglowodory aromatyczne. Podczas wykonywania reakcji z fenolami pamiętaj, że przebiegają one zwykle szybciej i w łagodniejszych warunkach niż analogiczne reakcje z benzenem.

Nazewnictwo różnych alkoholi i fenoli
Prawidłowe nazewnictwo alkoholi i fenoli jest kluczem do zrozumienia ich struktury i właściwości. Oto przykłady poprawnego nazywania:
Alkohole alifatyczne nazywamy podając najpierw nazwę węglowodoru, a następnie sufiks "-ol" z numerem wskazującym pozycję grupy -OH, np. butan-2-ol. W przypadku alkoholi cyklicznych używamy przedrostka "cyklo-", np. cykloheksan-1-ol.
Dla alkoholi aromatycznych, gdy grupa -OH jest przy łańcuchu bocznym (nie bezpośrednio przy pierścieniu), używamy nazwy fenylometanol (a nie alkohol benzylowy). Dla fenoli, gdy grupa -OH jest przyłączona bezpośrednio do pierścienia, używamy nazwy fenol z przedrostkami określającymi pozycje podstawników.
📝 Wskazówka egzaminacyjna: Na sprawdzianach często pojawiają się zadania wymagające nazwania skomplikowanych struktur alkoholi i fenoli. Pamiętaj o regułach pierwszeństwa przy numeracji i właściwych przedrostkach dla podstawników .
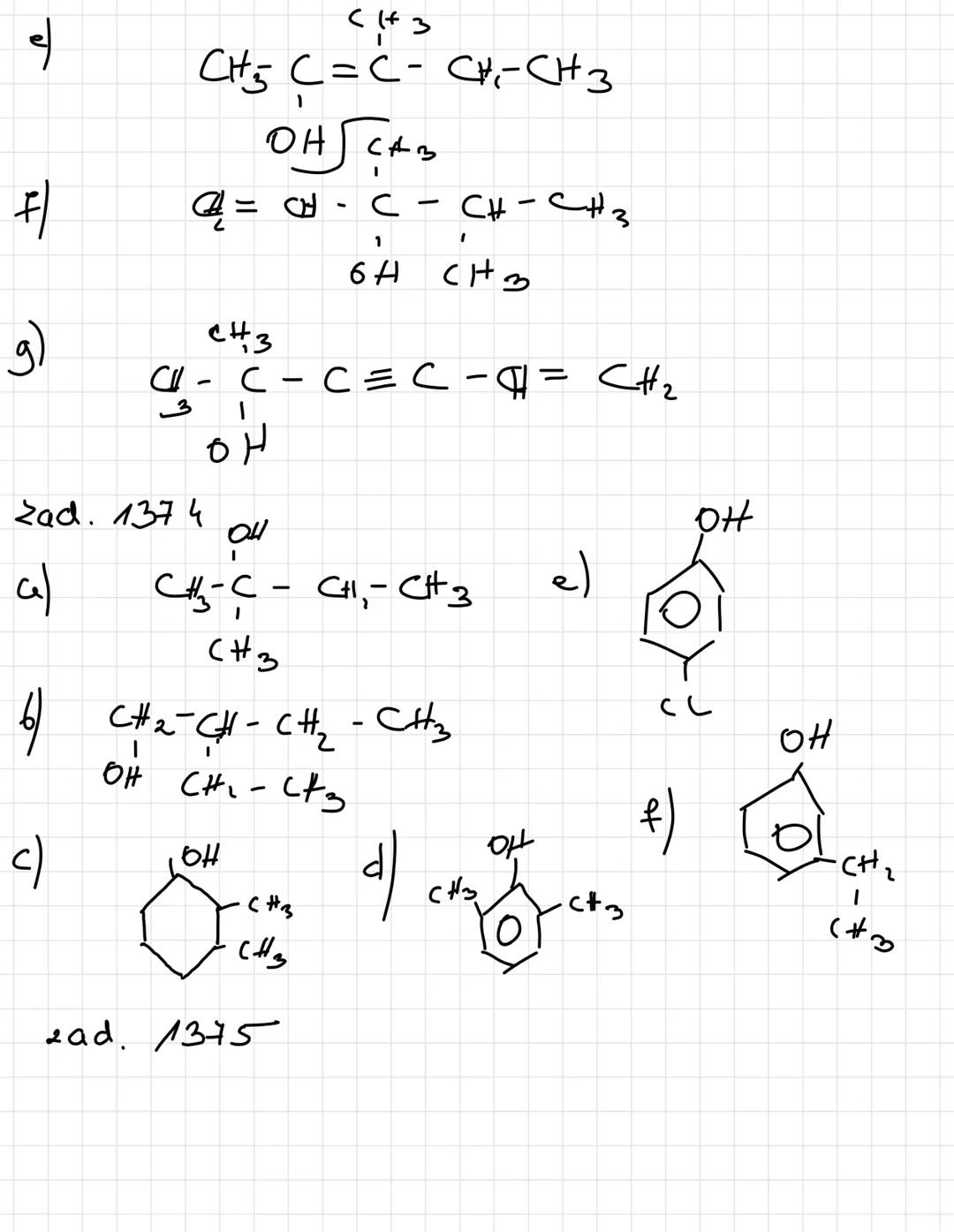
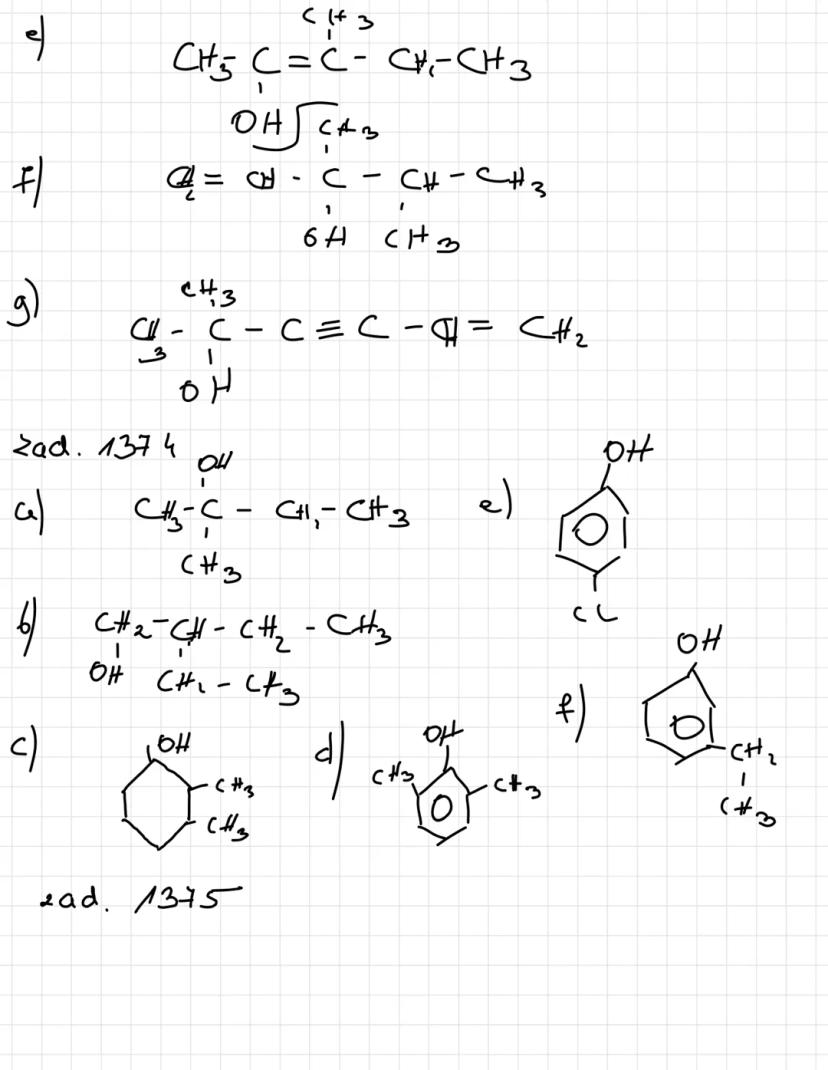
Przykłady struktur alkoholi nienasyconych i aromatycznych
Alkohole nienasycone zawierają w swojej strukturze zarówno grupę -OH jak i wiązania podwójne/potrójne. Przykładem jest but-3-en-2-ol, który zawiera wiązanie podwójne między 3. a 4. atomem węgla oraz grupę hydroksylową przy 2. atomie węgla.
W alkoholach aromatycznych grupa -OH może znajdować się przy pierścieniu aromatycznym lub przy łańcuchu bocznym. Na przykład 1-fenyloetan-1-ol ma grupę hydroksylową przy węglu sąsiadującym z pierścieniem benzenowym.
Struktury te można zapisywać na różne sposoby: wzorami strukturalnymi (z wyraźnym zaznaczeniem wszystkich wiązań i atomów) lub półstrukturalnymi (z grupami jak CH₃ zapisanymi w skróconej formie).
🔍 Ważne podczas nauki: Rysując struktury, zwracaj uwagę na poprawne umiejscowienie grupy hydroksylowej i numerację węgli. Błędy w tych elementach prowadzą do opisania zupełnie innego związku!

Klasyfikacja alkoholi i przykłady reakcji
Alkohole klasyfikujemy według liczby grup hydroksylowych oraz rzędowości atomu węgla z grupą -OH. Na przykład 3-metylobutan-2-ol to alkohol drugorzędowy, a 2,3-dimetylopenta-2,3-diol to alkohol trzeciorzędowy z dwiema grupami -OH.
Alkohole wchodzą w liczne reakcje chemiczne. Z wodorotlenkiem potasu tworzą alkoholany: CH₃-CH₂-CH(OH)-CH₃ + KOH → CH₃-CH₂-CH(OK)-CH₃ + H₂O.
W reakcjach utleniania alkohole pierwszorzędowe dają aldehydy, a następnie kwasy karboksylowe: CH₃-CH₂-OH + [O] → CH₃-CHO + H₂O. Alkohole drugorzędowe utleniają się do ketonów.
💫 Porada dla ambitnych: Reakcje alkoholi są podstawą wielu syntez organicznych. Opanowanie mechanizmów tych reakcji pozwoli Ci nie tylko rozwiązywać typowe zadania egzaminacyjne, ale także przewidywać produkty w bardziej złożonych reakcjach.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Alkohole i Fenole: Podstawy do Matury
Chemia organiczna to fascynująca dziedzina, a alkohole i fenole to jedne z najważniejszych grup związków organicznych. Poznamy ich budowę, właściwości i reakcje, które są kluczowe zarówno w laboratorium, jak i w przemyśle.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkohole - budowa i nazewnictwo
Alkohole to związki organiczne posiadające grupę hydroksylową -OH przyłączoną do węglowodoru. Ich ogólny wzór to CnH2n+1OH. Podstawowe alkohole to metanol (CH3OH) i etanol (CH3CH2OH).
W nazewnictwie alkoholi końcówka "-ol" wskazuje na obecność grupy hydroksylowej. Numer przed nazwą określa pozycję grupy -OH w łańcuchu, np. propan-2-ol to alkohol z grupą -OH przy drugim atomie węgla.
Alkohole możemy klasyfikować jako pierwszo-, drugo- lub trzeciorzędowe, w zależności od tego, ile grup węglowodorowych jest przyłączonych do atomu węgla z grupą -OH. Na przykład propan-2-ol jest alkoholem drugorzędowym.
💡 Szybka wskazówka: Przy tworzeniu nazw alkoholi najpierw zidentyfikuj główny łańcuch, potem numeruj go tak, by grupa -OH miała jak najniższy numer, a następnie dodaj przedrostki dla podstawników z numerami ich pozycji.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie alkoholi
Metanol można uzyskać kilkoma metodami. Jedną z nich jest synteza z tlenku węgla i wodoru: CO + 2H₂ → CH₃OH (z użyciem katalizatora). Inną metodą jest reakcja substytucji nukleofilowej: CH₃Br + NaOH → CH₃OH + NaBr.
Etanol produkuje się głównie przez fermentację alkoholową cukrów: C₆H₁₂O₆ → 2CH₃CH₂OH + 2CO₂. Ta reakcja zachodzi dzięki enzymom obecnym w drożdżach. Etanol można też otrzymać poprzez hydrolizę zasadową chloropochodnych: CH₃CH₂Cl + KOH → CH₃CH₂OH + KCl.
Zarówno metanol jak i etanol mają charakterystyczne właściwości fizyczne. Są bezbarwnymi cieczami o charakterystycznym zapachu i smaku. Mieszają się z wodą w każdym stosunku, co czyni je doskonałymi rozpuszczalnikami. Temperatura wrzenia metanolu to około 68°C, a etanolu około 78°C.
🧪 Warto wiedzieć: Fermentacja alkoholowa zachodzi tylko do stężenia około 15% etanolu, ponieważ przy wyższych stężeniach enzymy drożdży ulegają denaturacji i proces się zatrzymuje.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje utleniania alkoholi
Alkohole ulegają utlenianiu w obecności silnych utleniaczy. Przykładem takiej reakcji jest utlenianie etanolu za pomocą jonów miedzi(II): 3CH₃CH₂OH + 2Cu²⁺ + 8OH⁻ → 3CH₃CHO + 2Cu₂O + 6H₂O. W tej reakcji etanol (utleniacz) przechodzi w aldehyd octowy.
Przy mieszaniu alkoholu z wodą występuje zjawisko kontrakcji objętości - objętość mieszaniny jest mniejsza niż suma objętości składników. To efekt tworzenia wiązań wodorowych między cząsteczkami.
Spalanie alkoholi zachodzi z wydzieleniem znacznej ilości energii. Metanol spala się według równania: CH₃OH + 3/2O₂ → CO₂ + 2H₂O, dając charakterystyczny niebieski płomień.
🔥 Uwaga! Metanol jest silnie toksyczny - nawet mała ilość może powodować ślepotę lub śmierć. W przeciwieństwie do niego, etanol jest mniej toksyczny, ale nadal niebezpieczny w większych ilościach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje alkoholi z metalami i związki polihydroksylowe
Alkohole reagują z metalami aktywnymi (jak sód czy potas), wydzielając wodór. Na przykład: CH₃OH + K → CH₃OK + ½H₂. Produktami są alkoholany (np. metanolan potasu) i wodór.
W reakcji z halogenowodorami (np. HBr) tworzą się halogenki alkilowe: CH₃CH₂OH + HBr → CH₃CH₂Br + H₂O. To ważna reakcja w syntezie organicznej, pozwalająca na dalsze przekształcenia.
Alkohole polihydroksylowe to związki zawierające więcej niż jedną grupę -OH. Najważniejsze to glikol i glicerol . Glicerol to gęsta, oleista ciecz, dobrze rozpuszczalna w wodzie.
💧 Ciekawostka: Glicerol jest szeroko stosowany w kosmetykach jako środek nawilżający, a glikol jako składnik płynów do chłodnic samochodowych ze względu na niską temperaturę krzepnięcia.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie glikolu i glicerolu
Glikol etylenowy można uzyskać w reakcji utleniania etylenu z użyciem katalizatora: CH₂=CH₂ + O₂ → CH₂-CH₂. Produkt pośredni (tlenek etylenu) następnie hydrolizuje się do glikolu: HOCH₂-CH₂OH.
Glicerol otrzymuje się z propenu w kilku etapach. Najpierw propenowi dodaje się chlor: CH₂=CH-CH₃ + Cl₂ → CH₂=CH-CH₂Cl + HCl. Następnie produkt poddaje się reakcji z wodorotlenkiem sodu i utlenia: CH₂=CH-CH₂Cl + NaOH → CH₂=CH-CH₂OH + NaCl. Ostatecznie utlenia się do glicerolu: CH₂=CH-CH₂OH + H₂O₂ → CH₂-CH-CH₂(OH)₃.
Te procesy są kluczowe w przemyśle chemicznym, gdzie glikole i glicerol znajdują zastosowanie w produkcji polimerów, kosmetyków i wielu innych produktów codziennego użytku.
🏭 Zastosowanie w praktyce: Glikol etylenowy jest głównym składnikiem płynów przeciw zamarzaniu, a glicerol znajdziesz w większości kremów nawilżających i mydłach, gdzie pełni rolę substancji zmiękczającej skórę.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Fenole - wprowadzenie i właściwości
Fenole to związki zawierające grupę hydroksylową -OH połączoną bezpośrednio z pierścieniem aromatycznym. Najprostszym przykładem jest fenol (hydroksybenzen).
W przeciwieństwie do alkoholi, fenole są bardzo słabymi kwasami. Oznacza to, że mogą oddawać proton z grupy -OH, tworząc anion fenolanowy: C₆H₅OH ⇄ C₆H₅O⁻ + H⁺.
Fenol jest ciałem stałym o charakterystycznych właściwościach fizycznych. Jest bezbarwny, krystaliczny i słabo rozpuszczalny w zimnej wodzie (lepiej w wodzie powyżej 60°C). Jest lotny i ma charakterystyczny zapach.
🧪 Ciekawostka laboratoryjna: Fenol reaguje z metalami alkalicznymi (np. sód, potas) tworząc fenolany: C₆H₅OH + Na → C₆H₅ONa + ½H₂. Fenolany są znacznie bardziej rozpuszczalne w wodzie niż same fenole.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje fenoli
Fenole ulegają hydrolizie - rozpadowi pod wpływem wody: C₆H₅ONa + H₂O → C₆H₅OH + NaOH. W tej reakcji powstaje fenol i wodorotlenek sodu.
Obecność fenolu można wykryć za pomocą chlorku żelaza(III), który daje charakterystyczne zabarwienie z roztworami fenoli. To ważna reakcja analityczna.
Cechą charakterystyczną fenoli jest ich aromatyczny charakter z silnie polarną grupą -OH. Ta grupa aktywuje pierścień aromatyczny, co sprawia, że reakcje nitrowania i bromowania zachodzą bez katalizatora. Na przykład, fenol reaguje z bromem tworząc 2,4,6-tribromofenol: C₆H₅OH + 3Br₂ → C₆H₂Br₃OH + 3HBr.
⚗️ Praktyczna wskazówka: Fenole są znacznie bardziej reaktywne niż zwykłe węglowodory aromatyczne. Podczas wykonywania reakcji z fenolami pamiętaj, że przebiegają one zwykle szybciej i w łagodniejszych warunkach niż analogiczne reakcje z benzenem.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo różnych alkoholi i fenoli
Prawidłowe nazewnictwo alkoholi i fenoli jest kluczem do zrozumienia ich struktury i właściwości. Oto przykłady poprawnego nazywania:
Alkohole alifatyczne nazywamy podając najpierw nazwę węglowodoru, a następnie sufiks "-ol" z numerem wskazującym pozycję grupy -OH, np. butan-2-ol. W przypadku alkoholi cyklicznych używamy przedrostka "cyklo-", np. cykloheksan-1-ol.
Dla alkoholi aromatycznych, gdy grupa -OH jest przy łańcuchu bocznym (nie bezpośrednio przy pierścieniu), używamy nazwy fenylometanol (a nie alkohol benzylowy). Dla fenoli, gdy grupa -OH jest przyłączona bezpośrednio do pierścienia, używamy nazwy fenol z przedrostkami określającymi pozycje podstawników.
📝 Wskazówka egzaminacyjna: Na sprawdzianach często pojawiają się zadania wymagające nazwania skomplikowanych struktur alkoholi i fenoli. Pamiętaj o regułach pierwszeństwa przy numeracji i właściwych przedrostkach dla podstawników .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Przykłady struktur alkoholi nienasyconych i aromatycznych
Alkohole nienasycone zawierają w swojej strukturze zarówno grupę -OH jak i wiązania podwójne/potrójne. Przykładem jest but-3-en-2-ol, który zawiera wiązanie podwójne między 3. a 4. atomem węgla oraz grupę hydroksylową przy 2. atomie węgla.
W alkoholach aromatycznych grupa -OH może znajdować się przy pierścieniu aromatycznym lub przy łańcuchu bocznym. Na przykład 1-fenyloetan-1-ol ma grupę hydroksylową przy węglu sąsiadującym z pierścieniem benzenowym.
Struktury te można zapisywać na różne sposoby: wzorami strukturalnymi (z wyraźnym zaznaczeniem wszystkich wiązań i atomów) lub półstrukturalnymi (z grupami jak CH₃ zapisanymi w skróconej formie).
🔍 Ważne podczas nauki: Rysując struktury, zwracaj uwagę na poprawne umiejscowienie grupy hydroksylowej i numerację węgli. Błędy w tych elementach prowadzą do opisania zupełnie innego związku!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Klasyfikacja alkoholi i przykłady reakcji
Alkohole klasyfikujemy według liczby grup hydroksylowych oraz rzędowości atomu węgla z grupą -OH. Na przykład 3-metylobutan-2-ol to alkohol drugorzędowy, a 2,3-dimetylopenta-2,3-diol to alkohol trzeciorzędowy z dwiema grupami -OH.
Alkohole wchodzą w liczne reakcje chemiczne. Z wodorotlenkiem potasu tworzą alkoholany: CH₃-CH₂-CH(OH)-CH₃ + KOH → CH₃-CH₂-CH(OK)-CH₃ + H₂O.
W reakcjach utleniania alkohole pierwszorzędowe dają aldehydy, a następnie kwasy karboksylowe: CH₃-CH₂-OH + [O] → CH₃-CHO + H₂O. Alkohole drugorzędowe utleniają się do ketonów.
💫 Porada dla ambitnych: Reakcje alkoholi są podstawą wielu syntez organicznych. Opanowanie mechanizmów tych reakcji pozwoli Ci nie tylko rozwiązywać typowe zadania egzaminacyjne, ale także przewidywać produkty w bardziej złożonych reakcjach.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.