Aminy i amidy to kluczowe związki organiczne zawierające atom azotu,... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
707
•
Zaktualizowano May 10, 2026
•
Julia
@julia_vd
Aminy i amidy to kluczowe związki organiczne zawierające atom azotu,... Pokaż więcej
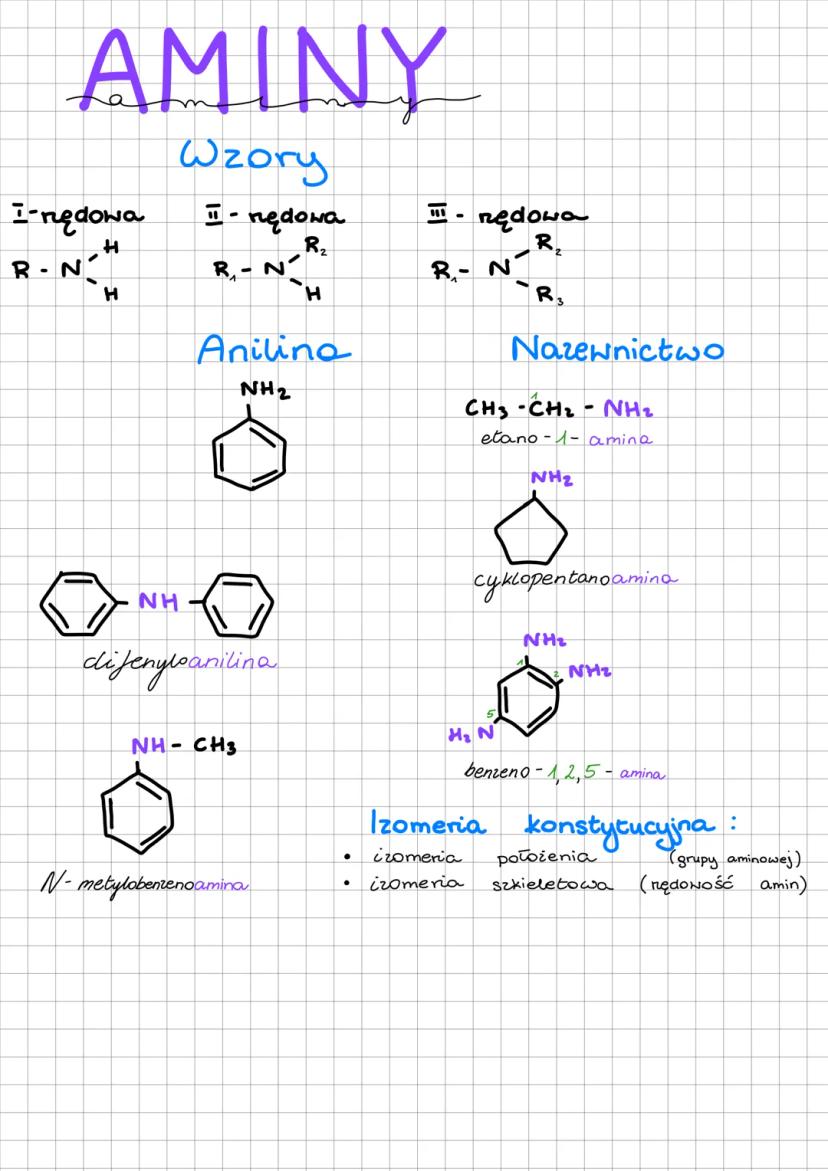


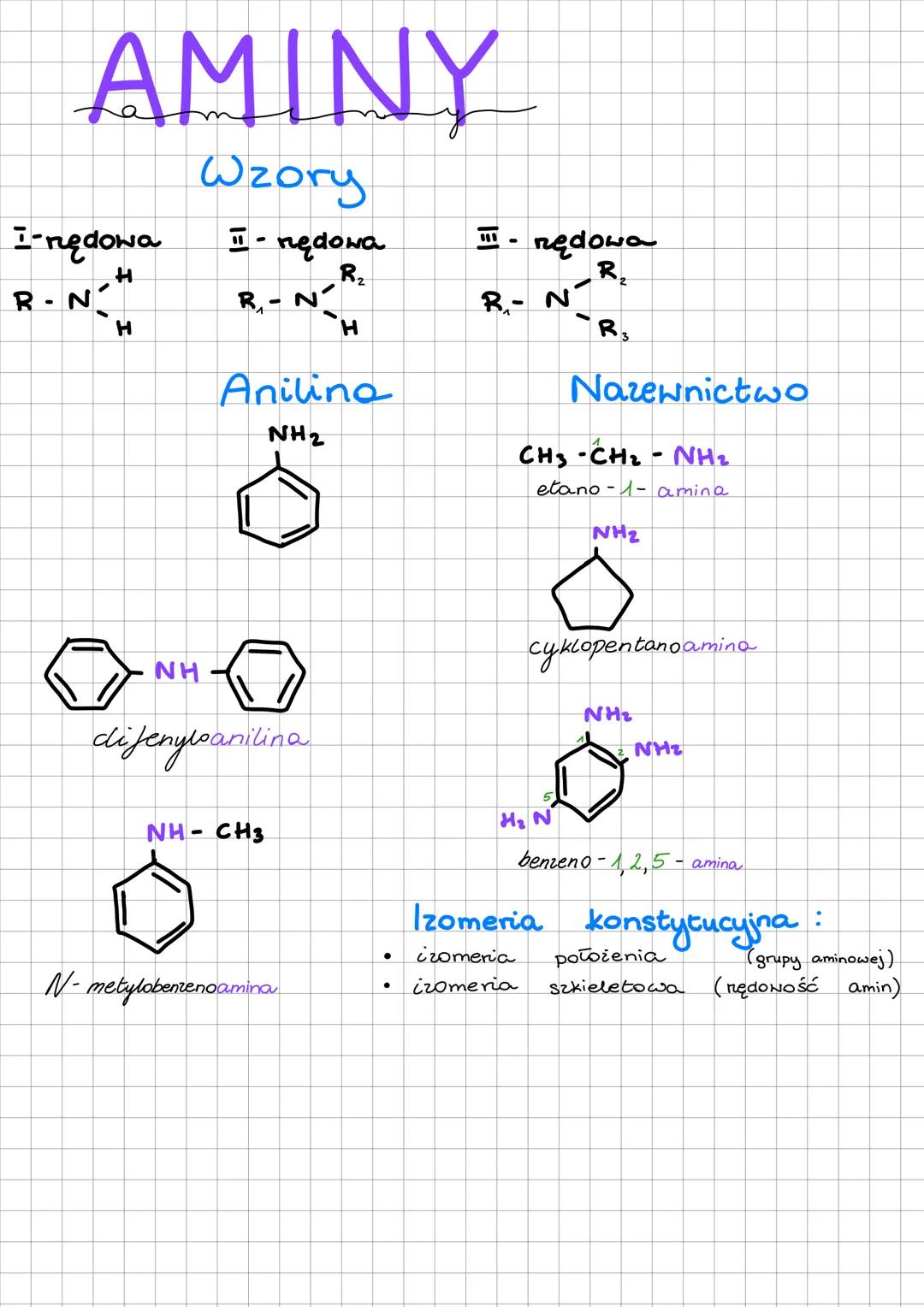
Aminy to pochodne amoniaku, w którym jeden lub więcej atomów wodoru zostały zastąpione grupami organicznymi. Dzielimy je według liczby podstawników przy atomie azotu:
Nazewnictwo amin jest dość proste - dodajemy przyrostek "-amino" lub "-amina" do nazwy związku macierzystego. Na przykład: etano-1-amina czy N-metylobenzenoamina.
W aminach występują różne rodzaje izomerii konstytucyjnej. Może to być izomeria położenia grupy aminowej (np. w różnych miejscach pierścienia) lub izomeria szkieletowa związana z rzędowością amin.
💡 Warto wiedzieć! Anilina (C₆H₅NH₂) to najprostsza aromatyczna amina, która ma ogromne znaczenie w przemyśle, zwłaszcza w produkcji barwników.

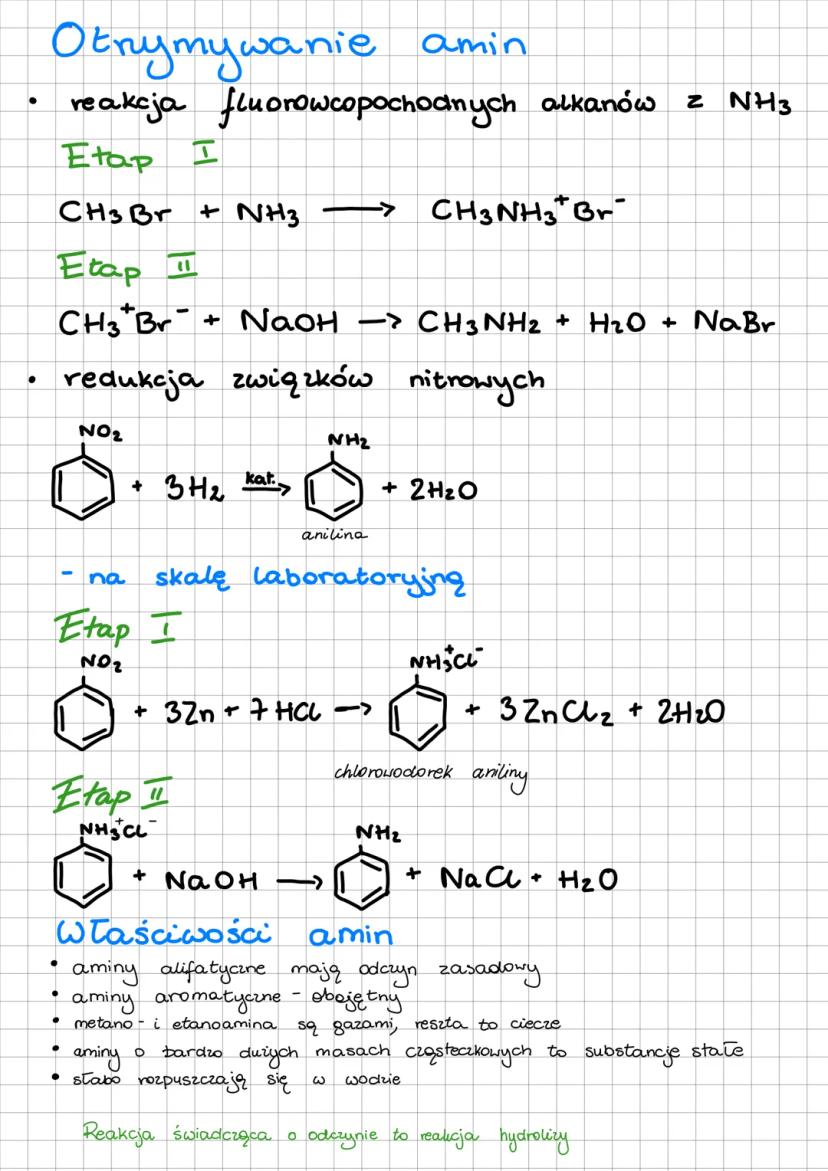
Aminy można otrzymać na kilka sposobów:
Reakcja fluorowcopochodnych alkanów z amoniakiem - proces przebiega dwuetapowo. Najpierw tworzy się sól amoniowa, a następnie pod wpływem zasady powstaje amina.
Redukcja związków nitrowych - zwłaszcza w przypadku amin aromatycznych, jak anilina. W warunkach laboratoryjnych często używa się cynku i kwasu solnego, a następnie neutralizuje wodorotlenkiem sodu.
Właściwości fizyczne amin zależą od ich masy cząsteczkowej:
⚠️ Pamiętaj! Aminy alifatyczne mają odczyn zasadowy, natomiast aminy aromatyczne (jak anilina) - praktycznie obojętny. Wynika to z wpływu pierścienia aromatycznego na parę elektronową azotu.

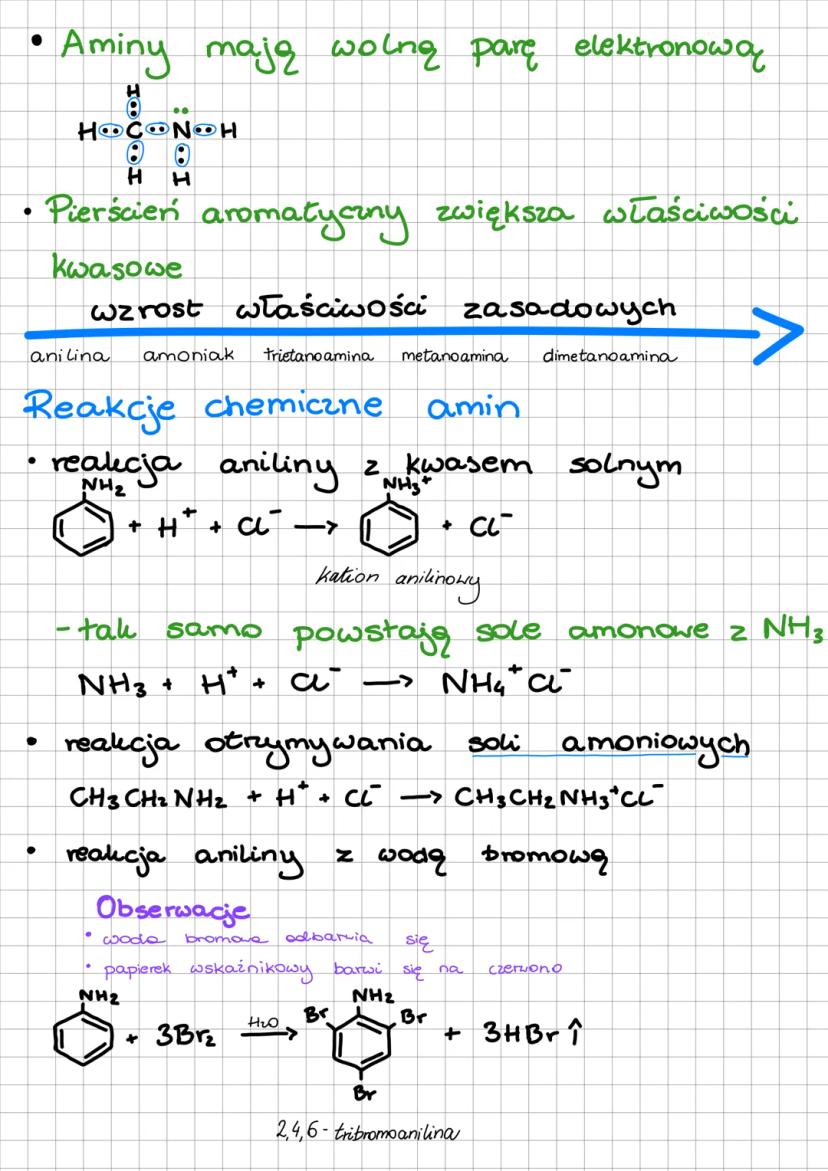
Aminy są związkami aktywnymi chemicznie dzięki wolnej parze elektronowej na atomie azotu. Ich zasadowość zmienia się w szeregu: anilina < amoniak < trietanoamina < metanoamina < dimetanoamina.
Najważniejsze reakcje amin to:
Reakcja z kwasami - aminy reagują z kwasami, tworząc sole amoniowe. Na przykład anilina reaguje z kwasem solnym, tworząc kation anilinowy: C₆H₅NH₂ + H⁺Cl⁻ → C₆H₅NH₃⁺Cl⁻
Reakcja aniliny z wodą bromową - to ważna reakcja identyfikacyjna, podczas której woda bromowa odbarwia się, a powstaje 2,4,6-tribromoanilina. Jest to przykład podstawienia elektrofilowego w pierścieniu aromatycznym.
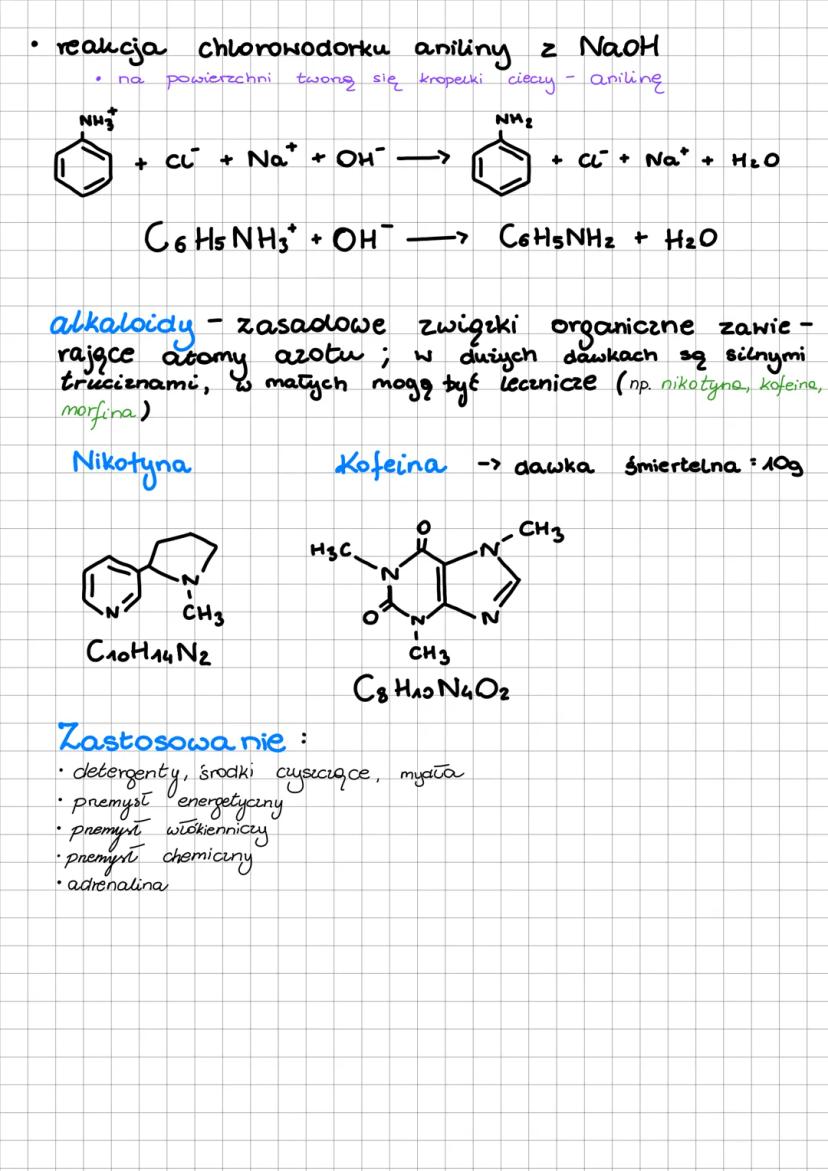
Rozkład soli aminowych - chlorowodorek aniliny reaguje z NaOH, uwalniając anilinę (widoczną jako kropelki cieczy).
💡 Ciekawostka! Pierścień aromatyczny zmniejsza zasadowość aminy, ponieważ para elektronowa atomu azotu wchodzi w sprzężenie z elektronami π pierścienia aromatycznego.

Aminy mają szerokie zastosowanie w różnych dziedzinach przemysłu:
Alkaloidy to naturalne związki zasadowe zawierające atom azotu, występujące głównie w roślinach. W małych dawkach mogą mieć działanie lecznicze, ale w dużych są silnymi truciznami.
Przykładami alkaloidów są:
⚠️ Uwaga! Dawka śmiertelna kofeiny dla człowieka wynosi około 10 gramów, co odpowiada wypiciu około 80-100 filiżanek kawy w krótkim czasie!
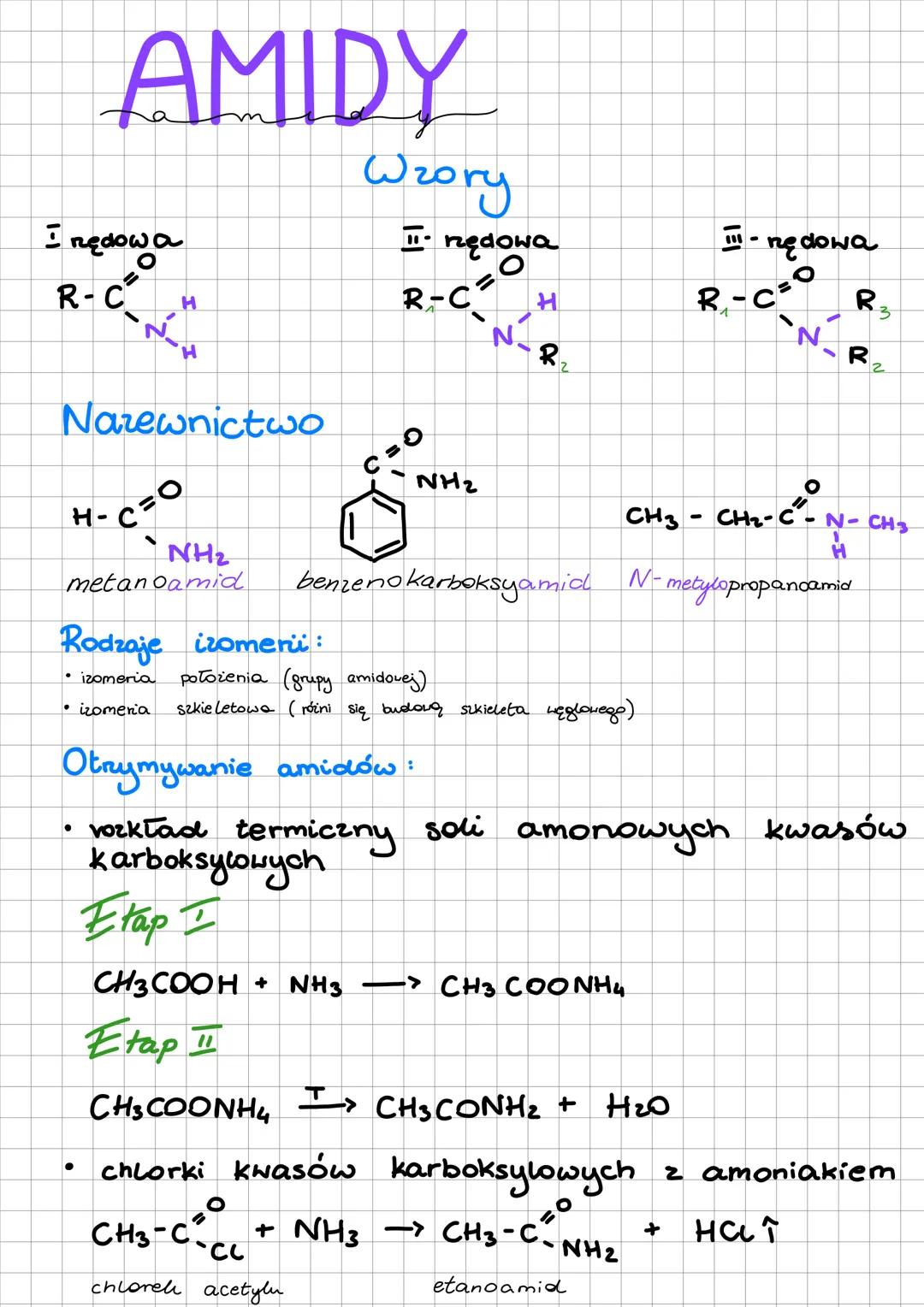
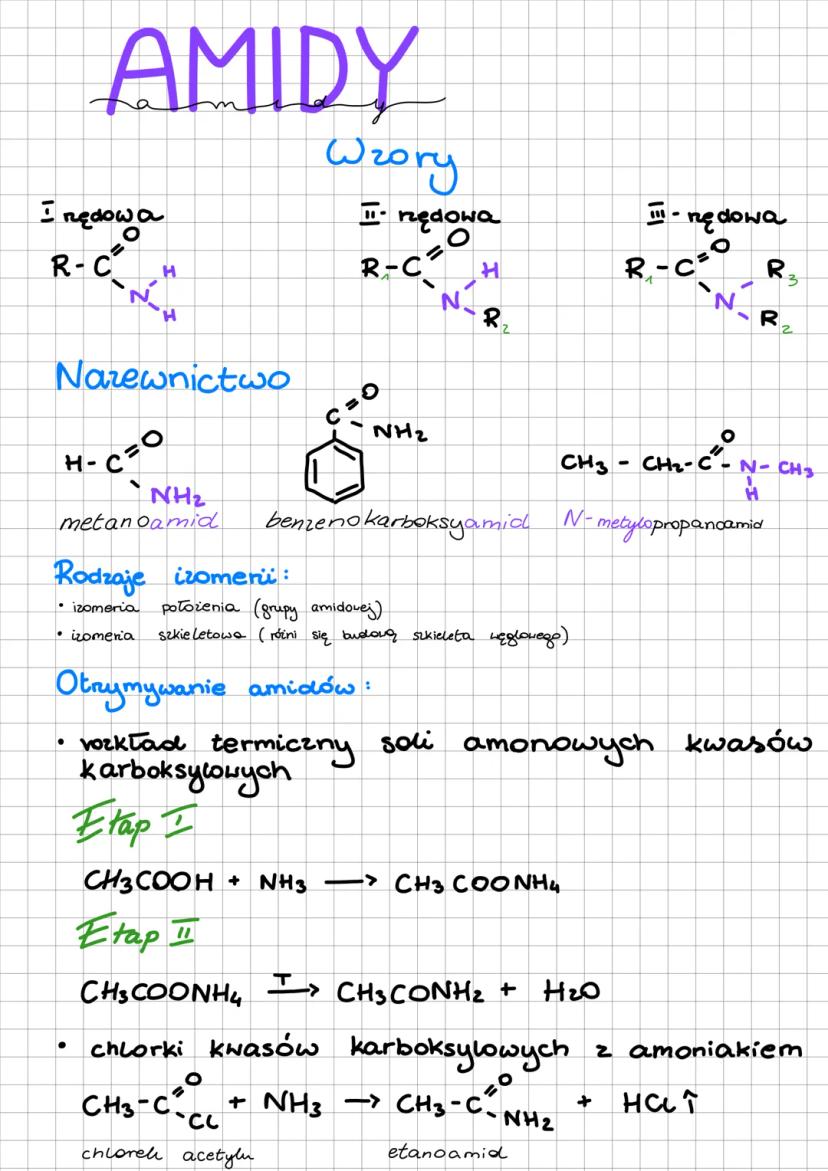
Amidy to pochodne kwasów karboksylowych, w których grupa -OH została zastąpiona grupą -NH₂, -NHR lub -NR₂. Podobnie jak w przypadku amin, wyróżniamy amidy:
W nazewnictwie amidów używamy przyrostka "-amid" lub "-karboksyamid", np. metanoamid (najprostszy amid) lub benzenokarboksyamid.
Amidy otrzymujemy głównie na dwa sposoby:
💡 Wskazówka! Amidy są mniej zasadowe niż aminy, ponieważ wolna para elektronowa atomu azotu wchodzi w sprzężenie z grupą karbonylową, co zmniejsza jej dostępność.

Amidy wykazują interesujące właściwości chemiczne:
Mocznik to najprostszy diamid, który jest produktem końcowym metabolizmu białek u ssaków. Jego ważne reakcje to:
Poliamidy to polimery zawierające wiązania peptydowe . Powstają w wyniku reakcji polikondensacji diamin z kwasami dikarboksylowymi. Przykładem jest nylon - elastyczne i wytrzymałe włókno.
💡 Ciekawostka! Wiązanie peptydowe można wykryć przy pomocy siarczanu(VI) miedzi(II) - pojawia się charakterystyczne fioletowe zabarwienie. Ta sama reakcja pozwala wykryć białka w próbkach biologicznych.

Poliuretany to polimery zawierające ugrupowanie uretanowe . Powstają w wyniku reakcji polikondensacji i mają cenne właściwości:
Amidy i ich polimery mają szerokie zastosowanie:
⚠️ Pamiętaj! Ugrupowanie uretanowe różni się od wiązania peptydowego obecnością dodatkowego atomu tlenu, co nadaje poliuretanom odmienne właściwości od poliamidów.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Julia
@julia_vd
Aminy i amidy to kluczowe związki organiczne zawierające atom azotu, które mają szerokie zastosowanie w przemyśle i medycynie. Poznamy ich budowę, nazewnictwo, metody otrzymywania oraz najważniejsze właściwości i reakcje.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Aminy to pochodne amoniaku, w którym jeden lub więcej atomów wodoru zostały zastąpione grupami organicznymi. Dzielimy je według liczby podstawników przy atomie azotu:
Nazewnictwo amin jest dość proste - dodajemy przyrostek "-amino" lub "-amina" do nazwy związku macierzystego. Na przykład: etano-1-amina czy N-metylobenzenoamina.
W aminach występują różne rodzaje izomerii konstytucyjnej. Może to być izomeria położenia grupy aminowej (np. w różnych miejscach pierścienia) lub izomeria szkieletowa związana z rzędowością amin.
💡 Warto wiedzieć! Anilina (C₆H₅NH₂) to najprostsza aromatyczna amina, która ma ogromne znaczenie w przemyśle, zwłaszcza w produkcji barwników.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Aminy można otrzymać na kilka sposobów:
Reakcja fluorowcopochodnych alkanów z amoniakiem - proces przebiega dwuetapowo. Najpierw tworzy się sól amoniowa, a następnie pod wpływem zasady powstaje amina.
Redukcja związków nitrowych - zwłaszcza w przypadku amin aromatycznych, jak anilina. W warunkach laboratoryjnych często używa się cynku i kwasu solnego, a następnie neutralizuje wodorotlenkiem sodu.
Właściwości fizyczne amin zależą od ich masy cząsteczkowej:
⚠️ Pamiętaj! Aminy alifatyczne mają odczyn zasadowy, natomiast aminy aromatyczne (jak anilina) - praktycznie obojętny. Wynika to z wpływu pierścienia aromatycznego na parę elektronową azotu.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Aminy są związkami aktywnymi chemicznie dzięki wolnej parze elektronowej na atomie azotu. Ich zasadowość zmienia się w szeregu: anilina < amoniak < trietanoamina < metanoamina < dimetanoamina.
Najważniejsze reakcje amin to:
Reakcja z kwasami - aminy reagują z kwasami, tworząc sole amoniowe. Na przykład anilina reaguje z kwasem solnym, tworząc kation anilinowy: C₆H₅NH₂ + H⁺Cl⁻ → C₆H₅NH₃⁺Cl⁻
Reakcja aniliny z wodą bromową - to ważna reakcja identyfikacyjna, podczas której woda bromowa odbarwia się, a powstaje 2,4,6-tribromoanilina. Jest to przykład podstawienia elektrofilowego w pierścieniu aromatycznym.
Rozkład soli aminowych - chlorowodorek aniliny reaguje z NaOH, uwalniając anilinę (widoczną jako kropelki cieczy).
💡 Ciekawostka! Pierścień aromatyczny zmniejsza zasadowość aminy, ponieważ para elektronowa atomu azotu wchodzi w sprzężenie z elektronami π pierścienia aromatycznego.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Aminy mają szerokie zastosowanie w różnych dziedzinach przemysłu:
Alkaloidy to naturalne związki zasadowe zawierające atom azotu, występujące głównie w roślinach. W małych dawkach mogą mieć działanie lecznicze, ale w dużych są silnymi truciznami.
Przykładami alkaloidów są:
⚠️ Uwaga! Dawka śmiertelna kofeiny dla człowieka wynosi około 10 gramów, co odpowiada wypiciu około 80-100 filiżanek kawy w krótkim czasie!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Amidy to pochodne kwasów karboksylowych, w których grupa -OH została zastąpiona grupą -NH₂, -NHR lub -NR₂. Podobnie jak w przypadku amin, wyróżniamy amidy:
W nazewnictwie amidów używamy przyrostka "-amid" lub "-karboksyamid", np. metanoamid (najprostszy amid) lub benzenokarboksyamid.
Amidy otrzymujemy głównie na dwa sposoby:
💡 Wskazówka! Amidy są mniej zasadowe niż aminy, ponieważ wolna para elektronowa atomu azotu wchodzi w sprzężenie z grupą karbonylową, co zmniejsza jej dostępność.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Amidy wykazują interesujące właściwości chemiczne:
Mocznik to najprostszy diamid, który jest produktem końcowym metabolizmu białek u ssaków. Jego ważne reakcje to:
Poliamidy to polimery zawierające wiązania peptydowe . Powstają w wyniku reakcji polikondensacji diamin z kwasami dikarboksylowymi. Przykładem jest nylon - elastyczne i wytrzymałe włókno.
💡 Ciekawostka! Wiązanie peptydowe można wykryć przy pomocy siarczanu(VI) miedzi(II) - pojawia się charakterystyczne fioletowe zabarwienie. Ta sama reakcja pozwala wykryć białka w próbkach biologicznych.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Poliuretany to polimery zawierające ugrupowanie uretanowe . Powstają w wyniku reakcji polikondensacji i mają cenne właściwości:
Amidy i ich polimery mają szerokie zastosowanie:
⚠️ Pamiętaj! Ugrupowanie uretanowe różni się od wiązania peptydowego obecnością dodatkowego atomu tlenu, co nadaje poliuretanom odmienne właściwości od poliamidów.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
12
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS