Węglowodory to podstawowe związki organiczne składające się tylko z węgla... Pokaż więcej
Co to są węglowodory - Podstawowe informacje






Podstawowe typy reakcji węglowodorów i alkany
Zanim przejdziemy do konkretnych grup, musisz znać trzy główne typy reakcji. Reakcja substytucji to podstawienie jednych atomów przez inne (jak zamiana H na Cl). Reakcja addycji to przyłączenie bez produktu ubocznego, a eliminacji - odłączenie małej cząsteczki.
Alkany to węglowodory nasycone o wzorze z końcówką -an. Mają tylko pojedyncze wiązania, więc są mało reaktywne - reagują głównie z fluorowcami w reakcjach substytucji.
Najważniejszą reakcją alkanów jest chlorowanie metanu, które przebiega stopniowo - od przez , , aż do . Mechanizm to reakcja rodnikowa rozpoczynana światłem UV.
Pamiętaj: Alkany to "spokojne" węglowodory - ich główną reakcją jest substytucja rodnikowa z fluorowcami.

Źródła i otrzymywanie alkanów
Alkany znajdziesz wszędzie wokół siebie - w ropie naftowej, gazie ziemnym (głównie metan) i podczas przetwarzania węgla kamiennego. To właśnie te źródła pokrywają większość naszych potrzeb energetycznych.
W laboratorium możesz otrzymać alkany na kilka sposobów. Klasyczna metoda to reakcja soli kwasu karboksylowego z wodorotlenkiem - np. octan sodu z NaOH daje metan. Ważna jest też hydrowania alkenów i alkinów z katalizatorami Pt, Pd lub Ni.
Synteza Würtza pozwala łączyć dwie cząsteczki - halogenopochodne reagują z sodem, tworząc dłuższy łańcuch węglowy. To świetny sposób na budowanie większych molekuł z mniejszych fragmentów.
Metan doskonale się pali - w pełnym spalaniu daje i wodę, a w niepełnym może powstać sadza. Te reakcje wykorzystujemy jako źródło energii w naszych domach i przemyśle.

Alkeny, alkiny i reguły eliminacji
Alkeny $C_nH_{2n}$, końcówka -en i alkiny $C_nH_{2n-2}$, końcówka -yn to węglowodory nienasycone z wiązaniami podwójnymi i potrójnymi. Są znacznie bardziej reaktywne niż alkany.
Możesz je otrzymać przez eliminację - piroliza alkanów, dehydratacja alkoholi z , czy eliminacja HBr i z halogenopochodnych. Każda metoda ma swoje zastosowanie w zależności od dostępnych substratów.
Reguła Zajcewa mówi, że w eliminacji powstaje głównie produkt bardziej rozgałęziony - mniej uwodorniony. To kluczowe przy przewidywaniu, który produkt będzie dominował w mieszaninie.
Szczególną metodą otrzymywania etynu (acetylenu) jest reakcja karbidowa - karbid wapnia z wodą. Ten gaz był kiedyś podstawowym źródłem światła w lampach górniczych.
Wskazówka: Alkeny i alkiny łatwo rozpoznać po charakterystycznych końcówkach nazw i wzorach sumarycznych.

Reakcje addycji alkenów i alkinów
Alkeny i alkiny uwielbiają reakcje addycji elektrofilowej - przyłączają różne cząsteczki do swojego wiązania wielokrotnego. To ich główna właściwość chemiczna, która odróżnia je od alkanów.
Najprostsze addycje to przyłączanie fluorowców $Br_2$, $Cl_2$, wodoru z katalizatorem czy cząsteczek HX (HBr, HCl). Alkiny mogą przyłączyć dwie cząsteczki, bo mają wiązanie potrójne.
Reguła Markownikowa jest kluczowa przy addycji HX do niesymetrycznych alkenów - wodór idzie do bardziej uwodornionego węgla. Dzięki temu możesz przewidzieć, który produkt powstanie.
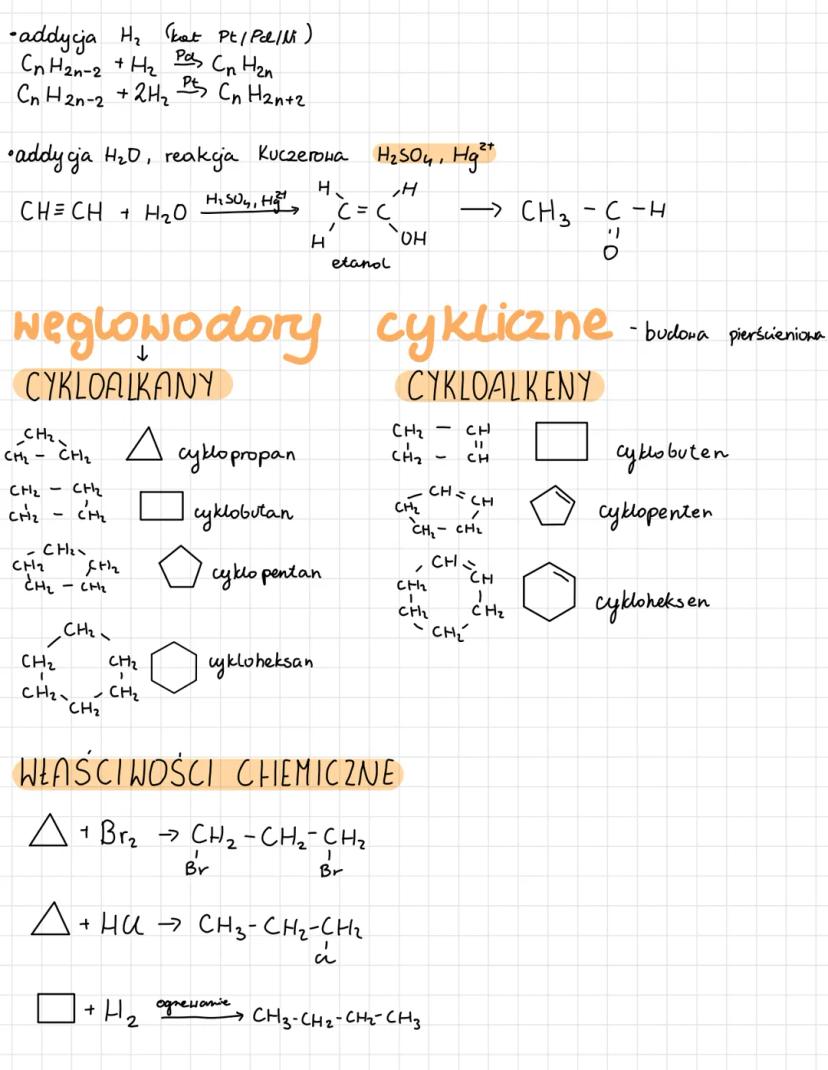
Addycja wody do alkinów (reakcja Kuczerowa) wymaga specjalnych warunków - i jako katalizator. Z etynu powstaje w ten sposób aldehyd octowy, który dalej się przekształca.
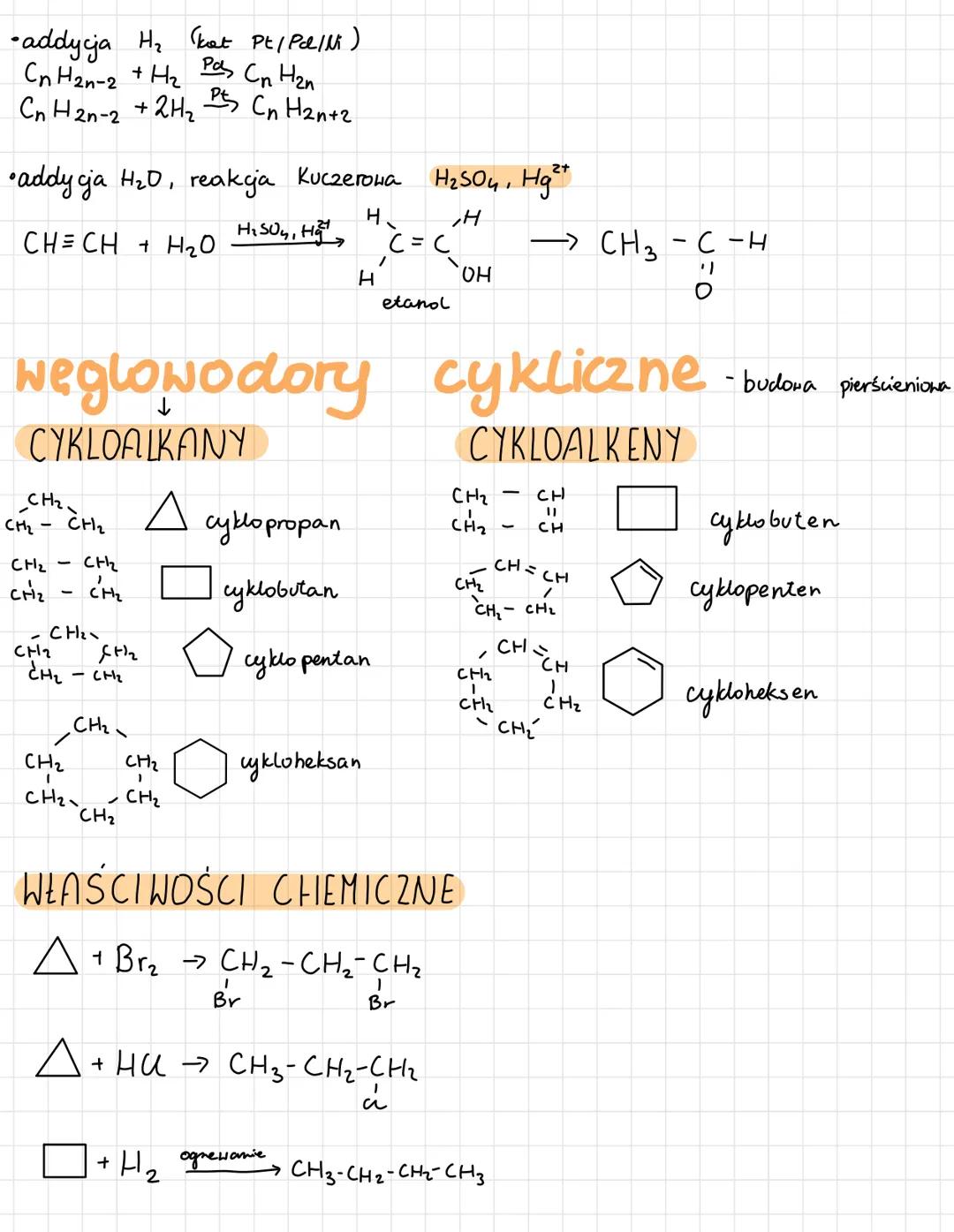
Węglowodory cykliczne
Cykloalkany i cykloalkeny to węglowodory o budowie pierścieniowej - od trójkąta (cyklopropan) przez czworoboki, pięciokąty aż do sześciokątów. Każdy pierścień ma swoje charakterystyczne właściwości.
Małe pierścienie są napięte i łatwo się otwierają w reakcjach addycji. Cyklopropan reaguje z czy HBr, dając produkty łańcuchowe - pierścień się rozpada.
Większe cykle są bardziej stabilne - cyklopentany i cykloheksany zachowują swoją strukturę, ale mogą ulegać substytucji. Cykloheksen może przyłączać , czy jak zwykły alken.
Otrzymywanie węglowodorów cyklicznych odbywa się przez cyklizację odpowiednich związków liniowych - eliminacja z dihalogenopochodnych czy dehydratacja cyklicznych alkoholi z .
Ciekawostka: Im mniejszy pierścień, tym bardziej "napięty" i reaktywny - cyklopropan to prawdziwy "energetyczny ładunek"!

Otrzymywanie cykli i wprowadzenie do polimerów
Tworzenie pierścieni z łańcuchów liniowych to fascynujący proces - dibrompochodne mogą zamykać się w cykle przez eliminację . Różne położenia grup bromowych dają różne produkty cykliczne.
Dehydratacja cykloheksanolu z to klasyczny sposób otrzymania cykloheksenu. Reakcja przebiega jak zwykła eliminacja wody, ale produkt zachowuje strukturę pierścieniową.
Polimery to gigantyczne cząsteczki zbudowane z powtarzających się jednostek - merów. Powstają przez łączenie małych molekuł (monomerów) w długie łańcuchy - to podstawa tworzyw sztucznych.
Proces polimeryzacji alkenów prowadzi do powstania polialkenów - z etylenu powstaje polietylen, z propylenu polipropylen. Te materiały otaczają nas w codziennym życiu jako plastikowe torby, butelki czy rury.
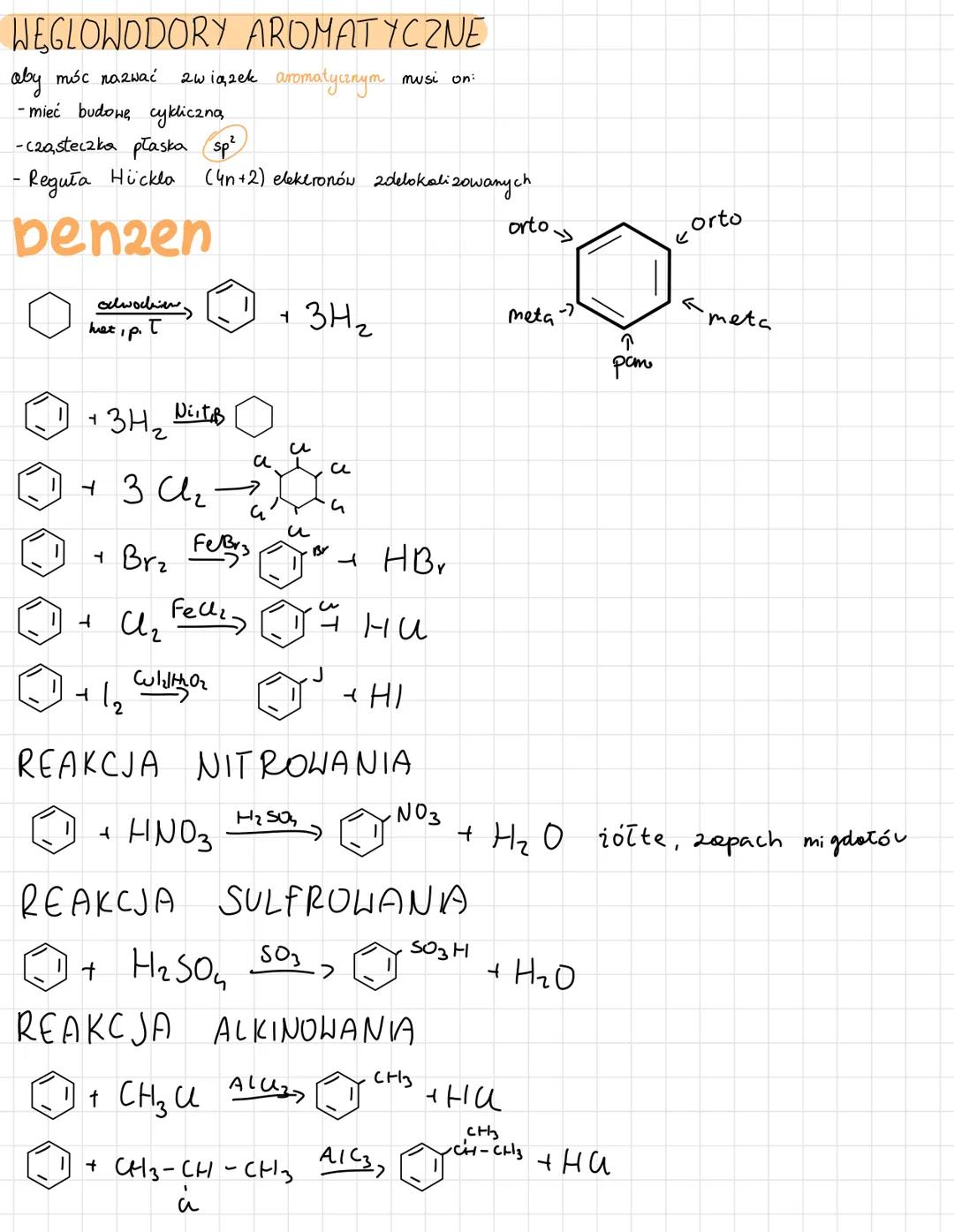
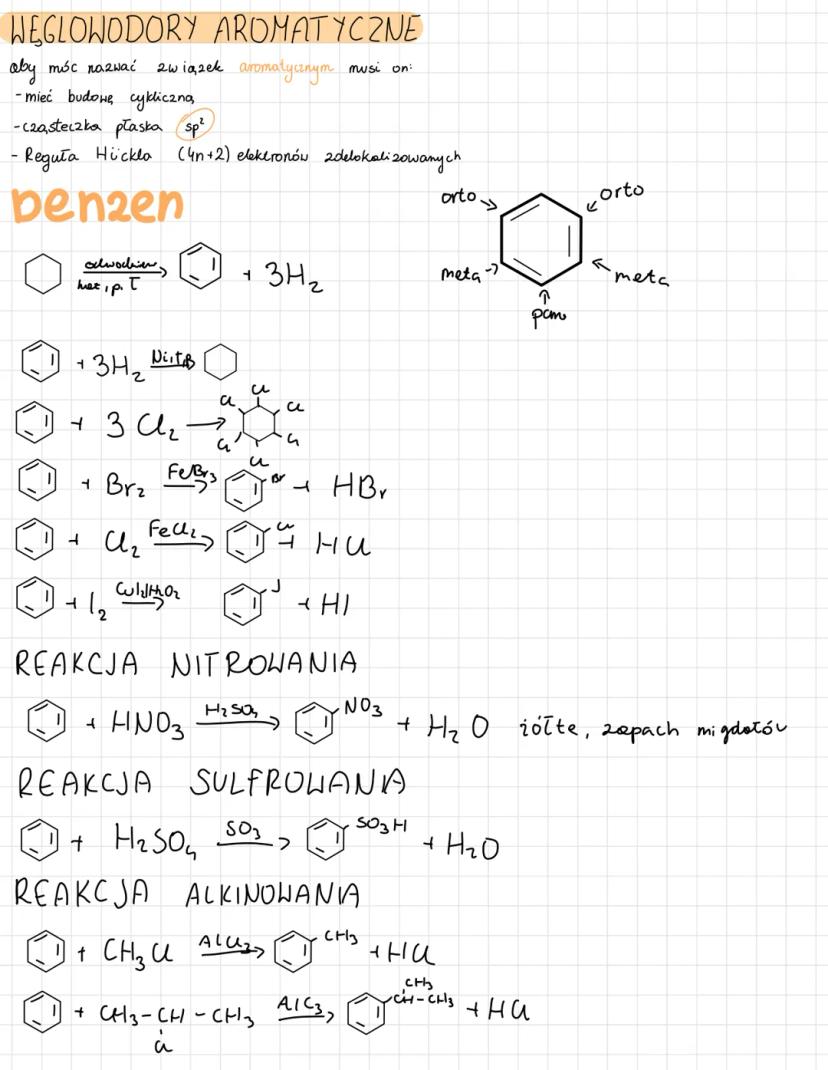
Węglowodory aromatyczne
Benzen i jego pochodne to szczególna grupa węglowodorów - aby związek był aromatyczny, musi mieć płaską budowę cykliczną i spełniać regułę Hückla .
Reakcje podstawienia elektrofilowego to główne reakcje benzenu. Nitrowanie z i daje nitrobenzen, sulfonowanie z - kwas benzenosulfonowy, a halogenowanie z - halogenobenzeny.
Alkilowanie benzenu pozwala wprowadzać grupy alkilowe z jako katalizatorem. Z chlorku metylu powstaje toluen, z chlorkiem izopropylu - izopropylobenzen.
Położenia w pierścieniu benzenu nazywamy orto (sąsiednie), meta (przez jeden) i para (naprzeciwko). Te nazwy pomagają określić, gdzie znajdują się podstawniki w cząsteczce.
Kluczowe: Benzen jest wyjątkowo stabilny przez aromatyczność - dlatego preferuje substytucję zamiast addycji!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Węglowodory kl8
Węglowodory
Węglowodory: Alkany, Alkeny, Alkiny
Zgłębiaj właściwości, reakcje i zastosowania węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o ich strukturze, procesach spalania, polimeryzacji oraz naturalnych źródłach. Idealne dla uczniów 8 klasy.
Węglowodory: Alkany, Alkeny, Alkiny
Zrozumienie węglowodorów nasyconych i nienasyconych: alkany, alkeny i alkiny. Dowiedz się o ich strukturze, właściwościach, zastosowaniach oraz reakcjach chemicznych. Idealne dla uczniów szkół podstawowych i średnich. Typ: Podsumowanie.
Alkiny
Chemia organiczna Notatka na podstawie portalu dlaucznia.pl i podręcznika Chemia Nowej Ery 8
Węglowodory sprawdzian Nowa Era
Test z nowej ery z chemii
Alkany: Właściwości i Reakcje
Odkryj kluczowe informacje o alkanach, ich właściwościach, nomenklaturze oraz reakcjach spalania. Dowiedz się, jak nazywać alkany i jakie mają zastosowania. Idealne dla studentów chemii. Typ: Podsumowanie.
Węglowodory: Alkan, Alken, Alkin
Zgłębiaj węglowodory, ich klasyfikację oraz reakcje spalania. Dowiedz się o alkanach, alkenach i alkinach, ich wzorach chemicznych oraz różnicach w reakcjach całkowitych i niecałkowitych. Idealne dla uczniów chemii.
Właściwości i Budowa Alkinów
Zgłębiaj właściwości, budowę i reakcje alkinów, w tym ich izomery i reakcje spalania. Dowiedz się, jak tworzyć nazwy alkinów oraz poznaj ich wzory strukturalne i ogólne. Idealne dla studentów chemii poszukujących zrozumienia węglowodorów nienasyconych.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Węglowodory kl8
Węglowodory
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Bohaterowie Zbrodni i Kary
Analiza postaci i kluczowych motywów w 'Zbrodni i karze' Fiodora Dostojewskiego. Zawiera szczegółowe opisy bohaterów, ich relacji oraz wpływu zbrodni na psychikę Raskolnikowa. Idealne dla studentów literatury i analizy psychologicznej. Typ: streszczenie i charakterystyka.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Co to są węglowodory - Podstawowe informacje
Węglowodory to podstawowe związki organiczne składające się tylko z węgla i wodoru - poznanie ich reakcji i właściwości to klucz do zrozumienia całej chemii organicznej. Dzielą się na nasycone (alkany) i nienasycone (alkeny, alkiny) oraz cykliczne i aromatyczne, a każda... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Podstawowe typy reakcji węglowodorów i alkany
Zanim przejdziemy do konkretnych grup, musisz znać trzy główne typy reakcji. Reakcja substytucji to podstawienie jednych atomów przez inne (jak zamiana H na Cl). Reakcja addycji to przyłączenie bez produktu ubocznego, a eliminacji - odłączenie małej cząsteczki.
Alkany to węglowodory nasycone o wzorze z końcówką -an. Mają tylko pojedyncze wiązania, więc są mało reaktywne - reagują głównie z fluorowcami w reakcjach substytucji.
Najważniejszą reakcją alkanów jest chlorowanie metanu, które przebiega stopniowo - od przez , , aż do . Mechanizm to reakcja rodnikowa rozpoczynana światłem UV.
Pamiętaj: Alkany to "spokojne" węglowodory - ich główną reakcją jest substytucja rodnikowa z fluorowcami.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Źródła i otrzymywanie alkanów
Alkany znajdziesz wszędzie wokół siebie - w ropie naftowej, gazie ziemnym (głównie metan) i podczas przetwarzania węgla kamiennego. To właśnie te źródła pokrywają większość naszych potrzeb energetycznych.
W laboratorium możesz otrzymać alkany na kilka sposobów. Klasyczna metoda to reakcja soli kwasu karboksylowego z wodorotlenkiem - np. octan sodu z NaOH daje metan. Ważna jest też hydrowania alkenów i alkinów z katalizatorami Pt, Pd lub Ni.
Synteza Würtza pozwala łączyć dwie cząsteczki - halogenopochodne reagują z sodem, tworząc dłuższy łańcuch węglowy. To świetny sposób na budowanie większych molekuł z mniejszych fragmentów.
Metan doskonale się pali - w pełnym spalaniu daje i wodę, a w niepełnym może powstać sadza. Te reakcje wykorzystujemy jako źródło energii w naszych domach i przemyśle.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkeny, alkiny i reguły eliminacji
Alkeny $C_nH_{2n}$, końcówka -en i alkiny $C_nH_{2n-2}$, końcówka -yn to węglowodory nienasycone z wiązaniami podwójnymi i potrójnymi. Są znacznie bardziej reaktywne niż alkany.
Możesz je otrzymać przez eliminację - piroliza alkanów, dehydratacja alkoholi z , czy eliminacja HBr i z halogenopochodnych. Każda metoda ma swoje zastosowanie w zależności od dostępnych substratów.
Reguła Zajcewa mówi, że w eliminacji powstaje głównie produkt bardziej rozgałęziony - mniej uwodorniony. To kluczowe przy przewidywaniu, który produkt będzie dominował w mieszaninie.
Szczególną metodą otrzymywania etynu (acetylenu) jest reakcja karbidowa - karbid wapnia z wodą. Ten gaz był kiedyś podstawowym źródłem światła w lampach górniczych.
Wskazówka: Alkeny i alkiny łatwo rozpoznać po charakterystycznych końcówkach nazw i wzorach sumarycznych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje addycji alkenów i alkinów
Alkeny i alkiny uwielbiają reakcje addycji elektrofilowej - przyłączają różne cząsteczki do swojego wiązania wielokrotnego. To ich główna właściwość chemiczna, która odróżnia je od alkanów.
Najprostsze addycje to przyłączanie fluorowców $Br_2$, $Cl_2$, wodoru z katalizatorem czy cząsteczek HX (HBr, HCl). Alkiny mogą przyłączyć dwie cząsteczki, bo mają wiązanie potrójne.
Reguła Markownikowa jest kluczowa przy addycji HX do niesymetrycznych alkenów - wodór idzie do bardziej uwodornionego węgla. Dzięki temu możesz przewidzieć, który produkt powstanie.
Addycja wody do alkinów (reakcja Kuczerowa) wymaga specjalnych warunków - i jako katalizator. Z etynu powstaje w ten sposób aldehyd octowy, który dalej się przekształca.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Węglowodory cykliczne
Cykloalkany i cykloalkeny to węglowodory o budowie pierścieniowej - od trójkąta (cyklopropan) przez czworoboki, pięciokąty aż do sześciokątów. Każdy pierścień ma swoje charakterystyczne właściwości.
Małe pierścienie są napięte i łatwo się otwierają w reakcjach addycji. Cyklopropan reaguje z czy HBr, dając produkty łańcuchowe - pierścień się rozpada.
Większe cykle są bardziej stabilne - cyklopentany i cykloheksany zachowują swoją strukturę, ale mogą ulegać substytucji. Cykloheksen może przyłączać , czy jak zwykły alken.
Otrzymywanie węglowodorów cyklicznych odbywa się przez cyklizację odpowiednich związków liniowych - eliminacja z dihalogenopochodnych czy dehydratacja cyklicznych alkoholi z .
Ciekawostka: Im mniejszy pierścień, tym bardziej "napięty" i reaktywny - cyklopropan to prawdziwy "energetyczny ładunek"!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie cykli i wprowadzenie do polimerów
Tworzenie pierścieni z łańcuchów liniowych to fascynujący proces - dibrompochodne mogą zamykać się w cykle przez eliminację . Różne położenia grup bromowych dają różne produkty cykliczne.
Dehydratacja cykloheksanolu z to klasyczny sposób otrzymania cykloheksenu. Reakcja przebiega jak zwykła eliminacja wody, ale produkt zachowuje strukturę pierścieniową.
Polimery to gigantyczne cząsteczki zbudowane z powtarzających się jednostek - merów. Powstają przez łączenie małych molekuł (monomerów) w długie łańcuchy - to podstawa tworzyw sztucznych.
Proces polimeryzacji alkenów prowadzi do powstania polialkenów - z etylenu powstaje polietylen, z propylenu polipropylen. Te materiały otaczają nas w codziennym życiu jako plastikowe torby, butelki czy rury.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Węglowodory aromatyczne
Benzen i jego pochodne to szczególna grupa węglowodorów - aby związek był aromatyczny, musi mieć płaską budowę cykliczną i spełniać regułę Hückla .
Reakcje podstawienia elektrofilowego to główne reakcje benzenu. Nitrowanie z i daje nitrobenzen, sulfonowanie z - kwas benzenosulfonowy, a halogenowanie z - halogenobenzeny.
Alkilowanie benzenu pozwala wprowadzać grupy alkilowe z jako katalizatorem. Z chlorku metylu powstaje toluen, z chlorkiem izopropylu - izopropylobenzen.
Położenia w pierścieniu benzenu nazywamy orto (sąsiednie), meta (przez jeden) i para (naprzeciwko). Te nazwy pomagają określić, gdzie znajdują się podstawniki w cząsteczce.
Kluczowe: Benzen jest wyjątkowo stabilny przez aromatyczność - dlatego preferuje substytucję zamiast addycji!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Węglowodory kl8
Węglowodory
Węglowodory: Alkany, Alkeny, Alkiny
Zgłębiaj właściwości, reakcje i zastosowania węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o ich strukturze, procesach spalania, polimeryzacji oraz naturalnych źródłach. Idealne dla uczniów 8 klasy.
Węglowodory: Alkany, Alkeny, Alkiny
Zrozumienie węglowodorów nasyconych i nienasyconych: alkany, alkeny i alkiny. Dowiedz się o ich strukturze, właściwościach, zastosowaniach oraz reakcjach chemicznych. Idealne dla uczniów szkół podstawowych i średnich. Typ: Podsumowanie.
Alkiny
Chemia organiczna Notatka na podstawie portalu dlaucznia.pl i podręcznika Chemia Nowej Ery 8
Węglowodory sprawdzian Nowa Era
Test z nowej ery z chemii
Alkany: Właściwości i Reakcje
Odkryj kluczowe informacje o alkanach, ich właściwościach, nomenklaturze oraz reakcjach spalania. Dowiedz się, jak nazywać alkany i jakie mają zastosowania. Idealne dla studentów chemii. Typ: Podsumowanie.
Węglowodory: Alkan, Alken, Alkin
Zgłębiaj węglowodory, ich klasyfikację oraz reakcje spalania. Dowiedz się o alkanach, alkenach i alkinach, ich wzorach chemicznych oraz różnicach w reakcjach całkowitych i niecałkowitych. Idealne dla uczniów chemii.
Właściwości i Budowa Alkinów
Zgłębiaj właściwości, budowę i reakcje alkinów, w tym ich izomery i reakcje spalania. Dowiedz się, jak tworzyć nazwy alkinów oraz poznaj ich wzory strukturalne i ogólne. Idealne dla studentów chemii poszukujących zrozumienia węglowodorów nienasyconych.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Węglowodory kl8
Węglowodory
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Bohaterowie Zbrodni i Kary
Analiza postaci i kluczowych motywów w 'Zbrodni i karze' Fiodora Dostojewskiego. Zawiera szczegółowe opisy bohaterów, ich relacji oraz wpływu zbrodni na psychikę Raskolnikowa. Idealne dla studentów literatury i analizy psychologicznej. Typ: streszczenie i charakterystyka.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.