Węglowodory stanowią podstawową grupę związków organicznych, zbudowanych wyłącznie z atomów... Pokaż więcej
Węglowodory – Notatka z Chemii




Alkany i ich właściwości
Właściwości alkanów
Alkany charakteryzują się:
- Wiązaniami pojedynczymi C-C
- Wzorem ogólnym: CnH2n+2
- Stabilną strukturą chemiczną
Przykłady alkanów:
- Metan (CH4)
- Etan (C2H6)
- Propan (C3H8)
- Butan (C4H10)
- Pentan (C5H12)
- Heksan (C6H14)
- Heptan (C7H16)
- Oktan (C8H18)
- Nonan (C9H20)
- Dekan (C10H22)
Właściwości fizyczne:
- Gęstość mniejsza od wody
- Niepolarność molekuł
- Nierozpuszczalność w wodzie
Właściwości chemiczne:
- Palność
- Tworzenie mieszanin wybuchowych z powietrzem (dla gazowych alkanów)
- Relatywna obojętność chemiczna w normalnych warunkach
Ważna reakcja: Podstawianie (substytucja) polega na zastąpieniu atomu wodoru w cząsteczce alkanu innym atomem lub grupą atomów. Przykładem jest reakcja: CH4 + Cl2 → CH3Cl + HCl, w wyniku której powstaje chlorometan.

Izomeria i alkeny - reakcje chemiczne
Izomeria strukturalna
Izomeria to zjawisko, które pozwala istnieć kilku różnym związkom o tym samym wzorze sumarycznym:
- Izomery mają taki sam skład pierwiastkowy, ale różną strukturę
- Przykład: butan i metylopropan (C4H10)
- butan: CH3-CH2-CH2-CH3 (łańcuch prosty)
- metylopropan: CH3-CH(CH3)-CH3 (łańcuch rozgałęziony)
Charakterystyka alkenów
Alkeny (CnH2n) posiadają:
- Co najmniej jedno wiązanie podwójne C=C
- Wysoką reaktywność chemiczną
- Szereg homologiczny: eten, propen, buten, penten, heksen, hepten, okten, nonen, deken
Właściwości fizyczne w zależności od długości łańcucha:
- Gazy: C2-C4
- Ciecze: C5-C10
- Ciała stałe: C11-C20
- Zależność: im dłuższy łańcuch węglowy, tym wyższa temperatura wrzenia i topnienia
Właściwości sensoryczne:
- Bezbarwne (formy gazowe i ciekłe)
- Lekko słodki smak
- Przyjemny zapach
Ważna reakcja: Addycja (przyłączenie) to charakterystyczna reakcja alkenów, w której następuje rozerwanie wiązania podwójnego i przyłączenie atomów lub grup atomów. Na przykład: H2C=CH2 + H2 → H3C-CH3. Ta reakcja umożliwia przekształcenie etenu w etan poprzez dodanie wodoru do wiązania podwójnego.

Polimeryzacja i właściwości alkinów
Polimeryzacja - kluczowy proces w przemyśle
Polimeryzacja to proces, w którym monomery (małe cząsteczki) łączą się ze sobą, tworząc polimery (duże cząsteczki).
- Równanie reakcji: n CH2=CH2 → n
- Substrat: eten (etylen)
- Produkt: polietylen (szeroko stosowany plastik)
- Proces ten jest podstawą produkcji wielu tworzyw sztucznych
Alkiny i ich charakterystyka
Alkiny to węglowodory nienasycone zawierające wiązanie potrójne między atomami węgla.
- Wzór ogólny: CnH2n-2
- Główni przedstawiciele szeregu homologicznego:
- Etin (acetylen) - C2H2
- Propyn - C3H4
- Butyn - C4H6
- Pentyn - C5H8
- Heksyn - C6H10
Właściwości fizyczne alkinów:
- Niepolarność cząsteczek
- Nierozpuszczalność w wodzie
- Zależność właściwości od długości łańcucha:
- Większa liczba atomów węgla → wyższa temperatura wrzenia
- Większa liczba atomów węgla → wyższa temperatura topnienia
Właściwości chemiczne alkinów:
- Wysoka palność - acetylen wykorzystywany w palnikach
- Etin (acetylen) jest bezwonnym gazem
- Duża reaktywność wiązania potrójnego
Zastosowanie praktyczne: Etin (acetylen) jest szeroko stosowany w spawalnictwie ze względu na wysoką temperaturę spalania (około 3000°C). Palniki acetylenowo-tlenowe umożliwiają spawanie i cięcie metali, co ma ogromne znaczenie w przemyśle.
Węglowodory aromatyczne - benzen i jego pochodne
Benzen i jego charakterystyka
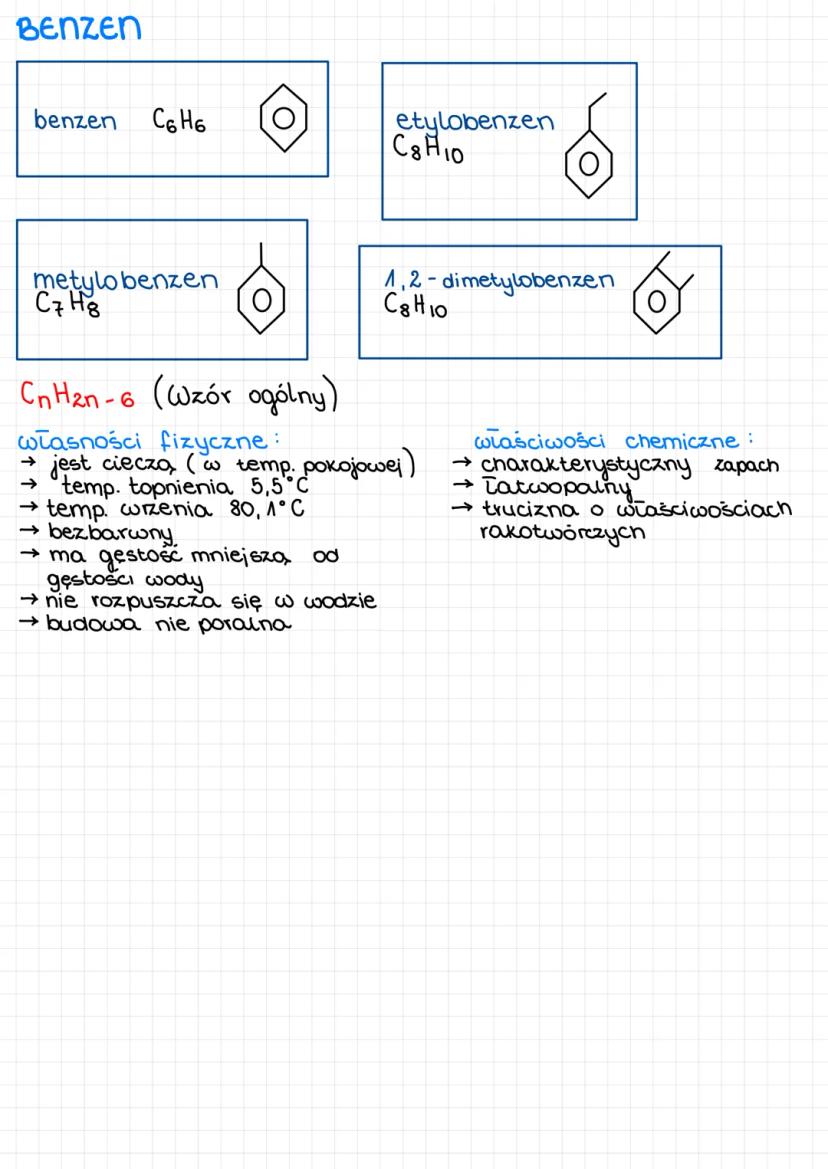
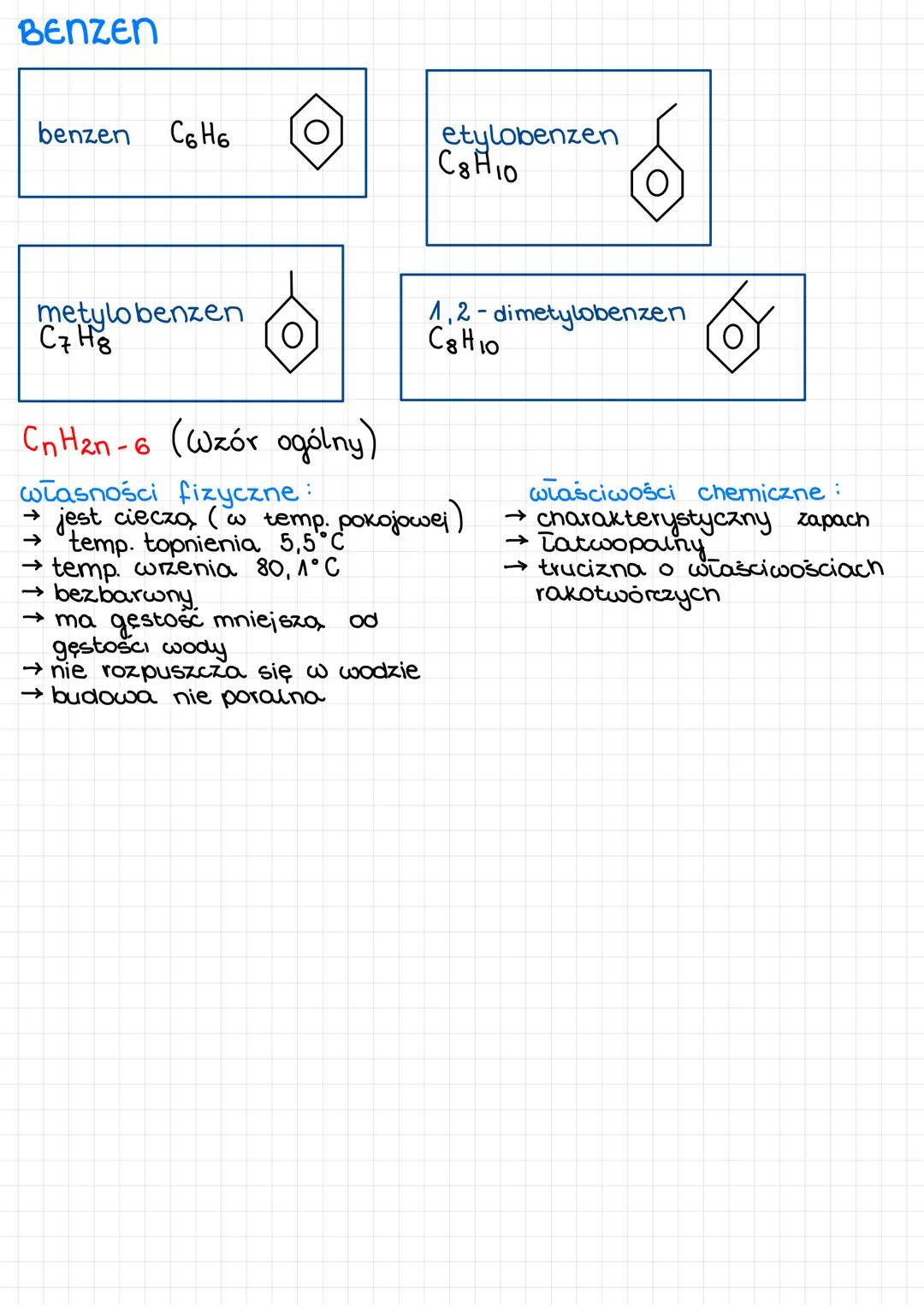
Benzen (C6H6) jest podstawowym przedstawicielem węglowodorów aromatycznych o charakterystycznej budowie pierścieniowej.
- Wzór ogólny węglowodorów aromatycznych: CnH2n-6
- Najważniejsze pochodne benzenu:
- Metylobenzen (toluen) - C7H8
- Etylobenzen - C8H10
- 1,2-dimetylobenzen - C8H10
Struktura benzenu:
- Pierścień sześcioczłonowy z naprzemiennymi wiązaniami pojedynczymi i podwójnymi
- Wysokie stabilizacja rezonansowa (delokalizacja elektronów)
- Płaska struktura molekularna
Właściwości fizyczne benzenu:
- Stan skupienia: ciecz (w temperaturze pokojowej)
- Temperatura topnienia: 5,5°C
- Temperatura wrzenia: 80,1°C
- Wygląd: bezbarwna ciecz
- Gęstość: mniejsza od wody
- Rozpuszczalność: nie rozpuszcza się w wodzie
- Charakter: niepolarny
Właściwości chemiczne benzenu:
- Zapach: charakterystyczny, aromatyczny
- Palność: łatwopalny
- Zagrożenia: silna toksyczność i działanie rakotwórcze
Zagrożenia zdrowotne: Benzen jest niebezpieczną substancją chemiczną o udowodnionym działaniu kancerogennym. Może powodować uszkodzenia szpiku kostnego i zwiększać ryzyko zachorowania na białaczkę. Z tego powodu jego użycie jest ściśle kontrolowane, a w wielu produktach codziennego użytku został zastąpiony bezpieczniejszymi substancjami.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Węglowodory – Notatka z Chemii
Węglowodory stanowią podstawową grupę związków organicznych, zbudowanych wyłącznie z atomów węgla i wodoru. Dzielimy je na dwie główne kategorie: alifatyczne (łańcuchowe) oraz aromatyczne (pierścieniowe). Węglowodory alifatyczne obejmują alkany (związki nasycone z wiązaniami pojedynczymi), alkeny (zawierające co najmniej jedno wiązanie podwójne)... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkany i ich właściwości
Właściwości alkanów
Alkany charakteryzują się:
- Wiązaniami pojedynczymi C-C
- Wzorem ogólnym: CnH2n+2
- Stabilną strukturą chemiczną
Przykłady alkanów:
- Metan (CH4)
- Etan (C2H6)
- Propan (C3H8)
- Butan (C4H10)
- Pentan (C5H12)
- Heksan (C6H14)
- Heptan (C7H16)
- Oktan (C8H18)
- Nonan (C9H20)
- Dekan (C10H22)
Właściwości fizyczne:
- Gęstość mniejsza od wody
- Niepolarność molekuł
- Nierozpuszczalność w wodzie
Właściwości chemiczne:
- Palność
- Tworzenie mieszanin wybuchowych z powietrzem (dla gazowych alkanów)
- Relatywna obojętność chemiczna w normalnych warunkach
Ważna reakcja: Podstawianie (substytucja) polega na zastąpieniu atomu wodoru w cząsteczce alkanu innym atomem lub grupą atomów. Przykładem jest reakcja: CH4 + Cl2 → CH3Cl + HCl, w wyniku której powstaje chlorometan.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Izomeria i alkeny - reakcje chemiczne
Izomeria strukturalna
Izomeria to zjawisko, które pozwala istnieć kilku różnym związkom o tym samym wzorze sumarycznym:
- Izomery mają taki sam skład pierwiastkowy, ale różną strukturę
- Przykład: butan i metylopropan (C4H10)
- butan: CH3-CH2-CH2-CH3 (łańcuch prosty)
- metylopropan: CH3-CH(CH3)-CH3 (łańcuch rozgałęziony)
Charakterystyka alkenów
Alkeny (CnH2n) posiadają:
- Co najmniej jedno wiązanie podwójne C=C
- Wysoką reaktywność chemiczną
- Szereg homologiczny: eten, propen, buten, penten, heksen, hepten, okten, nonen, deken
Właściwości fizyczne w zależności od długości łańcucha:
- Gazy: C2-C4
- Ciecze: C5-C10
- Ciała stałe: C11-C20
- Zależność: im dłuższy łańcuch węglowy, tym wyższa temperatura wrzenia i topnienia
Właściwości sensoryczne:
- Bezbarwne (formy gazowe i ciekłe)
- Lekko słodki smak
- Przyjemny zapach
Ważna reakcja: Addycja (przyłączenie) to charakterystyczna reakcja alkenów, w której następuje rozerwanie wiązania podwójnego i przyłączenie atomów lub grup atomów. Na przykład: H2C=CH2 + H2 → H3C-CH3. Ta reakcja umożliwia przekształcenie etenu w etan poprzez dodanie wodoru do wiązania podwójnego.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Polimeryzacja i właściwości alkinów
Polimeryzacja - kluczowy proces w przemyśle
Polimeryzacja to proces, w którym monomery (małe cząsteczki) łączą się ze sobą, tworząc polimery (duże cząsteczki).
- Równanie reakcji: n CH2=CH2 → n
- Substrat: eten (etylen)
- Produkt: polietylen (szeroko stosowany plastik)
- Proces ten jest podstawą produkcji wielu tworzyw sztucznych
Alkiny i ich charakterystyka
Alkiny to węglowodory nienasycone zawierające wiązanie potrójne między atomami węgla.
- Wzór ogólny: CnH2n-2
- Główni przedstawiciele szeregu homologicznego:
- Etin (acetylen) - C2H2
- Propyn - C3H4
- Butyn - C4H6
- Pentyn - C5H8
- Heksyn - C6H10
Właściwości fizyczne alkinów:
- Niepolarność cząsteczek
- Nierozpuszczalność w wodzie
- Zależność właściwości od długości łańcucha:
- Większa liczba atomów węgla → wyższa temperatura wrzenia
- Większa liczba atomów węgla → wyższa temperatura topnienia
Właściwości chemiczne alkinów:
- Wysoka palność - acetylen wykorzystywany w palnikach
- Etin (acetylen) jest bezwonnym gazem
- Duża reaktywność wiązania potrójnego
Zastosowanie praktyczne: Etin (acetylen) jest szeroko stosowany w spawalnictwie ze względu na wysoką temperaturę spalania (około 3000°C). Palniki acetylenowo-tlenowe umożliwiają spawanie i cięcie metali, co ma ogromne znaczenie w przemyśle.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Węglowodory aromatyczne - benzen i jego pochodne
Benzen i jego charakterystyka
Benzen (C6H6) jest podstawowym przedstawicielem węglowodorów aromatycznych o charakterystycznej budowie pierścieniowej.
- Wzór ogólny węglowodorów aromatycznych: CnH2n-6
- Najważniejsze pochodne benzenu:
- Metylobenzen (toluen) - C7H8
- Etylobenzen - C8H10
- 1,2-dimetylobenzen - C8H10
Struktura benzenu:
- Pierścień sześcioczłonowy z naprzemiennymi wiązaniami pojedynczymi i podwójnymi
- Wysokie stabilizacja rezonansowa (delokalizacja elektronów)
- Płaska struktura molekularna
Właściwości fizyczne benzenu:
- Stan skupienia: ciecz (w temperaturze pokojowej)
- Temperatura topnienia: 5,5°C
- Temperatura wrzenia: 80,1°C
- Wygląd: bezbarwna ciecz
- Gęstość: mniejsza od wody
- Rozpuszczalność: nie rozpuszcza się w wodzie
- Charakter: niepolarny
Właściwości chemiczne benzenu:
- Zapach: charakterystyczny, aromatyczny
- Palność: łatwopalny
- Zagrożenia: silna toksyczność i działanie rakotwórcze
Zagrożenia zdrowotne: Benzen jest niebezpieczną substancją chemiczną o udowodnionym działaniu kancerogennym. Może powodować uszkodzenia szpiku kostnego i zwiększać ryzyko zachorowania na białaczkę. Z tego powodu jego użycie jest ściśle kontrolowane, a w wielu produktach codziennego użytku został zastąpiony bezpieczniejszymi substancjami.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.