Wodorotlenki to związki chemiczne, które tworzą się z metali i... Pokaż więcej
Wodorotlenki, tlenki i wodorki - Proste wzory i reakcje








Wodorotlenki - wzór i otrzymywanie
Wodorotlenki to związki o wzorze ogólnym M(OH)ₓ, gdzie M to metal, a x to jego wartościowość. Każdy wodorotlenek zawiera grupę wodorotlenową OH⁻, która nadaje mu właściwości zasadowe.
Możesz otrzymać wodorotlenki na kilka sposobów. Najłatwiej jest zmieszać aktywne metale (jak sód czy potas) z wodą - wtedy powstanie wodorotlenek i wydziela się wodór: 2Na + 2H₂O → 2NaOH + H₂.
Inny sposób to rozpuszczenie tlenku metalu w wodzie lub reakcja soli metalu z gotową zasadą. Te reakcje są podstawą do produkcji wielu ważnych związków chemicznych.
💡 Pamiętaj: Reakcje metali z wodą mogą być bardzo gwałtowne - zawsze zachowaj ostrożność!

Dysocjacja wodorotlenków
Dysocjacja to proces, w którym wodorotlenki rozpadają się na jony pod wpływem wody. To dlatego roztwory wodorotlenków przewodzą prąd elektryczny!
Proste wodorotlenki jak NaOH rozpadają się od razu: NaOH ⇌ Na⁺ + OH⁻. Jony OH⁻ są odpowiedzialne za zasadowe właściwości roztworu.
Skomplikowane wodorotlenki jak Fe(OH)₃ rozpadają się stopniowo - najpierw odłącza się jeden jon OH⁻, potem kolejny, i tak dalej. Ten proces nazywamy dysocjacją stopniową i dlatego takie roztwory mają słabsze właściwości zasadowe.
💡 Wskazówka: Im więcej jonów OH⁻ powstanie, tym silniejszą zasadą będzie roztwór!

Wodorki - związki metali z wodorem
Wodorki to związki metali z wodorem o wzorze MHₓ. Metale z grup I i II tworzą wodorki jonowe, gdzie występuje anion wodorkowy H⁻ (nazywany też hydrydem).
Ciekawe są wodorki pozostałych metali - mają budowę podobną do metali i często występują w proporcjach niecałkowitych. Bertolidy to właśnie takie związki o składzie niestechiometrycznym, jak PdH₀,₆.
Niemetale z grup 16-17 też tworzą związki z wodorem, ale mają zupełnie inne właściwości. Przykłady to HCl (chlorowodór) czy H₂S (siarkowodór) - to gazy o ostrym zapachu.
💡 Ciekawostka: Wodór w wodorkach metali ma ładunek ujemny H⁻, co jest przeciwieństwem tego, co znasz z kwasów!

Otrzymywanie wodorków i amoniak
Amoniak (NH₃) to jeden z najważniejszych wodorków - w roztworze wodnym tworzy zasadę. Wodorki niemetali otrzymuje się przez bezpośrednie łączenie pierwiastków.
Niektóre reakcje zachodzą samorzutnie , inne wymagają iskry elektrycznej . Chlorowodór gazowy po rozpuszczeniu w wodzie daje kwas chlorowodorowy.
Pamiętaj podstawową zasadę: tlenki niemetali z wodą tworzą kwasy, a tlenki metali z wodą dają wodorotlenki. To pomoże ci przewidzieć produkty wielu reakcji.
💡 Do zapamiętania: Tlenki metali → wodorotlenki (zasady), tlenki niemetali → kwasy!

Tlenki - budowa i właściwości
Tlenki zawierają anion tlenkowy O²⁻ połączony z metalami lub niemetalami. Tlenki metali (jak Na₂O) mają właściwości zasadowe, a tlenki niemetali (jak CO₂) - kwaśne.
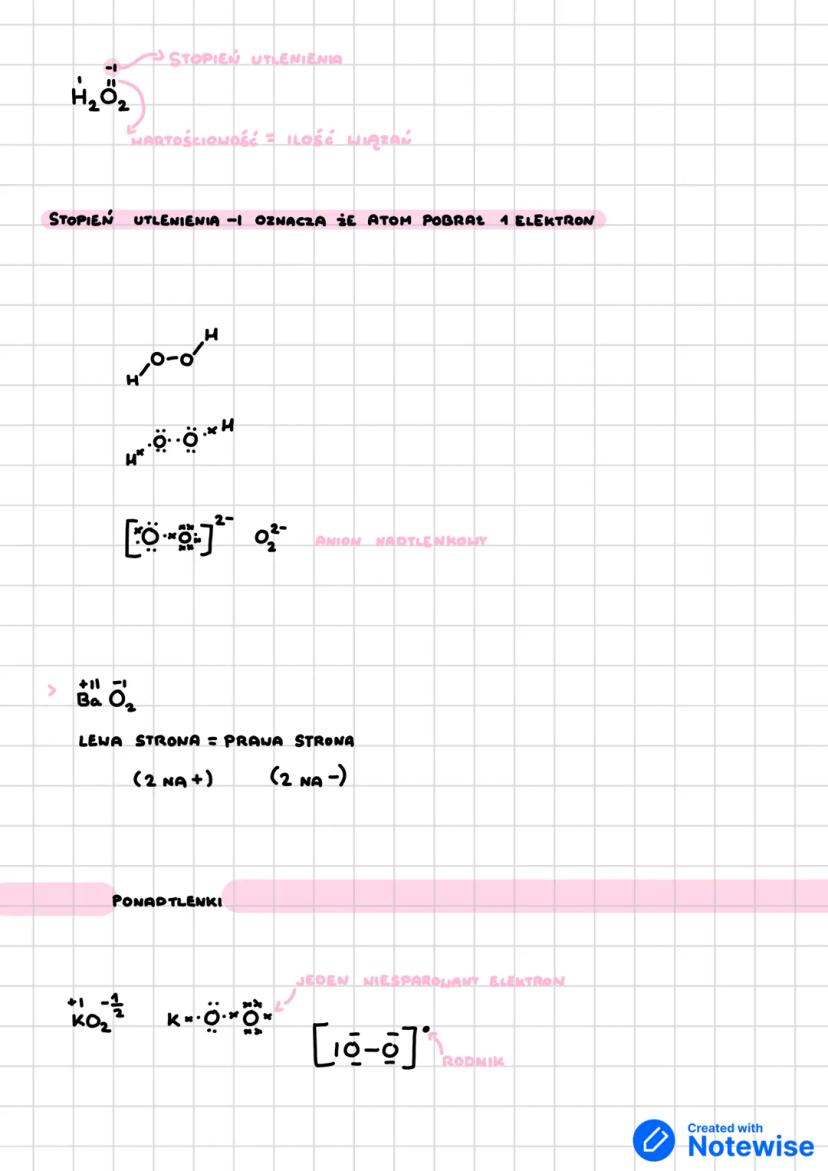
Nadtlenki to specjalna grupa związków tworzona przez litowce, berylowce i wodór. Zawierają grupę O₂²⁻ zamiast pojedynczego anionu tlenkowego.
Najważniejszy nadtlenek to nadtlenek wodoru H₂O₂ - znasz go jako wodę utlenioną. W aptece kupujesz 3% roztwór, ale istnieją też 30% roztwory zwane perhydrolem.
💡 Uwaga: Nadtlenek wodoru to silny utleniacz - używaj go ostrożnie!
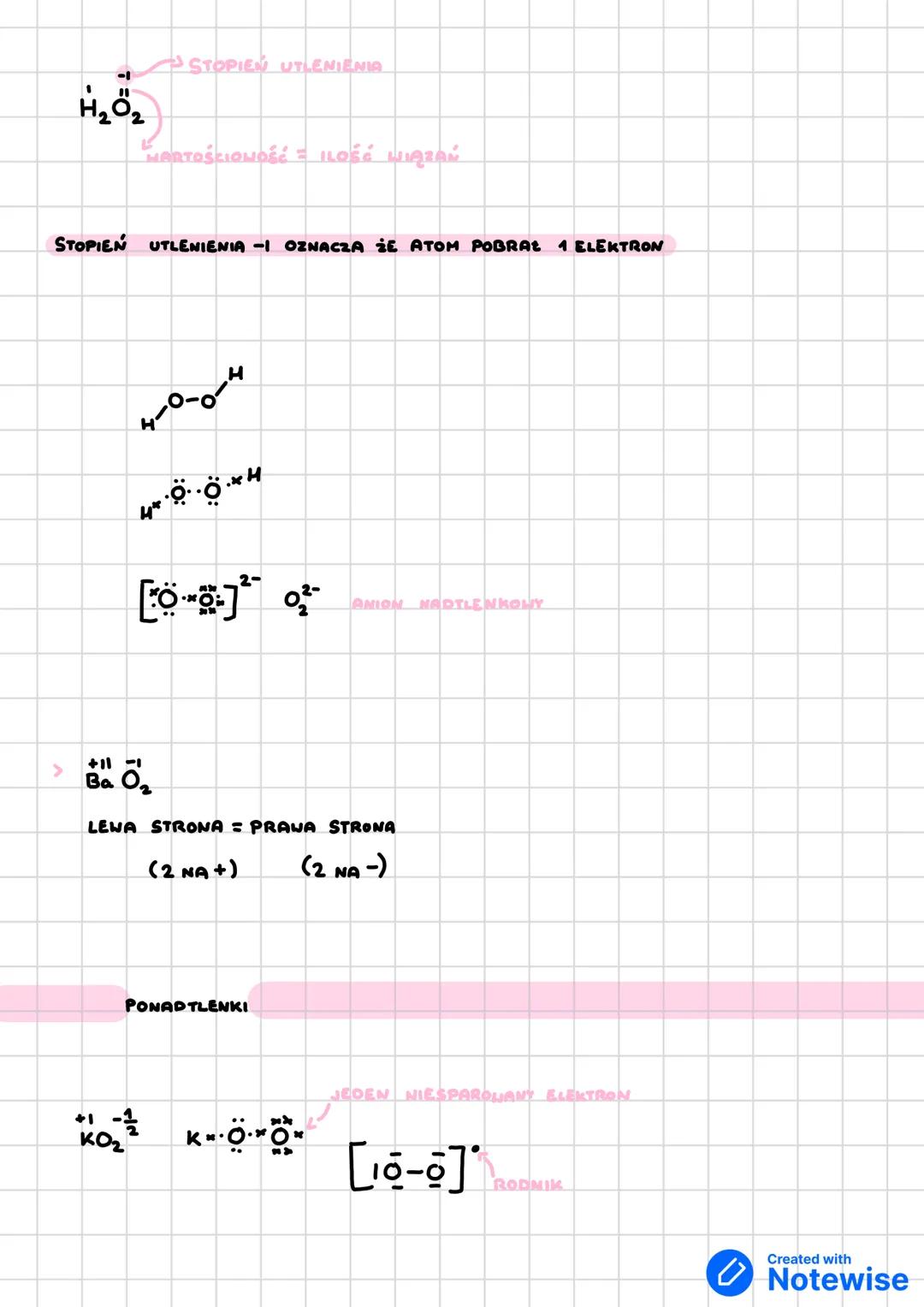
Nadtlenki i ponadtlenki
W nadtlenkach występuje anion nadtlenkowy O₂²⁻, gdzie każdy atom tlenu ma stopień utlenienia -1. To ważne dla zrozumienia właściwości tych związków.
Ponadtlenki (jak KO₂) zawierają jeszcze inną grupę - anion O₂⁻ z jednym niesparowanym elektronem. Taki układ nazywamy rodnikiem i jest bardzo reaktywny.
Stopień utlenienia pokazuje, ile elektronów atom pobiera (liczby ujemne) lub oddaje (liczby dodatnie). W nadtlenkach tlen ma stopień -1, co jest nietypowe, bo zwykle ma -2.
💡 Pamiętaj: Stopień utlenienia ≠ wartościowość! To różne pojęcia, choć czasem mają takie same wartości.

Właściwości i przykłady tlenków
Niektóre tlenki są barwne i mogą zmieniać kolor w zależności od temperatury. Przykład to N₂O₄ (bezbarwny) ⇌ 2NO₂ (brunatny).
Tlenek żelaza Fe₃O₄ to ciekawy przykład - zawiera atomy żelaza o różnych wartościowościach w jednej cząsteczce. Dwa atomy są 3-wartościowe, a jeden 2-wartościowy.
Substancje jonowe (w tym wiele tlenków) mają charakterystyczne właściwości: budowę krystaliczną, wysokie temperatury topnienia i przewodzą prąd po stopieniu. Tlenki metali bloku d są często barwne, co ułatwia ich rozpoznawanie.
💡 Wskazówka: Kolor związków metali przejściowych często pomaga w ich identyfikacji!

Otrzymywanie tlenków
Tlenki możesz otrzymać na trzy główne sposoby. Najprostszy to bezpośrednie łączenie pierwiastka z tlenem: C + O₂ → CO₂.
Drugi sposób to utlenianie tlenków niższych do wyższych. Przykład: 2CO + O₂ → 2CO₂ - tlenek węgla(II) utlenia się do tlenku węgla(IV).
Trzeci metoda to termiczny rozkład soli i wodorotlenków przy wysokiej temperaturze. CaCO₃ → CaO + CO₂ (rozkład węglanu wapnia) czy Cu(OH)₂ → CuO + H₂O (rozkład wodorotlenku miedzi).
💡 Praktyczne zastosowanie: Te reakcje są podstawą wielu procesów przemysłowych, jak produkcja wapna czy metali!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: tlenki
9Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Tlenki
Chemia poziom rozszerzony
Tlenki: Budowa i Reakcje
Zrozumienie tlenków, ich budowy, nazewnictwa oraz reakcji chemicznych. Obejmuje tlenki amfoteryczne, nadtlenki oraz metody otrzymywania tlenków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Tlenki i Wodorotlenki
Zrozumienie tlenków i wodorotlenków w chemii: definicje, przygotowanie, klasyfikacja oraz przykłady. Dowiedz się o tlenkach amfoterycznych, obojętnych oraz ich właściwościach. Idealne dla uczniów chemii na poziomie podstawowym.
Związki Nieorganiczne: Tlenki i Wodorotlenki
Odkryj kluczowe informacje na temat związków nieorganicznych, w tym tlenków, wodorotlenków i soli. Dowiedz się, jak przygotować tlenki i wodorotlenki, ich budowę oraz nazewnictwo. Idealne dla uczniów chemii, którzy chcą zrozumieć podstawowe reakcje chemiczne i właściwości tych związków.
Wartościowości Pierwiastków
Zrozumienie wartościowości pierwiastków jest kluczowe w chemii. Ten materiał omawia tlenek krzemu, tlenek azotu oraz zasady ustalania wartościowości, w tym metodę 'na krzy'. Dowiedz się, jak określić wartościowość atomów i zastosować te zasady w praktyce. Idealne dla uczniów chemii na każdym poziomie.
Tlenki
Tlenki Chemia rozszerzona klasa 1
Tlenki: Klasyfikacja i Właściwości
Odkryj kluczowe informacje o tlenkach, ich klasyfikacji, reakcjach oraz właściwościach chemicznych. Dowiedz się o tlenkach amfoterycznych, zasadowych i kwasowych, a także o ich zastosowaniach w chemii. Idealne materiały do nauki przed maturą.
Moc i Otrzymywanie Kwasów
Zrozumienie mocy kwasów tlenowych i beztlenowych, ich otrzymywanie oraz reakcje z metalami. Obejmuje metody syntezy, hybrydyzację, kształt cząsteczek oraz nazewnictwo związków nieorganicznych. Idealne dla studentów chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Wodorotlenki, tlenki i wodorki - Proste wzory i reakcje
Wodorotlenki to związki chemiczne, które tworzą się z metali i grup OH⁻. To podstawowe substancje zasadowe, które znajdziesz w wielu reakcjach chemicznych i są kluczowe do zrozumienia właściwości zasad.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wodorotlenki - wzór i otrzymywanie
Wodorotlenki to związki o wzorze ogólnym M(OH)ₓ, gdzie M to metal, a x to jego wartościowość. Każdy wodorotlenek zawiera grupę wodorotlenową OH⁻, która nadaje mu właściwości zasadowe.
Możesz otrzymać wodorotlenki na kilka sposobów. Najłatwiej jest zmieszać aktywne metale (jak sód czy potas) z wodą - wtedy powstanie wodorotlenek i wydziela się wodór: 2Na + 2H₂O → 2NaOH + H₂.
Inny sposób to rozpuszczenie tlenku metalu w wodzie lub reakcja soli metalu z gotową zasadą. Te reakcje są podstawą do produkcji wielu ważnych związków chemicznych.
💡 Pamiętaj: Reakcje metali z wodą mogą być bardzo gwałtowne - zawsze zachowaj ostrożność!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Dysocjacja wodorotlenków
Dysocjacja to proces, w którym wodorotlenki rozpadają się na jony pod wpływem wody. To dlatego roztwory wodorotlenków przewodzą prąd elektryczny!
Proste wodorotlenki jak NaOH rozpadają się od razu: NaOH ⇌ Na⁺ + OH⁻. Jony OH⁻ są odpowiedzialne za zasadowe właściwości roztworu.
Skomplikowane wodorotlenki jak Fe(OH)₃ rozpadają się stopniowo - najpierw odłącza się jeden jon OH⁻, potem kolejny, i tak dalej. Ten proces nazywamy dysocjacją stopniową i dlatego takie roztwory mają słabsze właściwości zasadowe.
💡 Wskazówka: Im więcej jonów OH⁻ powstanie, tym silniejszą zasadą będzie roztwór!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wodorki - związki metali z wodorem
Wodorki to związki metali z wodorem o wzorze MHₓ. Metale z grup I i II tworzą wodorki jonowe, gdzie występuje anion wodorkowy H⁻ (nazywany też hydrydem).
Ciekawe są wodorki pozostałych metali - mają budowę podobną do metali i często występują w proporcjach niecałkowitych. Bertolidy to właśnie takie związki o składzie niestechiometrycznym, jak PdH₀,₆.
Niemetale z grup 16-17 też tworzą związki z wodorem, ale mają zupełnie inne właściwości. Przykłady to HCl (chlorowodór) czy H₂S (siarkowodór) - to gazy o ostrym zapachu.
💡 Ciekawostka: Wodór w wodorkach metali ma ładunek ujemny H⁻, co jest przeciwieństwem tego, co znasz z kwasów!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie wodorków i amoniak
Amoniak (NH₃) to jeden z najważniejszych wodorków - w roztworze wodnym tworzy zasadę. Wodorki niemetali otrzymuje się przez bezpośrednie łączenie pierwiastków.
Niektóre reakcje zachodzą samorzutnie , inne wymagają iskry elektrycznej . Chlorowodór gazowy po rozpuszczeniu w wodzie daje kwas chlorowodorowy.
Pamiętaj podstawową zasadę: tlenki niemetali z wodą tworzą kwasy, a tlenki metali z wodą dają wodorotlenki. To pomoże ci przewidzieć produkty wielu reakcji.
💡 Do zapamiętania: Tlenki metali → wodorotlenki (zasady), tlenki niemetali → kwasy!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Tlenki - budowa i właściwości
Tlenki zawierają anion tlenkowy O²⁻ połączony z metalami lub niemetalami. Tlenki metali (jak Na₂O) mają właściwości zasadowe, a tlenki niemetali (jak CO₂) - kwaśne.
Nadtlenki to specjalna grupa związków tworzona przez litowce, berylowce i wodór. Zawierają grupę O₂²⁻ zamiast pojedynczego anionu tlenkowego.
Najważniejszy nadtlenek to nadtlenek wodoru H₂O₂ - znasz go jako wodę utlenioną. W aptece kupujesz 3% roztwór, ale istnieją też 30% roztwory zwane perhydrolem.
💡 Uwaga: Nadtlenek wodoru to silny utleniacz - używaj go ostrożnie!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nadtlenki i ponadtlenki
W nadtlenkach występuje anion nadtlenkowy O₂²⁻, gdzie każdy atom tlenu ma stopień utlenienia -1. To ważne dla zrozumienia właściwości tych związków.
Ponadtlenki (jak KO₂) zawierają jeszcze inną grupę - anion O₂⁻ z jednym niesparowanym elektronem. Taki układ nazywamy rodnikiem i jest bardzo reaktywny.
Stopień utlenienia pokazuje, ile elektronów atom pobiera (liczby ujemne) lub oddaje (liczby dodatnie). W nadtlenkach tlen ma stopień -1, co jest nietypowe, bo zwykle ma -2.
💡 Pamiętaj: Stopień utlenienia ≠ wartościowość! To różne pojęcia, choć czasem mają takie same wartości.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości i przykłady tlenków
Niektóre tlenki są barwne i mogą zmieniać kolor w zależności od temperatury. Przykład to N₂O₄ (bezbarwny) ⇌ 2NO₂ (brunatny).
Tlenek żelaza Fe₃O₄ to ciekawy przykład - zawiera atomy żelaza o różnych wartościowościach w jednej cząsteczce. Dwa atomy są 3-wartościowe, a jeden 2-wartościowy.
Substancje jonowe (w tym wiele tlenków) mają charakterystyczne właściwości: budowę krystaliczną, wysokie temperatury topnienia i przewodzą prąd po stopieniu. Tlenki metali bloku d są często barwne, co ułatwia ich rozpoznawanie.
💡 Wskazówka: Kolor związków metali przejściowych często pomaga w ich identyfikacji!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie tlenków
Tlenki możesz otrzymać na trzy główne sposoby. Najprostszy to bezpośrednie łączenie pierwiastka z tlenem: C + O₂ → CO₂.
Drugi sposób to utlenianie tlenków niższych do wyższych. Przykład: 2CO + O₂ → 2CO₂ - tlenek węgla(II) utlenia się do tlenku węgla(IV).
Trzeci metoda to termiczny rozkład soli i wodorotlenków przy wysokiej temperaturze. CaCO₃ → CaO + CO₂ (rozkład węglanu wapnia) czy Cu(OH)₂ → CuO + H₂O (rozkład wodorotlenku miedzi).
💡 Praktyczne zastosowanie: Te reakcje są podstawą wielu procesów przemysłowych, jak produkcja wapna czy metali!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: tlenki
9Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Tlenki
Chemia poziom rozszerzony
Tlenki: Budowa i Reakcje
Zrozumienie tlenków, ich budowy, nazewnictwa oraz reakcji chemicznych. Obejmuje tlenki amfoteryczne, nadtlenki oraz metody otrzymywania tlenków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Tlenki i Wodorotlenki
Zrozumienie tlenków i wodorotlenków w chemii: definicje, przygotowanie, klasyfikacja oraz przykłady. Dowiedz się o tlenkach amfoterycznych, obojętnych oraz ich właściwościach. Idealne dla uczniów chemii na poziomie podstawowym.
Związki Nieorganiczne: Tlenki i Wodorotlenki
Odkryj kluczowe informacje na temat związków nieorganicznych, w tym tlenków, wodorotlenków i soli. Dowiedz się, jak przygotować tlenki i wodorotlenki, ich budowę oraz nazewnictwo. Idealne dla uczniów chemii, którzy chcą zrozumieć podstawowe reakcje chemiczne i właściwości tych związków.
Wartościowości Pierwiastków
Zrozumienie wartościowości pierwiastków jest kluczowe w chemii. Ten materiał omawia tlenek krzemu, tlenek azotu oraz zasady ustalania wartościowości, w tym metodę 'na krzy'. Dowiedz się, jak określić wartościowość atomów i zastosować te zasady w praktyce. Idealne dla uczniów chemii na każdym poziomie.
Tlenki
Tlenki Chemia rozszerzona klasa 1
Tlenki: Klasyfikacja i Właściwości
Odkryj kluczowe informacje o tlenkach, ich klasyfikacji, reakcjach oraz właściwościach chemicznych. Dowiedz się o tlenkach amfoterycznych, zasadowych i kwasowych, a także o ich zastosowaniach w chemii. Idealne materiały do nauki przed maturą.
Moc i Otrzymywanie Kwasów
Zrozumienie mocy kwasów tlenowych i beztlenowych, ich otrzymywanie oraz reakcje z metalami. Obejmuje metody syntezy, hybrydyzację, kształt cząsteczek oraz nazewnictwo związków nieorganicznych. Idealne dla studentów chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.