Stechiometriato dział chemii, który zajmuje się obliczaniem ilości substancji... Pokaż więcej
Stechiometria: Praktyczne Zadania i Wskazówki





Stechiometria - podstawy
Stechiometria to twój klucz do rozwiązywania problemów chemicznych z liczbami. Wyobraź sobie, że to jak przepis kulinarny - musisz wiedzieć, ile składników potrzebujesz, żeby otrzymać odpowiednią ilość produktu.
W stechiometrii zawsze pracujesz z molami jako podstawową jednostką. Jeden mol to zawsze 6,02 × 10²³ cząsteczek (liczba Avogadra). To może wydawać się abstrakcyjne, ale to po prostu sposób na liczenie bardzo małych obiektów!
💡 Pamiętaj: 1 mol każdego gazu w warunkach normalnych zajmuje objętość 22,4 dm³
Najważniejsze wzory, które musisz znać to: n = m/M oraz pV = nRT dla gazów w różnych warunkach.

Podstawowe obliczenia stechiometryczne
Zacznijmy od prostych zadań, które pokażą ci, jak stechiometria działa w praktyce. Obliczanie liczby cząsteczek to świetny start - po prostu mnożysz liczbę moli przez liczbę Avogadra.
Gdy masz 0,35 mol azotu, to znaczy, że masz 0,35 × 6,02 × 10²³ = 2,107 × 10²³ cząsteczek N₂. Proste, prawda?
Obliczanie masy z liczby moli to kolejny podstawowy skill. Jeśli masz 0,45 mol miedzi, to masa wynosi: 0,45 mol × 64 g/mol = 28,8 g Cu. Wystarczy pomnożyć przez masę molową!
💡 Wskazówka: Zawsze sprawdzaj jednostki - to najłatwiejszy sposób na uniknięcie błędów w obliczeniach.
Dla objętości gazów w warunkach normalnych pamiętaj o magicznej liczbie 22,4 dm³/mol. Dla 2,5 mmol NH₃ objętość to po prostu 2,5 × 22,4 cm³ = 56 cm³.

Zaawansowane obliczenia i skład procentowy
Kiedy gaz nie jest w warunkach normalnych, używasz równania pV = nRT. Dla 12 dm³ CO₂ przy 1000 hPa i 25°C: n = (1000 × 12)/(83,1 × 298) ≈ 0,48 mol.
Skład procentowy to ważna umiejętność - musisz znać masę molową całego związku i masę interesującego cię pierwiastka. W Na₂S₂O₃ masa molowa to 158 g/mol, a siarki 64 g/mol.
Procent siarki = (64/158) × 100% ≈ 40,5%. To znaczy, że prawie połowę masy tego związku stanowi siarka!
💡 Pamiętaj: Przy przeliczaniu temperatur zawsze dodawaj 273 do stopni Celsjusza, żeby otrzymać Kelviny.
Te obliczenia wyglądają skomplikowanie, ale to tylko kwestia systematycznego podejścia i zapamiętania kilku wzorów.
Reakcje chemiczne i reagent limitujący
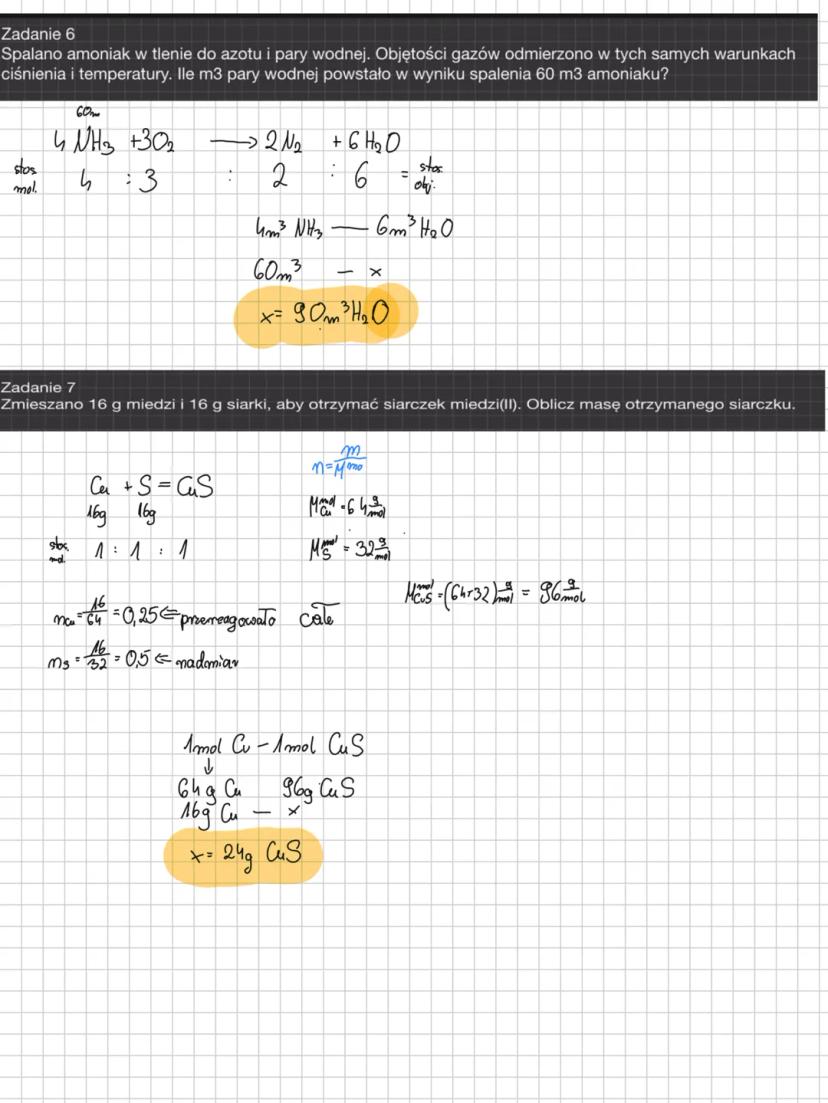
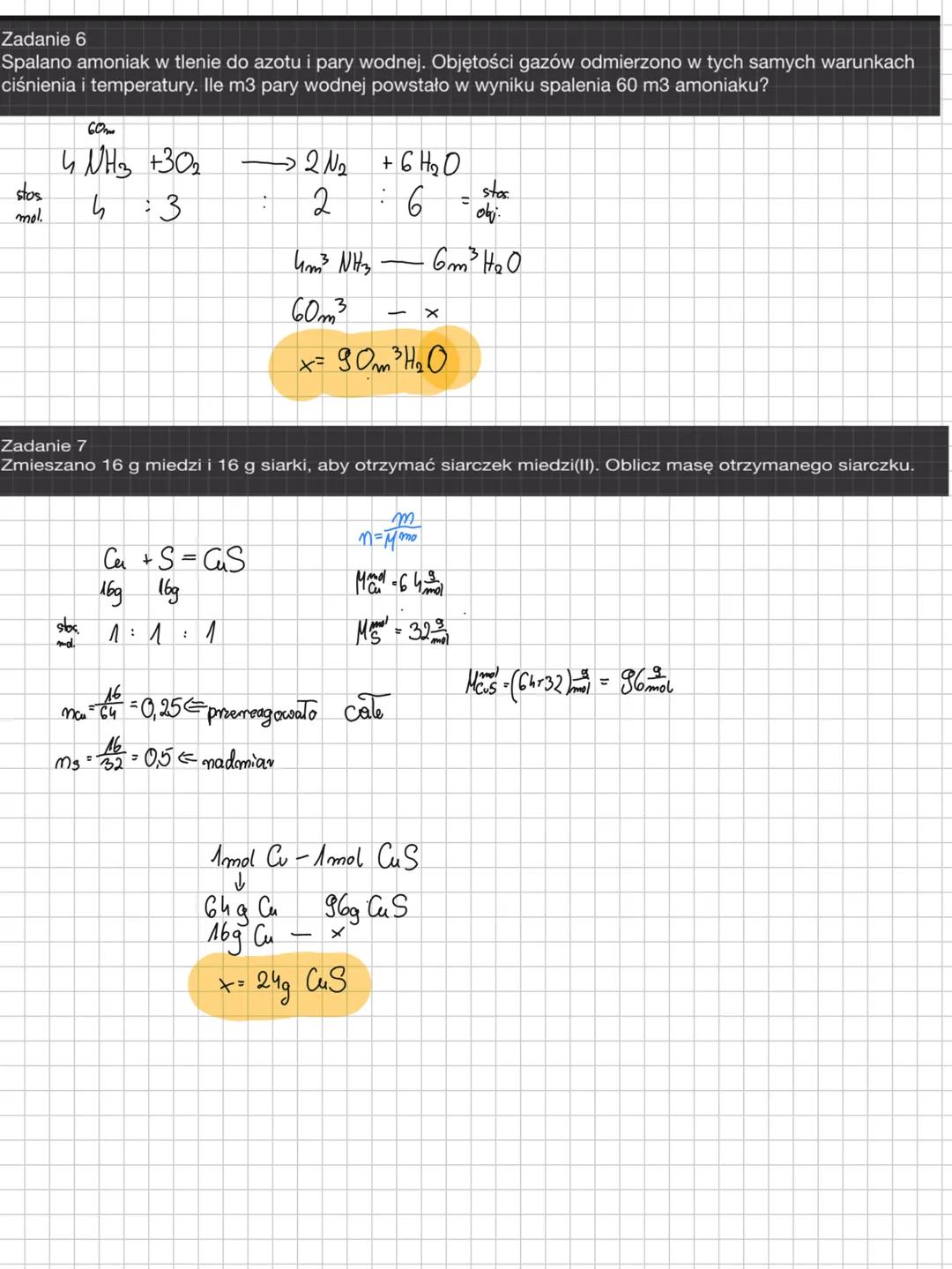
Stechiometria reakcji pokazuje ci, ile produktu możesz otrzymać z danych substratów. W spalaniu amoniaku: 4NH₃ + 3O₂ → 2N₂ + 6H₂O, proporcje molowe to klucz do sukcesu.
Z 60 m³ amoniaku powstanie 90 m³ pary wodnej, bo stosunek 4:6 w równaniu pokazuje, że z amoniaku zawsze powstaje półtora raza więcej wody.
Reagent limitujący to substancja, która kończy się pierwsza. Gdy masz 16 g miedzi (0,25 mol) i 16 g siarki (0,5 mol), to miedź się skończy pierwsza w reakcji Cu + S → CuS.
💡 Wskazówka: Zawsze sprawdzaj, który reagent jest limitujący - to on decyduje o ilości produktu!
Z 0,25 mol miedzi otrzymasz dokładnie 0,25 mol CuS, czyli 24 g siarczku miedzi. Nadmiar siarki po prostu pozostanie niespożyty.

Ćwiczenia praktyczne
Sprawdźmy twoje umiejętności na dodatkowych przykładach! Obliczanie moli z małych mas wymaga uwagi na jednostki - 48 mg tlenu to 1,5 mmol O₂.
Dla objętości gazów w warunkach normalnych zawsze używaj proporcji: 22,4 dm³ = 1 mol. Więc 5,6 dm³ CO₂ to 0,25 mol, czyli 11 g dwutlenku węgla.
Skład procentowy węgla w CaC₂O₄ obliczasz tak samo jak poprzednio. Masa molowa całego związku to 128 g/mol, masa węgla to 24 g/mol (2 × 12).
💡 Sukces: Jeśli potrafisz rozwiązać te zadania, opanowałeś podstawy stechiometrii!
Procent węgla wynosi (24/128) × 100% = 18,75%. Pamiętaj, że praktyka czyni mistrza - im więcej zadań rozwiążesz, tym łatwiejsze staną się te obliczenia.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Biologia
9biologia- ryby klasa 6
Przed odpowiedzią ustnią idealny do powtórki ❤️
Korzeń- organ podziemny rośliny
prawie wszystko w temacie "korzeń- organ podziemny rośliny "
Ekologia
Pojęcia, wykresy i wsztstko czego potrzebujesz😉
Ryby- kręgowce środowisk wodnych
to quiz o rybach z klasy 6
Mitoza i Mejoza
Zrozumienie cyklu komórkowego: szczegółowe omówienie mitozy i mejozy, ich etapów, znaczenia oraz różnic. Dowiedz się, jak te procesy wpływają na wzrost, rozwój i rozmnażanie organizmów. Idealne dla studentów biologii.
Funkcje i Struktura Układu Nerwowego
Zrozumienie funkcji i struktury układu nerwowego, w tym centralnego i obwodowego układu nerwowego, rodzajów neuronów oraz mechanizmów synaptycznych. Materiał obejmuje również odruchy, regulację autonomiczną oraz rolę neuroprzekaźników. Idealne dla uczniów biologii i studentów medycyny.
Wirusy, bakterie, protisty i grzyby - quiz
Puls życia - Dział III - quiz
Budowa i funkcje układu wydalniczego
Poznaj narządy tworzące układ wydalniczy, takie jak nerki i pęcherz moczowy, oraz dowiedz się, jaką rolę pełnią w organizmie.
Płazy
Biologia klasa 6
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Stechiometria: Praktyczne Zadania i Wskazówki
Stechiometria to dział chemii, który zajmuje się obliczaniem ilości substancji w reakcjach chemicznych. Dzięki niej możesz łatwo wyliczyć, ile produktu powstanie z określonej ilości reagentów lub jakie masy potrzebujesz do przeprowadzenia reakcji.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Stechiometria - podstawy
Stechiometria to twój klucz do rozwiązywania problemów chemicznych z liczbami. Wyobraź sobie, że to jak przepis kulinarny - musisz wiedzieć, ile składników potrzebujesz, żeby otrzymać odpowiednią ilość produktu.
W stechiometrii zawsze pracujesz z molami jako podstawową jednostką. Jeden mol to zawsze 6,02 × 10²³ cząsteczek (liczba Avogadra). To może wydawać się abstrakcyjne, ale to po prostu sposób na liczenie bardzo małych obiektów!
💡 Pamiętaj: 1 mol każdego gazu w warunkach normalnych zajmuje objętość 22,4 dm³
Najważniejsze wzory, które musisz znać to: n = m/M oraz pV = nRT dla gazów w różnych warunkach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Podstawowe obliczenia stechiometryczne
Zacznijmy od prostych zadań, które pokażą ci, jak stechiometria działa w praktyce. Obliczanie liczby cząsteczek to świetny start - po prostu mnożysz liczbę moli przez liczbę Avogadra.
Gdy masz 0,35 mol azotu, to znaczy, że masz 0,35 × 6,02 × 10²³ = 2,107 × 10²³ cząsteczek N₂. Proste, prawda?
Obliczanie masy z liczby moli to kolejny podstawowy skill. Jeśli masz 0,45 mol miedzi, to masa wynosi: 0,45 mol × 64 g/mol = 28,8 g Cu. Wystarczy pomnożyć przez masę molową!
💡 Wskazówka: Zawsze sprawdzaj jednostki - to najłatwiejszy sposób na uniknięcie błędów w obliczeniach.
Dla objętości gazów w warunkach normalnych pamiętaj o magicznej liczbie 22,4 dm³/mol. Dla 2,5 mmol NH₃ objętość to po prostu 2,5 × 22,4 cm³ = 56 cm³.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zaawansowane obliczenia i skład procentowy
Kiedy gaz nie jest w warunkach normalnych, używasz równania pV = nRT. Dla 12 dm³ CO₂ przy 1000 hPa i 25°C: n = (1000 × 12)/(83,1 × 298) ≈ 0,48 mol.
Skład procentowy to ważna umiejętność - musisz znać masę molową całego związku i masę interesującego cię pierwiastka. W Na₂S₂O₃ masa molowa to 158 g/mol, a siarki 64 g/mol.
Procent siarki = (64/158) × 100% ≈ 40,5%. To znaczy, że prawie połowę masy tego związku stanowi siarka!
💡 Pamiętaj: Przy przeliczaniu temperatur zawsze dodawaj 273 do stopni Celsjusza, żeby otrzymać Kelviny.
Te obliczenia wyglądają skomplikowanie, ale to tylko kwestia systematycznego podejścia i zapamiętania kilku wzorów.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje chemiczne i reagent limitujący
Stechiometria reakcji pokazuje ci, ile produktu możesz otrzymać z danych substratów. W spalaniu amoniaku: 4NH₃ + 3O₂ → 2N₂ + 6H₂O, proporcje molowe to klucz do sukcesu.
Z 60 m³ amoniaku powstanie 90 m³ pary wodnej, bo stosunek 4:6 w równaniu pokazuje, że z amoniaku zawsze powstaje półtora raza więcej wody.
Reagent limitujący to substancja, która kończy się pierwsza. Gdy masz 16 g miedzi (0,25 mol) i 16 g siarki (0,5 mol), to miedź się skończy pierwsza w reakcji Cu + S → CuS.
💡 Wskazówka: Zawsze sprawdzaj, który reagent jest limitujący - to on decyduje o ilości produktu!
Z 0,25 mol miedzi otrzymasz dokładnie 0,25 mol CuS, czyli 24 g siarczku miedzi. Nadmiar siarki po prostu pozostanie niespożyty.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Ćwiczenia praktyczne
Sprawdźmy twoje umiejętności na dodatkowych przykładach! Obliczanie moli z małych mas wymaga uwagi na jednostki - 48 mg tlenu to 1,5 mmol O₂.
Dla objętości gazów w warunkach normalnych zawsze używaj proporcji: 22,4 dm³ = 1 mol. Więc 5,6 dm³ CO₂ to 0,25 mol, czyli 11 g dwutlenku węgla.
Skład procentowy węgla w CaC₂O₄ obliczasz tak samo jak poprzednio. Masa molowa całego związku to 128 g/mol, masa węgla to 24 g/mol (2 × 12).
💡 Sukces: Jeśli potrafisz rozwiązać te zadania, opanowałeś podstawy stechiometrii!
Procent węgla wynosi (24/128) × 100% = 18,75%. Pamiętaj, że praktyka czyni mistrza - im więcej zadań rozwiążesz, tym łatwiejsze staną się te obliczenia.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Biologia
9biologia- ryby klasa 6
Przed odpowiedzią ustnią idealny do powtórki ❤️
Korzeń- organ podziemny rośliny
prawie wszystko w temacie "korzeń- organ podziemny rośliny "
Ekologia
Pojęcia, wykresy i wsztstko czego potrzebujesz😉
Ryby- kręgowce środowisk wodnych
to quiz o rybach z klasy 6
Mitoza i Mejoza
Zrozumienie cyklu komórkowego: szczegółowe omówienie mitozy i mejozy, ich etapów, znaczenia oraz różnic. Dowiedz się, jak te procesy wpływają na wzrost, rozwój i rozmnażanie organizmów. Idealne dla studentów biologii.
Funkcje i Struktura Układu Nerwowego
Zrozumienie funkcji i struktury układu nerwowego, w tym centralnego i obwodowego układu nerwowego, rodzajów neuronów oraz mechanizmów synaptycznych. Materiał obejmuje również odruchy, regulację autonomiczną oraz rolę neuroprzekaźników. Idealne dla uczniów biologii i studentów medycyny.
Wirusy, bakterie, protisty i grzyby - quiz
Puls życia - Dział III - quiz
Budowa i funkcje układu wydalniczego
Poznaj narządy tworzące układ wydalniczy, takie jak nerki i pęcherz moczowy, oraz dowiedz się, jaką rolę pełnią w organizmie.
Płazy
Biologia klasa 6
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.