Alkohol to związek organiczny o istotnym znaczeniu w chemii. Poznanie... Pokaż więcej
Alkohole w Chemii - Notatka dla Uczniów





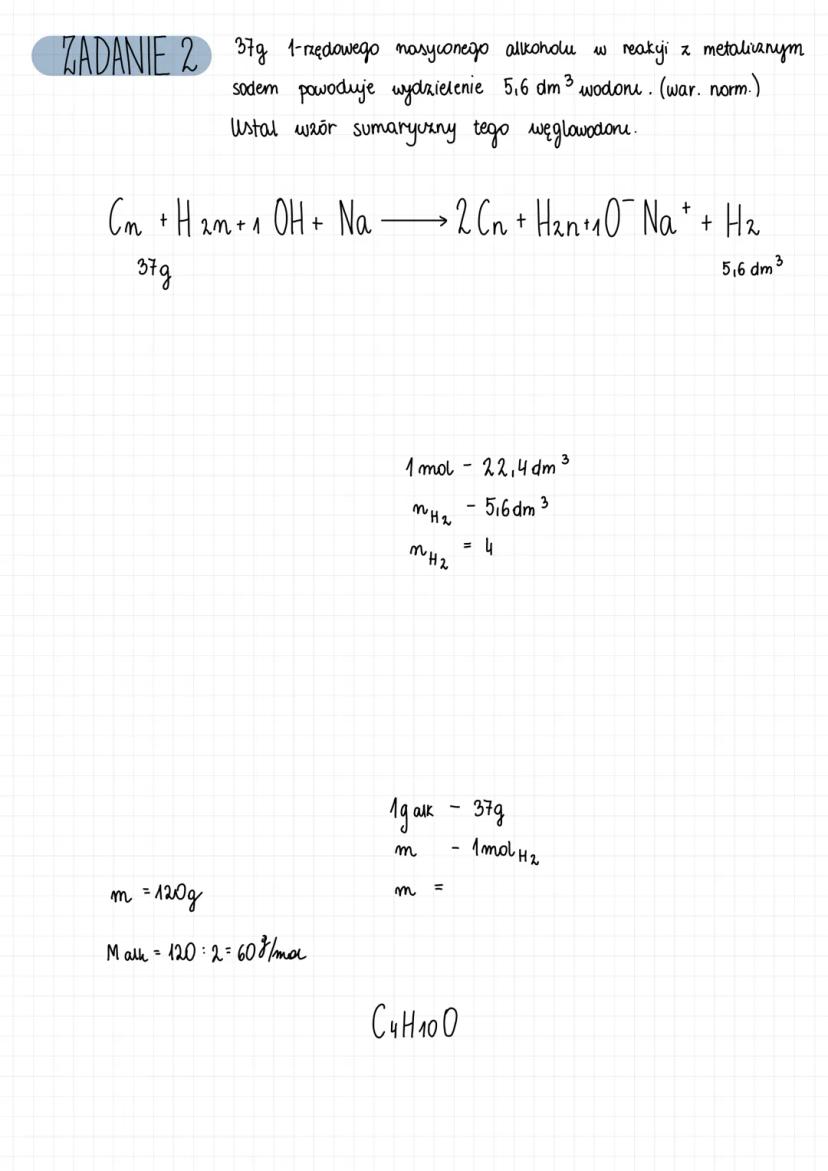


Alkohol - wprowadzenie
Alkohol to związek chemiczny zawierający grupę hydroksylową przyłączoną do węglowodoru. Ta grupa funkcyjna nadaje alkoholom ich charakterystyczne właściwości.
Najprostszym alkoholem jest metanol , a najbardziej znanym - etanol , czyli alkohol spożywczy. Zrozumienie ich budowy pomoże ci w rozwiązywaniu zadań z chemii organicznej.
💡 Ciekawostka: Grupa hydroksylowa jest kluczowa dla właściwości alkoholi - dzięki niej mogą tworzyć wiązania wodorowe, co wpływa na ich temperaturę wrzenia i rozpuszczalność!

Właściwości alkoholi
Alkohole mają wysoką temperaturę wrzenia w porównaniu do węglowodorów o podobnej masie. Wynika to z tworzenia wiązań wodorowych między cząsteczkami. Te międzycząsteczkowe wiązania są bardzo istotne dla zrozumienia właściwości alkoholi.
Alkohole jak etanol świetnie rozpuszczają się w wodzie. Dzieje się tak, ponieważ zarówno woda, jak i etanol są związkami polarnymi - ich cząsteczki mogą tworzyć wiązania wodorowe między sobą.
Ważnym pojęciem jest rzędowość alkoholu, która zależy od budowy atomu węgla związanego z grupą OH:
- Alkohol I-rzędowy: grupa OH przy węglu połączonym z jednym atomem węgla
- Alkohol II-rzędowy: grupa OH przy węglu połączonym z dwoma atomami węgla
- Alkohol III-rzędowy: grupa OH przy węglu połączonym z trzema atomami węgla
💡 Zapamiętaj: Rzędowość alkoholu wpływa na jego reaktywność w różnych reakcjach chemicznych!

Nazewnictwo alkoholi
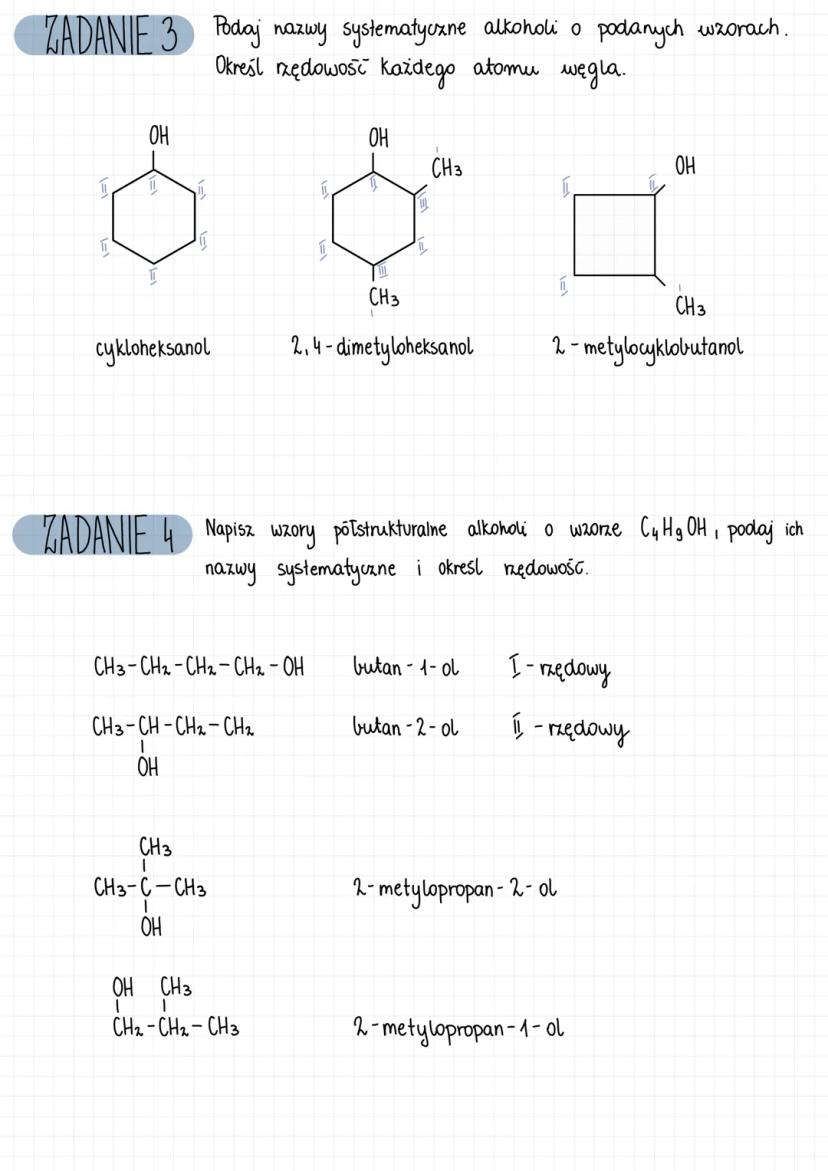
Nazwy systematyczne alkoholi tworzysz według kilku prostych zasad. Zawsze numerujemy łańcuch węglowy od końca bliższego grupie hydroksylowej, a następnie wskazujemy pozycję grupy -OH.
Przykłady alkoholi pierwszorzędowych:
- CH₃-CH₂-CH₂-CH₂-OH → butan-1-ol
- CH₃-CH-CH₂-OH → 2-metylopropan-1-ol | CH₃
Przykłady alkoholi drugorzędowych:
- CH₃-CH-CH₂-CH₃ → butan-2-ol | OH
- CH₃-CH=C-CH-CH₃ → but-3-yn-2-ol | OH
Przykład alkoholu trzeciorzędowego:
- CH₃-C-CH₃ → 2-metylopropan-2-ol | OH
💡 Wskazówka: Zapamiętaj, że przyrostek "-ol" oznacza obecność grupy hydroksylowej, a przedrostek określa liczbę atomów węgla i podstawniki!
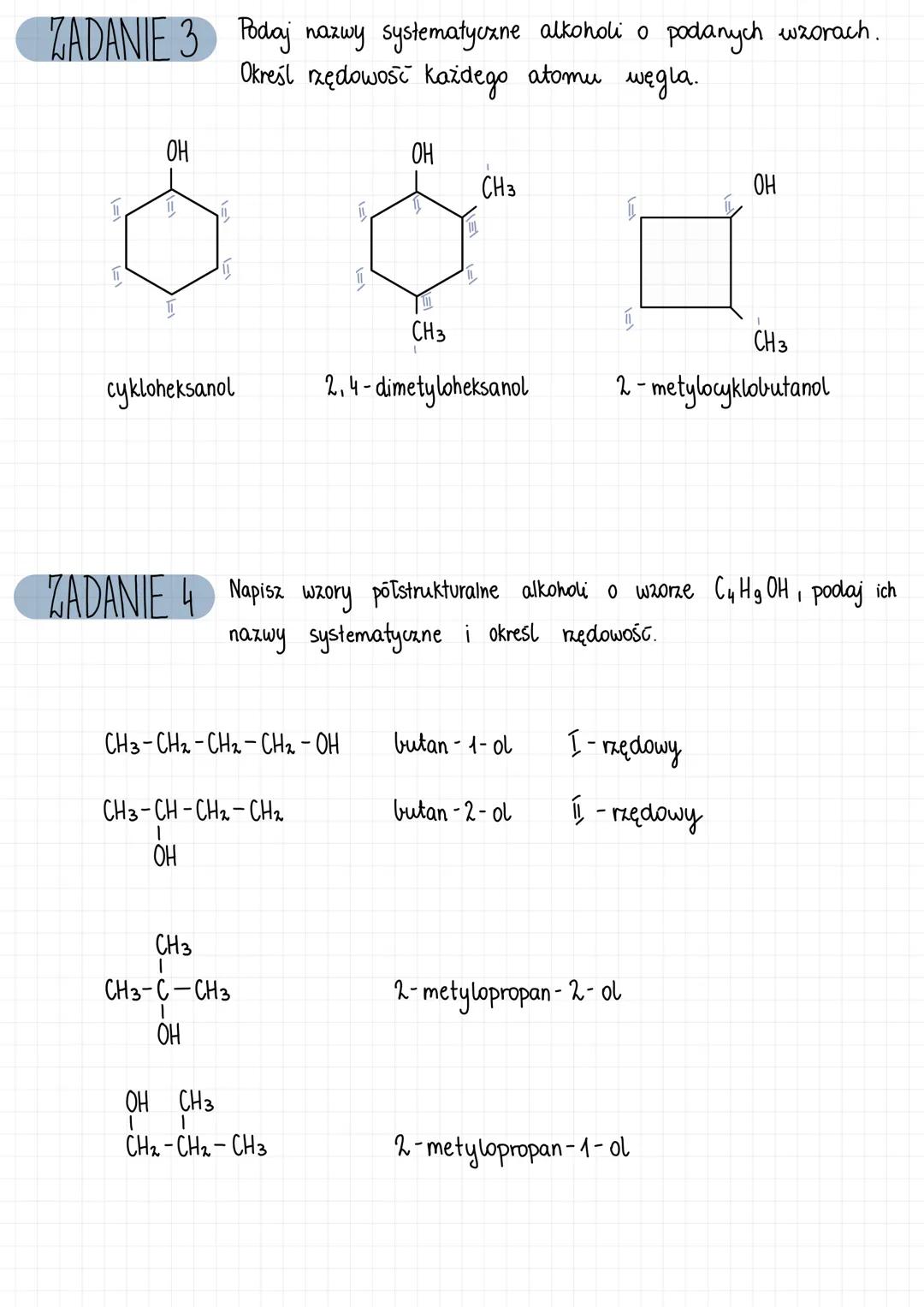
Rzędowość i izomeria alkoholi
Alkohol o tym samym wzorze sumarycznym może występować w różnych postaciach jako izomery. Na przykład, dla wzoru C₄H₁₀O możliwe są następujące izomery:
- CH₃-CH₂-CH₂-CH₂-OH → butan-1-ol
- CH₃-CH-CH₂-CH₃ → butan-2-ol | OH
- CH₃-C-CH₃ → 2-metylopropan-2-ol | OH
- CH₃-CH-CH₂-OH → 2-metylopropan-1-ol | CH₃
Alkohole mogą także tworzyć struktury cykliczne, np. cykloheksanol. W takim przypadku grupa OH jest przyłączona do pierścienia węglowego.
Określenie rzędowości atomu węgla z grupą OH jest kluczowe, gdyż wpływa to na reaktywność alkoholu. Sprawdź, ile grup alkilowych łączy się z węglem noszącym grupę OH.
💡 Pamiętaj: Im wyższa rzędowość alkoholu, tym trudniej zachodzi reakcja utleniania, ale łatwiej dehydratacja (odwodnienie)!

Obliczenia i reakcje alkoholi
Podczas obliczeń związanych z alkoholami często korzystamy z masy molowej i stężeń. Przykładowo, stężenie molowe 96% roztworu etanolu o gęstości 0,8 g/dm³ obliczamy dzieląc iloczyn stężenia procentowego i gęstości przez iloczyn masy molowej i 100%:
Cm = (Cp · d)/(M · 100%) = (96 · 800)/(46 · 100) = 16,7 mol/dm³
Alkohole uczestniczą w wielu ważnych reakcjach, m.in.:
- Dehydratacja - usunięcie wody z alkoholu, np. etanol → eten + woda
- Halogenowanie - zastąpienie grupy OH atomem halogenu
Przykład schematu reakcji: CH₃-CH₃ → CH₃-CH₂-Cl → CH₃-CH₂-OH → CH₂=CH₂ → CH₃-CH₂-Br → CH₃-CH₂-OH
💡 Wskazówka praktyczna: Podczas dehydratacji alkoholi często używa się katalizatorów, takich jak Al₂O₃ czy H₂SO₄, które ułatwiają oderwanie grupy OH!
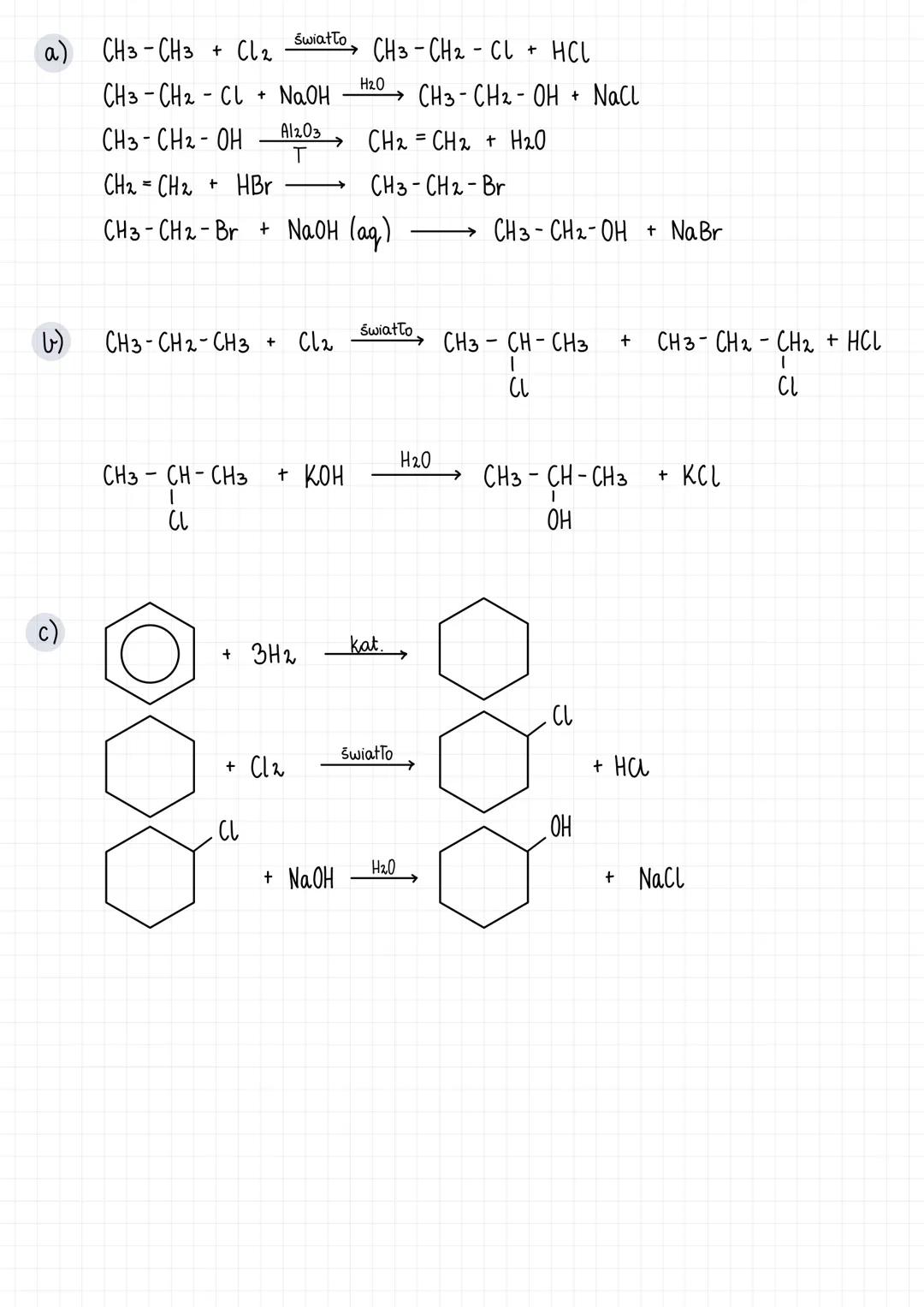
Ważne reakcje alkoholi
Alkohole wchodzą w liczne reakcje, które możesz przedstawić za pomocą równań chemicznych:
-
Chlorowanie alkanów z udziałem światła: CH₃-CH₃ + Cl₂ → CH₃-CH₂-Cl + HCl
-
Hydroliza chloropochodnych: CH₃-CH₂-Cl + NaOH (aq) → CH₃-CH₂-OH + NaCl
-
Dehydratacja alkoholi: CH₃-CH₂-OH → CH₂=CH₂ + H₂O (w obecności Al₂O₃, w podwyższonej temperaturze)
-
Bromowanie alkenu: CH₂=CH₂ + HBr → CH₃-CH₂-Br
Możesz też przekształcać inne związki w alkohole, np.:
- Propan → 2-chloropropan → propan-2-ol
- Benzen → cykloheksan → chlorocykloheksan → cykloheksanol
💡 Zapamiętaj schemat: Alkany można przekształcić w halogenopochodne, które następnie można przekształcić w alkohole poprzez reakcję hydrolizy!
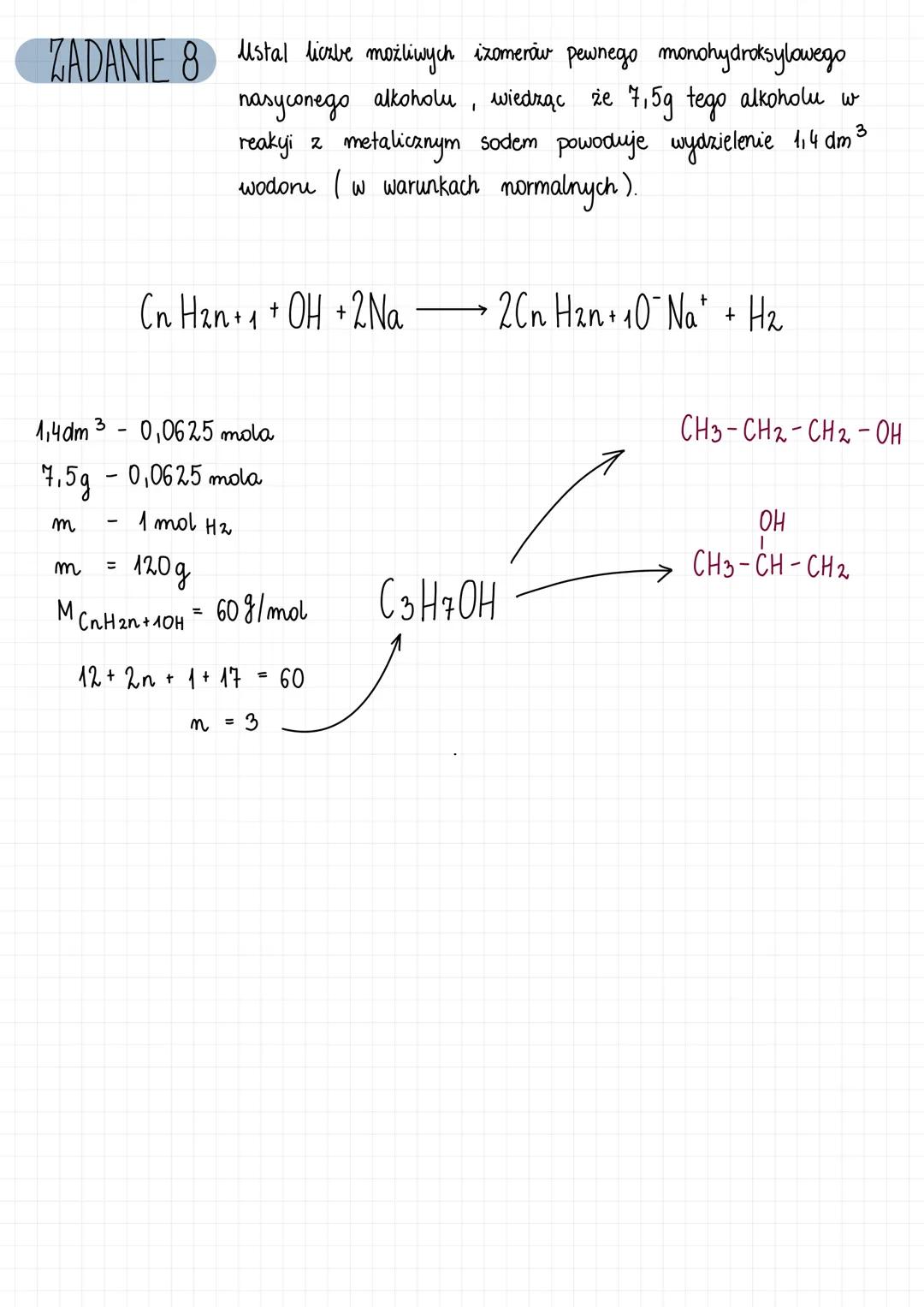
Rozwiązywanie zadań z alkoholami
Przy rozwiązywaniu zadań z alkoholami często musisz określić wzór związku na podstawie danych z reakcji. Spójrz na przykład:
Zadanie: Ustal liczbę możliwych izomerów pewnego monohydroksylowego nasyconego alkoholu, wiedząc że 7,5g tego alkoholu w reakcji z metalicznym sodem powoduje wydzielenie 1,4 dm³ wodoru (w warunkach normalnych).
Rozwiązanie:
- Zapisujemy równanie reakcji: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Z warunków normalnych: 1,4 dm³ H₂ = 0,0625 mola H₂
- Obliczamy masę molową alkoholu: 7,5g / 0,0625 mola = 120g/mol
- Masa molowa alkoholu to 60g/mol (bo z 1 mola alkoholu powstaje 0,5 mola H₂)
- Z równania 12n + 2n + 1 + 17 = 60 → n = 3
- Wzór to C₃H₇OH (propanol) z dwoma izomerami: propan-1-ol i propan-2-ol
💡 Wskazówka: Pamiętaj o przeliczaniu objętości gazu na liczbę moli za pomocą objętości molowej !

Obliczanie wzorów sumarycznych alkoholi
Rozwiązując zadania dotyczące wzoru sumarycznego alkoholu, często korzystamy z danych o reakcji z sodem. Zobaczmy na przykładzie:
Zadanie: W reakcji 1,5g alkoholu monohydroksylowego z sodem wydzieliło się 0,28 dm³ wodoru (warunki normalne). Ustal wzór sumaryczny tego alkoholu.
Rozwiązanie:
- Zapisujemy reakcję: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Obliczamy liczbę moli wodoru: nₕ₂ = 0,28 dm³ / 22,4 dm³/mol = 0,0125 mola
- Liczba moli alkoholu = 2 × liczba moli H₂ = 0,025 mola
- Masa molowa alkoholu = 1,5g / 0,025 mol = 60 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 60 → n = 3
- Zatem wzór sumaryczny to C₃H₈O (lub C₃H₇OH)
Pamiętaj, że wzór sumaryczny daje tylko informację o liczbie poszczególnych atomów, nie o strukturze. Dlatego C₃H₈O może oznaczać zarówno propan-1-ol, jak i propan-2-ol.
💡 Ważne: Podczas reakcji alkoholu z metalem (Na, K) zawsze powstaje połowa mola H₂ na każdy mol alkoholu - to klucz do tych obliczeń!
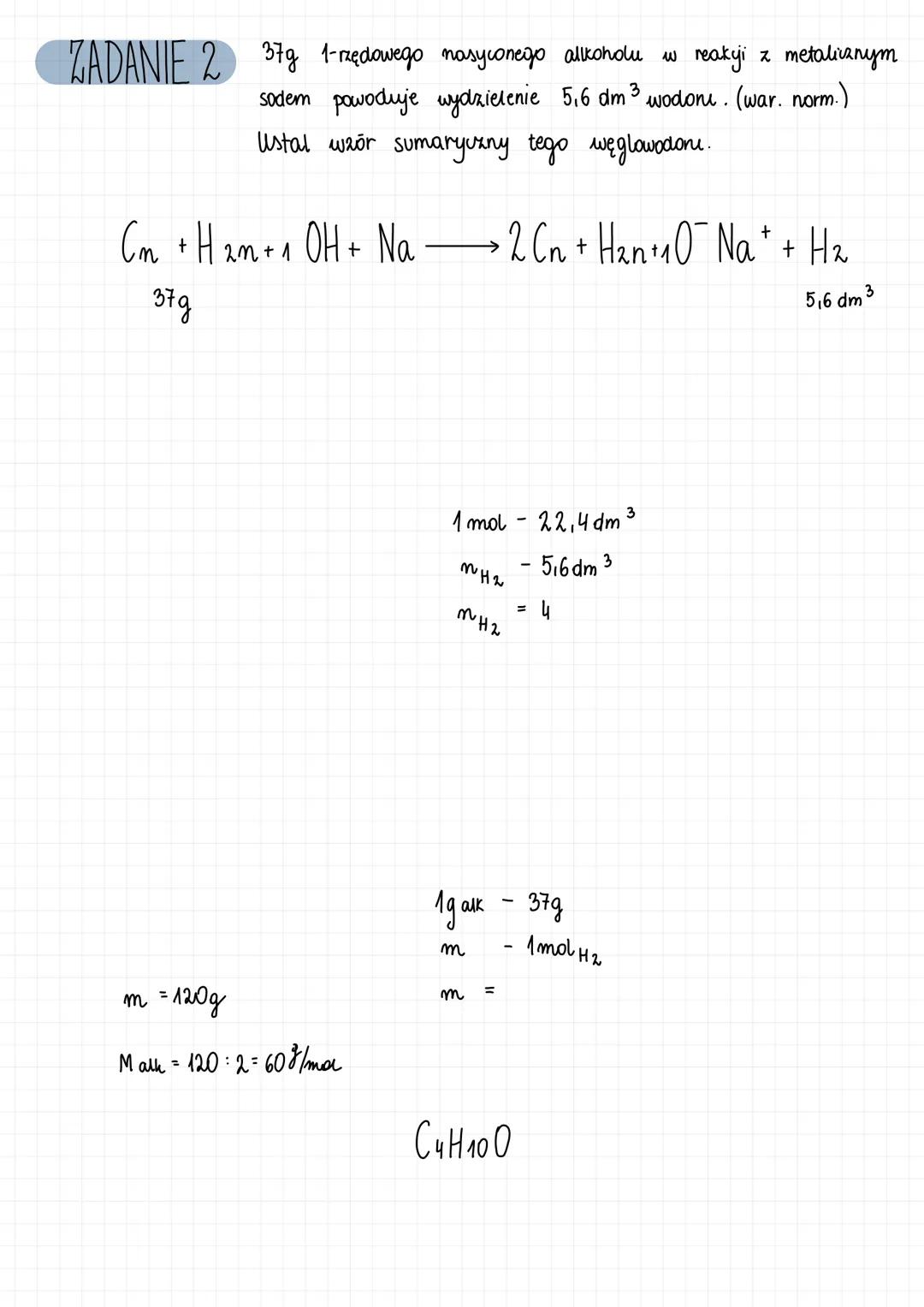
Alkohol pierwszorzędowy w reakcjach
W zadaniach z alkoholami pierwszorzędowymi również stosujemy podobne podejście obliczeniowe:
Zadanie: 37g pierwszorzędowego nasyconego alkoholu w reakcji z metalicznym sodem powoduje wydzielenie 5,6 dm³ wodoru (war. norm.). Ustal wzór sumaryczny tego węglowodoru.
Rozwiązanie:
- Zapisujemy reakcję: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Obliczamy liczbę moli wodoru: nₕ₂ = 5,6 dm³ / 22,4 dm³/mol = 0,25 mola
- Liczba moli alkoholu = 2 × 0,25 mol = 0,5 mola
- Masa molowa alkoholu = 37g / 0,5 mol = 74 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 74 → 14n = 56 → n = 4
- Zatem wzór sumaryczny to C₄H₁₀O (lub C₄H₉OH)
Ponieważ mowa o alkoholu pierwszorzędowym, struktura to CH₃-CH₂-CH₂-CH₂-OH lub CH₃-CH(CH₃)-CH₂-OH .
💡 Wskazówka: Gdy w zadaniu podano, że alkohol jest pierwszorzędowy, sprawdź wszystkie możliwe izomery i wybierz tylko te, które spełniają ten warunek!

Alkohol w reakcji z potasem
Potrafisz też obliczyć wzór alkoholu, gdy znasz liczbę cząsteczek wydzielonego wodoru:
Zadanie: Podaj wzór półstrukturalny nasyconego alkoholu R-OH, który w roztworze wodnym w reakcji 23g tego alkoholu z potasem wypiera 1,5·10²³ cząsteczek wodoru.
Rozwiązanie:
- Zapisujemy reakcję: 2CₙH₂ₙ₊₁OH + 2K → 2CₙH₂ₙ₊₁O⁻K⁺ + H₂
- Przeliczamy liczbę cząsteczek wodoru na mole: nₕ₂ = 1,5·10²³ / 6,02·10²³ = 0,25 mola
- Liczba moli alkoholu = 2 × 0,25 mol = 0,5 mola
- Masa molowa alkoholu = 23g / 0,5 mol = 46 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 46 → 14n = 28 → n = 2
- Zatem wzór półstrukturalny to CH₃-CH₂-OH (etanol)
Etanol to najprostszy alkohol, który spotykamy w życiu codziennym. Jest podstawowym składnikiem napojów alkoholowych, ale także ważnym rozpuszczalnikiem i surowcem w przemyśle.
💡 Ciekawostka: Etanol ma wiele zastosowań - oprócz napojów alkoholowych używa się go jako paliwo, rozpuszczalnik, środek dezynfekujący i surowiec do produkcji wielu związków chemicznych!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Alkohole w Chemii - Notatka dla Uczniów
Alkohol to związek organiczny o istotnym znaczeniu w chemii. Poznanie jego struktury, nazewnictwa i właściwości pomoże ci zrozumieć wiele reakcji chemicznych. Przyjrzyjmy się najważniejszym informacjom, które musisz znać o alkoholach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkohol - wprowadzenie
Alkohol to związek chemiczny zawierający grupę hydroksylową przyłączoną do węglowodoru. Ta grupa funkcyjna nadaje alkoholom ich charakterystyczne właściwości.
Najprostszym alkoholem jest metanol , a najbardziej znanym - etanol , czyli alkohol spożywczy. Zrozumienie ich budowy pomoże ci w rozwiązywaniu zadań z chemii organicznej.
💡 Ciekawostka: Grupa hydroksylowa jest kluczowa dla właściwości alkoholi - dzięki niej mogą tworzyć wiązania wodorowe, co wpływa na ich temperaturę wrzenia i rozpuszczalność!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości alkoholi
Alkohole mają wysoką temperaturę wrzenia w porównaniu do węglowodorów o podobnej masie. Wynika to z tworzenia wiązań wodorowych między cząsteczkami. Te międzycząsteczkowe wiązania są bardzo istotne dla zrozumienia właściwości alkoholi.
Alkohole jak etanol świetnie rozpuszczają się w wodzie. Dzieje się tak, ponieważ zarówno woda, jak i etanol są związkami polarnymi - ich cząsteczki mogą tworzyć wiązania wodorowe między sobą.
Ważnym pojęciem jest rzędowość alkoholu, która zależy od budowy atomu węgla związanego z grupą OH:
- Alkohol I-rzędowy: grupa OH przy węglu połączonym z jednym atomem węgla
- Alkohol II-rzędowy: grupa OH przy węglu połączonym z dwoma atomami węgla
- Alkohol III-rzędowy: grupa OH przy węglu połączonym z trzema atomami węgla
💡 Zapamiętaj: Rzędowość alkoholu wpływa na jego reaktywność w różnych reakcjach chemicznych!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo alkoholi
Nazwy systematyczne alkoholi tworzysz według kilku prostych zasad. Zawsze numerujemy łańcuch węglowy od końca bliższego grupie hydroksylowej, a następnie wskazujemy pozycję grupy -OH.
Przykłady alkoholi pierwszorzędowych:
- CH₃-CH₂-CH₂-CH₂-OH → butan-1-ol
- CH₃-CH-CH₂-OH → 2-metylopropan-1-ol | CH₃
Przykłady alkoholi drugorzędowych:
- CH₃-CH-CH₂-CH₃ → butan-2-ol | OH
- CH₃-CH=C-CH-CH₃ → but-3-yn-2-ol | OH
Przykład alkoholu trzeciorzędowego:
- CH₃-C-CH₃ → 2-metylopropan-2-ol | OH
💡 Wskazówka: Zapamiętaj, że przyrostek "-ol" oznacza obecność grupy hydroksylowej, a przedrostek określa liczbę atomów węgla i podstawniki!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Rzędowość i izomeria alkoholi
Alkohol o tym samym wzorze sumarycznym może występować w różnych postaciach jako izomery. Na przykład, dla wzoru C₄H₁₀O możliwe są następujące izomery:
- CH₃-CH₂-CH₂-CH₂-OH → butan-1-ol
- CH₃-CH-CH₂-CH₃ → butan-2-ol | OH
- CH₃-C-CH₃ → 2-metylopropan-2-ol | OH
- CH₃-CH-CH₂-OH → 2-metylopropan-1-ol | CH₃
Alkohole mogą także tworzyć struktury cykliczne, np. cykloheksanol. W takim przypadku grupa OH jest przyłączona do pierścienia węglowego.
Określenie rzędowości atomu węgla z grupą OH jest kluczowe, gdyż wpływa to na reaktywność alkoholu. Sprawdź, ile grup alkilowych łączy się z węglem noszącym grupę OH.
💡 Pamiętaj: Im wyższa rzędowość alkoholu, tym trudniej zachodzi reakcja utleniania, ale łatwiej dehydratacja (odwodnienie)!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczenia i reakcje alkoholi
Podczas obliczeń związanych z alkoholami często korzystamy z masy molowej i stężeń. Przykładowo, stężenie molowe 96% roztworu etanolu o gęstości 0,8 g/dm³ obliczamy dzieląc iloczyn stężenia procentowego i gęstości przez iloczyn masy molowej i 100%:
Cm = (Cp · d)/(M · 100%) = (96 · 800)/(46 · 100) = 16,7 mol/dm³
Alkohole uczestniczą w wielu ważnych reakcjach, m.in.:
- Dehydratacja - usunięcie wody z alkoholu, np. etanol → eten + woda
- Halogenowanie - zastąpienie grupy OH atomem halogenu
Przykład schematu reakcji: CH₃-CH₃ → CH₃-CH₂-Cl → CH₃-CH₂-OH → CH₂=CH₂ → CH₃-CH₂-Br → CH₃-CH₂-OH
💡 Wskazówka praktyczna: Podczas dehydratacji alkoholi często używa się katalizatorów, takich jak Al₂O₃ czy H₂SO₄, które ułatwiają oderwanie grupy OH!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Ważne reakcje alkoholi
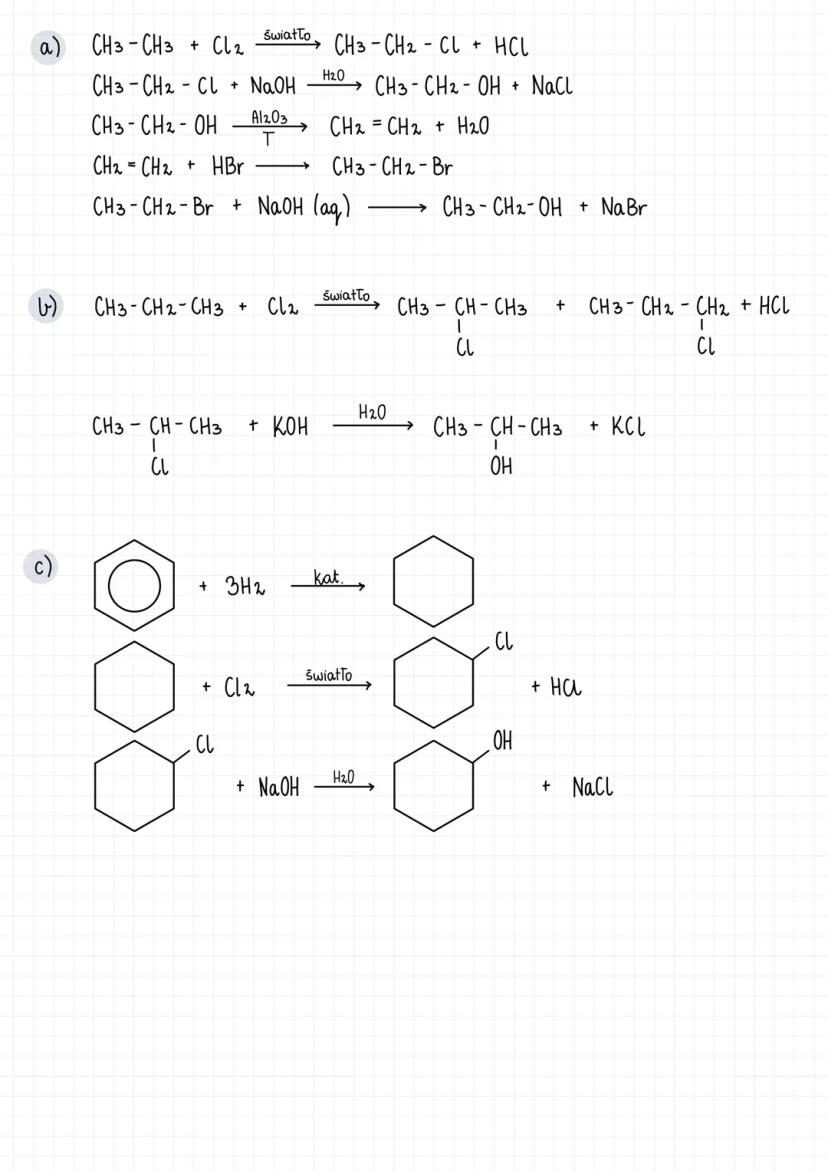
Alkohole wchodzą w liczne reakcje, które możesz przedstawić za pomocą równań chemicznych:
-
Chlorowanie alkanów z udziałem światła: CH₃-CH₃ + Cl₂ → CH₃-CH₂-Cl + HCl
-
Hydroliza chloropochodnych: CH₃-CH₂-Cl + NaOH (aq) → CH₃-CH₂-OH + NaCl
-
Dehydratacja alkoholi: CH₃-CH₂-OH → CH₂=CH₂ + H₂O (w obecności Al₂O₃, w podwyższonej temperaturze)
-
Bromowanie alkenu: CH₂=CH₂ + HBr → CH₃-CH₂-Br
Możesz też przekształcać inne związki w alkohole, np.:
- Propan → 2-chloropropan → propan-2-ol
- Benzen → cykloheksan → chlorocykloheksan → cykloheksanol
💡 Zapamiętaj schemat: Alkany można przekształcić w halogenopochodne, które następnie można przekształcić w alkohole poprzez reakcję hydrolizy!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Rozwiązywanie zadań z alkoholami
Przy rozwiązywaniu zadań z alkoholami często musisz określić wzór związku na podstawie danych z reakcji. Spójrz na przykład:
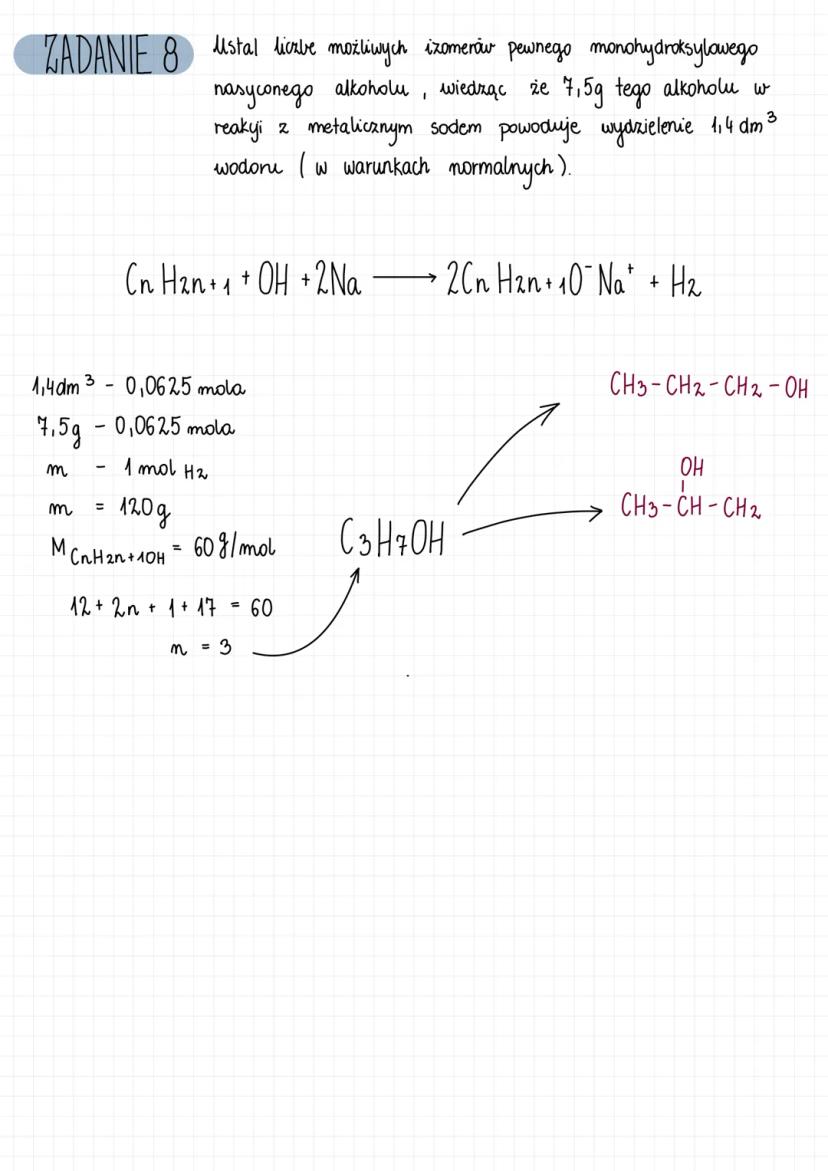
Zadanie: Ustal liczbę możliwych izomerów pewnego monohydroksylowego nasyconego alkoholu, wiedząc że 7,5g tego alkoholu w reakcji z metalicznym sodem powoduje wydzielenie 1,4 dm³ wodoru (w warunkach normalnych).
Rozwiązanie:
- Zapisujemy równanie reakcji: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Z warunków normalnych: 1,4 dm³ H₂ = 0,0625 mola H₂
- Obliczamy masę molową alkoholu: 7,5g / 0,0625 mola = 120g/mol
- Masa molowa alkoholu to 60g/mol (bo z 1 mola alkoholu powstaje 0,5 mola H₂)
- Z równania 12n + 2n + 1 + 17 = 60 → n = 3
- Wzór to C₃H₇OH (propanol) z dwoma izomerami: propan-1-ol i propan-2-ol
💡 Wskazówka: Pamiętaj o przeliczaniu objętości gazu na liczbę moli za pomocą objętości molowej !

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczanie wzorów sumarycznych alkoholi
Rozwiązując zadania dotyczące wzoru sumarycznego alkoholu, często korzystamy z danych o reakcji z sodem. Zobaczmy na przykładzie:
Zadanie: W reakcji 1,5g alkoholu monohydroksylowego z sodem wydzieliło się 0,28 dm³ wodoru (warunki normalne). Ustal wzór sumaryczny tego alkoholu.
Rozwiązanie:
- Zapisujemy reakcję: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Obliczamy liczbę moli wodoru: nₕ₂ = 0,28 dm³ / 22,4 dm³/mol = 0,0125 mola
- Liczba moli alkoholu = 2 × liczba moli H₂ = 0,025 mola
- Masa molowa alkoholu = 1,5g / 0,025 mol = 60 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 60 → n = 3
- Zatem wzór sumaryczny to C₃H₈O (lub C₃H₇OH)
Pamiętaj, że wzór sumaryczny daje tylko informację o liczbie poszczególnych atomów, nie o strukturze. Dlatego C₃H₈O może oznaczać zarówno propan-1-ol, jak i propan-2-ol.
💡 Ważne: Podczas reakcji alkoholu z metalem (Na, K) zawsze powstaje połowa mola H₂ na każdy mol alkoholu - to klucz do tych obliczeń!
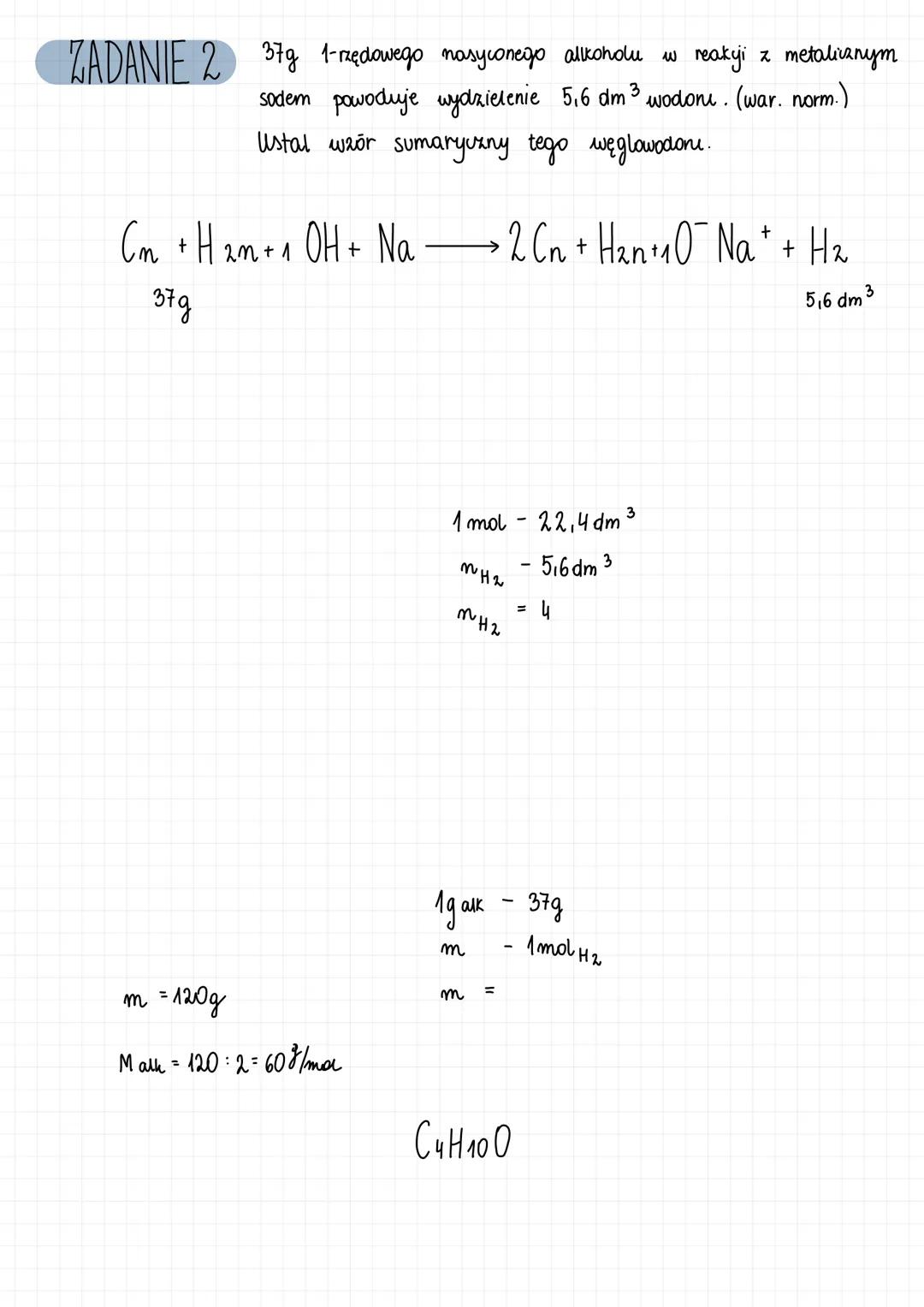
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkohol pierwszorzędowy w reakcjach
W zadaniach z alkoholami pierwszorzędowymi również stosujemy podobne podejście obliczeniowe:
Zadanie: 37g pierwszorzędowego nasyconego alkoholu w reakcji z metalicznym sodem powoduje wydzielenie 5,6 dm³ wodoru (war. norm.). Ustal wzór sumaryczny tego węglowodoru.
Rozwiązanie:
- Zapisujemy reakcję: CₙH₂ₙ₊₁OH + Na → CₙH₂ₙ₊₁O⁻Na⁺ + ½H₂
- Obliczamy liczbę moli wodoru: nₕ₂ = 5,6 dm³ / 22,4 dm³/mol = 0,25 mola
- Liczba moli alkoholu = 2 × 0,25 mol = 0,5 mola
- Masa molowa alkoholu = 37g / 0,5 mol = 74 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 74 → 14n = 56 → n = 4
- Zatem wzór sumaryczny to C₄H₁₀O (lub C₄H₉OH)
Ponieważ mowa o alkoholu pierwszorzędowym, struktura to CH₃-CH₂-CH₂-CH₂-OH lub CH₃-CH(CH₃)-CH₂-OH .
💡 Wskazówka: Gdy w zadaniu podano, że alkohol jest pierwszorzędowy, sprawdź wszystkie możliwe izomery i wybierz tylko te, które spełniają ten warunek!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkohol w reakcji z potasem
Potrafisz też obliczyć wzór alkoholu, gdy znasz liczbę cząsteczek wydzielonego wodoru:
Zadanie: Podaj wzór półstrukturalny nasyconego alkoholu R-OH, który w roztworze wodnym w reakcji 23g tego alkoholu z potasem wypiera 1,5·10²³ cząsteczek wodoru.
Rozwiązanie:
- Zapisujemy reakcję: 2CₙH₂ₙ₊₁OH + 2K → 2CₙH₂ₙ₊₁O⁻K⁺ + H₂
- Przeliczamy liczbę cząsteczek wodoru na mole: nₕ₂ = 1,5·10²³ / 6,02·10²³ = 0,25 mola
- Liczba moli alkoholu = 2 × 0,25 mol = 0,5 mola
- Masa molowa alkoholu = 23g / 0,5 mol = 46 g/mol
- Podstawiamy do wzoru: 12n + 2n + 1 + 17 = 46 → 14n = 28 → n = 2
- Zatem wzór półstrukturalny to CH₃-CH₂-OH (etanol)
Etanol to najprostszy alkohol, który spotykamy w życiu codziennym. Jest podstawowym składnikiem napojów alkoholowych, ale także ważnym rozpuszczalnikiem i surowcem w przemyśle.
💡 Ciekawostka: Etanol ma wiele zastosowań - oprócz napojów alkoholowych używa się go jako paliwo, rozpuszczalnik, środek dezynfekujący i surowiec do produkcji wielu związków chemicznych!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.