Czas poznać tajemnice atomu! To właśnie te malutkie cząsteczki budują... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
845
•
Zaktualizowano Mar 17, 2026
•
Amelia
@amelia_222
Czas poznać tajemnice atomu! To właśnie te malutkie cząsteczki budują... Pokaż więcej







Witaj w świecie chemii! To nauka, która wyjaśni Ci, dlaczego jedne substancje reagują ze sobą, a inne nie. Chemia to klucz do zrozumienia świata na poziomie atomowym.
Wszystko, co widzisz wokół siebie - od wody po telefon - składa się z atomów. To właśnie one są bohaterami chemicznych reakcji.
💡 Wskazówka: Chemia może wydawać się trudna, ale jak zrozumiesz budowę atomu, reszta będzie znacznie łatwiejsza!
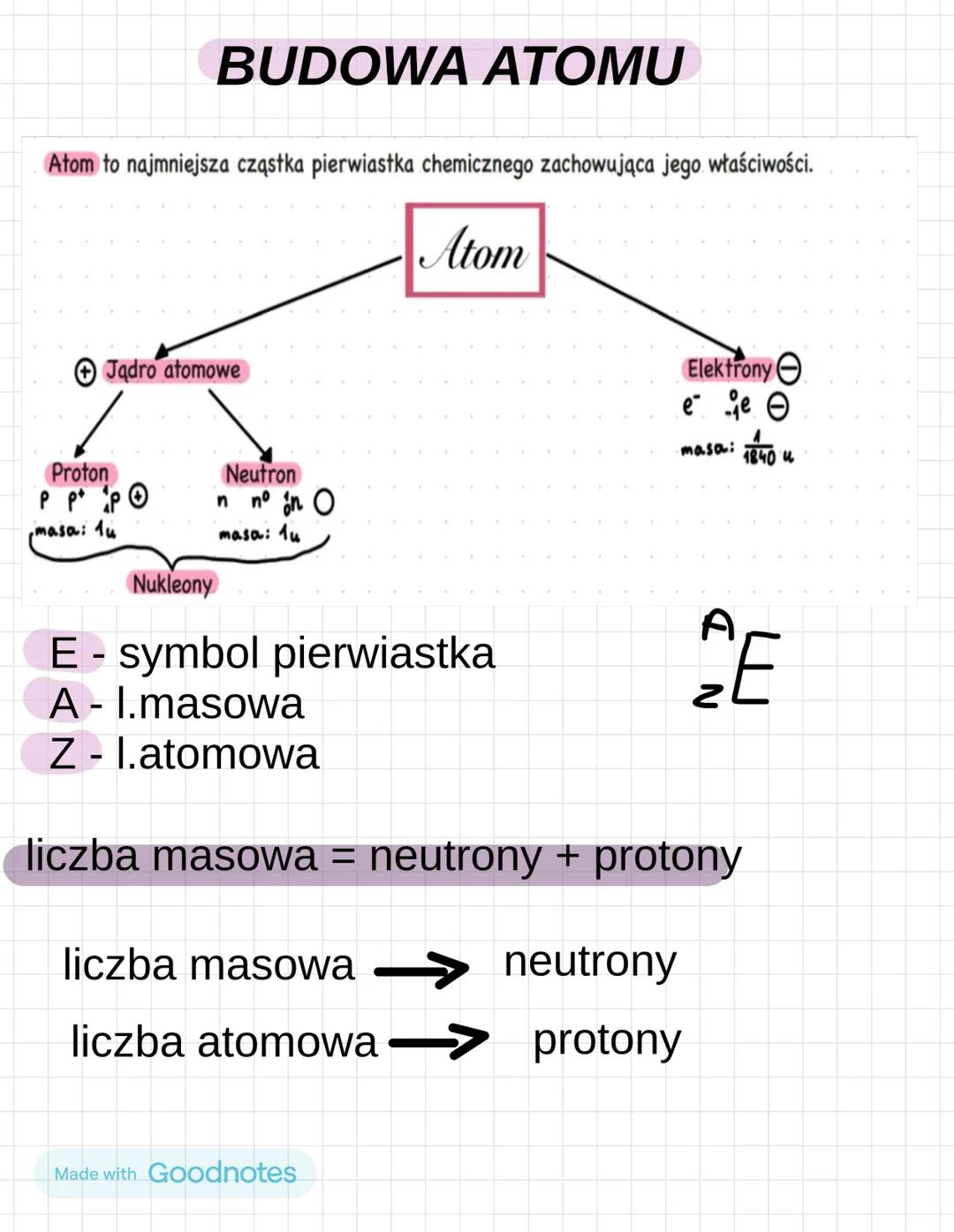
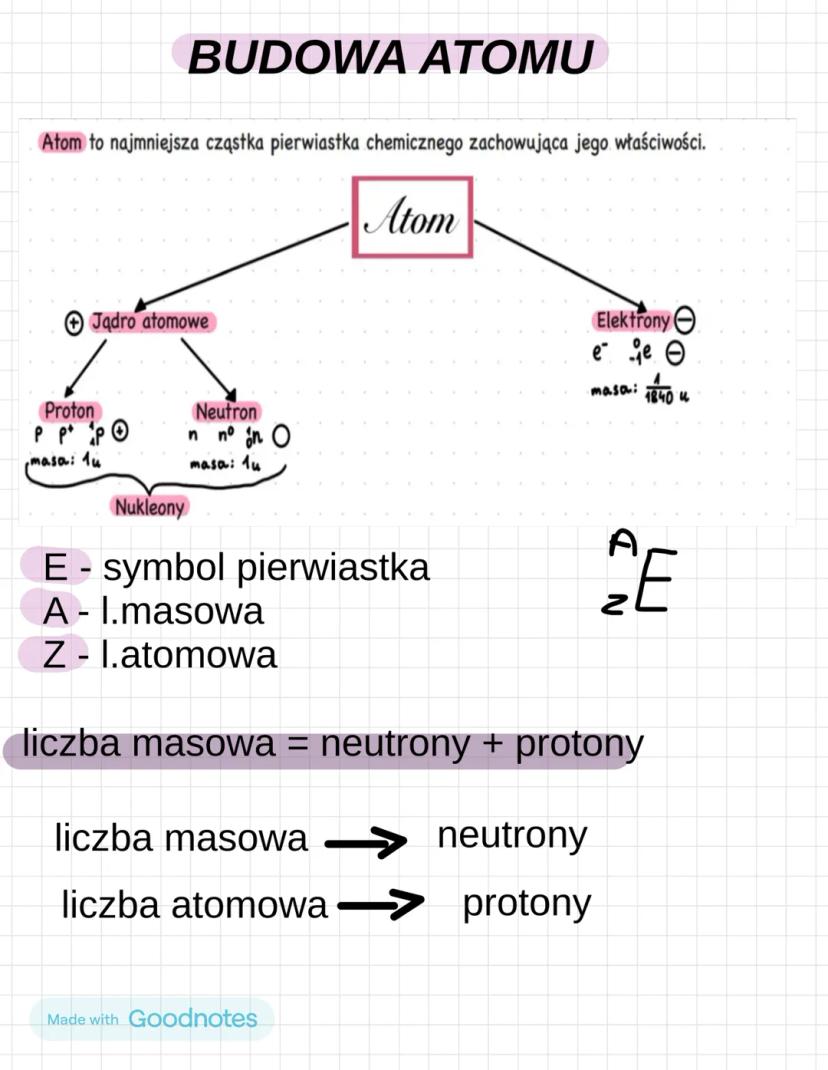
Atom to najmniejsza cząstka pierwiastka, która zachowuje wszystkie jego właściwości. Wyobraź sobie go jak miniaturny układ słoneczny!
W centrum znajduje się jądro atomowe składające się z nukleonów - czyli protonów (p⁺) i neutronów (n⁰). Protony mają ładunek dodatni, a neutrony są obojętne. Oba ważą około 1 u (jednostka masy atomowej).
Wokół jądra krążą elektrony (e⁻) - są one prawie 1840 razy lżejsze od protonów i mają ładunek ujemny. To właśnie elektrony odpowiadają za reakcje chemiczne!
Każdy pierwiastek ma swój symbol: ᴬ𝖹E, gdzie A to liczba masowa , a Z to liczba atomowa (liczba protonów).
💡 Pamiętaj: Liczba protonów = liczba elektronów w neutralnym atomie!

Weźmy przykład sodu: ²³₁₁Na. Z tego zapisu możesz wywnioskować wszystko o tym atomie!
Z = 11 (liczba atomowa) oznacza 11 protonów. W neutralnym atomie mamy też 11 elektronów - protony i elektrony są zawsze w równej liczbie!
A = 23 (liczba masowa) to suma protonów i neutronów. Skoro mamy 11 protonów, to neutronów jest: 23 - 11 = 12.
Prosty wzór: liczba masowa = protony + neutrony. To znaczy, że możesz łatwo obliczyć liczbę neutronów, odejmując liczbę atomową od liczby masowej.
💡 Szybka powtórka: P (protony) = Z, e (elektrony) = Z, n (neutrony) = A - Z

Izotopy to atomy tego samego pierwiastka z różną liczbą neutronów. Najlepszy przykład to wodór: ¹₁H (prot), ²₁H (deuter), ³₁H (tryt) - wszystkie mają 1 proton, ale różną liczbę neutronów!
Izotopy mają identyczne właściwości chemiczne, bo liczba elektronów jest taka sama. Różnią się tylko masą.
Powłoki elektronowe to obszary wokół jądra, gdzie znajdują się elektrony. Wyobraź sobie je jak warstwy cebuli - każda kolejna powłoka jest dalej od jądra.
Każda powłoka może pomieścić określoną maksymalną liczbę elektronów według wzoru 2n² (gdzie n to numer powłoki).
💡 Ciekawostka: Elektrony z zewnętrznej powłoki (walencyjnej) decydują o właściwościach chemicznych pierwiastka!
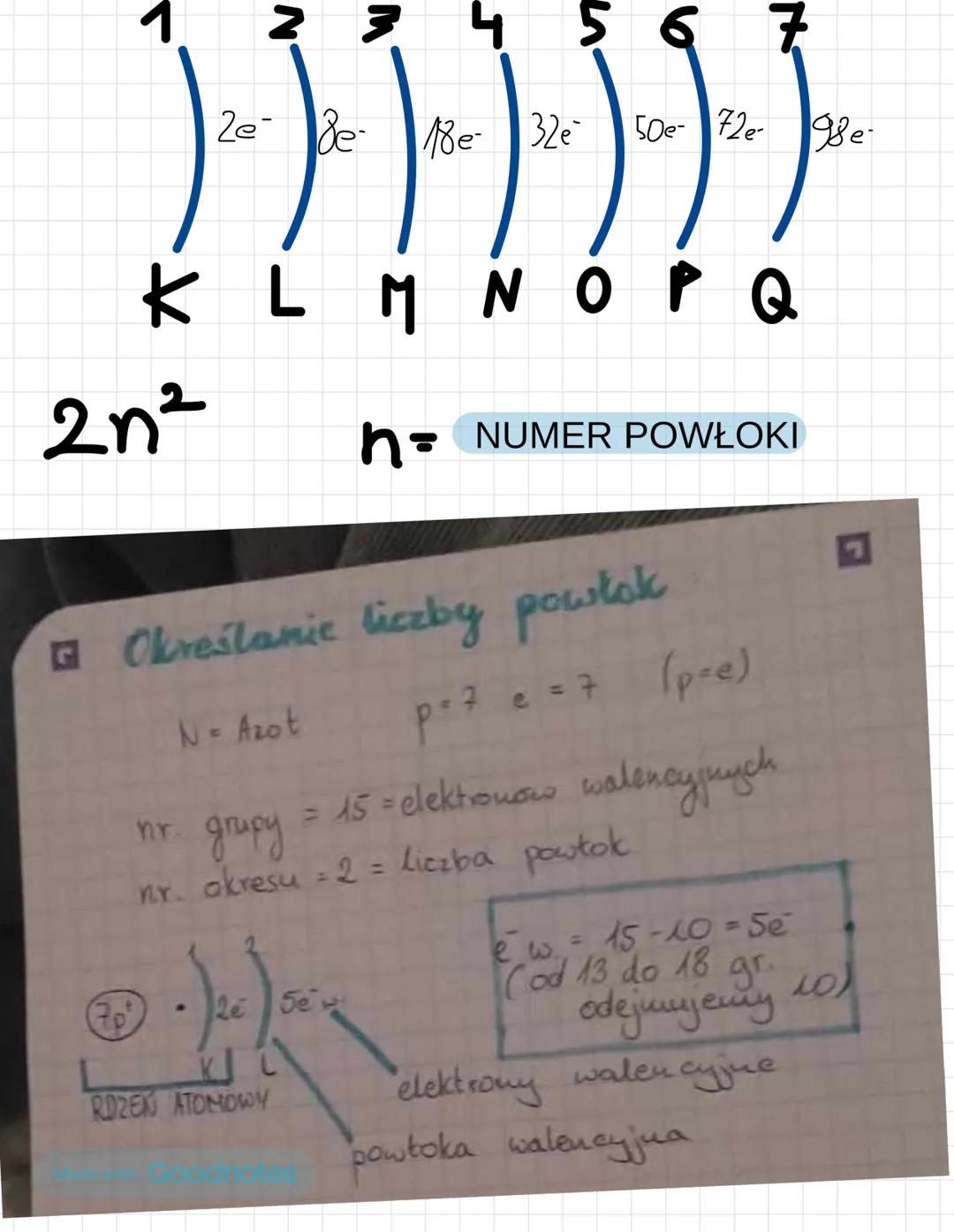
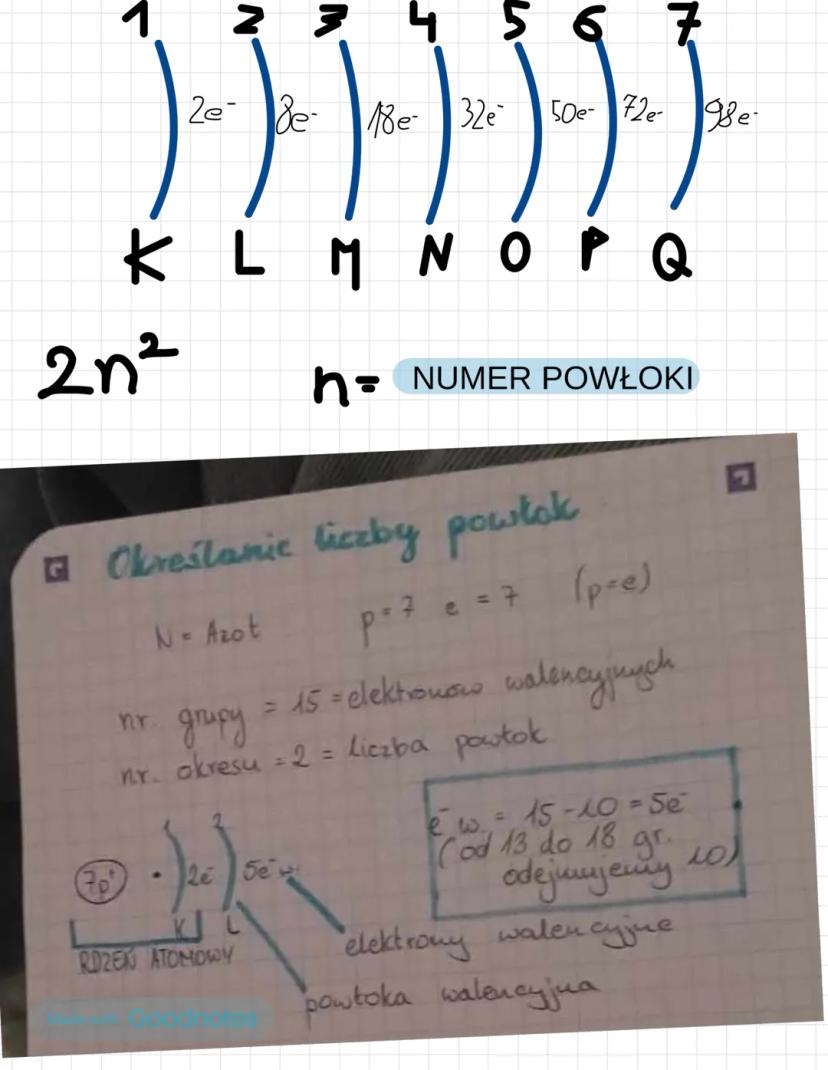
Powłoki mają nazwy K, L, M, N, O, P, Q i mogą pomieścić kolejno: 2, 8, 18, 32, 50, 72, 98 elektronów.
Żeby określić konfigurację elektronową, potrzebujesz układu okresowego! Numer okresu = liczba powłok, numer grupy pomaga określić elektrony walencyjne.
Przykład azotu (N): ma 7 elektronów, jest w 2. okresie (2 powłoki) i 15. grupie. Konfiguracja: K²L⁵ - czyli 2 elektrony w powłoce K, 5 w powłoce L.
Dla grup 13-18 elektrony walencyjne obliczasz: numer grupy - 10. Azot ma więc 15 - 10 = 5 elektronów walencyjnych.
💡 Trick: Elektrony walencyjne (zewnętrzne) to te, które uczestniczą w tworzeniu wiązań chemicznych!
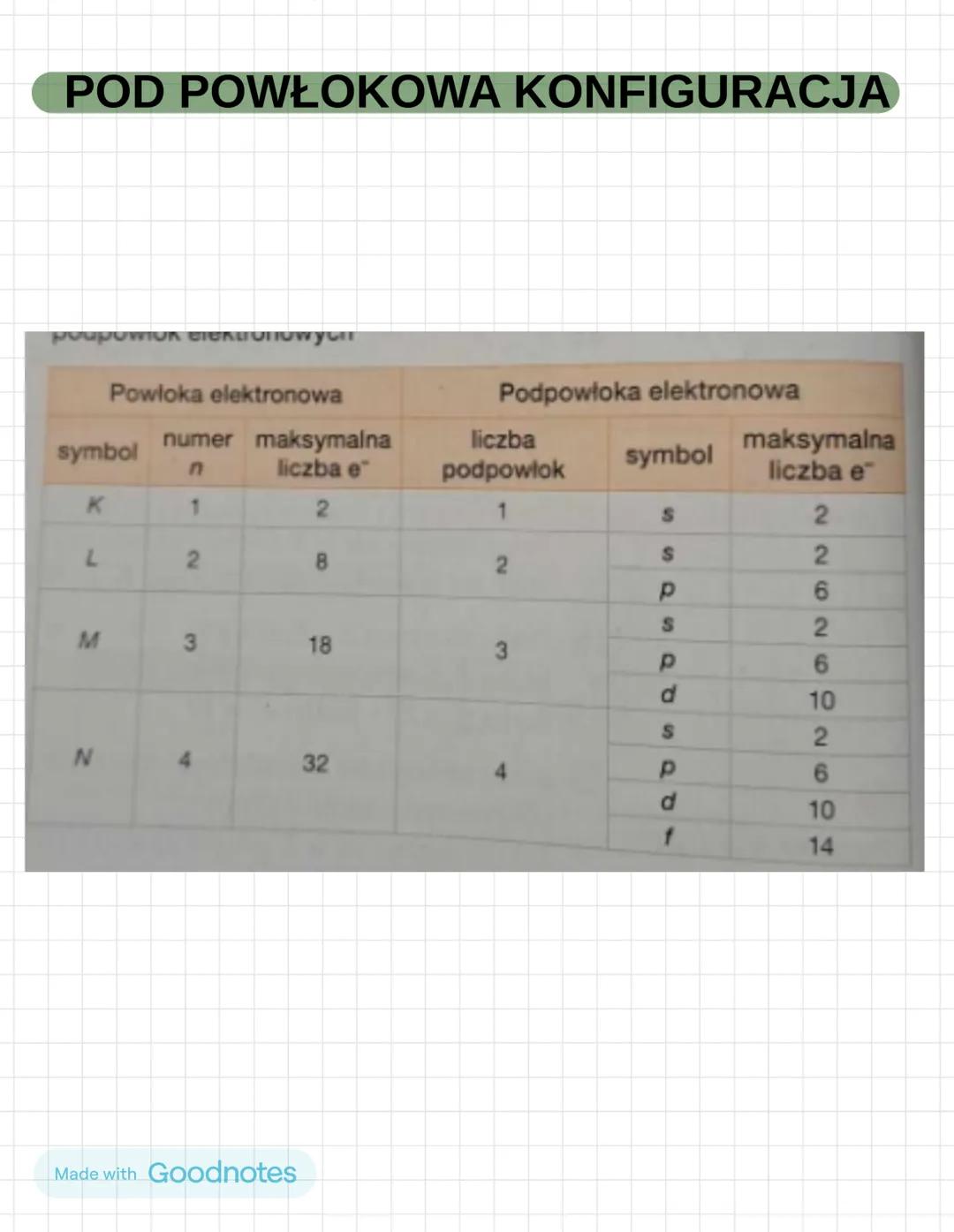
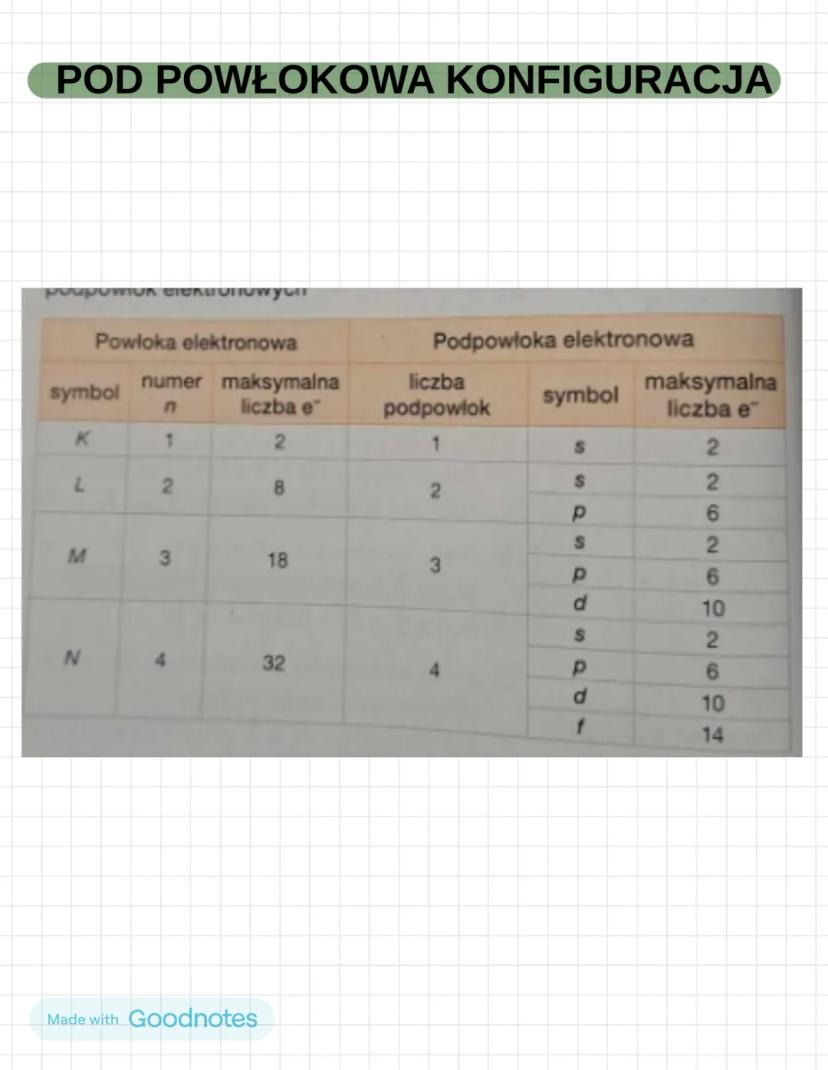
Każda powłoka dzieli się na podpowłoki oznaczone literami s, p, d, f. To jeszcze dokładniejszy sposób opisania, gdzie znajdują się elektrony.
Podpowłoki mają stałe pojemności: s - 2 elektrony, p - 6 elektronów, d - 10 elektronów, f - 14 elektronów.
Powłoka K ma tylko podpowłokę s. Powłoka L ma s i p. Powłoka M ma s, p i d. Powłoka N ma wszystkie cztery: s, p, d, f.
Ta wiedza pomoże Ci zrozumieć, dlaczego niektóre pierwiastki mają podobne właściwości - to przez podobną konfigurację elektronów walencyjnych!
💡 Zapamiętaj: Kolejność energii podpowłok: s < p < d < f (s ma najniższą energię)

Zobaczmy, jak napisać podpowłokową konfigurację elektronową dla litu (Li).
Lit jest w 2. okresie, więc ma 2 powłoki (K i L). Ma numer atomowy 3, więc 3 elektrony. Konfiguracja powłokowa: K²L¹.
Teraz zamieniamy na podpowłoki: powłoka K ma tylko podpowłokę s, więc 1s². Powłoka L ma 1 elektron w najniższej podpowłoce, czyli 2s¹.
Końcowy wynik: Li: 1s²2s¹. Czytasz to: "jeden-es-dwa, dwa-es-jeden".
Elektrony zawsze zapełniają najpierw podpowłoki o najniższej energii. To jak woda - zawsze spływa do najniższego miejsca!
💡 Ważne: Indeks górny pokazuje liczbę elektronów w danej podpowłoce, nie jej pojemność!
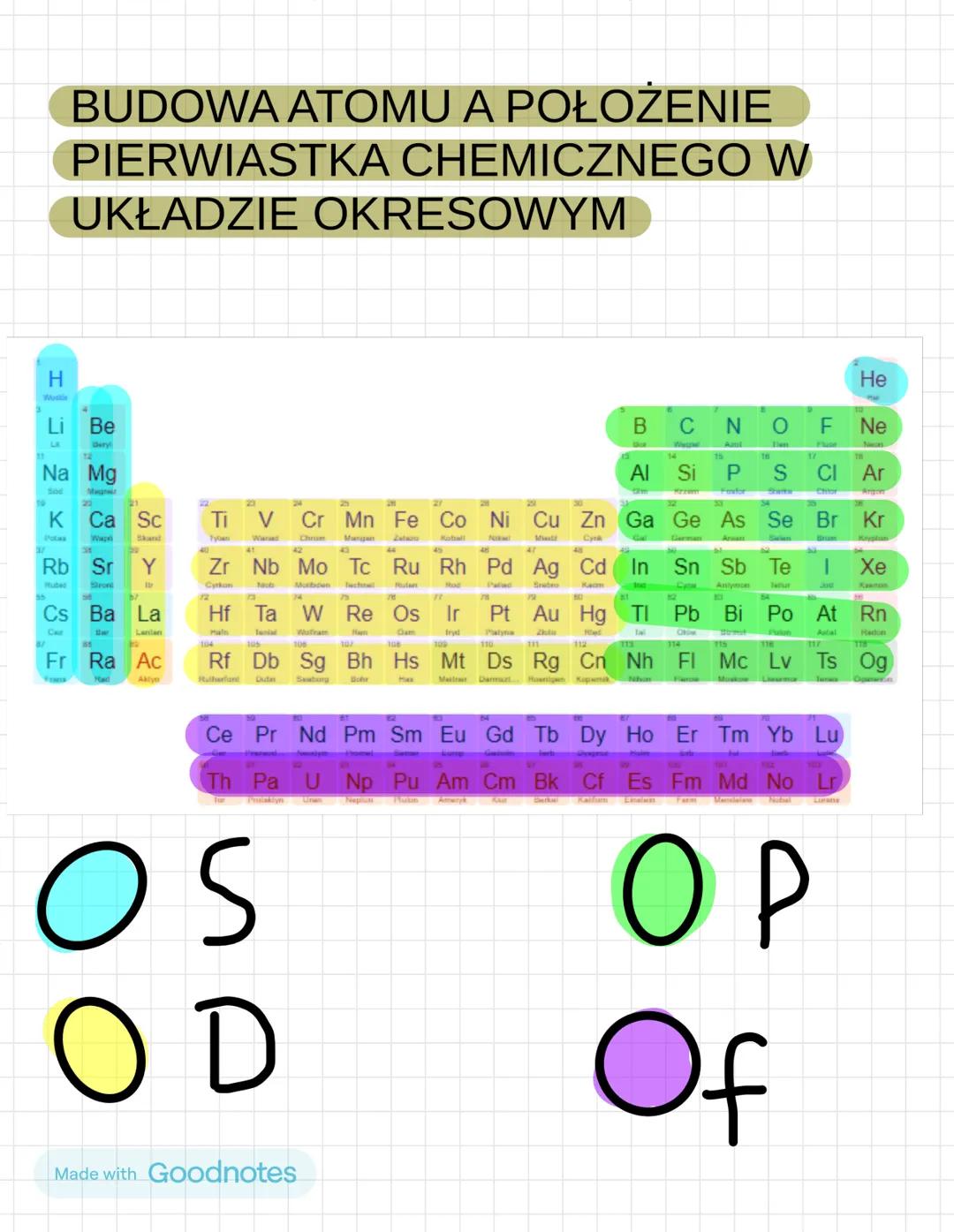
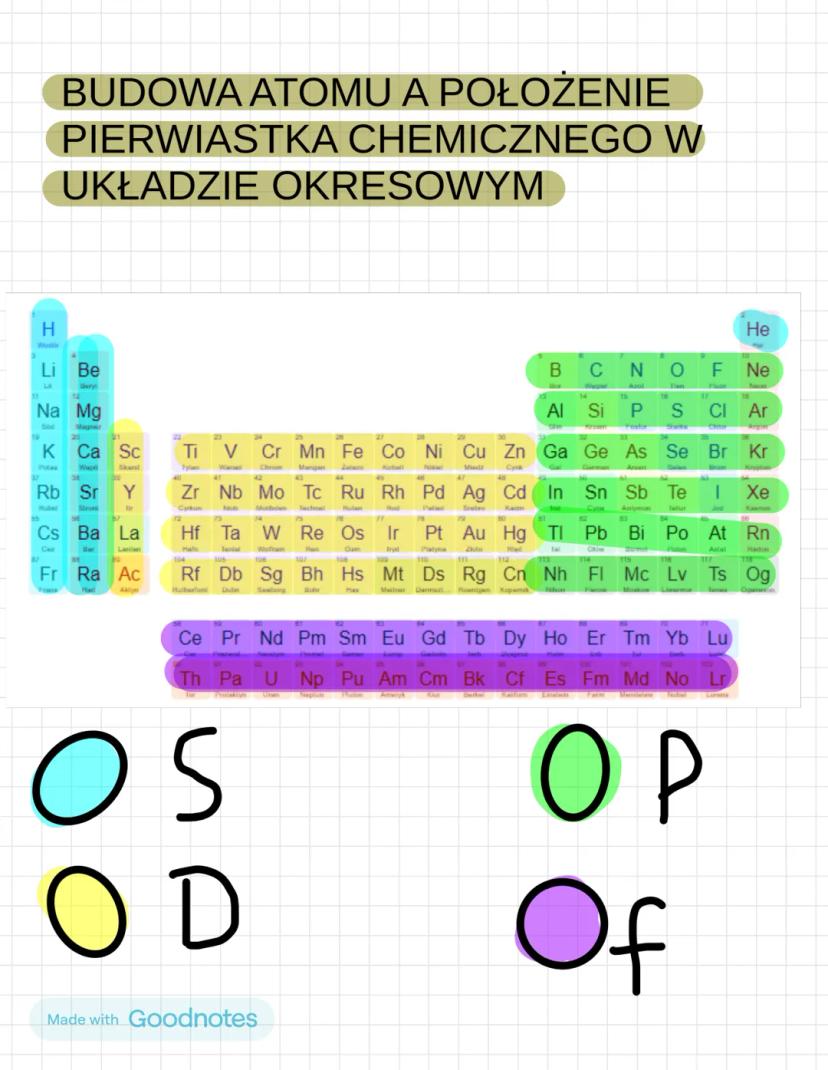
Układ okresowy to genialny wynalazek - od razu pokazuje budowę każdego atomu! Każde miejsce w tabeli odpowiada konkretnemu pierwiastkowi.
Poziome rzędy to okresy - pokazują liczbę powłok elektronowych. Pionowe kolumny to grupy - pierwiastki w tej samej grupie mają podobne właściwości.
Układ podzielony jest na bloki konfiguracyjne: blok s , blok p , blok d , blok f (lantanowce i aktynowce).
Położenie pierwiastka od razu mówi o jego konfiguracji elektronowej. To jak GPS dla chemików!
💡 Pro tip: Naucz się czytać układ okresowy - to najlepsze narzędzie chemika!

Najłatwiejszy sposób na konfigurację elektronową? Metoda blokowa z układem okresowym!
Znajdź fosfor (P) - grupa 15, okres 3. Teraz "idź" przez układ od wodoru do fosforu, przechodząc przez kolejne bloki.
1. okres: przechodzisz przez 2 pola bloku s → 1s²
2. okres: 2 pola bloku s + 6 pól bloku p → 2s²2p⁶
3. okres: 2 pola bloku s + 3 pola bloku p (do fosforu) → 3s²3p³
Każde pole w bloku to jeden elektron więcej w odpowiedniej podpowłoce!
💡 Genialny trick: Nie musisz pamiętać skomplikowanych reguł - wystarczy układ okresowy!

Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Amelia
@amelia_222
Czas poznać tajemnice atomu! To właśnie te malutkie cząsteczki budują cały wszechświat wokół nas. Dzisiaj dowiesz się, jak atomy są zbudowane i dlaczego to wiedza pomoże Ci zrozumieć całą chemię.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Witaj w świecie chemii! To nauka, która wyjaśni Ci, dlaczego jedne substancje reagują ze sobą, a inne nie. Chemia to klucz do zrozumienia świata na poziomie atomowym.
Wszystko, co widzisz wokół siebie - od wody po telefon - składa się z atomów. To właśnie one są bohaterami chemicznych reakcji.
💡 Wskazówka: Chemia może wydawać się trudna, ale jak zrozumiesz budowę atomu, reszta będzie znacznie łatwiejsza!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Atom to najmniejsza cząstka pierwiastka, która zachowuje wszystkie jego właściwości. Wyobraź sobie go jak miniaturny układ słoneczny!
W centrum znajduje się jądro atomowe składające się z nukleonów - czyli protonów (p⁺) i neutronów (n⁰). Protony mają ładunek dodatni, a neutrony są obojętne. Oba ważą około 1 u (jednostka masy atomowej).
Wokół jądra krążą elektrony (e⁻) - są one prawie 1840 razy lżejsze od protonów i mają ładunek ujemny. To właśnie elektrony odpowiadają za reakcje chemiczne!
Każdy pierwiastek ma swój symbol: ᴬ𝖹E, gdzie A to liczba masowa , a Z to liczba atomowa (liczba protonów).
💡 Pamiętaj: Liczba protonów = liczba elektronów w neutralnym atomie!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Weźmy przykład sodu: ²³₁₁Na. Z tego zapisu możesz wywnioskować wszystko o tym atomie!
Z = 11 (liczba atomowa) oznacza 11 protonów. W neutralnym atomie mamy też 11 elektronów - protony i elektrony są zawsze w równej liczbie!
A = 23 (liczba masowa) to suma protonów i neutronów. Skoro mamy 11 protonów, to neutronów jest: 23 - 11 = 12.
Prosty wzór: liczba masowa = protony + neutrony. To znaczy, że możesz łatwo obliczyć liczbę neutronów, odejmując liczbę atomową od liczby masowej.
💡 Szybka powtórka: P (protony) = Z, e (elektrony) = Z, n (neutrony) = A - Z

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Izotopy to atomy tego samego pierwiastka z różną liczbą neutronów. Najlepszy przykład to wodór: ¹₁H (prot), ²₁H (deuter), ³₁H (tryt) - wszystkie mają 1 proton, ale różną liczbę neutronów!
Izotopy mają identyczne właściwości chemiczne, bo liczba elektronów jest taka sama. Różnią się tylko masą.
Powłoki elektronowe to obszary wokół jądra, gdzie znajdują się elektrony. Wyobraź sobie je jak warstwy cebuli - każda kolejna powłoka jest dalej od jądra.
Każda powłoka może pomieścić określoną maksymalną liczbę elektronów według wzoru 2n² (gdzie n to numer powłoki).
💡 Ciekawostka: Elektrony z zewnętrznej powłoki (walencyjnej) decydują o właściwościach chemicznych pierwiastka!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Powłoki mają nazwy K, L, M, N, O, P, Q i mogą pomieścić kolejno: 2, 8, 18, 32, 50, 72, 98 elektronów.
Żeby określić konfigurację elektronową, potrzebujesz układu okresowego! Numer okresu = liczba powłok, numer grupy pomaga określić elektrony walencyjne.
Przykład azotu (N): ma 7 elektronów, jest w 2. okresie (2 powłoki) i 15. grupie. Konfiguracja: K²L⁵ - czyli 2 elektrony w powłoce K, 5 w powłoce L.
Dla grup 13-18 elektrony walencyjne obliczasz: numer grupy - 10. Azot ma więc 15 - 10 = 5 elektronów walencyjnych.
💡 Trick: Elektrony walencyjne (zewnętrzne) to te, które uczestniczą w tworzeniu wiązań chemicznych!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Każda powłoka dzieli się na podpowłoki oznaczone literami s, p, d, f. To jeszcze dokładniejszy sposób opisania, gdzie znajdują się elektrony.
Podpowłoki mają stałe pojemności: s - 2 elektrony, p - 6 elektronów, d - 10 elektronów, f - 14 elektronów.
Powłoka K ma tylko podpowłokę s. Powłoka L ma s i p. Powłoka M ma s, p i d. Powłoka N ma wszystkie cztery: s, p, d, f.
Ta wiedza pomoże Ci zrozumieć, dlaczego niektóre pierwiastki mają podobne właściwości - to przez podobną konfigurację elektronów walencyjnych!
💡 Zapamiętaj: Kolejność energii podpowłok: s < p < d < f (s ma najniższą energię)

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Zobaczmy, jak napisać podpowłokową konfigurację elektronową dla litu (Li).
Lit jest w 2. okresie, więc ma 2 powłoki (K i L). Ma numer atomowy 3, więc 3 elektrony. Konfiguracja powłokowa: K²L¹.
Teraz zamieniamy na podpowłoki: powłoka K ma tylko podpowłokę s, więc 1s². Powłoka L ma 1 elektron w najniższej podpowłoce, czyli 2s¹.
Końcowy wynik: Li: 1s²2s¹. Czytasz to: "jeden-es-dwa, dwa-es-jeden".
Elektrony zawsze zapełniają najpierw podpowłoki o najniższej energii. To jak woda - zawsze spływa do najniższego miejsca!
💡 Ważne: Indeks górny pokazuje liczbę elektronów w danej podpowłoce, nie jej pojemność!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Układ okresowy to genialny wynalazek - od razu pokazuje budowę każdego atomu! Każde miejsce w tabeli odpowiada konkretnemu pierwiastkowi.
Poziome rzędy to okresy - pokazują liczbę powłok elektronowych. Pionowe kolumny to grupy - pierwiastki w tej samej grupie mają podobne właściwości.
Układ podzielony jest na bloki konfiguracyjne: blok s , blok p , blok d , blok f (lantanowce i aktynowce).
Położenie pierwiastka od razu mówi o jego konfiguracji elektronowej. To jak GPS dla chemików!
💡 Pro tip: Naucz się czytać układ okresowy - to najlepsze narzędzie chemika!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Najłatwiejszy sposób na konfigurację elektronową? Metoda blokowa z układem okresowym!
Znajdź fosfor (P) - grupa 15, okres 3. Teraz "idź" przez układ od wodoru do fosforu, przechodząc przez kolejne bloki.
1. okres: przechodzisz przez 2 pola bloku s → 1s²
2. okres: 2 pola bloku s + 6 pól bloku p → 2s²2p⁶
3. okres: 2 pola bloku s + 3 pola bloku p (do fosforu) → 3s²3p³
Każde pole w bloku to jeden elektron więcej w odpowiedniej podpowłoce!
💡 Genialny trick: Nie musisz pamiętać skomplikowanych reguł - wystarczy układ okresowy!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
14
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
Zgłębiaj liczby kwantowe: n, l, m, ms oraz zasady zakazu Pauliego. Dowiedz się, jak te liczby definiują stany elektronowe w atomach i kształtują orbitale atomowe. Idealne dla studentów fizyki i chemii. Typ: Podsumowanie.
Zgłębiaj zasady mechaniki kwantowej i budowy atomów. Dowiedz się o liczbach kwantowych, konfiguracjach elektronowych oraz modelach atomowych, w tym modelu Bohra. Idealne dla studentów chemii i fizyki, którzy chcą zrozumieć podstawy struktury atomowej i zachowań elektronów.
Tablica Mendelejewa
Zgłębiaj kluczowe koncepcje budowy atomu oraz rodzaje orbitali atomowych. Ta notatka omawia cztery typy orbitali (s, p, d, f), ich kształty oraz zasady Heisenberga dotyczące położenia elektronów. Idealna dla uczniów chemii na poziomie rozszerzonym. Tematyka obejmuje również strukturę materii i podstawowe pojęcia chemiczne.
Zrozumienie budowy atomów, konfiguracji elektronowej oraz izotopów. Materiał obejmuje kluczowe pojęcia, takie jak liczba atomowa, masa atomowa, izotopy, oraz zasady dotyczące spinów elektronowych. Idealne dla uczniów przygotowujących się do matury z chemii. Typ: Podsumowanie.
Zrozumienie podpowłok elektronowych i konfiguracji elektronowej atomów. Ta notatka omawia struktury elektronowe, w tym powłokę walencyjną, liczby elektronów oraz zasady obliczania maksymalnej liczby elektronów w powłokach. Idealna dla uczniów chemii przygotowujących się do egzaminów.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS