Blok d to fascynujący zbiór pierwiastków chemicznych, które odgrywają kluczową... Pokaż więcej
Pierwiastki Chemiczne Bloku D



](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_1.webp&w=2048&q=75)
Chrom - właściwości i związki
Chrom to srebrzyste, twarde ciało stałe należące do 6 grupy i 4 okresu układu okresowego. Ma konfigurację elektronową [Ar] 3d⁵ 4s¹. Pasywuje, czyli nie reaguje z kwasami utleniającymi jak stężony i rozcieńczony HNO₃ czy H₂SO₄.
Można go otrzymać metodą aluminotermii: Cr₂O₃ + 2Al → 2Cr + Al₂O₃. Chrom tworzy tlenki o różnych właściwościach - CrO (zasadowy), Cr₂O₃ (amfoteryczny) i CrO₃ (kwasowy). CrO₃ ma wyjątkową właściwość - reaguje zarówno z zasadami , jak i z kwasami w reakcji redoks .
Wodorotlenki chromu to między innymi Cr(OH)₂ (niebieski osad) i Cr(OH)₃ (zielony osad o charakterze amfoterycznym). Sole chromu (II) dają niebieski roztwór (np. CrCl₂), a sole chromu (III) - zielony roztwór (np. CrCl₃).
Warto zapamiętać! Związki chromu są barwne i łatwo je rozpoznać - związki Cr(II) są niebieskie, związki Cr(III) zielone, a związki Cr(VI) żółte lub pomarańczowe.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_2.webp&w=2048&q=75)
Reakcje chromu i jego związków
W zależności od środowiska, związki chromu mogą przechodzić różne przemiany. Cr₂O₇²⁻ jest nietrwały w środowisku zasadowym, a CrO₄²⁻ jest nietrwały w środowisku kwasowym. Dzięki temu można kontrolować formę, w jakiej występuje chrom.
Chrom (III) może przechodzić reakcje z kwasami i zasadami. W środowisku kwasowym: 2Cr(OH)₃ + 6H⁺ → 2Cr³⁺ + 6H₂O. W środowisku zasadowym może tworzyć hydroksokompleksy: Cr(OH)₃ + 3OH⁻ → [Cr(OH)₆]³⁻.
Związki chromu (III) pod wpływem utleniaczy mogą przechodzić w związki chromu (VI). Na przykład: 2[Cr(OH)₄]⁻ + 3H₂O₂ + 2OH⁻ → 2CrO₄²⁻ + 8H₂O. Towarzyszy temu zmiana barwy z zielonej na żółtą, co jest ważną obserwacją w analizie chemicznej.
Dichromian potasu (K₂Cr₂O₇) jest silnym utleniaczem i może utleniać wiele związków, np. w reakcji: Cr₂O₇²⁻ + 14H⁺ + 6Fe²⁺ → 6Fe³⁺ + 2Cr³⁺ + 7H₂O.
Pamiętaj! W reakcjach redoks z udziałem związków chromu zawsze zwracaj uwagę na zmianę barwy - to ważna wskazówka pokazująca, że doszło do zmiany stopnia utlenienia.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_3.webp&w=2048&q=75)
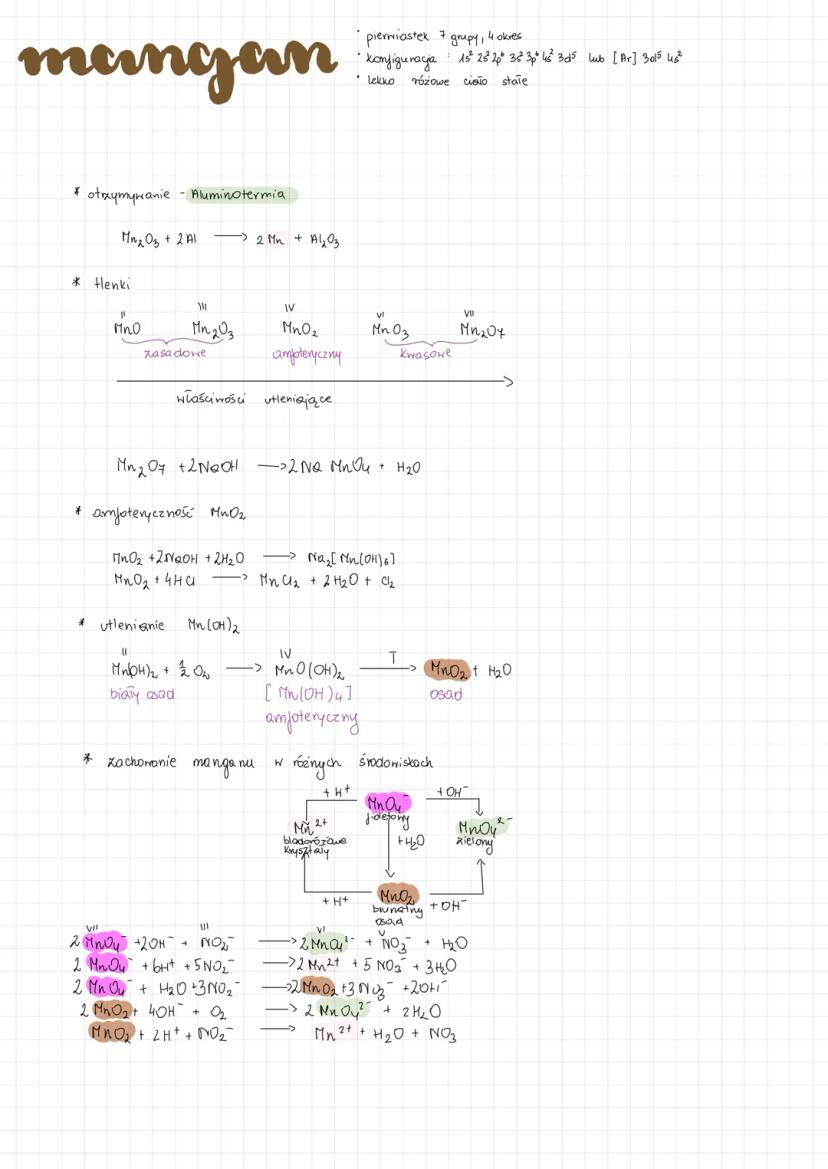
Mangan - właściwości i związki
Mangan to lekko różowe ciało stałe z 7 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 3d⁵ 4s². Podobnie jak chrom, można go otrzymać metodą aluminotermii: Mn₂O₃ + 2Al → 2Mn + Al₂O₃.
Mangan tworzy szereg tlenków o różnych właściwościach: MnO (zasadowy), Mn₂O₃ i MnO₂ (amfoteryczny), Mn₂O₇ (kwasowy). Tlenki manganu o wyższych stopniach utlenienia mają silne właściwości utleniające. Mn₂O₇ reaguje z zasadami: Mn₂O₇ + 2NaOH → 2NaMnO₄ + H₂O.
Wodorotlenek manganu (II) - Mn(OH)₂ to biały osad, który łatwo ulega utlenieniu tlenem z powietrza do związków manganu (III) i (IV). Związki manganu na różnych stopniach utlenienia mają charakterystyczne barwy: Mn²⁺ (bladopomarańczowy), MnO₄²⁻ (zielony), MnO₄⁻ (fioletowy), co ma ogromne znaczenie diagnostyczne.
Manganian (VII) potasu, czyli nadmanganian potasu (KMnO₄), jest silnym utleniaczem i w zależności od środowiska może redukować się do związków manganu na różnych stopniach utlenienia.
Ciekawostka! Nadmanganian potasu (KMnO₄) to popularny środek dezynfekujący znany jako "manganek" - jego intensywnie fioletowe roztwory łatwo odbarwiają się podczas reakcji redoks.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_4.webp&w=2048&q=75)
Żelazo - właściwości i związki
Żelazo to srebrzyste ciało stałe z 8 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s² 3d⁶. Ulega pasywacji w niektórych środowiskach, co chroni je przed dalszym utlenianiem. Można je otrzymać w reakcji redukcji tlenku żelaza węglem: C + FeO → CO + Fe.
Żelazo tworzy jony na dwóch głównych stopniach utlenienia: Fe²⁺ i Fe³⁺. Jon Fe³⁺ jest trwalszy, ponieważ ma mniej elektronów niesparowanych (wszystkie elektrony w orbitalu 3d są pojedynczo obsadzone).
Najważniejsze tlenki żelaza to: FeO (czarny, zasadowy), Fe₂O₃ (brunatny, amfoteryczny) i Fe₃O₄ (czarny magnetyt, mieszany tlenek FeO·Fe₂O₃). Żelazo reaguje z kwasami nieutleniającymi, np. Fe + 2HCl → FeCl₂ + H₂, ale ulega także reakcjom z kwasami utleniającymi i tlenem.
Wodorotlenki żelaza to Fe(OH)₂ i Fe(OH)₃ (rdzawobrązowy). Utlenianie Fe(OH)₂ tlenem z powietrza to reakcja: 4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃.
Praktyczna wskazówka! Rdzewienie żelaza to właśnie reakcja utleniania w obecności wody i tlenu z powietrza - dlatego metalowe konstrukcje trzeba chronić przed wilgocią i tlenem przez malowanie lub galwanizację.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_5.webp&w=2048&q=75)
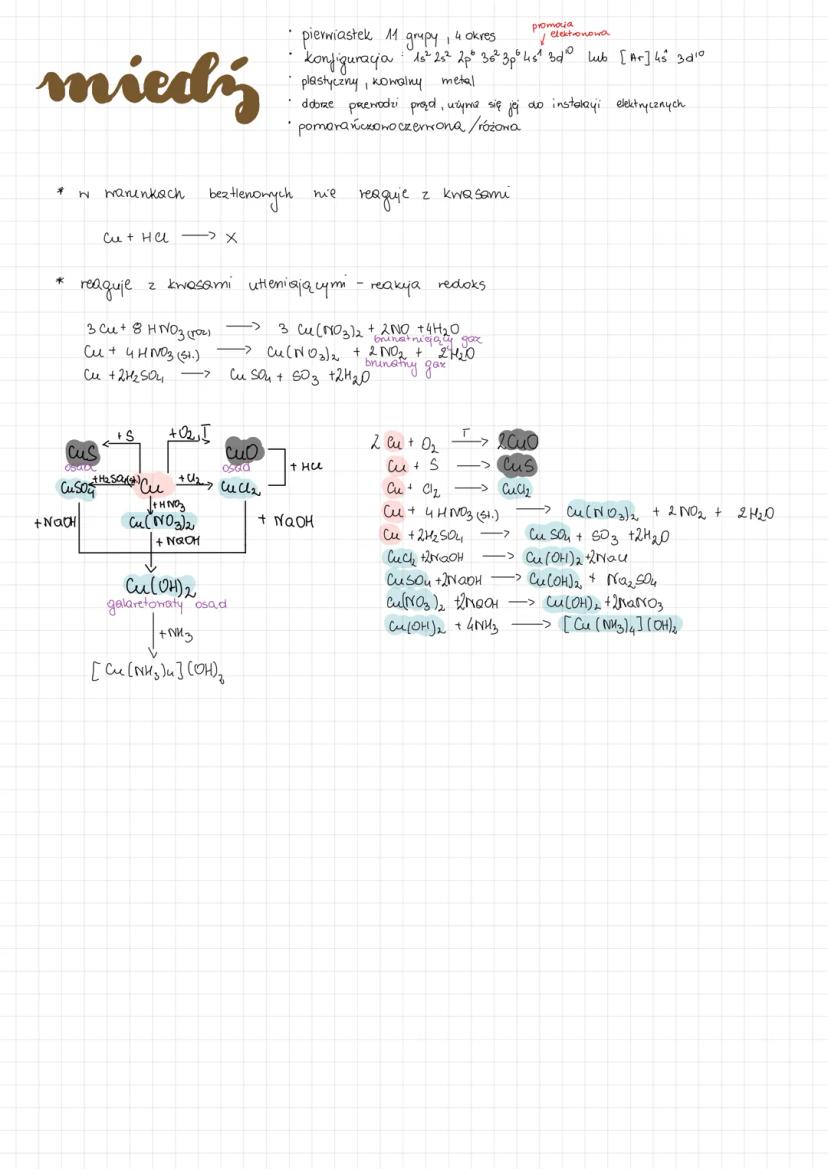
Miedź - właściwości i związki
Miedź to charakterystyczny pomarańczowo-czerwony metal z 11 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s¹ 3d¹⁰. Jest plastyczna, kowalna i świetnie przewodzi prąd elektryczny, dlatego jest powszechnie używana w instalacjach elektrycznych.
W przeciwieństwie do większości metali, miedź nie reaguje z kwasami beztlenowymi (jak HCl) - nie wypiera wodoru z kwasów. Reaguje natomiast z kwasami utleniającymi w reakcjach redoks: 3Cu + 8HNO₃(rozc.) → 3Cu(NO₃)₂ + 2NO + 4H₂O (brunatny gaz) lub Cu + 4HNO₃(stęż.) → Cu(NO₃)₂ + 2NO₂ + 2H₂O.
Miedź reaguje również ze stężonym kwasem siarkowym: Cu + 2H₂SO₄ → CuSO₄ + SO₂ + 2H₂O. Tworzy związki głównie na stopniach utlenienia +1 i +2, przy czym związki miedzi (II) są znacznie trwalsze i bardziej powszechne.
Uwaga! Charakterystyczne zabarwienie związków miedzi (II) to intensywny niebieski kolor, co jest spowodowane obecnością jonów Cu²⁺. Zjawisko to wykorzystuje się w testach chemicznych na obecność miedzi.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_6.webp&w=2048&q=75)
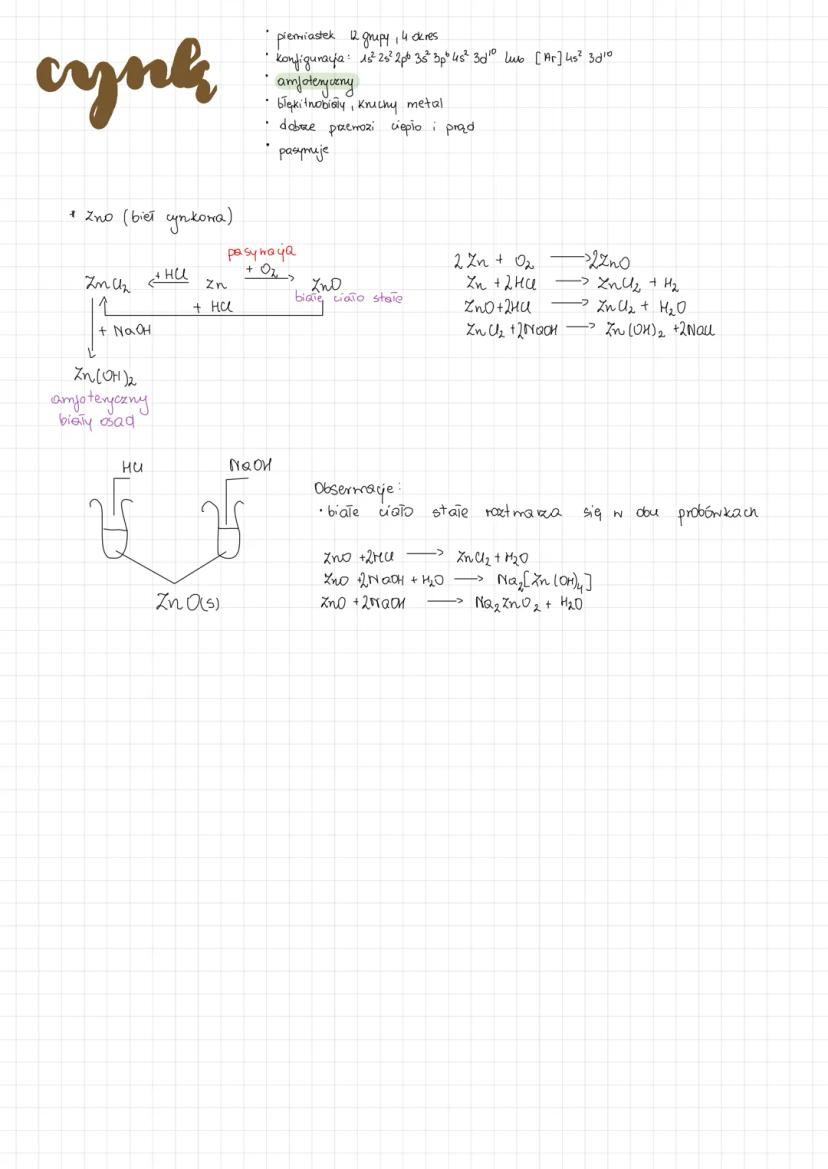
Cynk - właściwości i związki
Cynk to błękitnobiały, kruchy metal z 12 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s² 3d¹⁰. Dobrze przewodzi ciepło i prąd elektryczny. Jest pierwiastkiem amfoterycznym, co oznacza, że reaguje zarówno z kwasami, jak i z zasadami.
Tlenek cynku (ZnO), znany jako biel cynkowa, to białe ciało stałe powstające w reakcji: 2Zn + O₂ → 2ZnO. Jest związkiem amfoterycznym - reaguje z kwasami: ZnO + 2HCl → ZnCl₂ + H₂O, jak również z zasadami: ZnO + 2NaOH + H₂O → Na₂[Zn(OH)₄].
Cynk reaguje z kwasami, uwalniając wodór: Zn + 2HCl → ZnCl₂ + H₂. Wodorotlenek cynku Zn(OH)₂ to biały osad o właściwościach amfoterycznych, który można otrzymać w reakcji: ZnCl₂ + 2NaOH → Zn(OH)₂ + 2NaCl.
W środowisku silnie zasadowym cynk tworzy hydroksocynkany: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄] lub Na₂ZnO₂ + H₂O.
Praktyczne zastosowanie! Dzięki amfoteryczności cynk jest używany do galwanizacji (cynkowania) żelaza, co chroni je przed korozją. Nawet gdy warstwa cynku zostanie uszkodzona, nadal chroni żelazo, działając jako anoda ochronna.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Reakcje redoks
9Ogniwa Galwaniczne i Redoks
Zrozumienie ogniw galwanicznych, reakcji redoks oraz stopni utlenienia pierwiastków. Dowiedz się o korozji metali, metodach ochrony oraz zastosowaniach ogniw Daniella. Idealne dla uczniów chemii i studentów przygotowujących się do egzaminów.
Reguły Stopni Utlenienia
Zrozumienie stopni utlenienia pierwiastków chemicznych oraz ich roli w reakcjach redoks. Notatka obejmuje definicje, kluczowe zasady ustalania stopni utlenienia, przykłady oraz wyjaśnienia dotyczące utleniaczy i reduktorów. Idealna dla uczniów chemii.
Właściwości Metali D-Block
Zgłębiaj właściwości i reakcje metali bloku D, takich jak mangan, chrom, żelazo, miedź i cynk. Dowiedz się o ich związkach, amfoterycznych tlenkach oraz doświadczeniach laboratoryjnych. Idealne dla studentów chemii, którzy chcą zrozumieć chemiczne zachowanie metali i ich zastosowania.
Chemia Bloku D: Metale
Zgłębiaj charakterystykę metali bloku D, w tym srebra, cynku, żelaza i manganu. Dowiedz się o reakcjach chemicznych, stanach utlenienia oraz właściwościach amfoterycznych. Idealne materiały do nauki dla studentów chemii.
Elektrochemia: Zasady i Reakcje
Kompleksowe notatki z elektrochemii obejmujące kluczowe zagadnienia, takie jak reakcje redoks, prawo Faradaya, procesy elektrolizy oraz właściwości elektrolitów. Idealne dla uczniów przygotowujących się do egzaminów z chemii na poziomie rozszerzonym.
Pierwiastki bloku D
Pierwiastki bloku D : chrom, miedź, żelazo, cynk
Reakcje Redoks: Przykłady i Zasady
Zrozumienie reakcji redoks, w tym reakcji dysproporcjonowania i synproporcjonowania. Przykłady reakcji chemicznych, obliczanie stopni utlenienia oraz bilans elektronowy. Idealne dla studentów chemii, którzy chcą zgłębić temat utleniania i redukcji.
Redoks
Notatka do na nauki reakcji utleniania i redukcji do matury/na sprawdzian/ na karkówkę
Reakcje Redoks i Utlenianie
Zrozumienie reakcji utleniania-redukcji, półogniw oraz bilansowania równań chemicznych. Obejmuje kluczowe pojęcia, takie jak stopnie utlenienia, elektrody, oraz przykłady reakcji redoks. Idealne materiały do nauki przed sprawdzianem.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Pierwiastki Chemiczne Bloku D
Blok d to fascynujący zbiór pierwiastków chemicznych, które odgrywają kluczową rolę w wielu procesach. W tych notatkach omówimy najważniejsze pierwiastki tego bloku: chrom, mangan, żelazo, miedź i cynk - poznając ich właściwości, związki i reakcje chemiczne.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_1.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Chrom - właściwości i związki
Chrom to srebrzyste, twarde ciało stałe należące do 6 grupy i 4 okresu układu okresowego. Ma konfigurację elektronową [Ar] 3d⁵ 4s¹. Pasywuje, czyli nie reaguje z kwasami utleniającymi jak stężony i rozcieńczony HNO₃ czy H₂SO₄.
Można go otrzymać metodą aluminotermii: Cr₂O₃ + 2Al → 2Cr + Al₂O₃. Chrom tworzy tlenki o różnych właściwościach - CrO (zasadowy), Cr₂O₃ (amfoteryczny) i CrO₃ (kwasowy). CrO₃ ma wyjątkową właściwość - reaguje zarówno z zasadami , jak i z kwasami w reakcji redoks .
Wodorotlenki chromu to między innymi Cr(OH)₂ (niebieski osad) i Cr(OH)₃ (zielony osad o charakterze amfoterycznym). Sole chromu (II) dają niebieski roztwór (np. CrCl₂), a sole chromu (III) - zielony roztwór (np. CrCl₃).
Warto zapamiętać! Związki chromu są barwne i łatwo je rozpoznać - związki Cr(II) są niebieskie, związki Cr(III) zielone, a związki Cr(VI) żółte lub pomarańczowe.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_2.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje chromu i jego związków
W zależności od środowiska, związki chromu mogą przechodzić różne przemiany. Cr₂O₇²⁻ jest nietrwały w środowisku zasadowym, a CrO₄²⁻ jest nietrwały w środowisku kwasowym. Dzięki temu można kontrolować formę, w jakiej występuje chrom.
Chrom (III) może przechodzić reakcje z kwasami i zasadami. W środowisku kwasowym: 2Cr(OH)₃ + 6H⁺ → 2Cr³⁺ + 6H₂O. W środowisku zasadowym może tworzyć hydroksokompleksy: Cr(OH)₃ + 3OH⁻ → [Cr(OH)₆]³⁻.
Związki chromu (III) pod wpływem utleniaczy mogą przechodzić w związki chromu (VI). Na przykład: 2[Cr(OH)₄]⁻ + 3H₂O₂ + 2OH⁻ → 2CrO₄²⁻ + 8H₂O. Towarzyszy temu zmiana barwy z zielonej na żółtą, co jest ważną obserwacją w analizie chemicznej.
Dichromian potasu (K₂Cr₂O₇) jest silnym utleniaczem i może utleniać wiele związków, np. w reakcji: Cr₂O₇²⁻ + 14H⁺ + 6Fe²⁺ → 6Fe³⁺ + 2Cr³⁺ + 7H₂O.
Pamiętaj! W reakcjach redoks z udziałem związków chromu zawsze zwracaj uwagę na zmianę barwy - to ważna wskazówka pokazująca, że doszło do zmiany stopnia utlenienia.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_3.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Mangan - właściwości i związki
Mangan to lekko różowe ciało stałe z 7 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 3d⁵ 4s². Podobnie jak chrom, można go otrzymać metodą aluminotermii: Mn₂O₃ + 2Al → 2Mn + Al₂O₃.
Mangan tworzy szereg tlenków o różnych właściwościach: MnO (zasadowy), Mn₂O₃ i MnO₂ (amfoteryczny), Mn₂O₇ (kwasowy). Tlenki manganu o wyższych stopniach utlenienia mają silne właściwości utleniające. Mn₂O₇ reaguje z zasadami: Mn₂O₇ + 2NaOH → 2NaMnO₄ + H₂O.
Wodorotlenek manganu (II) - Mn(OH)₂ to biały osad, który łatwo ulega utlenieniu tlenem z powietrza do związków manganu (III) i (IV). Związki manganu na różnych stopniach utlenienia mają charakterystyczne barwy: Mn²⁺ (bladopomarańczowy), MnO₄²⁻ (zielony), MnO₄⁻ (fioletowy), co ma ogromne znaczenie diagnostyczne.
Manganian (VII) potasu, czyli nadmanganian potasu (KMnO₄), jest silnym utleniaczem i w zależności od środowiska może redukować się do związków manganu na różnych stopniach utlenienia.
Ciekawostka! Nadmanganian potasu (KMnO₄) to popularny środek dezynfekujący znany jako "manganek" - jego intensywnie fioletowe roztwory łatwo odbarwiają się podczas reakcji redoks.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_4.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Żelazo - właściwości i związki
Żelazo to srebrzyste ciało stałe z 8 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s² 3d⁶. Ulega pasywacji w niektórych środowiskach, co chroni je przed dalszym utlenianiem. Można je otrzymać w reakcji redukcji tlenku żelaza węglem: C + FeO → CO + Fe.
Żelazo tworzy jony na dwóch głównych stopniach utlenienia: Fe²⁺ i Fe³⁺. Jon Fe³⁺ jest trwalszy, ponieważ ma mniej elektronów niesparowanych (wszystkie elektrony w orbitalu 3d są pojedynczo obsadzone).
Najważniejsze tlenki żelaza to: FeO (czarny, zasadowy), Fe₂O₃ (brunatny, amfoteryczny) i Fe₃O₄ (czarny magnetyt, mieszany tlenek FeO·Fe₂O₃). Żelazo reaguje z kwasami nieutleniającymi, np. Fe + 2HCl → FeCl₂ + H₂, ale ulega także reakcjom z kwasami utleniającymi i tlenem.
Wodorotlenki żelaza to Fe(OH)₂ i Fe(OH)₃ (rdzawobrązowy). Utlenianie Fe(OH)₂ tlenem z powietrza to reakcja: 4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃.
Praktyczna wskazówka! Rdzewienie żelaza to właśnie reakcja utleniania w obecności wody i tlenu z powietrza - dlatego metalowe konstrukcje trzeba chronić przed wilgocią i tlenem przez malowanie lub galwanizację.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_5.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Miedź - właściwości i związki
Miedź to charakterystyczny pomarańczowo-czerwony metal z 11 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s¹ 3d¹⁰. Jest plastyczna, kowalna i świetnie przewodzi prąd elektryczny, dlatego jest powszechnie używana w instalacjach elektrycznych.
W przeciwieństwie do większości metali, miedź nie reaguje z kwasami beztlenowymi (jak HCl) - nie wypiera wodoru z kwasów. Reaguje natomiast z kwasami utleniającymi w reakcjach redoks: 3Cu + 8HNO₃(rozc.) → 3Cu(NO₃)₂ + 2NO + 4H₂O (brunatny gaz) lub Cu + 4HNO₃(stęż.) → Cu(NO₃)₂ + 2NO₂ + 2H₂O.
Miedź reaguje również ze stężonym kwasem siarkowym: Cu + 2H₂SO₄ → CuSO₄ + SO₂ + 2H₂O. Tworzy związki głównie na stopniach utlenienia +1 i +2, przy czym związki miedzi (II) są znacznie trwalsze i bardziej powszechne.
Uwaga! Charakterystyczne zabarwienie związków miedzi (II) to intensywny niebieski kolor, co jest spowodowane obecnością jonów Cu²⁺. Zjawisko to wykorzystuje się w testach chemicznych na obecność miedzi.
](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c10-3b3e-725b-94a1-91ceacd5dd02_image_page_6.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Cynk - właściwości i związki
Cynk to błękitnobiały, kruchy metal z 12 grupy, 4 okresu, o konfiguracji elektronowej [Ar] 4s² 3d¹⁰. Dobrze przewodzi ciepło i prąd elektryczny. Jest pierwiastkiem amfoterycznym, co oznacza, że reaguje zarówno z kwasami, jak i z zasadami.
Tlenek cynku (ZnO), znany jako biel cynkowa, to białe ciało stałe powstające w reakcji: 2Zn + O₂ → 2ZnO. Jest związkiem amfoterycznym - reaguje z kwasami: ZnO + 2HCl → ZnCl₂ + H₂O, jak również z zasadami: ZnO + 2NaOH + H₂O → Na₂[Zn(OH)₄].
Cynk reaguje z kwasami, uwalniając wodór: Zn + 2HCl → ZnCl₂ + H₂. Wodorotlenek cynku Zn(OH)₂ to biały osad o właściwościach amfoterycznych, który można otrzymać w reakcji: ZnCl₂ + 2NaOH → Zn(OH)₂ + 2NaCl.
W środowisku silnie zasadowym cynk tworzy hydroksocynkany: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄] lub Na₂ZnO₂ + H₂O.
Praktyczne zastosowanie! Dzięki amfoteryczności cynk jest używany do galwanizacji (cynkowania) żelaza, co chroni je przed korozją. Nawet gdy warstwa cynku zostanie uszkodzona, nadal chroni żelazo, działając jako anoda ochronna.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Reakcje redoks
9Ogniwa Galwaniczne i Redoks
Zrozumienie ogniw galwanicznych, reakcji redoks oraz stopni utlenienia pierwiastków. Dowiedz się o korozji metali, metodach ochrony oraz zastosowaniach ogniw Daniella. Idealne dla uczniów chemii i studentów przygotowujących się do egzaminów.
Reguły Stopni Utlenienia
Zrozumienie stopni utlenienia pierwiastków chemicznych oraz ich roli w reakcjach redoks. Notatka obejmuje definicje, kluczowe zasady ustalania stopni utlenienia, przykłady oraz wyjaśnienia dotyczące utleniaczy i reduktorów. Idealna dla uczniów chemii.
Właściwości Metali D-Block
Zgłębiaj właściwości i reakcje metali bloku D, takich jak mangan, chrom, żelazo, miedź i cynk. Dowiedz się o ich związkach, amfoterycznych tlenkach oraz doświadczeniach laboratoryjnych. Idealne dla studentów chemii, którzy chcą zrozumieć chemiczne zachowanie metali i ich zastosowania.
Chemia Bloku D: Metale
Zgłębiaj charakterystykę metali bloku D, w tym srebra, cynku, żelaza i manganu. Dowiedz się o reakcjach chemicznych, stanach utlenienia oraz właściwościach amfoterycznych. Idealne materiały do nauki dla studentów chemii.
Elektrochemia: Zasady i Reakcje
Kompleksowe notatki z elektrochemii obejmujące kluczowe zagadnienia, takie jak reakcje redoks, prawo Faradaya, procesy elektrolizy oraz właściwości elektrolitów. Idealne dla uczniów przygotowujących się do egzaminów z chemii na poziomie rozszerzonym.
Pierwiastki bloku D
Pierwiastki bloku D : chrom, miedź, żelazo, cynk
Reakcje Redoks: Przykłady i Zasady
Zrozumienie reakcji redoks, w tym reakcji dysproporcjonowania i synproporcjonowania. Przykłady reakcji chemicznych, obliczanie stopni utlenienia oraz bilans elektronowy. Idealne dla studentów chemii, którzy chcą zgłębić temat utleniania i redukcji.
Redoks
Notatka do na nauki reakcji utleniania i redukcji do matury/na sprawdzian/ na karkówkę
Reakcje Redoks i Utlenianie
Zrozumienie reakcji utleniania-redukcji, półogniw oraz bilansowania równań chemicznych. Obejmuje kluczowe pojęcia, takie jak stopnie utlenienia, elektrody, oraz przykłady reakcji redoks. Idealne materiały do nauki przed sprawdzianem.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.