Teraz poznasz właściwości kluczowych pierwiastków z układu okresowego - od... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
4,810
•
Zaktualizowano May 23, 2026
•
:33
@shigsu
Teraz poznasz właściwości kluczowych pierwiastków z układu okresowego - od... Pokaż więcej









![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_1.webp&w=2048&q=75)
Glin to prawdziwy chameleон chemiczny - może reagować zarówno z kwasami, jak i zasadami! Ten srebrzyste metal z 13. grupy ma konfigurację [Ne] 3s² 3p¹ i posiada właściwości amfoteryczne.
Z kwasami zachowuje się jak typowy metal: 2 Al + 6HCl → 2 AlCl₃ + 3H₂. Ale uwaga - z zasadami też reaguje! Z wodorotlenkiem sodu tworzy kompleks: 2 Al + 2NaOH + 6H₂O → 2 Na[Al(OH)₄] + 3H₂.
Kwas siarkowy rozcieńczony daje normalną reakcję, ale stężony to już inna historia - powstaje SO₂ zamiast wodoru. Tlenek Al₂O₃ i wodorotlenek Al(OH)₃ to białe osady, które również są amfoteryczne.
Zapamiętaj: Glin nie reaguje ze stężonym HNO₃ - ulega pasywacji!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_2.webp&w=2048&q=75)
Węgiel z 14. grupy to absolutny mistrz chemii organicznej! Ma unikalną zdolność katenacji - tworzenia niesamowicie długich i stabilnych łańcuchów C-C. Dzięki temu powstają wszystkie węglowodory, jak metan CH₄.
Odmiany alotropowe węgla to prawdziwe ekstremalne przeciwieństwa. Diament - najtwardszy, bezbarwny, nie przewodzi prądu. Grafit - miękki, kruchy, doskonale przewodzi. Grafen - płaska struktura jak plaster miodu, supermocarny i przewodzący.
Fulereny to fascynujące "piłki" złożone z 28-1500 atomów węgla. Mają metaliczny połysk i mogą być nadprzewodnikami! CO₂ otrzymujesz z węglanów: Na₂CO₃ + 2HCl → 2NaCl + CO₂ + H₂O.
Uwaga: CO to śmiertelnie niebezpieczny czad - bezwonny i bezbarwny!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_3.webp&w=2048&q=75)
Krzem to sąsiad węgla z 14. grupy (3. okres), ale ma zupełnie inny charakter. Ten połyskujący półmetal o konfiguracji [Ne] 3s² 3p² jest głównym składnikiem piasku i szkła.
Krzemionka SiO₂ to prawdziwa twierdza - reaguje tylko z fluorowodorem na zimno i zasadami na gorąco. Równanie SiO₂ + 4HF → SiF₄ + 2H₂O to sposób na trawienie szkła!
Kwas metakremowy H₂SiO₃ to biały, galaretowaty osad o charakterze kwaśnym. Otrzymujesz go z krzemianów: Na₂SiO₃ + 2HCl → H₂SiO₃ + 2NaCl. Krzem otrzymujesz redukcją magnezem z krzemionki.
Ciekawostka: Reakcja z HF służy do pisania na szkle - dlatego kwas fluorowodorowy przechowuje się w plastiku!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_4.webp&w=2048&q=75)
Cyna z 14. grupy (5. okres) to srebrzysto-biały metal o konfiguracji [Kr]4d¹⁰5s²5p². Ma właściwości amfoteryczne i służy jako protektor przed korozją.
Z mocnymi kwasami reaguje normalnie: Sn + 2HCl → SnCl₂ + H₂, ale z zasadami tworzy kompleksy: Sn + 2NaOH + 4H₂O → Na₂[Sn(OH)₆] + 2H₂. Kwas azotowy daje różne produkty zależnie od stężenia.
Fluorek cyny(II) SnF₂ znajdziesz w pastach do zębów - ma właściwości antybakteryjne! W wysokiej temperaturze tlenek cyny(II) ulega reakcji dysproporcjonowania: 2SnO → SnO₂ + Sn.
Zastosowanie: Cyna pokrywa puszki konserwowe, chroniąc je przed rdzą!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_5.webp&w=2048&q=75)
Azot z 15. grupy to 78% powietrza, którym oddychasz! Ten bezbarwny, bezwonny gaz o konfiguracji [He] 2s² 2p³ jest podstawą wszystkich białek.
Tlenki azotu to prawdziwa kolekcja chemicznych osobowości. N₂O - obojętny "gaz rozweselający", NO - bezbarwny, ale brunatniejący na powietrzu, NO₂ - brunatny, toksyczny i kwaśny. Równanie 2NO + O₂ → 2NO₂ pokazuje, dlaczego NO brązowieje.
Kwas azotowy(V) w różnych stężeniach daje różne produkty z miedzią. Stężony tworzy brunatny NO₂, rozcieńczony - bezbarwny NO. Bezwodniki N₂O₃ i N₂O₅ z wodą dają odpowiednio HNO₂ i HNO₃.
Rozpoznawanie: Brunatny gaz = NO₂ ze stężonego HNO₃, bezbarwny = NO z rozcieńczonego!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_6.webp&w=2048&q=75)
Amoniak NH₃ to bezbarwny gaz o charakterystycznym, ostrym zapachu. W wodzie zachowuje się jak zasada: NH₃ + H₂O → NH₄⁺ + OH⁻. Otrzymujesz go podgrzewając chlorek amonu z wodorotlenkiem: NH₄Cl + NaOH → NH₃ + NaCl + H₂O.
Azotany to prawdziwe chemiczne złoto - wszystkie są doskonale rozpuszczalne w wodzie i mają silne właściwości utleniające. Znajdziesz je jako saletry: amonową NH₄NO₃, potasową KNO₃, sodową NaNO₃.
Azot wchodzi w skład najważniejszych związków organicznych: amin, amidów, aminokwasów i białek. Te związki tworzą podstawę życia na Ziemi!
Pamiętaj: Wszystkie azotany są rozpuszczalne - to jedna z najważniejszych zasad rozpuszczalności!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_7.webp&w=2048&q=75)
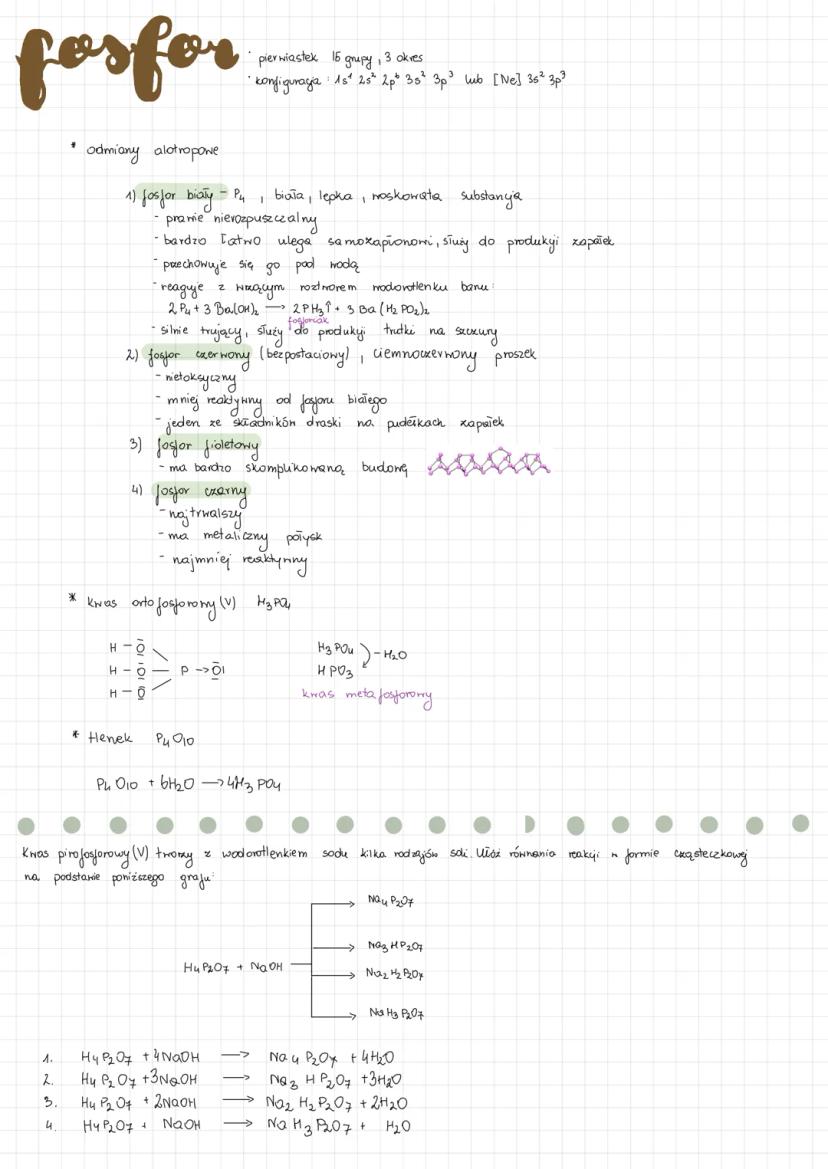
Fosfor ma cztery twarze - od śmiertelnie niebezpiecznego białego do stabilnego czarnego. Fosfor biały P₄ to lepka, woskowana substancja, która samozapala się na powietrzu - dlatego przechowuje się go pod wodą!
Fosfor czerwony to ciemnoczerwony proszek na pudełkach zapałek - nietoksyczny i mniej reaktywny. Fosfor czarny to najtrwalszy, z metalicznym połyskiem, a fioletowy ma bardzo skomplikowaną strukturę.
Kwas ortofosforowy(V) H₃PO₄ powstaje z tlenku: P₄O₁₀ + 6H₂O → 4H₃PO₄. Może tworzyć różne sole z NaOH - od Na₄P₂O₇ (4 mole NaOH) do NaH₃P₂O₇ (1 mol NaOH).
Bezpieczeństwo: Fosfor biały to śmiertelna trucizna - jeden z najniebezpieczniejszych pierwiastków!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_8.webp&w=2048&q=75)
Siarka z 16. grupy to jasnożółte ciało stałe o konfiguracji [Ne]3s²3p⁴. Spala się charakterystycznym niebieskim płomieniem, tworząc SO₂ - bezbarwny gaz o gryzącym zapachu.
Tlenki siarki pokazują jej różne oblicza. SO₂ (IV) to bakteriobójczy gaz, który z wodą daje słaby kwas: SO₂ + H₂O ⇌ H₂SO₃. SO₃ (VI) to bezbarwna ciecz, która gwałtownie reaguje z wodą: SO₃ + H₂O → H₂SO₄.
Kwas siarkowy(VI) H₂SO₄ to jeden z najmocniejszych kwasów - bezbarwna, gęsta, higroskopijny. W stężeniu jest silnym utleniaczem: 2H₂SO₄ + Cu → CuSO₄ + SO₂ + 2H₂O. Siarkowodór H₂S to trujący gaz o zapachu zgniłych jaj.
Uwaga: H₂SO₄ niszczy białka - nigdy nie dodawaj wody do kwasu, tylko kwas do wody!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_9.webp&w=2048&q=75)
Chlor z 17. grupy to żółtozielony, duszący i toksyczny gaz o konfiguracji [Ne] 3s² 3p⁵. Jest bardzo reaktywny i ma silne właściwości utleniające - występuje jako dwuatomowe cząsteczki Cl₂.
Stopnie utlenienia chloru tworzą kompletną rodzinę kwasów: od najsłabszego HClO do najmocniejszego HClO₄. Moc rośnie ze stopniem utlenienia: HClO < HClO₂ < HClO₃ < HClO₄.
Kwas solny HCl to silnie żrący, przezroczysty kwas, który znajdziesz w swoim żołądku! Metale przed wodorem w szeregu aktywności wypierają z niego wodór: Zn + 2HCl → ZnCl₂ + H₂.
Pamiętaj: Równomolowa mieszanina tlenków chloru z wodą daje dwa kwasy: 2Cl₂O₂ + H₂O → HClO₂ + HClO₃!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_10.webp&w=2048&q=75)
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
:33
@shigsu
Teraz poznasz właściwości kluczowych pierwiastków z układu okresowego - od amfoterycznego glinu, przez wszechstronny węgiel, aż po reaktywne halogeny. Te pierwiastki otaczają cię na co dzień i pojawiają się w większości zadań z chemii!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_1.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Glin to prawdziwy chameleон chemiczny - może reagować zarówno z kwasami, jak i zasadami! Ten srebrzyste metal z 13. grupy ma konfigurację [Ne] 3s² 3p¹ i posiada właściwości amfoteryczne.
Z kwasami zachowuje się jak typowy metal: 2 Al + 6HCl → 2 AlCl₃ + 3H₂. Ale uwaga - z zasadami też reaguje! Z wodorotlenkiem sodu tworzy kompleks: 2 Al + 2NaOH + 6H₂O → 2 Na[Al(OH)₄] + 3H₂.
Kwas siarkowy rozcieńczony daje normalną reakcję, ale stężony to już inna historia - powstaje SO₂ zamiast wodoru. Tlenek Al₂O₃ i wodorotlenek Al(OH)₃ to białe osady, które również są amfoteryczne.
Zapamiętaj: Glin nie reaguje ze stężonym HNO₃ - ulega pasywacji!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_2.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Węgiel z 14. grupy to absolutny mistrz chemii organicznej! Ma unikalną zdolność katenacji - tworzenia niesamowicie długich i stabilnych łańcuchów C-C. Dzięki temu powstają wszystkie węglowodory, jak metan CH₄.
Odmiany alotropowe węgla to prawdziwe ekstremalne przeciwieństwa. Diament - najtwardszy, bezbarwny, nie przewodzi prądu. Grafit - miękki, kruchy, doskonale przewodzi. Grafen - płaska struktura jak plaster miodu, supermocarny i przewodzący.
Fulereny to fascynujące "piłki" złożone z 28-1500 atomów węgla. Mają metaliczny połysk i mogą być nadprzewodnikami! CO₂ otrzymujesz z węglanów: Na₂CO₃ + 2HCl → 2NaCl + CO₂ + H₂O.
Uwaga: CO to śmiertelnie niebezpieczny czad - bezwonny i bezbarwny!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_3.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Krzem to sąsiad węgla z 14. grupy (3. okres), ale ma zupełnie inny charakter. Ten połyskujący półmetal o konfiguracji [Ne] 3s² 3p² jest głównym składnikiem piasku i szkła.
Krzemionka SiO₂ to prawdziwa twierdza - reaguje tylko z fluorowodorem na zimno i zasadami na gorąco. Równanie SiO₂ + 4HF → SiF₄ + 2H₂O to sposób na trawienie szkła!
Kwas metakremowy H₂SiO₃ to biały, galaretowaty osad o charakterze kwaśnym. Otrzymujesz go z krzemianów: Na₂SiO₃ + 2HCl → H₂SiO₃ + 2NaCl. Krzem otrzymujesz redukcją magnezem z krzemionki.
Ciekawostka: Reakcja z HF służy do pisania na szkle - dlatego kwas fluorowodorowy przechowuje się w plastiku!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_4.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Cyna z 14. grupy (5. okres) to srebrzysto-biały metal o konfiguracji [Kr]4d¹⁰5s²5p². Ma właściwości amfoteryczne i służy jako protektor przed korozją.
Z mocnymi kwasami reaguje normalnie: Sn + 2HCl → SnCl₂ + H₂, ale z zasadami tworzy kompleksy: Sn + 2NaOH + 4H₂O → Na₂[Sn(OH)₆] + 2H₂. Kwas azotowy daje różne produkty zależnie od stężenia.
Fluorek cyny(II) SnF₂ znajdziesz w pastach do zębów - ma właściwości antybakteryjne! W wysokiej temperaturze tlenek cyny(II) ulega reakcji dysproporcjonowania: 2SnO → SnO₂ + Sn.
Zastosowanie: Cyna pokrywa puszki konserwowe, chroniąc je przed rdzą!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_5.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Azot z 15. grupy to 78% powietrza, którym oddychasz! Ten bezbarwny, bezwonny gaz o konfiguracji [He] 2s² 2p³ jest podstawą wszystkich białek.
Tlenki azotu to prawdziwa kolekcja chemicznych osobowości. N₂O - obojętny "gaz rozweselający", NO - bezbarwny, ale brunatniejący na powietrzu, NO₂ - brunatny, toksyczny i kwaśny. Równanie 2NO + O₂ → 2NO₂ pokazuje, dlaczego NO brązowieje.
Kwas azotowy(V) w różnych stężeniach daje różne produkty z miedzią. Stężony tworzy brunatny NO₂, rozcieńczony - bezbarwny NO. Bezwodniki N₂O₃ i N₂O₅ z wodą dają odpowiednio HNO₂ i HNO₃.
Rozpoznawanie: Brunatny gaz = NO₂ ze stężonego HNO₃, bezbarwny = NO z rozcieńczonego!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_6.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Amoniak NH₃ to bezbarwny gaz o charakterystycznym, ostrym zapachu. W wodzie zachowuje się jak zasada: NH₃ + H₂O → NH₄⁺ + OH⁻. Otrzymujesz go podgrzewając chlorek amonu z wodorotlenkiem: NH₄Cl + NaOH → NH₃ + NaCl + H₂O.
Azotany to prawdziwe chemiczne złoto - wszystkie są doskonale rozpuszczalne w wodzie i mają silne właściwości utleniające. Znajdziesz je jako saletry: amonową NH₄NO₃, potasową KNO₃, sodową NaNO₃.
Azot wchodzi w skład najważniejszych związków organicznych: amin, amidów, aminokwasów i białek. Te związki tworzą podstawę życia na Ziemi!
Pamiętaj: Wszystkie azotany są rozpuszczalne - to jedna z najważniejszych zasad rozpuszczalności!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_7.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Fosfor ma cztery twarze - od śmiertelnie niebezpiecznego białego do stabilnego czarnego. Fosfor biały P₄ to lepka, woskowana substancja, która samozapala się na powietrzu - dlatego przechowuje się go pod wodą!
Fosfor czerwony to ciemnoczerwony proszek na pudełkach zapałek - nietoksyczny i mniej reaktywny. Fosfor czarny to najtrwalszy, z metalicznym połyskiem, a fioletowy ma bardzo skomplikowaną strukturę.
Kwas ortofosforowy(V) H₃PO₄ powstaje z tlenku: P₄O₁₀ + 6H₂O → 4H₃PO₄. Może tworzyć różne sole z NaOH - od Na₄P₂O₇ (4 mole NaOH) do NaH₃P₂O₇ (1 mol NaOH).
Bezpieczeństwo: Fosfor biały to śmiertelna trucizna - jeden z najniebezpieczniejszych pierwiastków!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_8.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Siarka z 16. grupy to jasnożółte ciało stałe o konfiguracji [Ne]3s²3p⁴. Spala się charakterystycznym niebieskim płomieniem, tworząc SO₂ - bezbarwny gaz o gryzącym zapachu.
Tlenki siarki pokazują jej różne oblicza. SO₂ (IV) to bakteriobójczy gaz, który z wodą daje słaby kwas: SO₂ + H₂O ⇌ H₂SO₃. SO₃ (VI) to bezbarwna ciecz, która gwałtownie reaguje z wodą: SO₃ + H₂O → H₂SO₄.
Kwas siarkowy(VI) H₂SO₄ to jeden z najmocniejszych kwasów - bezbarwna, gęsta, higroskopijny. W stężeniu jest silnym utleniaczem: 2H₂SO₄ + Cu → CuSO₄ + SO₂ + 2H₂O. Siarkowodór H₂S to trujący gaz o zapachu zgniłych jaj.
Uwaga: H₂SO₄ niszczy białka - nigdy nie dodawaj wody do kwasu, tylko kwas do wody!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_9.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Chlor z 17. grupy to żółtozielony, duszący i toksyczny gaz o konfiguracji [Ne] 3s² 3p⁵. Jest bardzo reaktywny i ma silne właściwości utleniające - występuje jako dwuatomowe cząsteczki Cl₂.
Stopnie utlenienia chloru tworzą kompletną rodzinę kwasów: od najsłabszego HClO do najmocniejszego HClO₄. Moc rośnie ze stopniem utlenienia: HClO < HClO₂ < HClO₃ < HClO₄.
Kwas solny HCl to silnie żrący, przezroczysty kwas, który znajdziesz w swoim żołądku! Metale przed wodorem w szeregu aktywności wypierają z niego wodór: Zn + 2HCl → ZnCl₂ + H₂.
Pamiętaj: Równomolowa mieszanina tlenków chloru z wodą daje dwa kwasy: 2Cl₂O₂ + H₂O → HClO₂ + HClO₃!
![# blok p
glin
* pierwiastek 13 grupy, 3 okres
* konfiguragia $1s^2 2s^2 2p^6 3s^2 3p^1$ lub $[Ne] 3s^2 3p^1$
* sreboxyste ciało staj](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018e8c0f-7fbe-772b-a921-947df01352c3_image_page_10.webp&w=2048&q=75)
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
101
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS