Chemia bloków s to fascynujący dział nauki o pierwiastkach, który... Pokaż więcej
Pierwiastki z bloku s









Wodór - najprostszy pierwiastek
Wodór to wyjątkowy pierwiastek należący do 1 grupy, 1 okresu układu okresowego. Posiada najprostszą konfigurację elektronową (1s¹) i występuje jako bezbarwny, bezwonny gaz, który jest palny. Jest niemetalem i doskonałym przewodnikiem ciepła.
Wodór można otrzymać na kilka sposobów. Jednym z nich jest reakcja węgla z parą wodną lub metan z parą wodną . W roztworach wodnych jon H⁺ ulega hydratacji, tworząc kation hydroksoniowy (H₃O⁺).
Wodór występuje w trzech izotopach: prot (¹H) zawierający tylko proton, deuter (²H) z protonem i neutronem, oraz tryt (³H) z protonem i dwoma neutronami. Tylko tryt jest izotopem niestabilnym, pozostałe są stabilne.
Warto zapamiętać! Wodór tworzy różne tlenki, w tym wodę (H₂O), nadtlenek wodoru (H₂O₂) będący silnym utleniaczem i substancją żrącą, oraz nietrwały tritlenek wodoru (H₂O₃).

Lit - najlżejszy metal
Lit to pierwiastek 1 grupy, 2 okresu o konfiguracji elektronowej 1s²2s¹ lub [He]2s¹. Jest miękkim, srebrzystym metalem, który pali się charakterystycznym karminowym płomieniem. Ze względu na dużą reaktywność przechowuje się go pod warstwą parafiny.
Jako najlżejszy metal lit unosi się na wodzie i reaguje z nią, tworząc wodorotlenek litu i wodór . Wyjątkową właściwością litu jest zdolność do reagowania z azotem w warunkach normalnych , czego nie potrafią inne metale.
Lit tworzy różne związki chemiczne, w tym tlenki i sole. LiCl i LiBr są silnie higroskopijne, a stały LiOH stosuje się do usuwania CO₂ z powietrza w statkach kosmicznych .
Ciekawostka! Azotek litu reaguje z wodą, tworząc wodorotlenek litu i amoniak , co jest wyjątkową reakcją wśród związków azotu.

Sód - metal o wszechstronnym zastosowaniu
Sód to srebrzystobiały, miękki metal z 1 grupy, 3 okresu o konfiguracji elektronowej [Ne]3s¹. Jest niezwykle reaktywny i musi być przechowywany w nafcie, aby zapobiec jego reakcji z tlenem z powietrza. Charakterystycznie pali się żółtym płomieniem.
Metaliczny sód można otrzymać poprzez redukcję węglanu sodu węglem . Z wodą reaguje gwałtownie, wydzielając wodór i tworząc silną zasadę - wodorotlenek sodu . Jest to reakcja egzotermiczna, wydzielająca dużo energii.
Sód tworzy różne tlenki: tlenek sodu (Na₂O) i nadtlenek sodu (Na₂O₂). Wszystkie tlenki sodu reagują z wodą, dając roztwory o odczynie zasadowym . Z kwasami tworzą sole i wodę, co potwierdza ich zasadowy charakter.
Uwaga chemiku! Sód reaguje z alkoholami, tworząc alkoholany, np. z metanolem powstaje metanolan sodu . Te związki są ważnymi odczynnikami w syntezie organicznej.
Reakcje sodu i jego związków
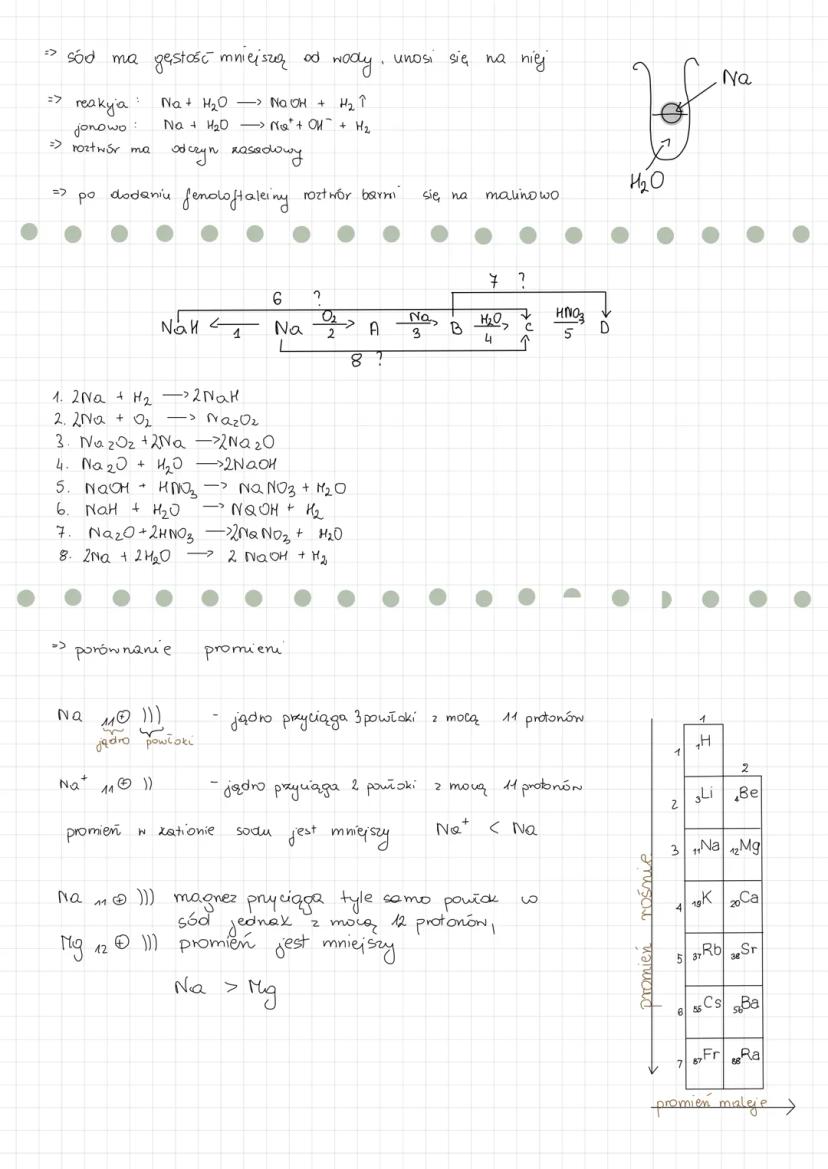
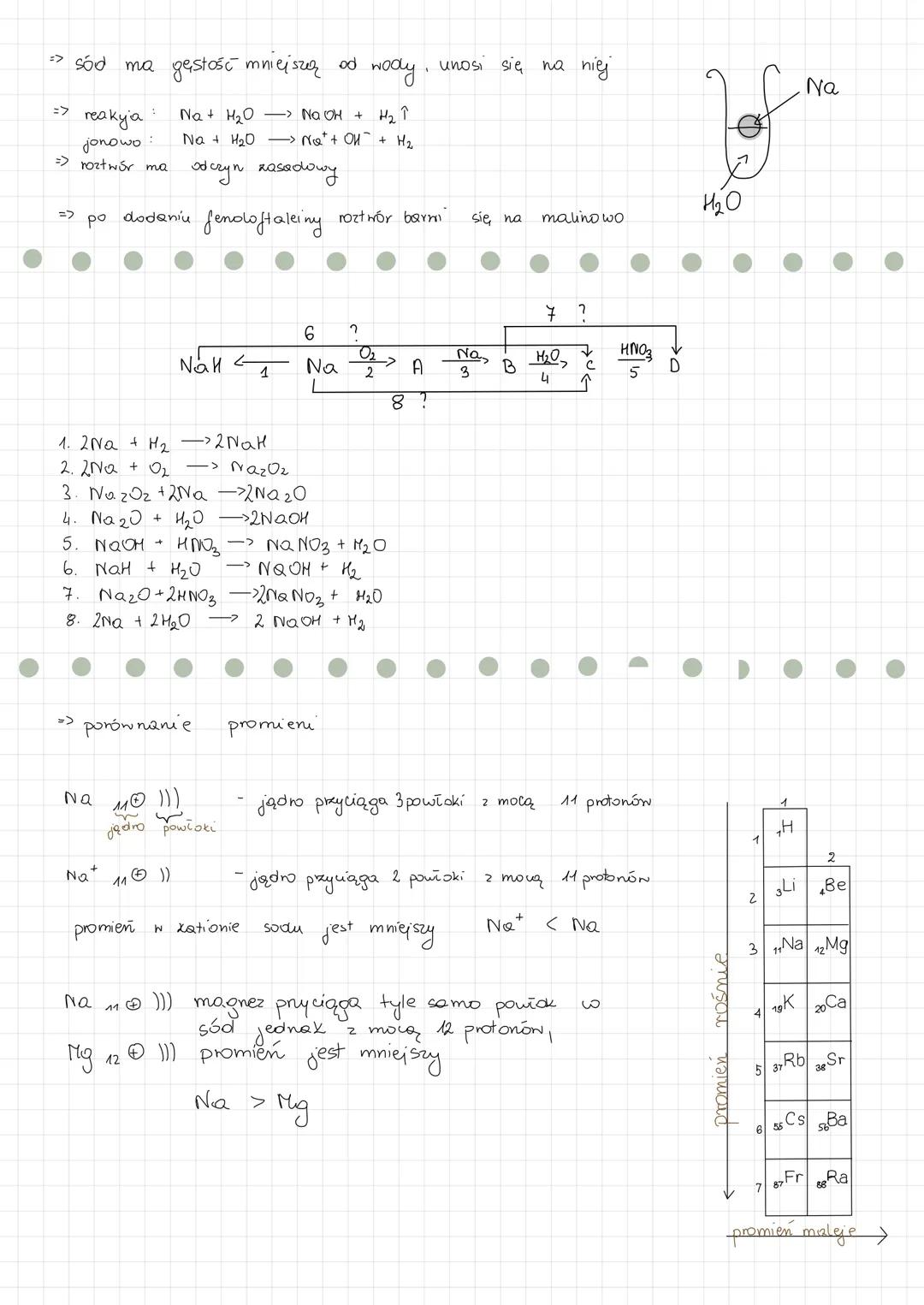
Sód ma gęstość mniejszą od wody, dlatego unosi się na jej powierzchni. Podczas tej reakcji powstaje wodorotlenek sodu, wodór i wydziela się dużo ciepła . Roztwór po tej reakcji ma odczyn zasadowy i barwi fenoloftaleinę na malinowo.
Sód tworzy cały szereg związków poprzez różne reakcje chemiczne. Reaguje z wodorem, tworząc wodorek sodu , z tlenem dając nadtlenek sodu , który można dalej przekształcić w tlenek sodu .
Porównanie wielkości atomów i jonów jest istotne dla zrozumienia właściwości chemicznych pierwiastków. Kation sodu (Na⁺) ma mniejszy promień niż atom sodu, ponieważ jądro przyciąga mniej powłok elektronowych z tą samą mocą 11 protonów. Z kolei atom sodu ma większy promień niż atom magnezu, mimo że znajdują się obok siebie w układzie okresowym.
Zapamiętaj to! Sód reaguje z wodą, tworząc roztwór o odczynie zasadowym, co łatwo wykryć za pomocą fenoloftaleiny - wskaźnika, który zabarwia się na malinowo w środowisku zasadowym.

Potas - niezwykle reaktywny metal
Potas to pierwiastek 1 grupy, 4 okresu o konfiguracji elektronowej [Ar]4s¹. Jest miękkim, srebrzystobiałym metalem, który charakteryzuje się wyjątkową reaktywnością. Pali się różowo-fioletowym płomieniem, co pozwala na jego identyfikację.
Ze względu na wysoką reaktywność potas przechowuje się w naczyniach z naftą. W kontakcie z wodą lub kwasami często zapala się, a nawet może wybuchać . Ta reakcja jest silnie egzotermiczna, co oznacza, że wydziela dużo energii.
Podobnie jak inne metale grupy 1, potas tworzy różne tlenki, np. nadtlenek potasu . Tlenki te reagują z wodą, dając roztwory o odczynie zasadowym . Z kwasami reagują, tworząc odpowiednie sole i wodę.
Pamiętaj! Potas tworzy alkoholany w reakcji z alkoholami , które są silnymi zasadami stosowanymi w syntezie organicznej. Ważnym związkiem potasu jest też saletra potasowa (KNO₃).

Beryl - wyjątkowy metal amfoteryczny
Beryl to pierwiastek 2 grupy, 2 okresu o konfiguracji elektronowej [He]2s². Jest twardym, lekkim i kruchym metalem o stalowoszarej barwie. Jego wyjątkowość polega na tym, że jest jedynym amfoterycznym pierwiastkiem bloku s, czyli reaguje zarówno z kwasami, jak i z zasadami.
Amfoteryczny charakter berylu potwierdza jego reakcja z kwasem oraz z zasadą . Podobnie zachowują się jego tlenek (BeO) i wodorotlenek (Be(OH)₂). W reakcjach z zasadami tworzą się związki kompleksowe o liczbie koordynacyjnej 4.
Wodorotlenek berylu otrzymuje się w reakcji chlorku berylu z wodorotlenkiem sodu . Jest to białe ciało stałe, które podczas ogrzewania rozkłada się do tlenku berylu i wody .
Ciekawostka! W przeciwieństwie do wodorotlenku magnezu (Mg(OH)₂), który reaguje tylko z kwasami, wodorotlenek berylu (Be(OH)₂) reaguje zarówno z kwasami, jak i z zasadami, co jest dowodem jego amfoterycznego charakteru.

Magnez - metal o szerokim zastosowaniu
Magnez to srebrzystobiałe ciało stałe należące do 2 grupy, 3 okresu o konfiguracji elektronowej [Ne]3s². Jest metalem ziem alkalicznych, który pali się oślepiającym, białym płomieniem. Ten spektakularny efekt często wykorzystuje się w pirotechnice.
Magnez można otrzymać przez redukcję tlenku magnezu węglem w wysokiej temperaturze . Spala się w powietrzu, tworząc tlenek magnezu i azotek magnezu . Tlenek magnezu to biały proszek, który reaguje z wodą, tworząc wodorotlenek magnezu.
Jony magnezu (Mg²⁺) wraz z jonami wapnia (Ca²⁺) wchodzą w skład twardej wody, powodując osadzanie się kamienia. Można je usunąć, dodając jony węglanowe, które tworzą nierozpuszczalny węglan magnezu .
Warto wiedzieć! Siarczan magnezu (MgSO₄), znany jako sól gorzka, ma szerokie zastosowanie medyczne - działa przeczyszczająco i obniża ciśnienie krwi. Powstaje w reakcji wodorotlenku magnezu z kwasem siarkowym .

Wapń - budulec kości i skał
Wapń to srebrzystobiałe ciało stałe z 2 grupy, 4 okresu o konfiguracji elektronowej [Ar]4s². Jest ważnym pierwiastkiem w przyrodzie, występującym głównie w postaci węglanu wapnia (CaCO₃). Barwi płomień na charakterystyczny ceglastoczerwony kolor.
Wapń można otrzymać w reakcji tlenku wapnia z glinem . Węglan wapnia pod wpływem wysokiej temperatury rozkłada się do tlenku wapnia, zwanego wapnem palonym . Ten z kolei reaguje z wodą, tworząc wodorotlenek wapnia, czyli wapno gaszone .
Woda wapienna (nasycony roztwór Ca(OH)₂) mętnieje w kontakcie z dwutlenkiem węgla, co jest reakcją charakterystyczną dla wykrywania CO₂ . Gips budowlany powstaje w wyniku reakcji uwodnienia półwodnego siarczanu wapnia .
Pamiętaj! Karbid reaguje z wodą, tworząc acetylen i wodorotlenek wapnia . Ta reakcja była dawniej wykorzystywana do wytwarzania gazu do lamp górniczych.

Reakcje i zastosowania związków wapnia
Sole wapnia i magnezu często występują jako trudnorozpuszczalne osady. Można je otrzymać w reakcji rozpuszczalnych chlorków z węglanem sodu: CaCl₂ + Na₂CO₃ → CaCO₃↓ + 2NaCl oraz MgCl₂ + Na₂CO₃ → MgCO₃↓ + 2NaCl. Te reakcje strąceniowe są podstawą usuwania twardości wody.
Wapń tworzy szereg użytecznych związków. Z wodą reaguje, wydzielając wodór i tworząc wodorotlenek wapnia . Diwodorofosforan wapnia reaguje z tlenkiem wapnia, tworząc fosforan wapnia i wodę .
Zawartość wody w kryształach ma znaczący wpływ na właściwości minerałów. Gips dwuwodny (CaSO₄·2H₂O) zawiera 26,5% wody, podczas gdy gips półwodny ((CaSO₄)₂·H₂O) tylko 6,62%. Ta różnica wpływa na ich właściwości budowlane i czas twardnienia.
Ciekawostka praktyczna! Tlenek wapnia (CaO) reaguje z kwasami, tworząc sole i wodę, natomiast z wodą reaguje, tworząc wodorotlenek wapnia o silnie zasadowym odczynie. Ta właściwość czyni go cennym składnikiem w przemyśle budowlanym i rolnictwie.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: silna zasada
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Pierwiastki z bloku s
Chemia bloków s to fascynujący dział nauki o pierwiastkach, który pozwala zrozumieć podstawowe właściwości i reakcje kluczowych pierwiastków układu okresowego. Poznanie tych pierwiastków pomoże Ci wyjaśnić wiele zjawisk chemicznych spotykanych w codziennym życiu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wodór - najprostszy pierwiastek
Wodór to wyjątkowy pierwiastek należący do 1 grupy, 1 okresu układu okresowego. Posiada najprostszą konfigurację elektronową (1s¹) i występuje jako bezbarwny, bezwonny gaz, który jest palny. Jest niemetalem i doskonałym przewodnikiem ciepła.
Wodór można otrzymać na kilka sposobów. Jednym z nich jest reakcja węgla z parą wodną lub metan z parą wodną . W roztworach wodnych jon H⁺ ulega hydratacji, tworząc kation hydroksoniowy (H₃O⁺).
Wodór występuje w trzech izotopach: prot (¹H) zawierający tylko proton, deuter (²H) z protonem i neutronem, oraz tryt (³H) z protonem i dwoma neutronami. Tylko tryt jest izotopem niestabilnym, pozostałe są stabilne.
Warto zapamiętać! Wodór tworzy różne tlenki, w tym wodę (H₂O), nadtlenek wodoru (H₂O₂) będący silnym utleniaczem i substancją żrącą, oraz nietrwały tritlenek wodoru (H₂O₃).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Lit - najlżejszy metal
Lit to pierwiastek 1 grupy, 2 okresu o konfiguracji elektronowej 1s²2s¹ lub [He]2s¹. Jest miękkim, srebrzystym metalem, który pali się charakterystycznym karminowym płomieniem. Ze względu na dużą reaktywność przechowuje się go pod warstwą parafiny.
Jako najlżejszy metal lit unosi się na wodzie i reaguje z nią, tworząc wodorotlenek litu i wodór . Wyjątkową właściwością litu jest zdolność do reagowania z azotem w warunkach normalnych , czego nie potrafią inne metale.
Lit tworzy różne związki chemiczne, w tym tlenki i sole. LiCl i LiBr są silnie higroskopijne, a stały LiOH stosuje się do usuwania CO₂ z powietrza w statkach kosmicznych .
Ciekawostka! Azotek litu reaguje z wodą, tworząc wodorotlenek litu i amoniak , co jest wyjątkową reakcją wśród związków azotu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Sód - metal o wszechstronnym zastosowaniu
Sód to srebrzystobiały, miękki metal z 1 grupy, 3 okresu o konfiguracji elektronowej [Ne]3s¹. Jest niezwykle reaktywny i musi być przechowywany w nafcie, aby zapobiec jego reakcji z tlenem z powietrza. Charakterystycznie pali się żółtym płomieniem.
Metaliczny sód można otrzymać poprzez redukcję węglanu sodu węglem . Z wodą reaguje gwałtownie, wydzielając wodór i tworząc silną zasadę - wodorotlenek sodu . Jest to reakcja egzotermiczna, wydzielająca dużo energii.
Sód tworzy różne tlenki: tlenek sodu (Na₂O) i nadtlenek sodu (Na₂O₂). Wszystkie tlenki sodu reagują z wodą, dając roztwory o odczynie zasadowym . Z kwasami tworzą sole i wodę, co potwierdza ich zasadowy charakter.
Uwaga chemiku! Sód reaguje z alkoholami, tworząc alkoholany, np. z metanolem powstaje metanolan sodu . Te związki są ważnymi odczynnikami w syntezie organicznej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje sodu i jego związków
Sód ma gęstość mniejszą od wody, dlatego unosi się na jej powierzchni. Podczas tej reakcji powstaje wodorotlenek sodu, wodór i wydziela się dużo ciepła . Roztwór po tej reakcji ma odczyn zasadowy i barwi fenoloftaleinę na malinowo.
Sód tworzy cały szereg związków poprzez różne reakcje chemiczne. Reaguje z wodorem, tworząc wodorek sodu , z tlenem dając nadtlenek sodu , który można dalej przekształcić w tlenek sodu .
Porównanie wielkości atomów i jonów jest istotne dla zrozumienia właściwości chemicznych pierwiastków. Kation sodu (Na⁺) ma mniejszy promień niż atom sodu, ponieważ jądro przyciąga mniej powłok elektronowych z tą samą mocą 11 protonów. Z kolei atom sodu ma większy promień niż atom magnezu, mimo że znajdują się obok siebie w układzie okresowym.
Zapamiętaj to! Sód reaguje z wodą, tworząc roztwór o odczynie zasadowym, co łatwo wykryć za pomocą fenoloftaleiny - wskaźnika, który zabarwia się na malinowo w środowisku zasadowym.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Potas - niezwykle reaktywny metal
Potas to pierwiastek 1 grupy, 4 okresu o konfiguracji elektronowej [Ar]4s¹. Jest miękkim, srebrzystobiałym metalem, który charakteryzuje się wyjątkową reaktywnością. Pali się różowo-fioletowym płomieniem, co pozwala na jego identyfikację.
Ze względu na wysoką reaktywność potas przechowuje się w naczyniach z naftą. W kontakcie z wodą lub kwasami często zapala się, a nawet może wybuchać . Ta reakcja jest silnie egzotermiczna, co oznacza, że wydziela dużo energii.
Podobnie jak inne metale grupy 1, potas tworzy różne tlenki, np. nadtlenek potasu . Tlenki te reagują z wodą, dając roztwory o odczynie zasadowym . Z kwasami reagują, tworząc odpowiednie sole i wodę.
Pamiętaj! Potas tworzy alkoholany w reakcji z alkoholami , które są silnymi zasadami stosowanymi w syntezie organicznej. Ważnym związkiem potasu jest też saletra potasowa (KNO₃).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Beryl - wyjątkowy metal amfoteryczny
Beryl to pierwiastek 2 grupy, 2 okresu o konfiguracji elektronowej [He]2s². Jest twardym, lekkim i kruchym metalem o stalowoszarej barwie. Jego wyjątkowość polega na tym, że jest jedynym amfoterycznym pierwiastkiem bloku s, czyli reaguje zarówno z kwasami, jak i z zasadami.
Amfoteryczny charakter berylu potwierdza jego reakcja z kwasem oraz z zasadą . Podobnie zachowują się jego tlenek (BeO) i wodorotlenek (Be(OH)₂). W reakcjach z zasadami tworzą się związki kompleksowe o liczbie koordynacyjnej 4.
Wodorotlenek berylu otrzymuje się w reakcji chlorku berylu z wodorotlenkiem sodu . Jest to białe ciało stałe, które podczas ogrzewania rozkłada się do tlenku berylu i wody .
Ciekawostka! W przeciwieństwie do wodorotlenku magnezu (Mg(OH)₂), który reaguje tylko z kwasami, wodorotlenek berylu (Be(OH)₂) reaguje zarówno z kwasami, jak i z zasadami, co jest dowodem jego amfoterycznego charakteru.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Magnez - metal o szerokim zastosowaniu
Magnez to srebrzystobiałe ciało stałe należące do 2 grupy, 3 okresu o konfiguracji elektronowej [Ne]3s². Jest metalem ziem alkalicznych, który pali się oślepiającym, białym płomieniem. Ten spektakularny efekt często wykorzystuje się w pirotechnice.
Magnez można otrzymać przez redukcję tlenku magnezu węglem w wysokiej temperaturze . Spala się w powietrzu, tworząc tlenek magnezu i azotek magnezu . Tlenek magnezu to biały proszek, który reaguje z wodą, tworząc wodorotlenek magnezu.
Jony magnezu (Mg²⁺) wraz z jonami wapnia (Ca²⁺) wchodzą w skład twardej wody, powodując osadzanie się kamienia. Można je usunąć, dodając jony węglanowe, które tworzą nierozpuszczalny węglan magnezu .
Warto wiedzieć! Siarczan magnezu (MgSO₄), znany jako sól gorzka, ma szerokie zastosowanie medyczne - działa przeczyszczająco i obniża ciśnienie krwi. Powstaje w reakcji wodorotlenku magnezu z kwasem siarkowym .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wapń - budulec kości i skał
Wapń to srebrzystobiałe ciało stałe z 2 grupy, 4 okresu o konfiguracji elektronowej [Ar]4s². Jest ważnym pierwiastkiem w przyrodzie, występującym głównie w postaci węglanu wapnia (CaCO₃). Barwi płomień na charakterystyczny ceglastoczerwony kolor.
Wapń można otrzymać w reakcji tlenku wapnia z glinem . Węglan wapnia pod wpływem wysokiej temperatury rozkłada się do tlenku wapnia, zwanego wapnem palonym . Ten z kolei reaguje z wodą, tworząc wodorotlenek wapnia, czyli wapno gaszone .
Woda wapienna (nasycony roztwór Ca(OH)₂) mętnieje w kontakcie z dwutlenkiem węgla, co jest reakcją charakterystyczną dla wykrywania CO₂ . Gips budowlany powstaje w wyniku reakcji uwodnienia półwodnego siarczanu wapnia .
Pamiętaj! Karbid reaguje z wodą, tworząc acetylen i wodorotlenek wapnia . Ta reakcja była dawniej wykorzystywana do wytwarzania gazu do lamp górniczych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje i zastosowania związków wapnia
Sole wapnia i magnezu często występują jako trudnorozpuszczalne osady. Można je otrzymać w reakcji rozpuszczalnych chlorków z węglanem sodu: CaCl₂ + Na₂CO₃ → CaCO₃↓ + 2NaCl oraz MgCl₂ + Na₂CO₃ → MgCO₃↓ + 2NaCl. Te reakcje strąceniowe są podstawą usuwania twardości wody.
Wapń tworzy szereg użytecznych związków. Z wodą reaguje, wydzielając wodór i tworząc wodorotlenek wapnia . Diwodorofosforan wapnia reaguje z tlenkiem wapnia, tworząc fosforan wapnia i wodę .
Zawartość wody w kryształach ma znaczący wpływ na właściwości minerałów. Gips dwuwodny (CaSO₄·2H₂O) zawiera 26,5% wody, podczas gdy gips półwodny ((CaSO₄)₂·H₂O) tylko 6,62%. Ta różnica wpływa na ich właściwości budowlane i czas twardnienia.
Ciekawostka praktyczna! Tlenek wapnia (CaO) reaguje z kwasami, tworząc sole i wodę, natomiast z wodą reaguje, tworząc wodorotlenek wapnia o silnie zasadowym odczynie. Ta właściwość czyni go cennym składnikiem w przemyśle budowlanym i rolnictwie.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: silna zasada
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.