Czas na prawdziwą podróż w głąb materii! Budowa atomu to... Pokaż więcej
Budowa atomu - Podstawy chemii rozszerzonej






Budowa atomu i izotopy
Każdy atom to jak mała planeta z jądrem w środku i elektronami krążącymi wokół. Liczba atomowa (Z) mówi ci, ile protonów ma atom, a liczba masowa (A) to suma protonów i neutronów.
Izotopy to jak rodzeństwo tego samego pierwiastka - mają tę samą liczbę protonów, ale różną liczbę neutronów. Najlepszy przykład? Wodór ma trzy "braci": zwykły wodór (1 proton), deuter i tryt .
Masa atomowa pierwiastka to średnia ważona mas wszystkich jego naturalnych izotopów. Obliczasz ją wzorem: Mat = / 100%. To dlatego masa atomowa chloru w tablicy to 35,5 - bo to średnia z dwóch głównych izotopów!
💡 Pamiętaj: Nie wszystkie jądra są stabilne. Te niestabilne (jak wszystkie pierwiastki cięższe od bizmutu) rozpadają się radioaktywnie!

Radioaktywność i rozpady jąder
Gdy jądro atomowe jest niestabilne, pozbywa się nadmiaru energii przez rozpad radioaktywny. To jak wyrzucanie balastu z tonącego statku - jądro "wyrzuca" różne cząstki, żeby się ustabilizować.
Promieniowanie alfa (α) to wyrzucenie jądra helu - atom traci 4 jednostki masy i 2 protony. Promieniowanie beta (β) to przekształcenie neutronu w proton z emisją elektronu. Promieniowanie gamma (γ) to czysta energia - jak błysk światła, ale niewidoczny.
Okres półtrwania to czas, po którym połowa radioaktywnych atomów się rozpadnie. Niektóre izotopy mają okres kilku sekund, inne - miliardy lat! To jak odliczanie do zera, ale zawsze zostaje połowa z tego, co było.
💡 Ciekawostka: Izotopy sztuczne powstają w akceleratorach cząstek - bombardujemy stabilne jądra, żeby stworzyć nowe, niestabilne pierwiastki!

Elektrony i ich rozmieszczenie
Elektrony to nie małe kulki krążące wokół jądra - to orbitale, czyli obszary gdzie prawdopodobnie znajdziesz elektron. Wyobraź sobie to jak "chmury prawdopodobieństwa" o różnych kształtach.
Zasada Pauliego mówi, że na jednym orbitalu mogą być maksymalnie 2 elektrony, ale muszą mieć przeciwne spiny (jak para tańczących ludzi). Reguła Hunda to zasada "każdy na swoje miejsce" - elektrony wolą zajmować osobne orbitale tego samego typu, zanim zaczną się parować.
Konfiguracja elektronowa to adres każdego elektronu w atomie. Możesz ją zapisać na kilka sposobów - od prostego powłokowego (K, L, M, N) po szczegółowy klatkowy ze strzałkami pokazującymi spiny.
Promocja elektronowa to wyjątek od reguły - czasem elektron "skacze" na wyższy orbital, bo to bardziej opłacalne energetycznie. Tak robią chrom i miedź!
💡 Tip na egzamin: Pamiętaj kolejność zapełniania: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p... To jak instrukcja IKEA - krok po kroku!
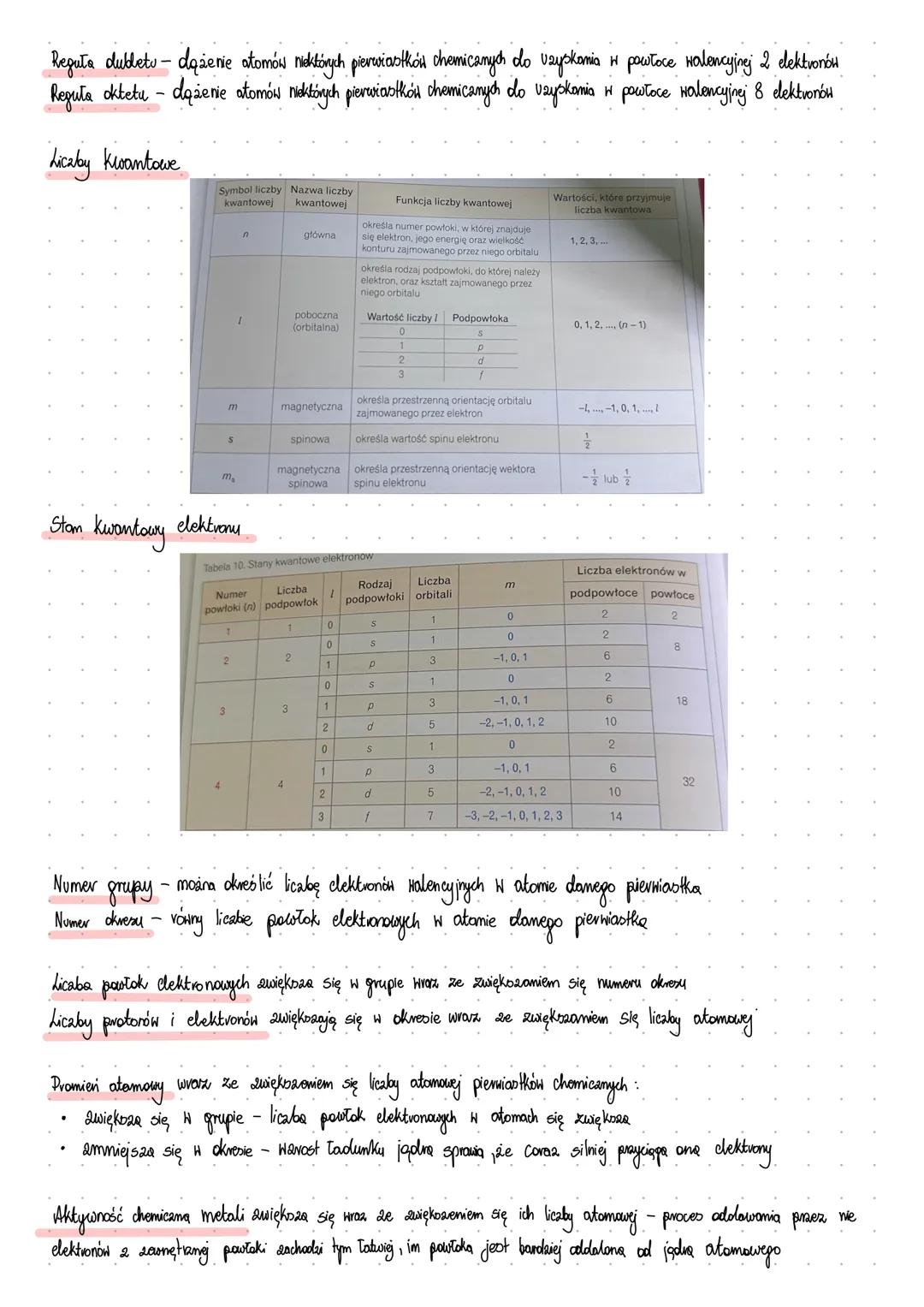
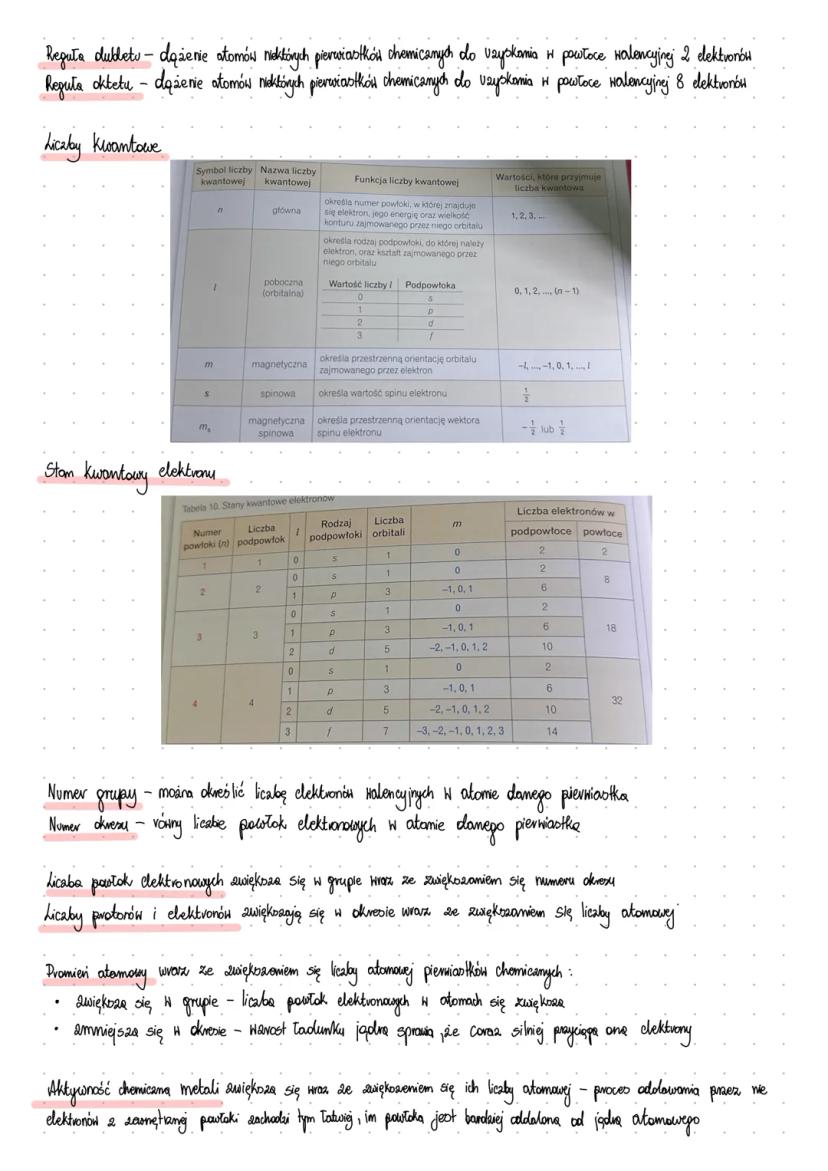
Liczby kwantowe i układ okresowy
Każdy elektron ma swój unikalny "kod pocztowy" składający się z czterech liczb kwantowych. Główna (n) to numer "dzielnicy" (powłoki), poboczna (l) to typ "ulicy" (orbital s, p, d, f), magnetyczna (m) to konkretny "adres", a spinowa to "kierunek obrotu".
Układ okresowy to mapa właściwości pierwiastków. Numer grupy = liczba elektronów walencyjnych, numer okresu = liczba powłok elektronowych. Proste jak drut!
Promień atomowy zmienia się przewidywalnie: rośnie w dół grupy i maleje w prawo w okresie .
Aktywność chemiczna metali rośnie w dół grupy - im dalej elektrony od jądra, tym łatwiej je oddać. U niemetali jest odwrotnie - im mniejszy atom, tym chętniej przyciąga dodatkowe elektrony.
💡 Mnemotechnika: Pamiętaj "GDPM" - Grupa Daje Promień Maleje (w okresie), Grupa Daje Promień Rośnie (w grupie)!

Wiązania chemiczne i elektroujemność
Elektroujemność to "siła ssania" elektronów przez atom. Im większa różnica elektroujemności między atomami, tym bardziej polarne wiązanie. Wzór jest prosty: ΔE < 0,4 = wiązanie kowalencyjne niespolaryzowane, 0,4-1,7 = spolaryzowane, >1,7 = jonowe.
Jony mają inne rozmiary niż atomy - kationy (dodatnie) są mniejsze bo straciły elektrony, aniony (ujemne) są większe bo zyskały elektrony. To jak rozdęte vs ściśnięte balony.
Wiązanie koordynacyjne to specjalny typ wiązania kowalencyjnego - jeden atom "pożycza" parę elektronów drugiemu. Często spotykasz to w kompleksach metali.
Hybrydzacja (sp³, sp², sp) to "miksowanie" orbitali atomowych, żeby stworzyć nowe, lepiej dopasowane do tworzenia wiązań. To jak przygotowanie idealnych "gniazd" dla elektronów.
💡 Praktyczna rada: Liczba podstawników + wolne pary elektronowe = typ hybrydzacji. 4 = sp³, 3 = sp², 2 = sp!

Oddziaływania międzycząsteczkowe
Wiązania wodorowe to najsilniejsze oddziaływania między cząsteczkami - powstają gdy wodór związany z F, O lub N "przyciąga" kolejny atom tych pierwiastków. To dlatego woda ma tak wysoką temperaturę wrzenia!
Oddziaływania dipol-dipol to przyciąganie między częściowymi ładunkami w cząsteczkach polarnych. Wyobraź sobie to jak małe magnesy - plus przyciąga minus.
Związki tworzące wiązania wodorowe mają wyższe temperatury topnienia i wrzenia, lepiej rozpuszczają się w wodzie i są bardziej "klejące". To kluczowe dla zrozumienia właściwości wielu substancji!
💡 Zapamiętaj: Wiązania wodorowe = wysoka temperatura wrzenia. Dlatego HF wrze w 20°C, a HCl już w -85°C!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: układ elektronowy
9Zasady konfiguracji elektronowej
Odkryj zasady konfiguracji elektronowej atomów, w tym kolejność zapełniania powłok, zakaz Hunda oraz sposób zapisu konfiguracji. Dowiedz się, jak określić elektrony walencyjne i maksymalną liczbę elektronów w powłokach. Idealne dla uczniów przygotowujących się do lekcji chemii.
Konfiguracja elektronowa/powłoki
Jak rozpisywać elektrony na powłokach elektronowych :)
Atom, konfigurację elektronowe, liczby kwantowe
Liczby kwantowe, konfigurację elektronowe
Orbitalne Struktury Atomowe
Zrozumienie struktury atomowej i orbitali w chemii kwantowej. Dowiedz się o podpowokach elektronowych, typach orbitali (s, p, d, f) oraz zasadach dotyczących spinów elektronów. Idealne dla uczniów przygotowujących się do matury z chemii.
Konfiguracja Elektronowa Atomów
Zrozumienie konfiguracji powłokowej i podpowłokowej atomów. Dowiedz się, jak zapisywać konfiguracje elektronowe, w tym skrócone zapisy z wykorzystaniem gazów szlachetnych. Materiał obejmuje kluczowe pojęcia, takie jak liczba elektronów, podpowłoki oraz ich energia. Idealne dla uczniów chemii.
Struktura Atomu i Liczby Kwantowe
Zgłębiaj zasady budowy atomu, konfiguracji elektronowej oraz liczby kwantowe. Ta notatka z chemii rozszerzonej omawia kluczowe pojęcia, takie jak nukleony, izotopy, oraz różne typy orbitali atomowych. Idealna dla uczniów przygotowujących się do egzaminów z chemii.
Podpowłoki Elektronowe
Zrozumienie podpowłok elektronowych i konfiguracji elektronowej atomów. Ta notatka omawia struktury elektronowe, w tym powłokę walencyjną, liczby elektronów oraz zasady obliczania maksymalnej liczby elektronów w powłokach. Idealna dla uczniów chemii przygotowujących się do egzaminów.
Konfiguracje Atomowe: Stan Wzbudzony
Zrozumienie konfiguracji elektronowych atomów, w tym stanu podstawowego i wzbudzonego. Omówienie promocji elektronowej dla atomów Cr, Cu i Ag oraz ich wpływu na właściwości chemiczne. Idealne dla studentów chemii szukających szczegółowych informacji na temat struktury atomowej.
Konfiguracja Elektronowa Atomu
Zrozumienie konfiguracji elektronowej atomów jest kluczowe dla matury z chemii. Ten materiał omawia liczby kwantowe, stany wzbudzone oraz zasady rozkładu elektronów w orbitalach. Idealny dla uczniów przygotowujących się do egzaminów. Typ: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Budowa atomu - Podstawy chemii rozszerzonej
Czas na prawdziwą podróż w głąb materii! Budowa atomu to klucz do zrozumienia całej chemii - od tego, dlaczego niektóre pierwiastki "lubią się" ze sobą, po to, jak powstaje promieniowanie radioaktywne.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa atomu i izotopy
Każdy atom to jak mała planeta z jądrem w środku i elektronami krążącymi wokół. Liczba atomowa (Z) mówi ci, ile protonów ma atom, a liczba masowa (A) to suma protonów i neutronów.
Izotopy to jak rodzeństwo tego samego pierwiastka - mają tę samą liczbę protonów, ale różną liczbę neutronów. Najlepszy przykład? Wodór ma trzy "braci": zwykły wodór (1 proton), deuter i tryt .
Masa atomowa pierwiastka to średnia ważona mas wszystkich jego naturalnych izotopów. Obliczasz ją wzorem: Mat = / 100%. To dlatego masa atomowa chloru w tablicy to 35,5 - bo to średnia z dwóch głównych izotopów!
💡 Pamiętaj: Nie wszystkie jądra są stabilne. Te niestabilne (jak wszystkie pierwiastki cięższe od bizmutu) rozpadają się radioaktywnie!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Radioaktywność i rozpady jąder
Gdy jądro atomowe jest niestabilne, pozbywa się nadmiaru energii przez rozpad radioaktywny. To jak wyrzucanie balastu z tonącego statku - jądro "wyrzuca" różne cząstki, żeby się ustabilizować.
Promieniowanie alfa (α) to wyrzucenie jądra helu - atom traci 4 jednostki masy i 2 protony. Promieniowanie beta (β) to przekształcenie neutronu w proton z emisją elektronu. Promieniowanie gamma (γ) to czysta energia - jak błysk światła, ale niewidoczny.
Okres półtrwania to czas, po którym połowa radioaktywnych atomów się rozpadnie. Niektóre izotopy mają okres kilku sekund, inne - miliardy lat! To jak odliczanie do zera, ale zawsze zostaje połowa z tego, co było.
💡 Ciekawostka: Izotopy sztuczne powstają w akceleratorach cząstek - bombardujemy stabilne jądra, żeby stworzyć nowe, niestabilne pierwiastki!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Elektrony i ich rozmieszczenie
Elektrony to nie małe kulki krążące wokół jądra - to orbitale, czyli obszary gdzie prawdopodobnie znajdziesz elektron. Wyobraź sobie to jak "chmury prawdopodobieństwa" o różnych kształtach.
Zasada Pauliego mówi, że na jednym orbitalu mogą być maksymalnie 2 elektrony, ale muszą mieć przeciwne spiny (jak para tańczących ludzi). Reguła Hunda to zasada "każdy na swoje miejsce" - elektrony wolą zajmować osobne orbitale tego samego typu, zanim zaczną się parować.
Konfiguracja elektronowa to adres każdego elektronu w atomie. Możesz ją zapisać na kilka sposobów - od prostego powłokowego (K, L, M, N) po szczegółowy klatkowy ze strzałkami pokazującymi spiny.
Promocja elektronowa to wyjątek od reguły - czasem elektron "skacze" na wyższy orbital, bo to bardziej opłacalne energetycznie. Tak robią chrom i miedź!
💡 Tip na egzamin: Pamiętaj kolejność zapełniania: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p... To jak instrukcja IKEA - krok po kroku!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Liczby kwantowe i układ okresowy
Każdy elektron ma swój unikalny "kod pocztowy" składający się z czterech liczb kwantowych. Główna (n) to numer "dzielnicy" (powłoki), poboczna (l) to typ "ulicy" (orbital s, p, d, f), magnetyczna (m) to konkretny "adres", a spinowa to "kierunek obrotu".
Układ okresowy to mapa właściwości pierwiastków. Numer grupy = liczba elektronów walencyjnych, numer okresu = liczba powłok elektronowych. Proste jak drut!
Promień atomowy zmienia się przewidywalnie: rośnie w dół grupy i maleje w prawo w okresie .
Aktywność chemiczna metali rośnie w dół grupy - im dalej elektrony od jądra, tym łatwiej je oddać. U niemetali jest odwrotnie - im mniejszy atom, tym chętniej przyciąga dodatkowe elektrony.
💡 Mnemotechnika: Pamiętaj "GDPM" - Grupa Daje Promień Maleje (w okresie), Grupa Daje Promień Rośnie (w grupie)!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wiązania chemiczne i elektroujemność
Elektroujemność to "siła ssania" elektronów przez atom. Im większa różnica elektroujemności między atomami, tym bardziej polarne wiązanie. Wzór jest prosty: ΔE < 0,4 = wiązanie kowalencyjne niespolaryzowane, 0,4-1,7 = spolaryzowane, >1,7 = jonowe.
Jony mają inne rozmiary niż atomy - kationy (dodatnie) są mniejsze bo straciły elektrony, aniony (ujemne) są większe bo zyskały elektrony. To jak rozdęte vs ściśnięte balony.
Wiązanie koordynacyjne to specjalny typ wiązania kowalencyjnego - jeden atom "pożycza" parę elektronów drugiemu. Często spotykasz to w kompleksach metali.
Hybrydzacja (sp³, sp², sp) to "miksowanie" orbitali atomowych, żeby stworzyć nowe, lepiej dopasowane do tworzenia wiązań. To jak przygotowanie idealnych "gniazd" dla elektronów.
💡 Praktyczna rada: Liczba podstawników + wolne pary elektronowe = typ hybrydzacji. 4 = sp³, 3 = sp², 2 = sp!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Oddziaływania międzycząsteczkowe
Wiązania wodorowe to najsilniejsze oddziaływania między cząsteczkami - powstają gdy wodór związany z F, O lub N "przyciąga" kolejny atom tych pierwiastków. To dlatego woda ma tak wysoką temperaturę wrzenia!
Oddziaływania dipol-dipol to przyciąganie między częściowymi ładunkami w cząsteczkach polarnych. Wyobraź sobie to jak małe magnesy - plus przyciąga minus.
Związki tworzące wiązania wodorowe mają wyższe temperatury topnienia i wrzenia, lepiej rozpuszczają się w wodzie i są bardziej "klejące". To kluczowe dla zrozumienia właściwości wielu substancji!
💡 Zapamiętaj: Wiązania wodorowe = wysoka temperatura wrzenia. Dlatego HF wrze w 20°C, a HCl już w -85°C!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: układ elektronowy
9Zasady konfiguracji elektronowej
Odkryj zasady konfiguracji elektronowej atomów, w tym kolejność zapełniania powłok, zakaz Hunda oraz sposób zapisu konfiguracji. Dowiedz się, jak określić elektrony walencyjne i maksymalną liczbę elektronów w powłokach. Idealne dla uczniów przygotowujących się do lekcji chemii.
Konfiguracja elektronowa/powłoki
Jak rozpisywać elektrony na powłokach elektronowych :)
Atom, konfigurację elektronowe, liczby kwantowe
Liczby kwantowe, konfigurację elektronowe
Orbitalne Struktury Atomowe
Zrozumienie struktury atomowej i orbitali w chemii kwantowej. Dowiedz się o podpowokach elektronowych, typach orbitali (s, p, d, f) oraz zasadach dotyczących spinów elektronów. Idealne dla uczniów przygotowujących się do matury z chemii.
Konfiguracja Elektronowa Atomów
Zrozumienie konfiguracji powłokowej i podpowłokowej atomów. Dowiedz się, jak zapisywać konfiguracje elektronowe, w tym skrócone zapisy z wykorzystaniem gazów szlachetnych. Materiał obejmuje kluczowe pojęcia, takie jak liczba elektronów, podpowłoki oraz ich energia. Idealne dla uczniów chemii.
Struktura Atomu i Liczby Kwantowe
Zgłębiaj zasady budowy atomu, konfiguracji elektronowej oraz liczby kwantowe. Ta notatka z chemii rozszerzonej omawia kluczowe pojęcia, takie jak nukleony, izotopy, oraz różne typy orbitali atomowych. Idealna dla uczniów przygotowujących się do egzaminów z chemii.
Podpowłoki Elektronowe
Zrozumienie podpowłok elektronowych i konfiguracji elektronowej atomów. Ta notatka omawia struktury elektronowe, w tym powłokę walencyjną, liczby elektronów oraz zasady obliczania maksymalnej liczby elektronów w powłokach. Idealna dla uczniów chemii przygotowujących się do egzaminów.
Konfiguracje Atomowe: Stan Wzbudzony
Zrozumienie konfiguracji elektronowych atomów, w tym stanu podstawowego i wzbudzonego. Omówienie promocji elektronowej dla atomów Cr, Cu i Ag oraz ich wpływu na właściwości chemiczne. Idealne dla studentów chemii szukających szczegółowych informacji na temat struktury atomowej.
Konfiguracja Elektronowa Atomu
Zrozumienie konfiguracji elektronowej atomów jest kluczowe dla matury z chemii. Ten materiał omawia liczby kwantowe, stany wzbudzone oraz zasady rozkładu elektronów w orbitalach. Idealny dla uczniów przygotowujących się do egzaminów. Typ: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.