Chemia organiczna to fascynujący dział chemii, który bada związki zawierające... Pokaż więcej
Podstawy chemii organicznej - Przegląd dla maturzystów
Alkohole i reakcje związków organicznych
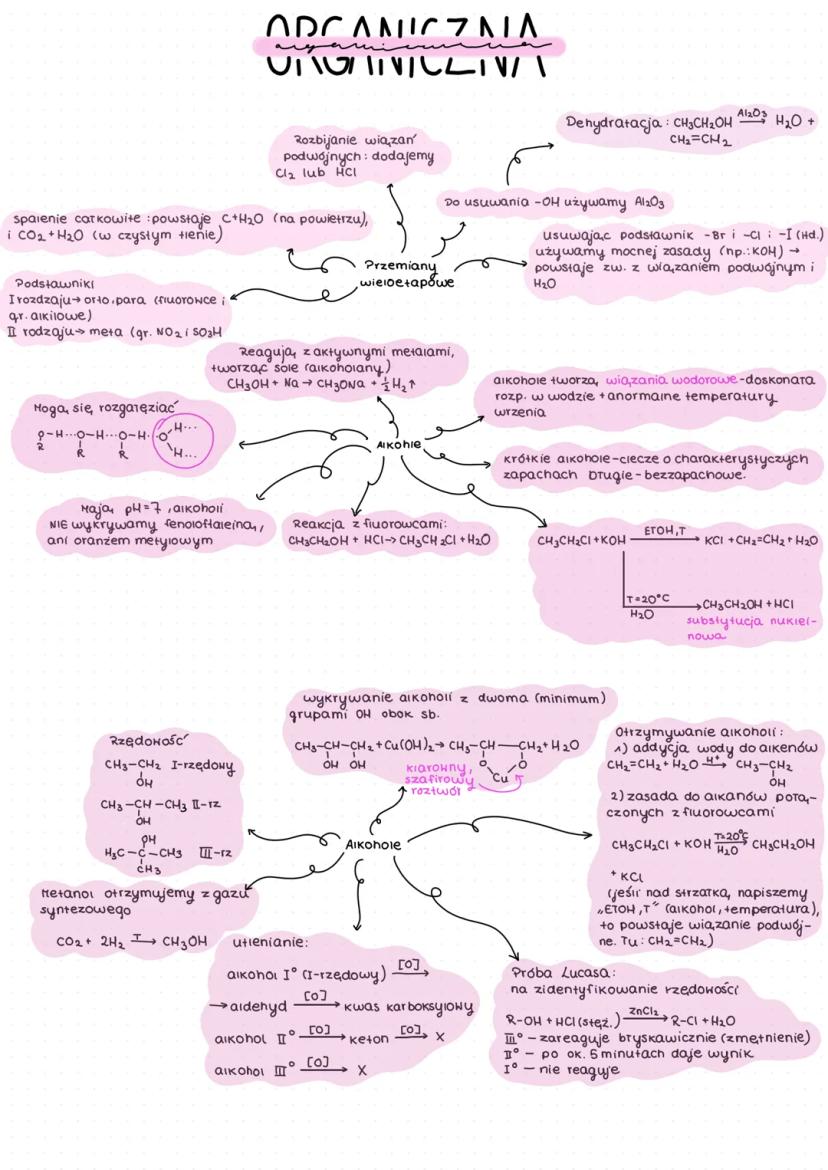
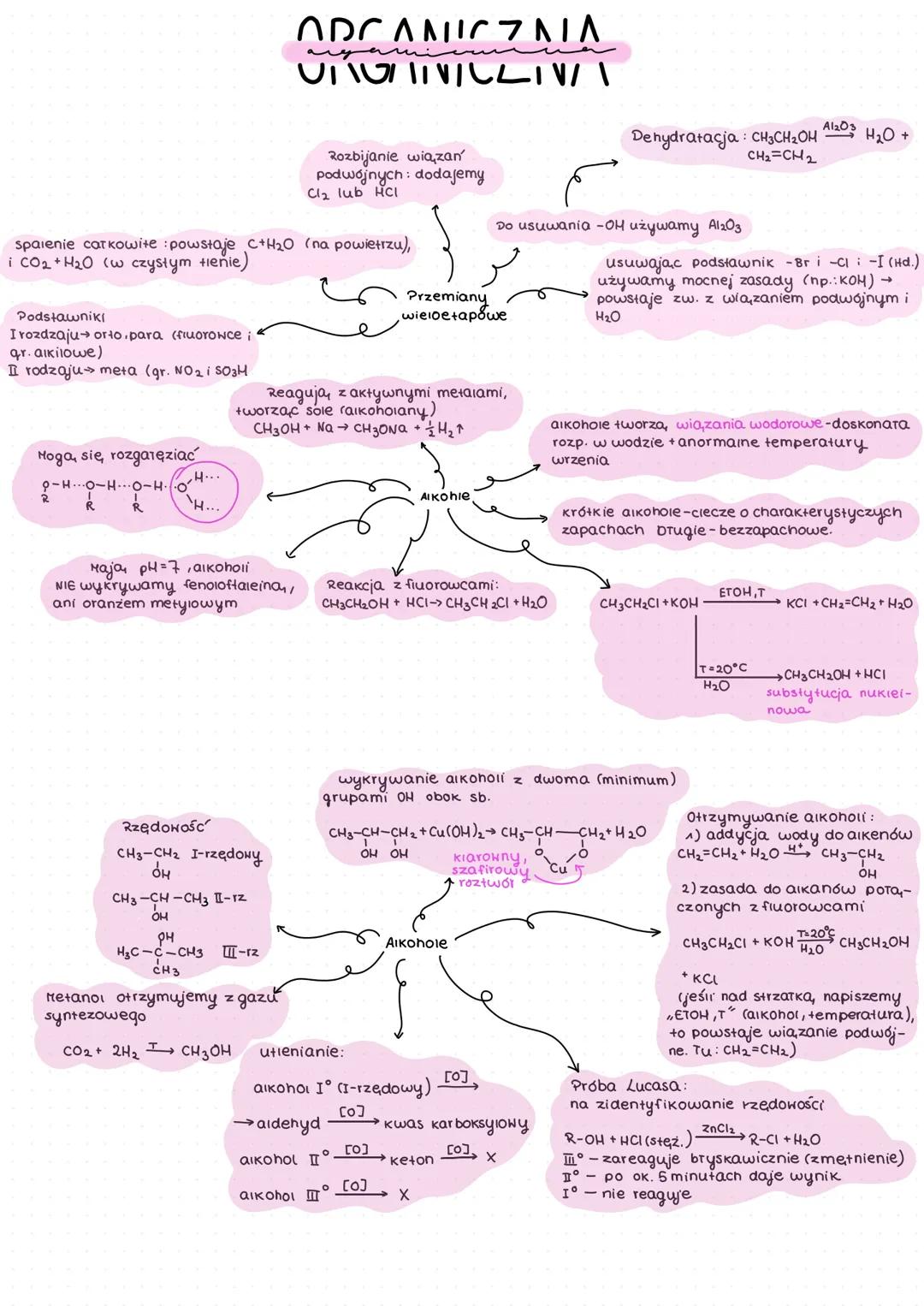
Alkohole to związki zawierające grupę hydroksylową połączoną z atomem węgla. Ich reaktywność zależy od rzędowości, czyli ilości atomów węgla połączonych z atomem węgla przy grupie -OH.
Alkohole możemy podzielić na:
- I-rzędowe - grupa -OH przy węglu skrajnym (połączonym z tylko jednym atomem węgla)
- II-rzędowe - grupa -OH przy węglu połączonym z dwoma atomami węgla
- III-rzędowe - grupa -OH przy węglu połączonym z trzema atomami węgla
Alkohole tworzą wiązania wodorowe, co wpływa na ich dobre rozpuszczanie w wodzie oraz podwyższenie temperatury wrzenia. Reagują z aktywnymi metalami tworząc alkolanolany (sole).
💡 Próba Lucasa pozwala określić rzędowość alkoholi: alkohol III-rzędowy reaguje błyskawicznie (widoczne zmętnienie), II-rzędowy po około 6 minutach, a I-rzędowy nie reaguje.
Podczas dehydratacji alkoholi (w obecności Al₂O₃) powstają alkeny i woda, np.: CH₃CH₂OH → CH₂=CH₂ + H₂O.
Alkohole można otrzymać poprzez:
- Addycję wody do alkenów
- Reakcję zasad z alkanami połączonymi z fluorowcami
Ponadto w notatce znajdziemy informacje o rozbijaniu wiązań podwójnych (addycja Cl₂ lub HCl), spalaniu całkowitym oraz o reaktywności podstawników w pierścieniach aromatycznych.
Fenole i właściwości aromatów
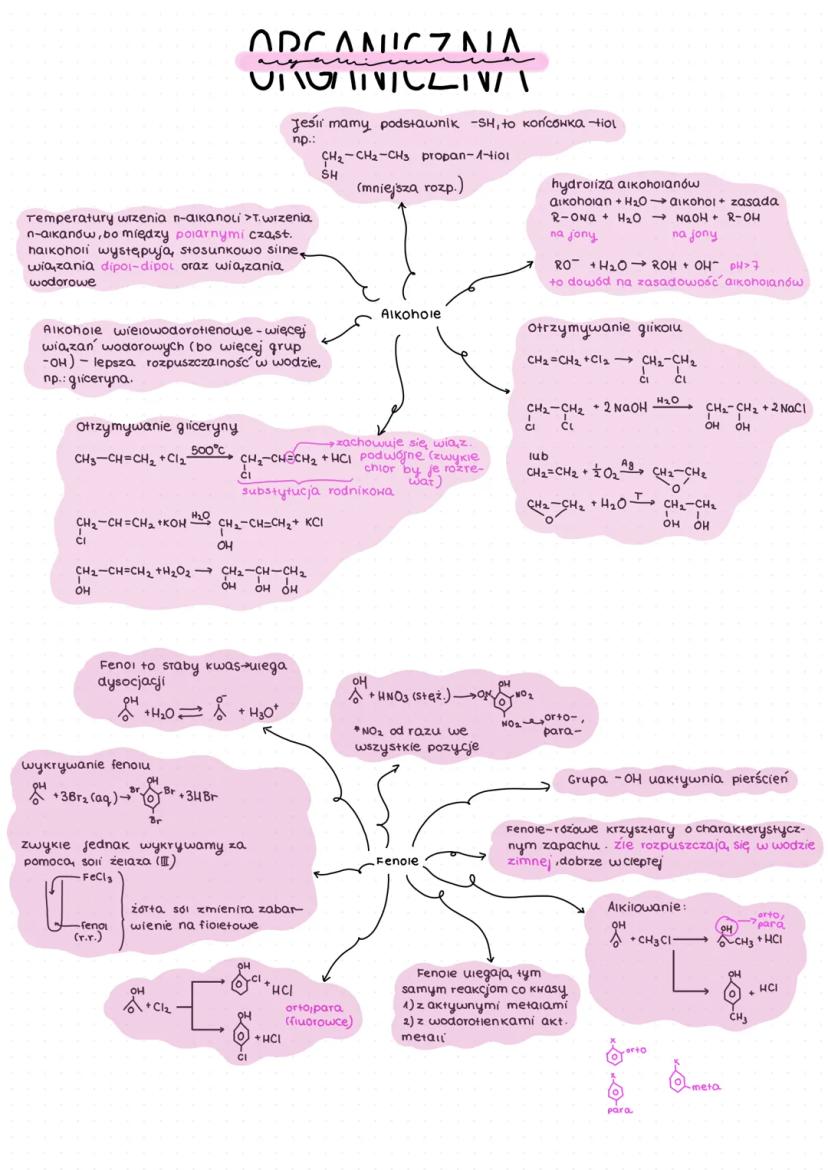
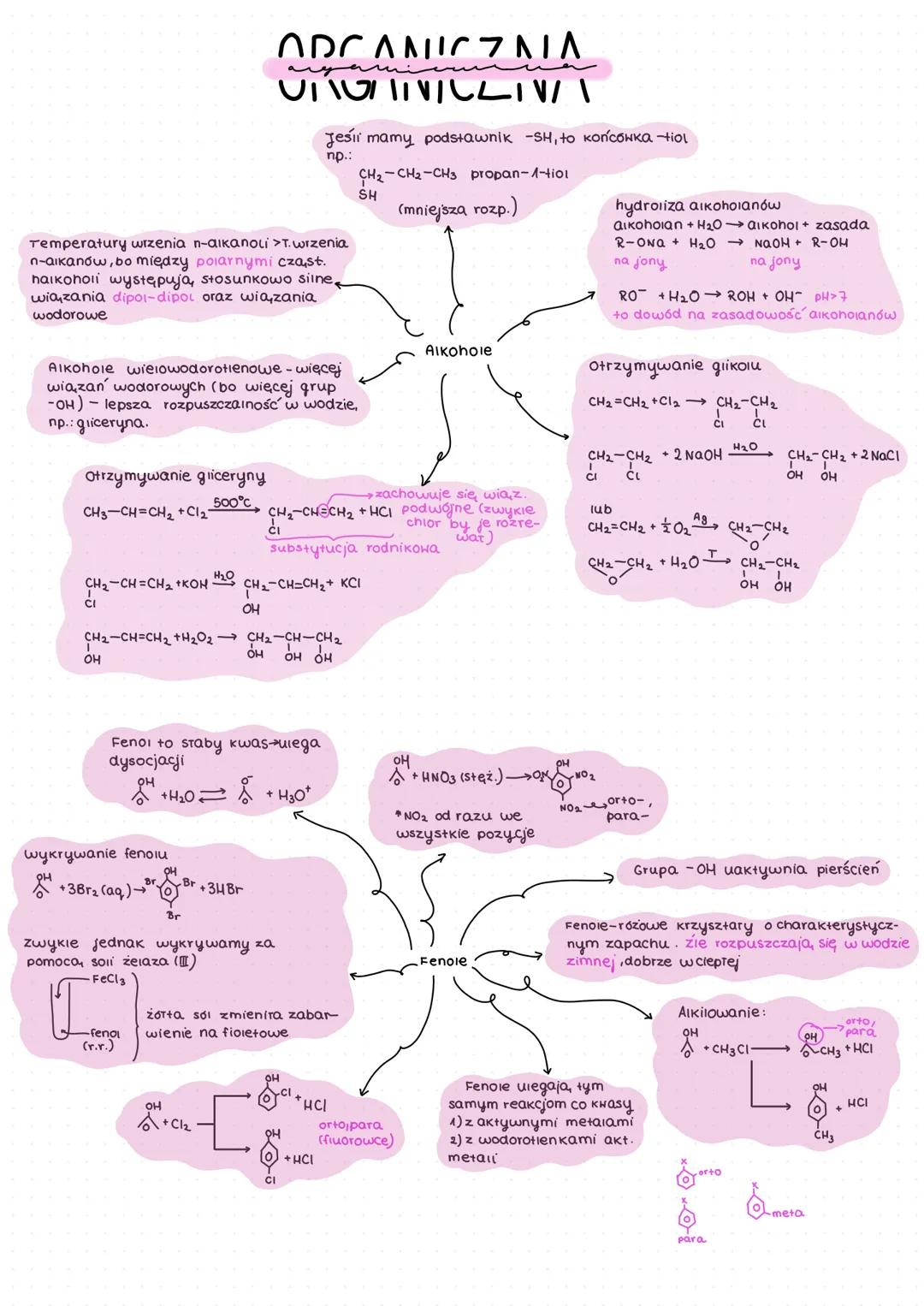
Fenole to związki organiczne, w których grupa hydroksylowa jest bezpośrednio połączona z pierścieniem aromatycznym. W przeciwieństwie do alkoholi, fenole mają właściwości kwasowe.
Fenol to związek w postaci różowych kryształów o charakterystycznym zapachu. Słabo rozpuszcza się w zimnej wodzie, lepiej w ciepłej. Grupa -OH w fenolu uaktywnia pierścień, co wpływa na jego reaktywność.
Fenole możemy łatwo wykryć za pomocą chlorku żelaza(III):
fenol + FeCl₃ → żółta sól zmienia zabarwienie na fioletowe
💡 Grupa -OH w fenolach kieruje podstawniki do pozycji orto i para, co jest ważne w reakcjach substytucji.
Fenole mogą reagować z:
- Aktywnymi metalami
- Halogenami (dając produkty podstawienia w pozycji orto i para)
- Kwasami (podobnie jak inne alkohole)
- Wodą i CO₂, tworząc wodorowęglany
Związki z końcówką -tiol zawierają grupę -SH zamiast -OH, np. propan-1-tiol. Mają one mniejszą rozpuszczalność w wodzie.
Temperatury wrzenia alkoholi są wyższe niż odpowiadających im alkanów ze względu na wiązania wodorowe. Alkohole wielowodorotlenowe (np. gliceryna) mają więcej wiązań wodorowych, co dodatkowo poprawia ich rozpuszczalność w wodzie.
Aldehydy i ich właściwości
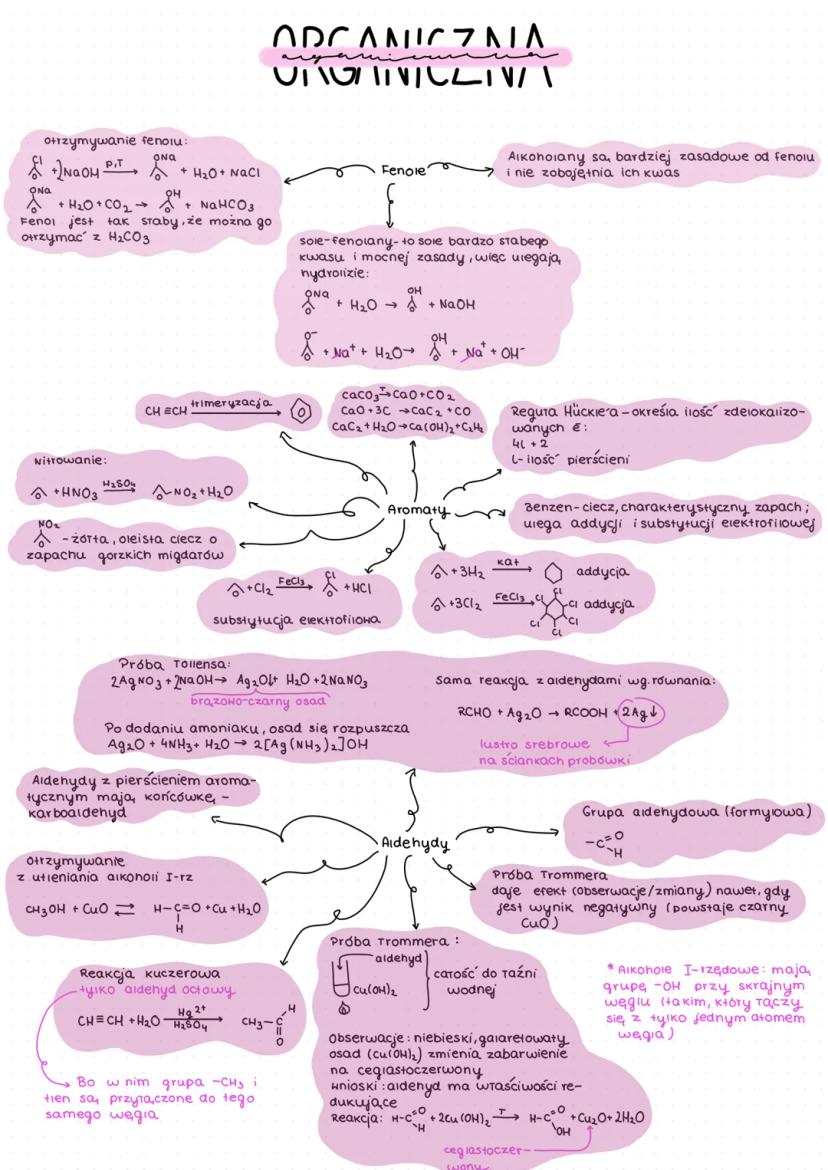
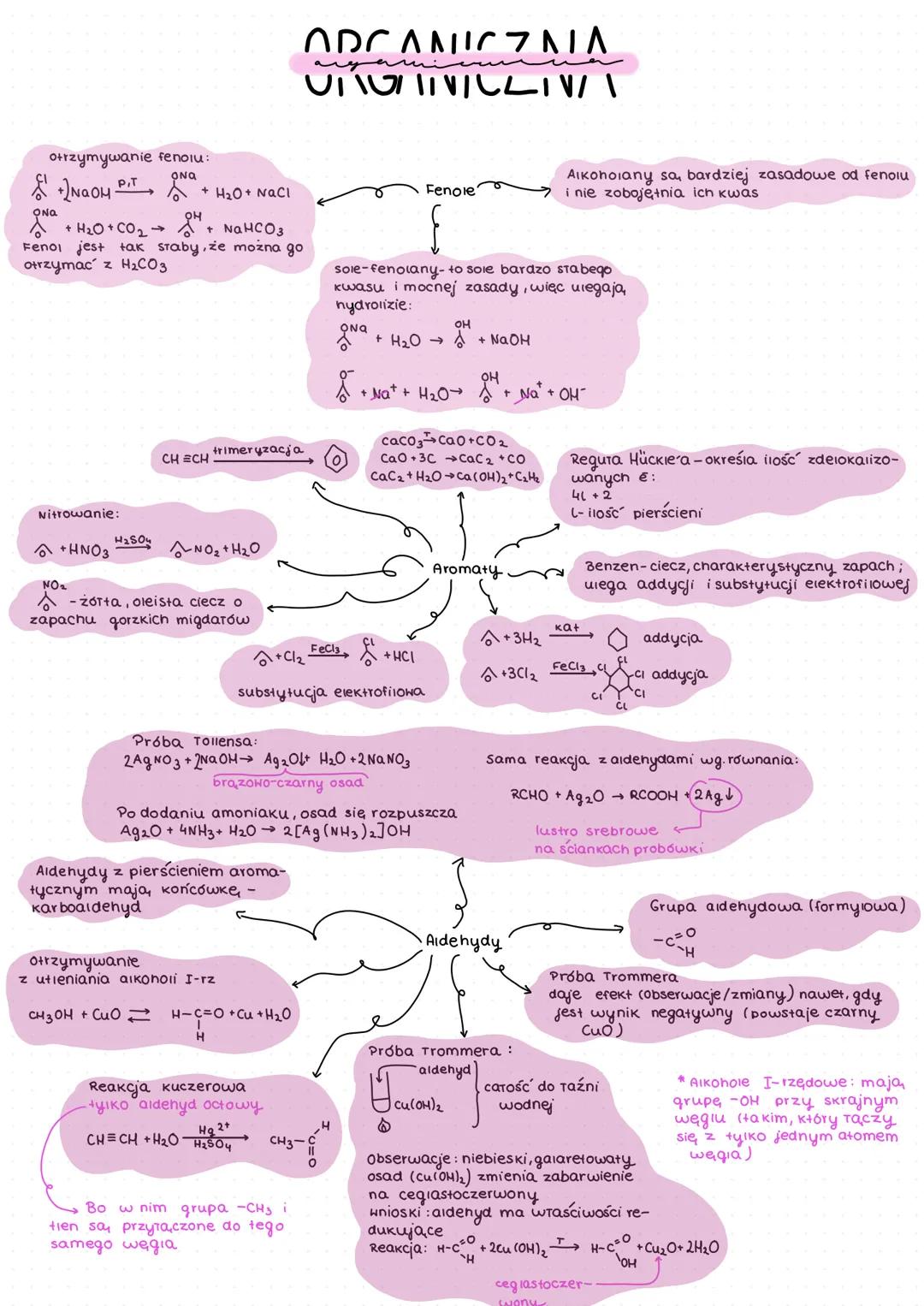
Aldehydy to związki organiczne zawierające grupę formylową , której charakterystyczną cechą są silne właściwości redukujące.
Aldehydy możemy wykryć za pomocą dwóch ważnych prób:
-
Próba Tollensa: aldehydy reagują z amoniakalnym roztworem tlenku srebra, tworząc metaliczne srebro (lustro srebrowe na ściankach probówki)
RCHO + Ag₂O → RCOOH + 2Ag↓ -
Próba Trommera: aldehydy redukują niebieski osad Cu(OH)₂ do ceglastoczerwonego Cu₂O
R-CHO + 2Cu(OH)₂ → R-COOH + Cu₂O↓ + 2H₂O
💡 Aldehydy z pierścieniem aromatycznym mają końcówkę "-karboaldehyd" w nazwie.
Aldehydy można otrzymać poprzez:
- Utlenianie alkoholi I-rzędowych
- Reakcję Kuczerowską, w której alkiny reagują z wodą w obecności jonów rtęci
Aldehydy i ketony są dla siebie izomerami - mają ten sam wzór sumaryczny, ale różnią się budową.
Podczas utleniania alkoholi:
- Alkohole I-rzędowe → aldehydy → kwasy karboksylowe
- Alkohole II-rzędowe → ketony
- Alkohole III-rzędowe nie ulegają utlenianiu
Ketony i kwasy karboksylowe
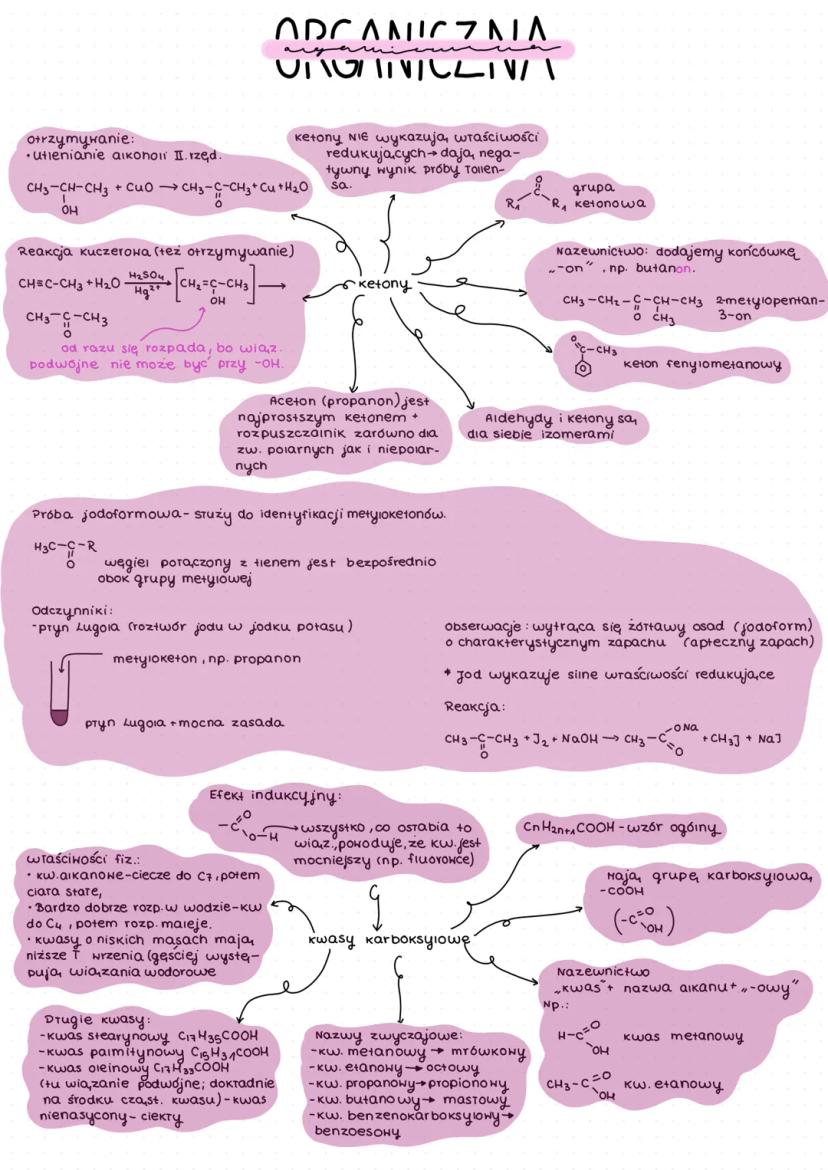
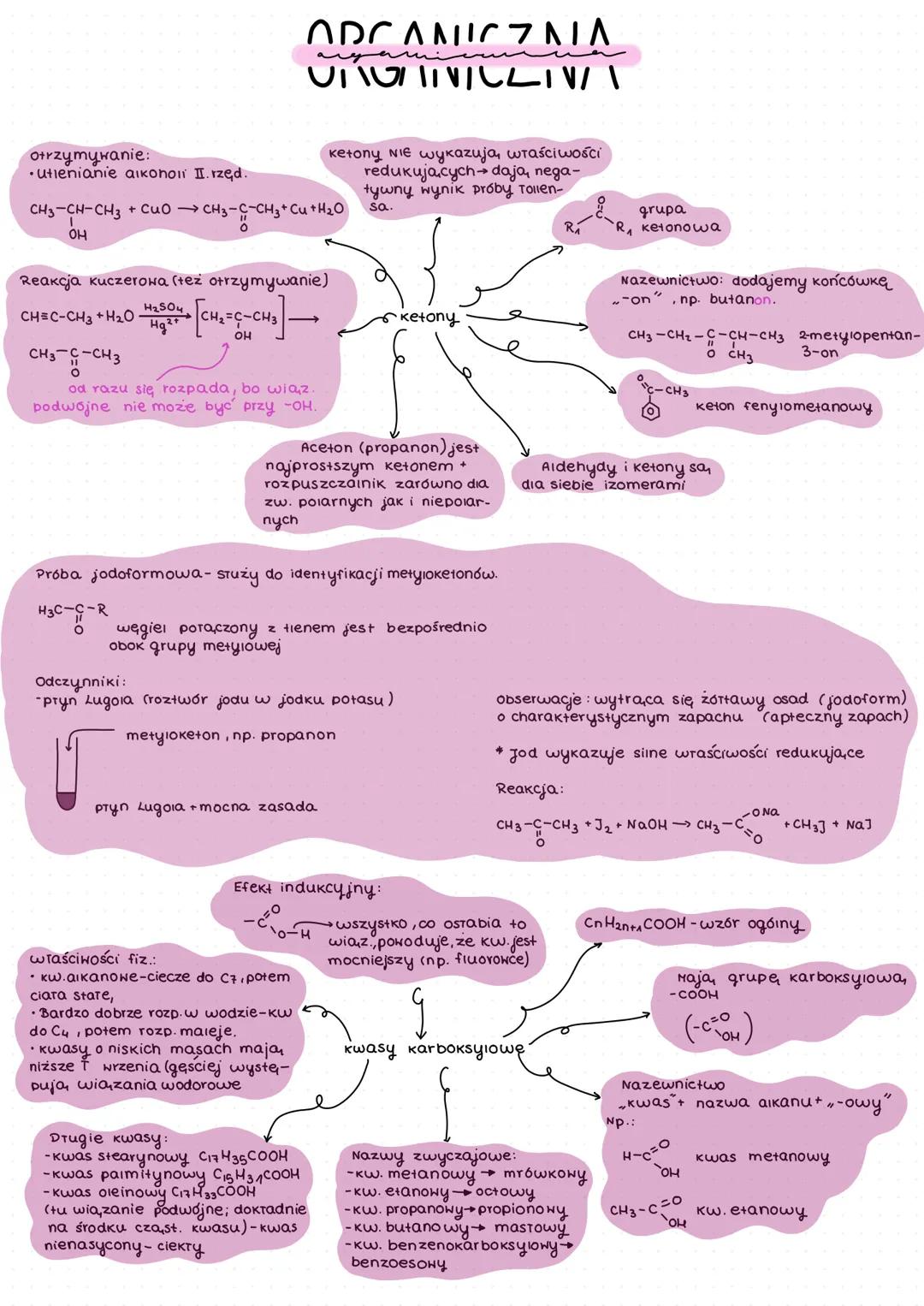
Ketony to związki zawierające grupę ketonową umieszczoną pomiędzy dwoma atomami węgla. W przeciwieństwie do aldehydów, nie wykazują właściwości redukujących - dają negatywny wynik próby Tollensa.
Najprostszym ketonem jest aceton (propanon), który jest doskonałym rozpuszczalnikiem dla związków polarnych i niepolarnych. Ketony nazywamy dodając końcówkę "-on" do nazwy alkanu.
Próba jodoformowa służy do identyfikacji metyloketonów (grupa ketonowa sąsiadująca z grupą metylową). Podczas tej reakcji powstaje jodoform - żółtawy osad o charakterystycznym aptecznym zapachu.
💡 Ketony można otrzymać poprzez utlenianie alkoholi II-rzędowych lub w zmodyfikowanej reakcji Kuczerowskiej.
Kwasy karboksylowe zawierają grupę karboksylową . Ich ogólny wzór to CₙH₂ₙ₊₁COOH. Krótsze kwasy są cieczami dobrze rozpuszczalnymi w wodzie, mają charakterystyczne zapachy.
Kwasy karboksylowe można rozpoznać, bo:
- Reagują z aktywnymi metalami wydzielając wodór
- Reagują z zasadami tworząc sole
- Reagują z tlenkami metali
- Mogą być redukowane do aldehydów
Na moc kwasów wpływa efekt indukcyjny - podstawniki przyciągające elektrony (np. fluorowce) zwiększają moc kwasu. Im bliżej grupy karboksylowej znajduje się podstawnik, tym silniejszy jest jego wpływ.
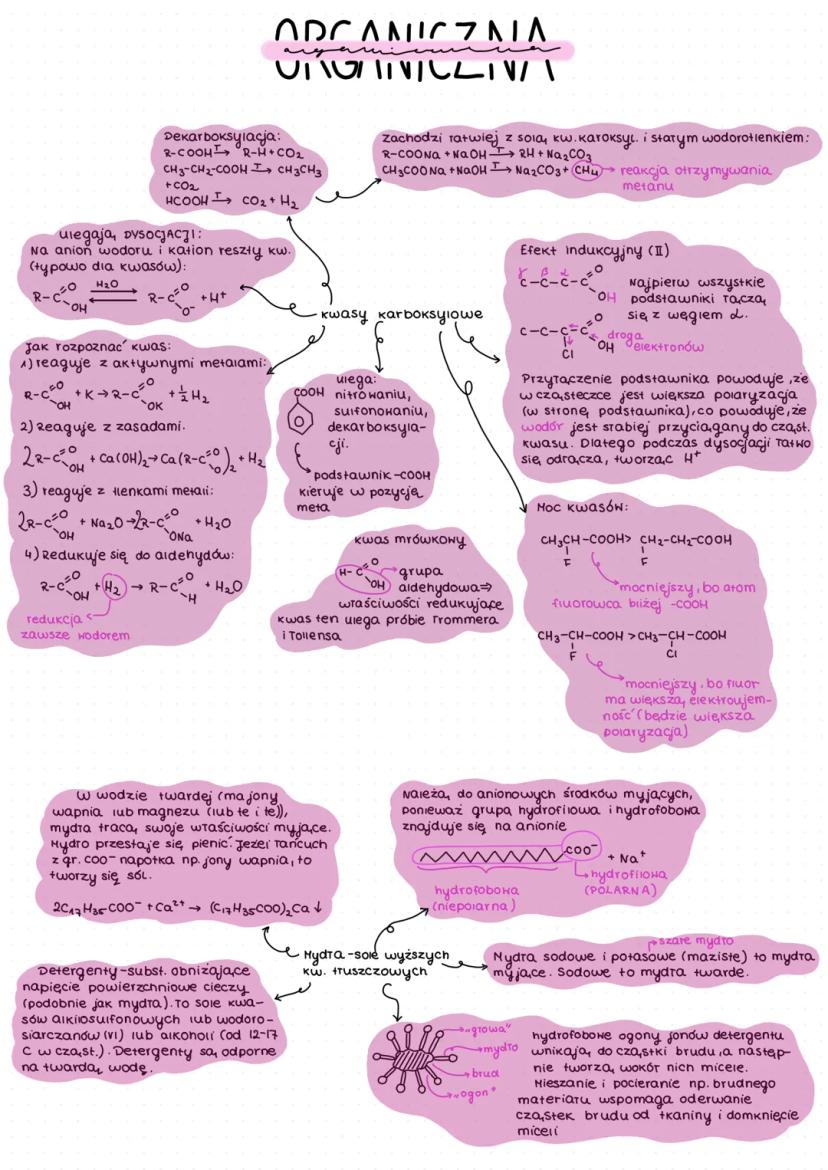
Mydła, detergenty i właściwości kwasów
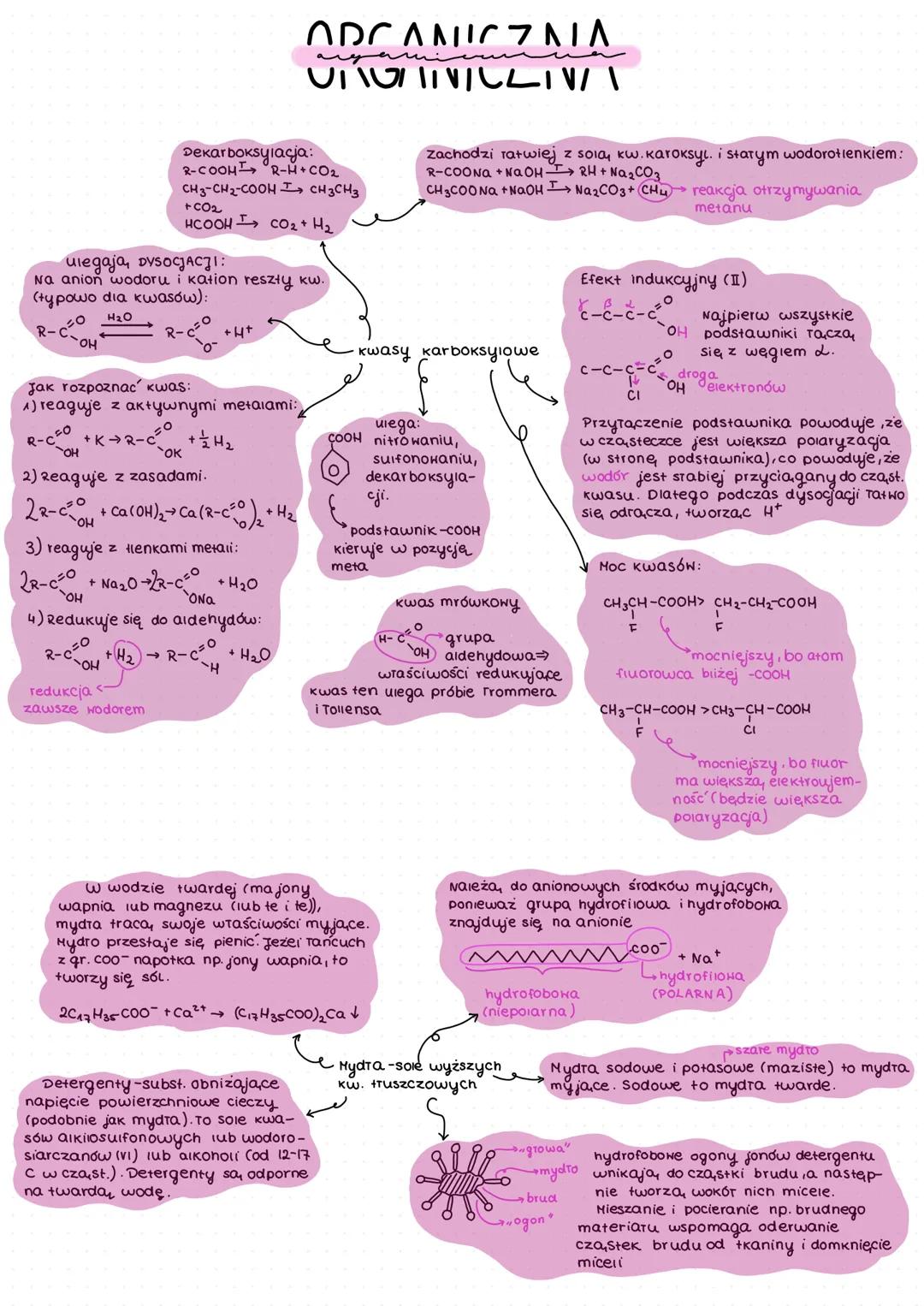
Kwasy karboksylowe w wodzie dysocjują na anion wodoru i kation reszty kwasowej. Mogą ulegać dekarboksylacji, podczas której tracą cząsteczkę CO₂.
Kwas mrówkowy (metanowy) ma właściwości redukujące i jako jedyny z kwasów karboksylowych daje pozytywny wynik w próbie Trommera i Tollensa. Grupa -COOH w pierścieniu aromatycznym kieruje podstawniki w pozycję meta.
Mydła to sole wyższych kwasów tłuszczowych. Mają budowę amfifilową - zawierają część hydrofilową (polarną, COO⁻Na⁺) i część hydrofobową (niepolarną, długi łańcuch węglowy). Dzięki tej budowie są zdolne do usuwania brudu.
💡 W twardej wodzie (zawierającej jony wapnia i magnezu) mydła tracą swoje właściwości myjące, ponieważ tworzą nierozpuszczalne sole.
Detergenty to substancje obniżające napięcie powierzchniowe cieczy. Są solami kwasów alkilosulfonowych lub wodorosiarczanów(VI) alkoholi. W przeciwieństwie do mydeł, są odporne na twardą wodę.
Cząsteczki mydła lub detergentu tworzą wokół cząstek brudu micele - struktury, w których hydrofobowe "ogony" są skierowane do wewnątrz (gdzie znajduje się brud), a hydrofilowe "głowy" na zewnątrz (gdzie jest woda). Mieszanie i pocieranie podczas prania pomaga oderwać cząstki brudu od tkaniny i zamknąć je w micelach.
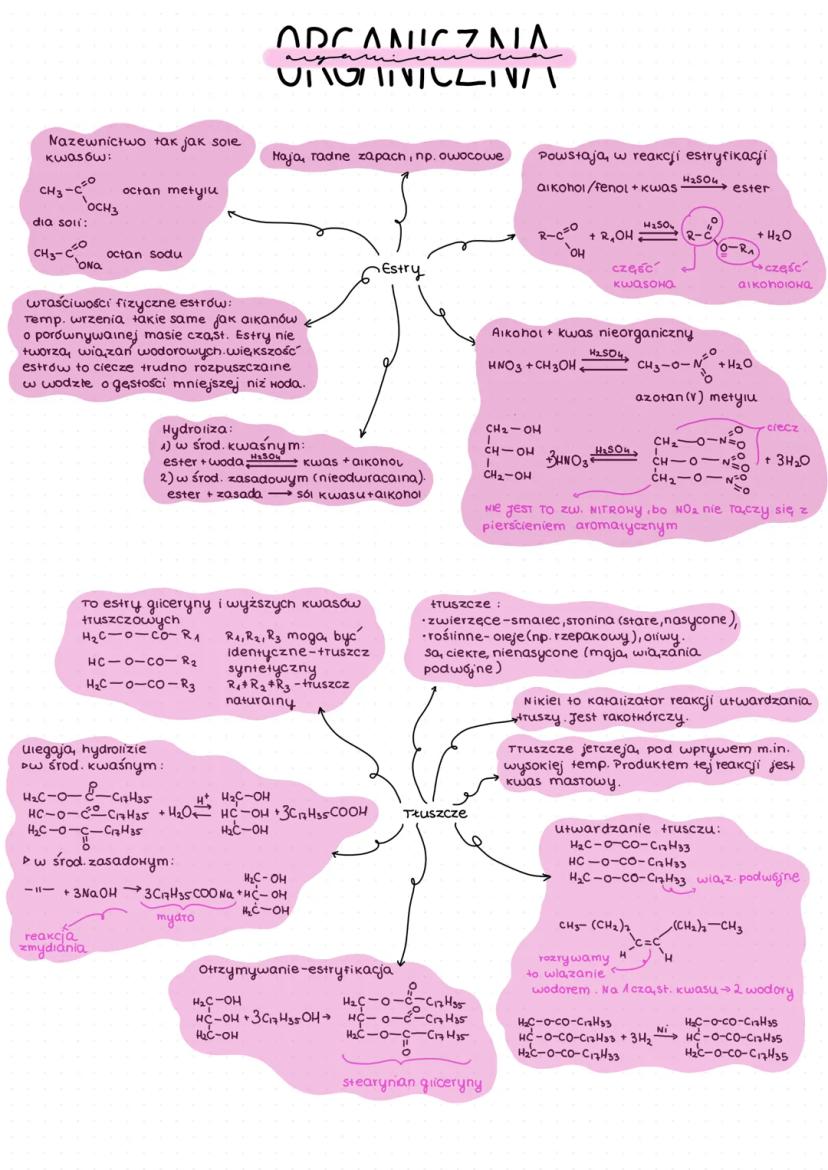
Estry i tłuszcze
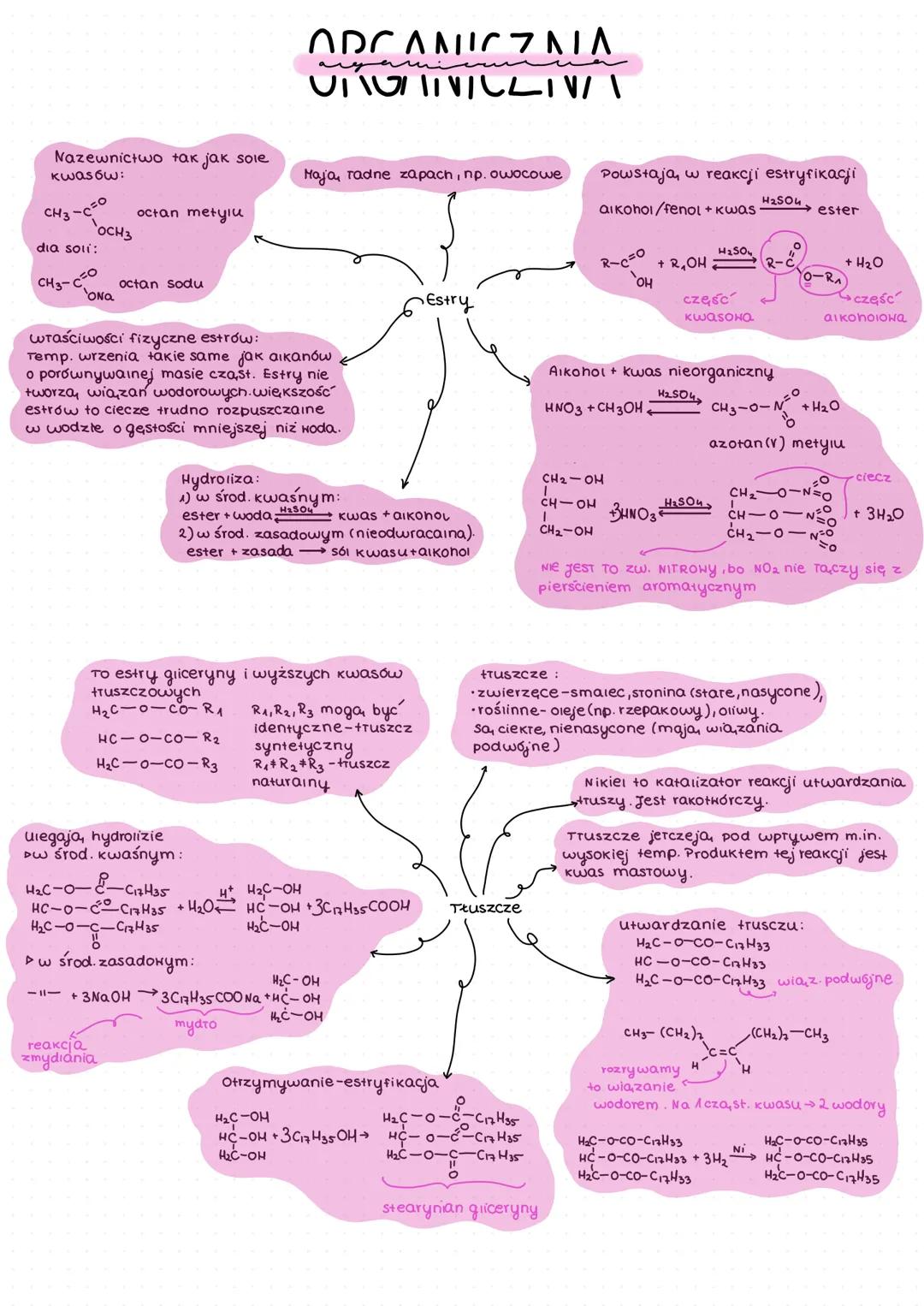
Estry to związki powstające w reakcji estryfikacji między alkoholem/fenolem a kwasem (w obecności H₂SO₄):
R-COOH + ROH ⇄ R-COOR' + H₂O
Estry mają przyjemny, owocowy zapach. Ich temperatury wrzenia są podobne do alkanów o porównywalnej masie cząsteczkowej. Nie tworzą wiązań wodorowych, większość z nich to ciecze trudno rozpuszczalne w wodzie.
Estry mogą ulegać hydrolizie:
- W środowisku kwaśnym: ester + woda → kwas + alkohol
- W środowisku zasadowym (nieodwracalna): ester + zasada → sól kwasu + alkohol
💡 Estry możemy nazywać podobnie jak sole kwasów, np. octan metylu (CH₃COOCH₃).
Tłuszcze to estry gliceryny i wyższych kwasów tłuszczowych:
H₂C-O-CO-R₁
|
HC-O-CO-R₂
|
H₂C-O-CO-R₃
Gdzie R₁, R₂, R₃ mogą być identyczne (tłuszcz syntetyczny) lub różne (tłuszcz naturalny).
Tłuszcze dzielimy na:
- Zwierzęce - zazwyczaj stałe, nasycone (smalec, słonina)
- Roślinne - zazwyczaj ciekłe, nienasycone, zawierają wiązania podwójne (oleje, oliwy)
Tłuszcze nienasycone można utwardzać poprzez addycję wodoru do wiązań podwójnych. Katalizatorem tej reakcji jest nikiel, który niestety jest rakotwórczy.
Tłuszcze ulegają hydrolizie (zmydlaniu) w środowisku zasadowym, dając mydła:
tłuszcz + 3NaOH → 3R-COONa + gliceryna
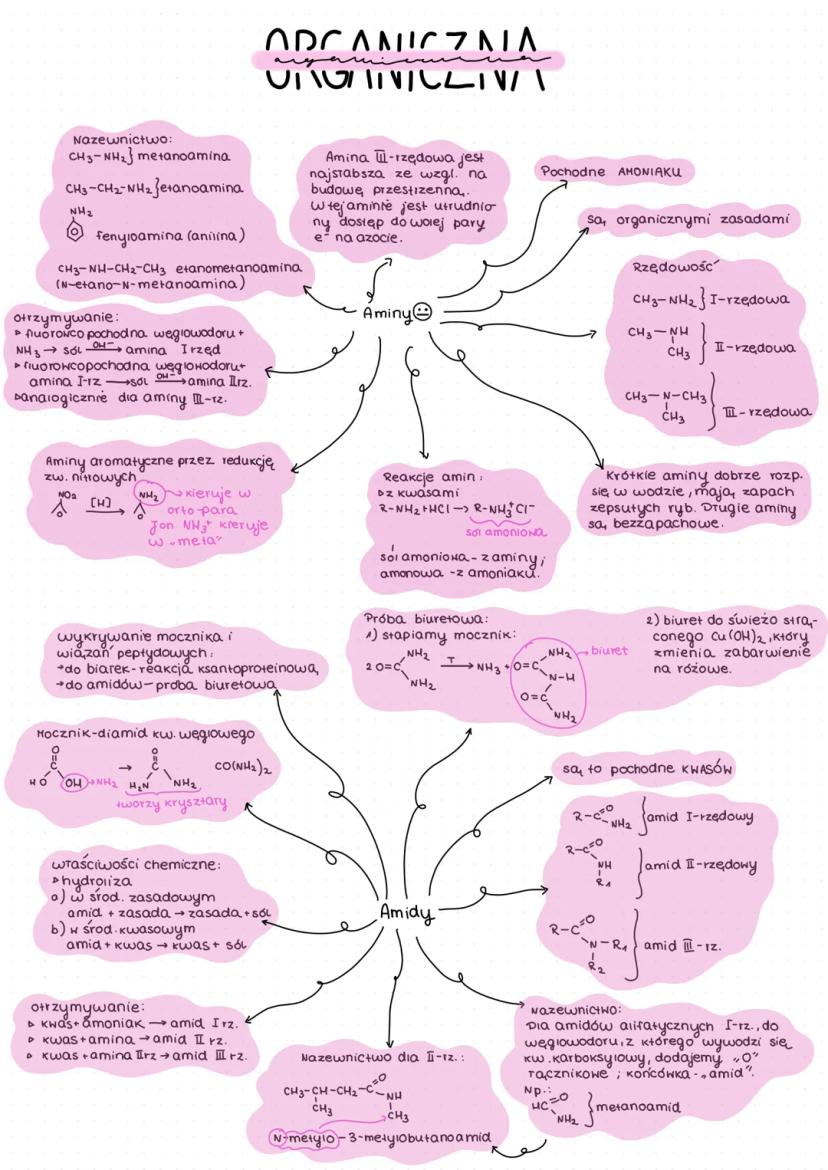
Aminy, amidy i pochodne amoniaku
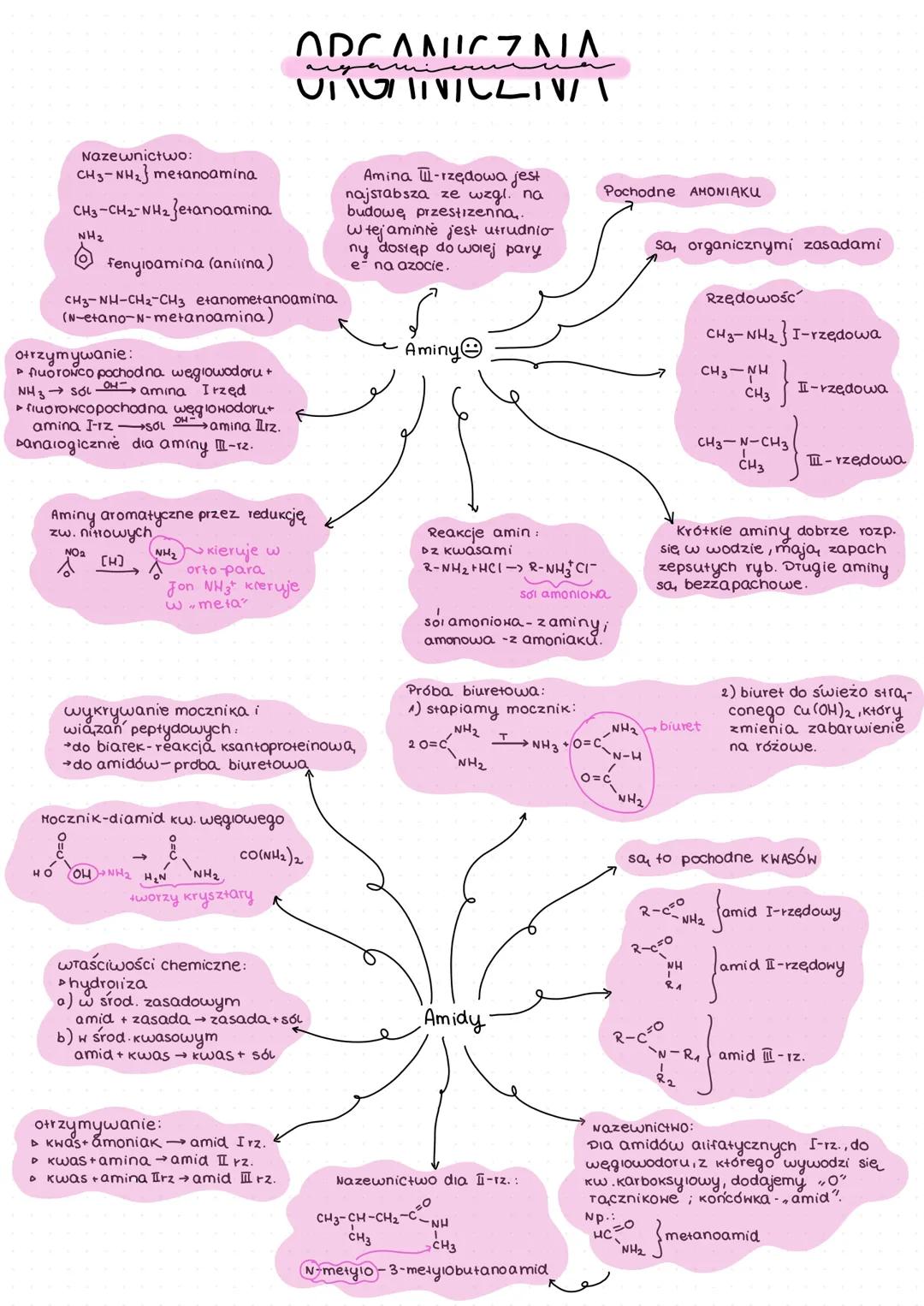
Aminy to organiczne pochodne amoniaku, w których atomy wodoru zostały zastąpione grupami alkilowymi lub arylowymi. Dzielimy je na:
- I-rzędowe: R-NH₂
- II-rzędowe: R-NH-R'
- III-rzędowe: R-N(R')(R'')
Krótkie aminy dobrze rozpuszczają się w wodzie i mają zapach przypominający zepsute ryby. Dłuższe aminy są bezzapachowe.
Aminy są zasadami organicznymi - reagują z kwasami tworząc sole amoniowe:
R-NH₂ + HCl → R-NH₃⁺Cl⁻
💡 Aminy III-rzędowe są najsłabszymi zasadami ze względu na utrudniony dostęp do wolnej pary elektronowej na azocie.
Amidy to pochodne kwasów karboksylowych, w których grupa -OH została zastąpiona grupą aminową lub jej pochodnymi. Dzielimy je na:
- I-rzędowe: R-CO-NH₂
- II-rzędowe: R-CO-NH-R'
- III-rzędowe: R-CO-N(R')(R'')
Amidy ulegają hydrolizie:
- W środowisku zasadowym: amid + zasada → zasada + sól
- W środowisku kwasowym: amid + kwas → kwas + sól
Mocznik to diamid kwasu węglowego, CO(NH₂)₂. Wykrywamy go za pomocą próby biuretowej - mocznik ogrzewany traci amoniak i tworzy biuret, który z Cu(OH)₂ daje różowe zabarwienie.
Aminy aromatyczne otrzymujemy przez redukcję związków nitrowych. Grupa -NH₂ w pierścieniu aromatycznym kieruje podstawniki do pozycji orto i para.
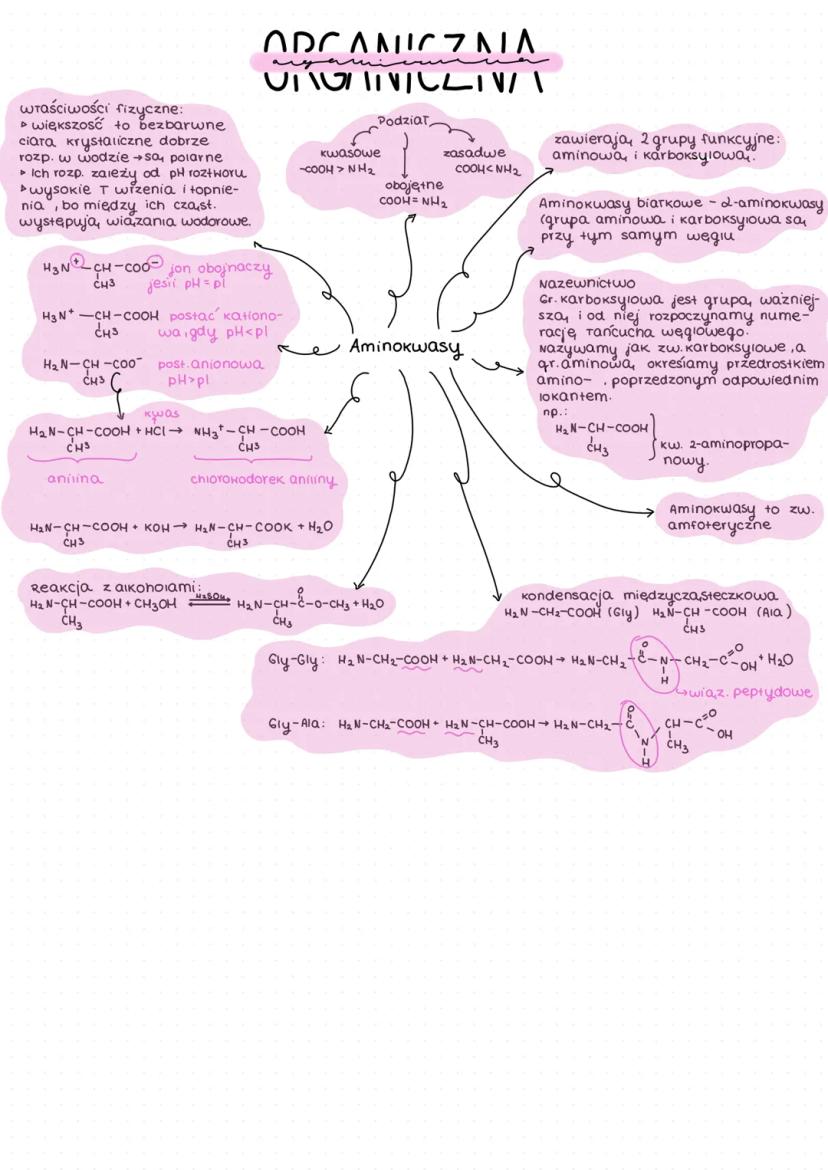
Aminokwasy i ich właściwości
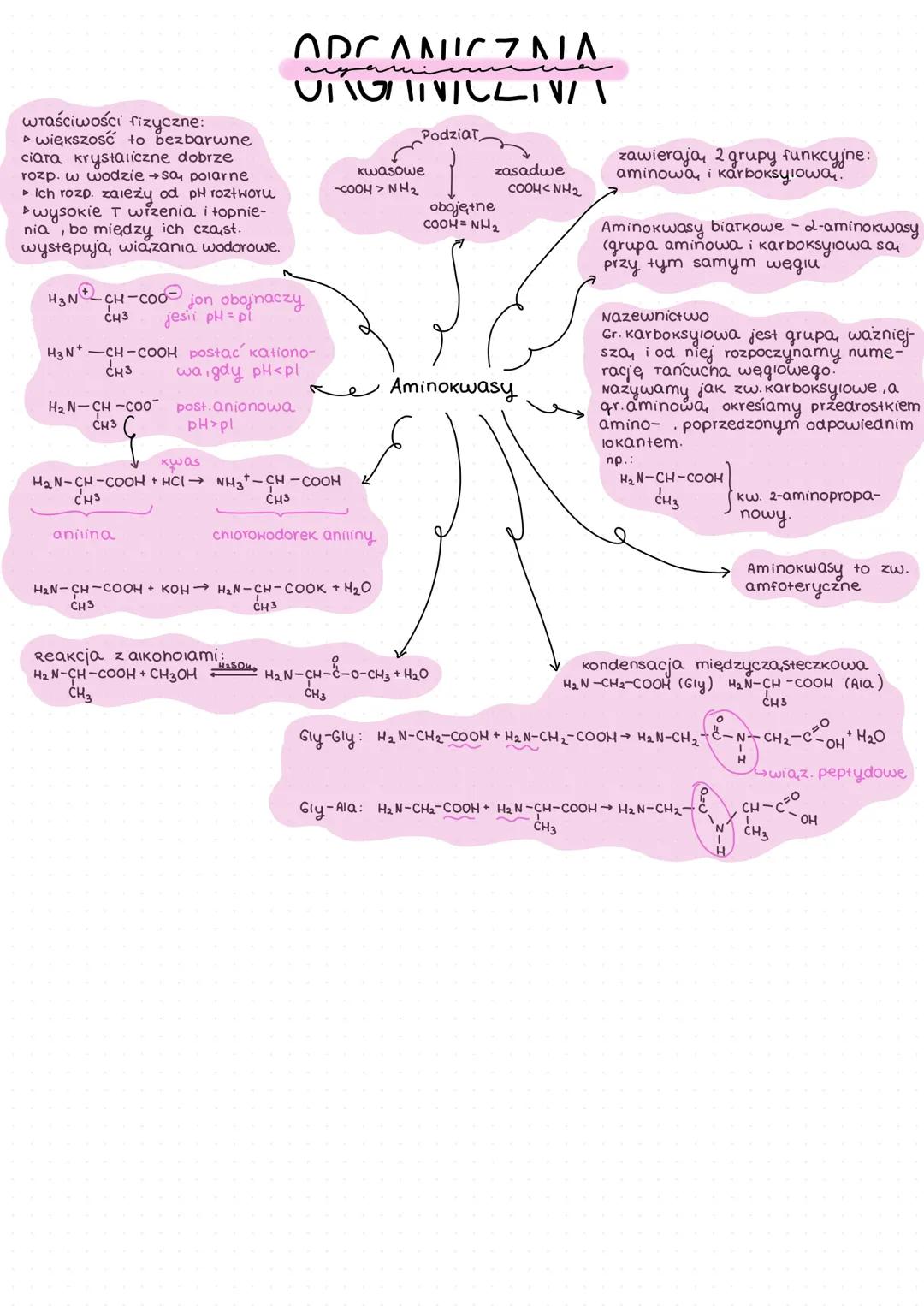
Aminokwasy zawierają dwie grupy funkcyjne: aminową i karboksylową . Aminokwasy białkowe to najczęściej α-aminokwasy (grupa aminowa i karboksylowa są przy tym samym atomie węgla).
Aminokwasy to związki amfoteryczne - mogą zachowywać się zarówno jak kwasy, jak i zasady, w zależności od środowiska:
- W roztworze o pH = pI (punkt izoelektryczny): jon obojnaczy H₃N⁺-CH(R)-COO⁻
- W roztworze kwaśnym (pH < pI): postać kationowa H₃N⁺-CH(R)-COOH
- W roztworze zasadowym (pH > pI): postać anionowa H₂N-CH(R)-COO⁻
💡 Rozpuszczalność aminokwasów zależy od pH roztworu. Najgorzej rozpuszczają się w swoim punkcie izoelektrycznym.
Aminokwasy mogą reagować ze sobą, tworząc wiązania peptydowe:
H₂N-CH₂-COOH + H₂N-CH(CH₃)-COOH → H₂N-CH₂-CO-NH-CH(CH₃)-COOH + H₂O
(Gly) (Ala) (Gly-Ala)
Ze względu na siłę grup funkcyjnych, aminokwasy możemy podzielić na:
- Kwasowe: siła -COOH > -NH₂
- Zasadowe: siła -COOH < -NH₂
- Obojętne: siła -COOH = -NH₂
Aminokwasy mają wysokie temperatury wrzenia i topnienia, ponieważ między ich cząsteczkami występują silne wiązania wodorowe. Większość aminokwasów to bezbarwne ciała krystaliczne dobrze rozpuszczalne w wodzie.
Izomeria związków organicznych
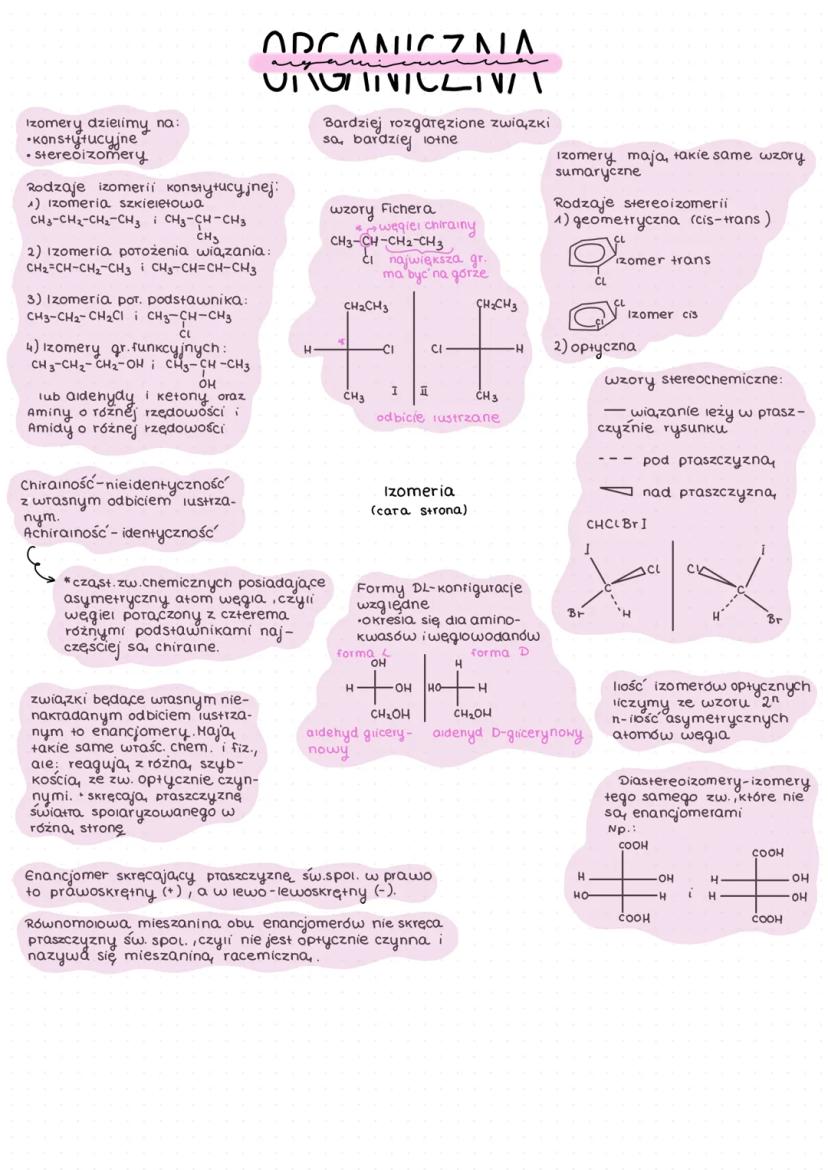
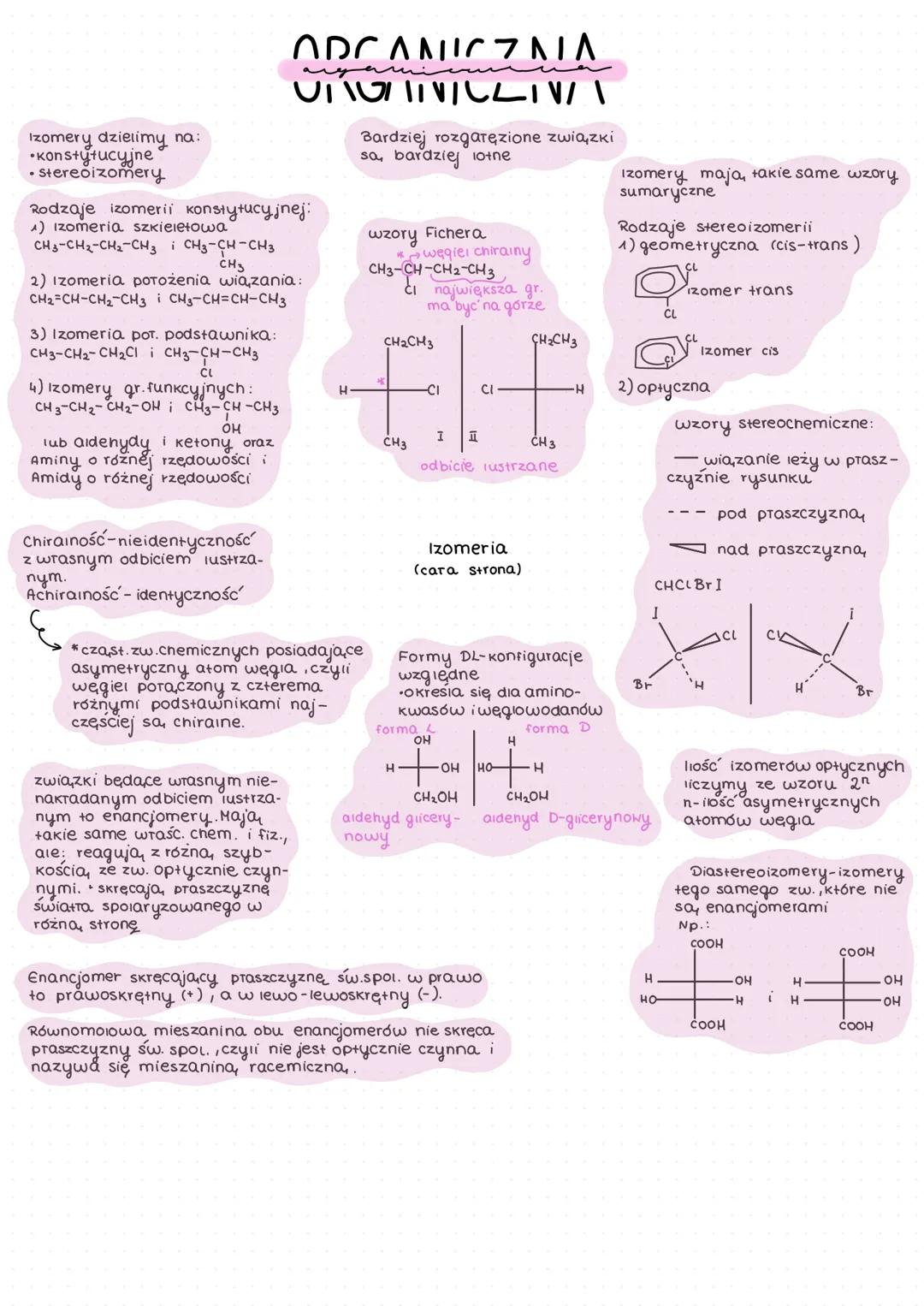
Izomery to związki o takim samym wzorze sumarycznym, ale różnej budowie. Dzielimy je na:
-
Izomery konstytucyjne - różnią się kolejnością atomów w cząsteczce
- Izomeria szkieletowa (różny układ łańcucha węglowego)
- Izomeria położenia wiązania (różna lokalizacja wiązań podwójnych lub potrójnych)
- Izomeria położenia podstawnika (różna lokalizacja grup funkcyjnych)
- Izomeria grup funkcyjnych (różne grupy funkcyjne, np. aldehydy i ketony)
-
Stereoizomery - różnią się ułożeniem atomów w przestrzeni
- Izomeria geometryczna - różne ułożenie podstawników względem płaszczyzny wiązania podwójnego
- Izomeria optyczna - związki będące swoim odbiciem lustrzanym
💡 Chiralność to nieidentyczność z własnym odbiciem lustrzanym. Cząsteczki chiralne najczęściej posiadają asymetryczny atom węgla - połączony z czterema różnymi podstawnikami.
Enancjomery to związki będące swoim nieprzystającym odbiciem lustrzanym. Mają takie same właściwości chemiczne i fizyczne, ale:
- Reagują z różną szybkością ze związkami optycznie czynnymi
- Skręcają płaszczyznę światła spolaryzowanego w przeciwne strony
Równomolowa mieszanina obu enancjomerów nazywa się mieszaniną racemiczną i nie jest optycznie czynna.
Ilość możliwych izomerów optycznych możemy obliczyć ze wzoru: 2ⁿ, gdzie n to liczba asymetrycznych atomów węgla w cząsteczce.
Diastereoizomery to stereizomery tego samego związku, które nie są enancjomerami.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: chemia organiczna
9Węglowodory nienasycone - alkeny
Notatka chemia rozszerzona- alkeny, chemia organiczna
Zatrucie i Właściwości Benzenu
Odkryj kluczowe informacje na temat benzenu, jego właściwości fizycznych i chemicznych, objawów zatrucia oraz reakcji chemicznych. Materiał obejmuje mechanizmy reakcji, takie jak bromowanie, nitrowanie i alkilowanie, a także skutki zdrowotne związane z narażeniem na benzen. Idealne dla studentów chemii i biologii.
Fluorowcopochodne Węglowodorów
Zrozumienie fluorowcopochodnych węglowodorów: ich struktura, właściwości oraz metody syntezy. Dowiedz się o reakcjach substytucji, eliminacji i addycji, a także o zastosowaniach praktycznych, takich jak produkcja teflonu i innych polimerów. Idealne dla studentów chemii organicznej.
Charakterystyczne Reakcje Chemii Organicznej
Odkryj kluczowe reakcje charakterystyczne w chemii organicznej, w tym reakcje biuretowe, ksantoproteinowe oraz próby Trommera i Tollensa. Zrozum, jak różne grupy funkcyjne, takie jak aminokwasy, cukry i fenole, reagują w różnych warunkach. Idealne dla studentów chemii poszukujących praktycznych informacji o reakcjach organicznych.
Chemia Benzenowa
Zgłębiaj chemię benzenową i jej reakcje. Dowiedz się o mechanizmach substytucji elektrofilowej, właściwościach benzenowych i toluenu, a także o reakcjach nitrowania, sulfonowania i alkilowania. Idealne dla studentów chemii, którzy chcą zrozumieć aromatyczne węglowodory i ich zastosowania.
Reakcje Chemiczne: Kluczowe Procesy
Kompleksowy przegląd najważniejszych reakcji chemicznych w chemii organicznej i nieorganicznej. Obejmuje reakcje amin, amidów, kwasów karboksylowych, hydrolizę, reakcje metali oraz doświadczenia takie jak próba Trommera i reakcja biuretowa. Idealne dla studentów przygotowujących się do egzaminów.
Aromatyczne Węglowodory: Benzen
Zgłębiaj właściwości benzenu, jego strukturę oraz mechanizmy reakcji, w tym substytucję i nitrowanie. Dowiedz się, jak benzen spełnia regułę Hückla i jakie cechy definiują węglowodory aromatyczne. Idealne dla studentów chemii.
Właściwości i Nazewnictwo Alkanów
Zgłębiaj właściwości fizyczne i chemiczne alkanów, ich nazewnictwo oraz metody syntezy. Notatka zawiera szczegółowe informacje o reakcjach spalania, charakterystyce węglowodorów nasyconych oraz przykłady zadań. Idealna dla studentów chemii organicznej.
Chemia związków węgla
Notatka z 1 tematu chemii organicznej - węgiel 6C i jego związki chemiczne na podstawie podr. Nowej Ery dla rozszerzenia
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Podstawy chemii organicznej - Przegląd dla maturzystów
Chemia organiczna to fascynujący dział chemii, który bada związki zawierające węgiel. W tych notatkach znajdziesz najważniejsze informacje dotyczące różnych grup związków organicznych - od alkoholi i fenoli, przez aldehydy i ketony, aż po kwasy karboksylowe, estry, aminy i aminokwasy.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkohole i reakcje związków organicznych
Alkohole to związki zawierające grupę hydroksylową połączoną z atomem węgla. Ich reaktywność zależy od rzędowości, czyli ilości atomów węgla połączonych z atomem węgla przy grupie -OH.
Alkohole możemy podzielić na:
- I-rzędowe - grupa -OH przy węglu skrajnym (połączonym z tylko jednym atomem węgla)
- II-rzędowe - grupa -OH przy węglu połączonym z dwoma atomami węgla
- III-rzędowe - grupa -OH przy węglu połączonym z trzema atomami węgla
Alkohole tworzą wiązania wodorowe, co wpływa na ich dobre rozpuszczanie w wodzie oraz podwyższenie temperatury wrzenia. Reagują z aktywnymi metalami tworząc alkolanolany (sole).
💡 Próba Lucasa pozwala określić rzędowość alkoholi: alkohol III-rzędowy reaguje błyskawicznie (widoczne zmętnienie), II-rzędowy po około 6 minutach, a I-rzędowy nie reaguje.
Podczas dehydratacji alkoholi (w obecności Al₂O₃) powstają alkeny i woda, np.: CH₃CH₂OH → CH₂=CH₂ + H₂O.
Alkohole można otrzymać poprzez:
- Addycję wody do alkenów
- Reakcję zasad z alkanami połączonymi z fluorowcami
Ponadto w notatce znajdziemy informacje o rozbijaniu wiązań podwójnych (addycja Cl₂ lub HCl), spalaniu całkowitym oraz o reaktywności podstawników w pierścieniach aromatycznych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Fenole i właściwości aromatów
Fenole to związki organiczne, w których grupa hydroksylowa jest bezpośrednio połączona z pierścieniem aromatycznym. W przeciwieństwie do alkoholi, fenole mają właściwości kwasowe.
Fenol to związek w postaci różowych kryształów o charakterystycznym zapachu. Słabo rozpuszcza się w zimnej wodzie, lepiej w ciepłej. Grupa -OH w fenolu uaktywnia pierścień, co wpływa na jego reaktywność.
Fenole możemy łatwo wykryć za pomocą chlorku żelaza(III):
fenol + FeCl₃ → żółta sól zmienia zabarwienie na fioletowe
💡 Grupa -OH w fenolach kieruje podstawniki do pozycji orto i para, co jest ważne w reakcjach substytucji.
Fenole mogą reagować z:
- Aktywnymi metalami
- Halogenami (dając produkty podstawienia w pozycji orto i para)
- Kwasami (podobnie jak inne alkohole)
- Wodą i CO₂, tworząc wodorowęglany
Związki z końcówką -tiol zawierają grupę -SH zamiast -OH, np. propan-1-tiol. Mają one mniejszą rozpuszczalność w wodzie.
Temperatury wrzenia alkoholi są wyższe niż odpowiadających im alkanów ze względu na wiązania wodorowe. Alkohole wielowodorotlenowe (np. gliceryna) mają więcej wiązań wodorowych, co dodatkowo poprawia ich rozpuszczalność w wodzie.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Aldehydy i ich właściwości
Aldehydy to związki organiczne zawierające grupę formylową , której charakterystyczną cechą są silne właściwości redukujące.
Aldehydy możemy wykryć za pomocą dwóch ważnych prób:
-
Próba Tollensa: aldehydy reagują z amoniakalnym roztworem tlenku srebra, tworząc metaliczne srebro (lustro srebrowe na ściankach probówki)
RCHO + Ag₂O → RCOOH + 2Ag↓ -
Próba Trommera: aldehydy redukują niebieski osad Cu(OH)₂ do ceglastoczerwonego Cu₂O
R-CHO + 2Cu(OH)₂ → R-COOH + Cu₂O↓ + 2H₂O
💡 Aldehydy z pierścieniem aromatycznym mają końcówkę "-karboaldehyd" w nazwie.
Aldehydy można otrzymać poprzez:
- Utlenianie alkoholi I-rzędowych
- Reakcję Kuczerowską, w której alkiny reagują z wodą w obecności jonów rtęci
Aldehydy i ketony są dla siebie izomerami - mają ten sam wzór sumaryczny, ale różnią się budową.
Podczas utleniania alkoholi:
- Alkohole I-rzędowe → aldehydy → kwasy karboksylowe
- Alkohole II-rzędowe → ketony
- Alkohole III-rzędowe nie ulegają utlenianiu

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Ketony i kwasy karboksylowe
Ketony to związki zawierające grupę ketonową umieszczoną pomiędzy dwoma atomami węgla. W przeciwieństwie do aldehydów, nie wykazują właściwości redukujących - dają negatywny wynik próby Tollensa.
Najprostszym ketonem jest aceton (propanon), który jest doskonałym rozpuszczalnikiem dla związków polarnych i niepolarnych. Ketony nazywamy dodając końcówkę "-on" do nazwy alkanu.
Próba jodoformowa służy do identyfikacji metyloketonów (grupa ketonowa sąsiadująca z grupą metylową). Podczas tej reakcji powstaje jodoform - żółtawy osad o charakterystycznym aptecznym zapachu.
💡 Ketony można otrzymać poprzez utlenianie alkoholi II-rzędowych lub w zmodyfikowanej reakcji Kuczerowskiej.
Kwasy karboksylowe zawierają grupę karboksylową . Ich ogólny wzór to CₙH₂ₙ₊₁COOH. Krótsze kwasy są cieczami dobrze rozpuszczalnymi w wodzie, mają charakterystyczne zapachy.
Kwasy karboksylowe można rozpoznać, bo:
- Reagują z aktywnymi metalami wydzielając wodór
- Reagują z zasadami tworząc sole
- Reagują z tlenkami metali
- Mogą być redukowane do aldehydów
Na moc kwasów wpływa efekt indukcyjny - podstawniki przyciągające elektrony (np. fluorowce) zwiększają moc kwasu. Im bliżej grupy karboksylowej znajduje się podstawnik, tym silniejszy jest jego wpływ.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Mydła, detergenty i właściwości kwasów
Kwasy karboksylowe w wodzie dysocjują na anion wodoru i kation reszty kwasowej. Mogą ulegać dekarboksylacji, podczas której tracą cząsteczkę CO₂.
Kwas mrówkowy (metanowy) ma właściwości redukujące i jako jedyny z kwasów karboksylowych daje pozytywny wynik w próbie Trommera i Tollensa. Grupa -COOH w pierścieniu aromatycznym kieruje podstawniki w pozycję meta.
Mydła to sole wyższych kwasów tłuszczowych. Mają budowę amfifilową - zawierają część hydrofilową (polarną, COO⁻Na⁺) i część hydrofobową (niepolarną, długi łańcuch węglowy). Dzięki tej budowie są zdolne do usuwania brudu.
💡 W twardej wodzie (zawierającej jony wapnia i magnezu) mydła tracą swoje właściwości myjące, ponieważ tworzą nierozpuszczalne sole.
Detergenty to substancje obniżające napięcie powierzchniowe cieczy. Są solami kwasów alkilosulfonowych lub wodorosiarczanów(VI) alkoholi. W przeciwieństwie do mydeł, są odporne na twardą wodę.
Cząsteczki mydła lub detergentu tworzą wokół cząstek brudu micele - struktury, w których hydrofobowe "ogony" są skierowane do wewnątrz (gdzie znajduje się brud), a hydrofilowe "głowy" na zewnątrz (gdzie jest woda). Mieszanie i pocieranie podczas prania pomaga oderwać cząstki brudu od tkaniny i zamknąć je w micelach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Estry i tłuszcze
Estry to związki powstające w reakcji estryfikacji między alkoholem/fenolem a kwasem (w obecności H₂SO₄):
R-COOH + ROH ⇄ R-COOR' + H₂O
Estry mają przyjemny, owocowy zapach. Ich temperatury wrzenia są podobne do alkanów o porównywalnej masie cząsteczkowej. Nie tworzą wiązań wodorowych, większość z nich to ciecze trudno rozpuszczalne w wodzie.
Estry mogą ulegać hydrolizie:
- W środowisku kwaśnym: ester + woda → kwas + alkohol
- W środowisku zasadowym (nieodwracalna): ester + zasada → sól kwasu + alkohol
💡 Estry możemy nazywać podobnie jak sole kwasów, np. octan metylu (CH₃COOCH₃).
Tłuszcze to estry gliceryny i wyższych kwasów tłuszczowych:
H₂C-O-CO-R₁
|
HC-O-CO-R₂
|
H₂C-O-CO-R₃
Gdzie R₁, R₂, R₃ mogą być identyczne (tłuszcz syntetyczny) lub różne (tłuszcz naturalny).
Tłuszcze dzielimy na:
- Zwierzęce - zazwyczaj stałe, nasycone (smalec, słonina)
- Roślinne - zazwyczaj ciekłe, nienasycone, zawierają wiązania podwójne (oleje, oliwy)
Tłuszcze nienasycone można utwardzać poprzez addycję wodoru do wiązań podwójnych. Katalizatorem tej reakcji jest nikiel, który niestety jest rakotwórczy.
Tłuszcze ulegają hydrolizie (zmydlaniu) w środowisku zasadowym, dając mydła:
tłuszcz + 3NaOH → 3R-COONa + gliceryna

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Aminy, amidy i pochodne amoniaku
Aminy to organiczne pochodne amoniaku, w których atomy wodoru zostały zastąpione grupami alkilowymi lub arylowymi. Dzielimy je na:
- I-rzędowe: R-NH₂
- II-rzędowe: R-NH-R'
- III-rzędowe: R-N(R')(R'')
Krótkie aminy dobrze rozpuszczają się w wodzie i mają zapach przypominający zepsute ryby. Dłuższe aminy są bezzapachowe.
Aminy są zasadami organicznymi - reagują z kwasami tworząc sole amoniowe:
R-NH₂ + HCl → R-NH₃⁺Cl⁻
💡 Aminy III-rzędowe są najsłabszymi zasadami ze względu na utrudniony dostęp do wolnej pary elektronowej na azocie.
Amidy to pochodne kwasów karboksylowych, w których grupa -OH została zastąpiona grupą aminową lub jej pochodnymi. Dzielimy je na:
- I-rzędowe: R-CO-NH₂
- II-rzędowe: R-CO-NH-R'
- III-rzędowe: R-CO-N(R')(R'')
Amidy ulegają hydrolizie:
- W środowisku zasadowym: amid + zasada → zasada + sól
- W środowisku kwasowym: amid + kwas → kwas + sól
Mocznik to diamid kwasu węglowego, CO(NH₂)₂. Wykrywamy go za pomocą próby biuretowej - mocznik ogrzewany traci amoniak i tworzy biuret, który z Cu(OH)₂ daje różowe zabarwienie.
Aminy aromatyczne otrzymujemy przez redukcję związków nitrowych. Grupa -NH₂ w pierścieniu aromatycznym kieruje podstawniki do pozycji orto i para.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Aminokwasy i ich właściwości
Aminokwasy zawierają dwie grupy funkcyjne: aminową i karboksylową . Aminokwasy białkowe to najczęściej α-aminokwasy (grupa aminowa i karboksylowa są przy tym samym atomie węgla).
Aminokwasy to związki amfoteryczne - mogą zachowywać się zarówno jak kwasy, jak i zasady, w zależności od środowiska:
- W roztworze o pH = pI (punkt izoelektryczny): jon obojnaczy H₃N⁺-CH(R)-COO⁻
- W roztworze kwaśnym (pH < pI): postać kationowa H₃N⁺-CH(R)-COOH
- W roztworze zasadowym (pH > pI): postać anionowa H₂N-CH(R)-COO⁻
💡 Rozpuszczalność aminokwasów zależy od pH roztworu. Najgorzej rozpuszczają się w swoim punkcie izoelektrycznym.
Aminokwasy mogą reagować ze sobą, tworząc wiązania peptydowe:
H₂N-CH₂-COOH + H₂N-CH(CH₃)-COOH → H₂N-CH₂-CO-NH-CH(CH₃)-COOH + H₂O
(Gly) (Ala) (Gly-Ala)
Ze względu na siłę grup funkcyjnych, aminokwasy możemy podzielić na:
- Kwasowe: siła -COOH > -NH₂
- Zasadowe: siła -COOH < -NH₂
- Obojętne: siła -COOH = -NH₂
Aminokwasy mają wysokie temperatury wrzenia i topnienia, ponieważ między ich cząsteczkami występują silne wiązania wodorowe. Większość aminokwasów to bezbarwne ciała krystaliczne dobrze rozpuszczalne w wodzie.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Izomeria związków organicznych
Izomery to związki o takim samym wzorze sumarycznym, ale różnej budowie. Dzielimy je na:
-
Izomery konstytucyjne - różnią się kolejnością atomów w cząsteczce
- Izomeria szkieletowa (różny układ łańcucha węglowego)
- Izomeria położenia wiązania (różna lokalizacja wiązań podwójnych lub potrójnych)
- Izomeria położenia podstawnika (różna lokalizacja grup funkcyjnych)
- Izomeria grup funkcyjnych (różne grupy funkcyjne, np. aldehydy i ketony)
-
Stereoizomery - różnią się ułożeniem atomów w przestrzeni
- Izomeria geometryczna - różne ułożenie podstawników względem płaszczyzny wiązania podwójnego
- Izomeria optyczna - związki będące swoim odbiciem lustrzanym
💡 Chiralność to nieidentyczność z własnym odbiciem lustrzanym. Cząsteczki chiralne najczęściej posiadają asymetryczny atom węgla - połączony z czterema różnymi podstawnikami.
Enancjomery to związki będące swoim nieprzystającym odbiciem lustrzanym. Mają takie same właściwości chemiczne i fizyczne, ale:
- Reagują z różną szybkością ze związkami optycznie czynnymi
- Skręcają płaszczyznę światła spolaryzowanego w przeciwne strony
Równomolowa mieszanina obu enancjomerów nazywa się mieszaniną racemiczną i nie jest optycznie czynna.
Ilość możliwych izomerów optycznych możemy obliczyć ze wzoru: 2ⁿ, gdzie n to liczba asymetrycznych atomów węgla w cząsteczce.
Diastereoizomery to stereizomery tego samego związku, które nie są enancjomerami.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: chemia organiczna
9Węglowodory nienasycone - alkeny
Notatka chemia rozszerzona- alkeny, chemia organiczna
Zatrucie i Właściwości Benzenu
Odkryj kluczowe informacje na temat benzenu, jego właściwości fizycznych i chemicznych, objawów zatrucia oraz reakcji chemicznych. Materiał obejmuje mechanizmy reakcji, takie jak bromowanie, nitrowanie i alkilowanie, a także skutki zdrowotne związane z narażeniem na benzen. Idealne dla studentów chemii i biologii.
Fluorowcopochodne Węglowodorów
Zrozumienie fluorowcopochodnych węglowodorów: ich struktura, właściwości oraz metody syntezy. Dowiedz się o reakcjach substytucji, eliminacji i addycji, a także o zastosowaniach praktycznych, takich jak produkcja teflonu i innych polimerów. Idealne dla studentów chemii organicznej.
Charakterystyczne Reakcje Chemii Organicznej
Odkryj kluczowe reakcje charakterystyczne w chemii organicznej, w tym reakcje biuretowe, ksantoproteinowe oraz próby Trommera i Tollensa. Zrozum, jak różne grupy funkcyjne, takie jak aminokwasy, cukry i fenole, reagują w różnych warunkach. Idealne dla studentów chemii poszukujących praktycznych informacji o reakcjach organicznych.
Chemia Benzenowa
Zgłębiaj chemię benzenową i jej reakcje. Dowiedz się o mechanizmach substytucji elektrofilowej, właściwościach benzenowych i toluenu, a także o reakcjach nitrowania, sulfonowania i alkilowania. Idealne dla studentów chemii, którzy chcą zrozumieć aromatyczne węglowodory i ich zastosowania.
Reakcje Chemiczne: Kluczowe Procesy
Kompleksowy przegląd najważniejszych reakcji chemicznych w chemii organicznej i nieorganicznej. Obejmuje reakcje amin, amidów, kwasów karboksylowych, hydrolizę, reakcje metali oraz doświadczenia takie jak próba Trommera i reakcja biuretowa. Idealne dla studentów przygotowujących się do egzaminów.
Aromatyczne Węglowodory: Benzen
Zgłębiaj właściwości benzenu, jego strukturę oraz mechanizmy reakcji, w tym substytucję i nitrowanie. Dowiedz się, jak benzen spełnia regułę Hückla i jakie cechy definiują węglowodory aromatyczne. Idealne dla studentów chemii.
Właściwości i Nazewnictwo Alkanów
Zgłębiaj właściwości fizyczne i chemiczne alkanów, ich nazewnictwo oraz metody syntezy. Notatka zawiera szczegółowe informacje o reakcjach spalania, charakterystyce węglowodorów nasyconych oraz przykłady zadań. Idealna dla studentów chemii organicznej.
Chemia związków węgla
Notatka z 1 tematu chemii organicznej - węgiel 6C i jego związki chemiczne na podstawie podr. Nowej Ery dla rozszerzenia
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.