Czas na chemię! To właśnie tu dowiesz się, z czego... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
389
•
Zaktualizowano Mar 12, 2026
•
lech
@lechhn
Czas na chemię! To właśnie tu dowiesz się, z czego... Pokaż więcej










Zacznijmy od najważniejszego - atom to najmniejsza cząstka pierwiastka, która zachowuje wszystkie jego właściwości. Wyobraź sobie, że to jak najmniejszy kawałek LEGO, z którego zbudowany jest cały świat!
Każdy atom składa się z trzech głównych części. Jądro atomowe zawiera protony (dodatnio naładowane) i neutrony (bez ładunku), które mają masę 1u. Wokół jądra krąży chmura elektronowa - to miejsce, gdzie znajdziesz elektrony (ujemnie naładowane), które są prawie 2000 razy lżejsze!
Izotopy to jak różne wersje tego samego pierwiastka - mają tę samą liczbę protonów, ale różną liczbę neutronów. Odmiany alotropowe to z kolei różne sposoby połączenia atomów tego samego pierwiastka.
💡 Zapamiętaj: p⁺ + n⁰ = A (liczba masowa), a liczba protonów = liczba elektronów w neutralnym atomie!

Stan kwantowy elektronu w atomie opisują cztery liczby kwantowe - to jak adres elektronów w atomie! Główna liczba kwantowa (n) określa energię i tworzy powłoki K, L, M, N. Poboczna liczba kwantowa (l) opisuje kształt orbitali: s, p, d, f.
Magnetyczna liczba kwantowa (m) pokazuje orientację orbitali w przestrzeni. Magnetyczna spinowa liczba kwantowa (ms) to kierunek "wirowania" elektronu wokół własnej osi - może być +1/2 lub -1/2.
Zakaz Pauliego mówi, że w atomie nie mogą być dwa identyczne elektrony - każdy musi mieć unikalny "adres"! Na każdej powłoce może być maksymalnie 2n² elektronów: K=2, L=8, M=18.
💡 Przykład: 13Al ma konfigurację K²L⁸M³ - oznacza to 2 elektrony na powłoce K, 8 na L i 3 na M!

Zjawiska fizyczne to zmiany, które nie tworzą nowych substancji (jak topnienie lodu). Przemiany chemiczne to reakcje, gdzie powstają zupełnie nowe substancje z nowymi właściwościami!
Trzy najważniejsze prawa, które musisz znać: Prawo zachowania masy - w reakcji nic nie ginie, masa substratów = masa produktów. Prawo stałości układu - stosunek mas pierwiastków w związku jest zawsze taki sam.
Prawo Avogadra mówi, że jednakowe objętości gazów w tych samych warunkach zawierają tyle samo cząsteczek. W warunkach normalnych jeden mol gazu zajmuje 22,415 dm³ i zawiera 6,023 × 10²³ cząsteczek.
💡 Do zapamiętania: Liczba Avogadra (6,023 × 10²³) to jak "chemiczna tuzin" - uniwersalna jednostka liczenia cząsteczek!

Układ okresowy to genialna mapa wszystkich pierwiastków! Okresy (poziomo) grupują atomy z tą samą liczbą powłok elektronowych. Grupy (pionowo) zawierają pierwiastki o tej samej liczbie elektronów walencyjnych.
Reguła oktetu i dubletu wyjaśnia, dlaczego atomy się łączą - każdy chce mieć konfigurację najbliższego gazu szlachetnego, bo to najstabilniejszy stan. Sód (Na) oddaje jeden elektron i staje się jak neon!
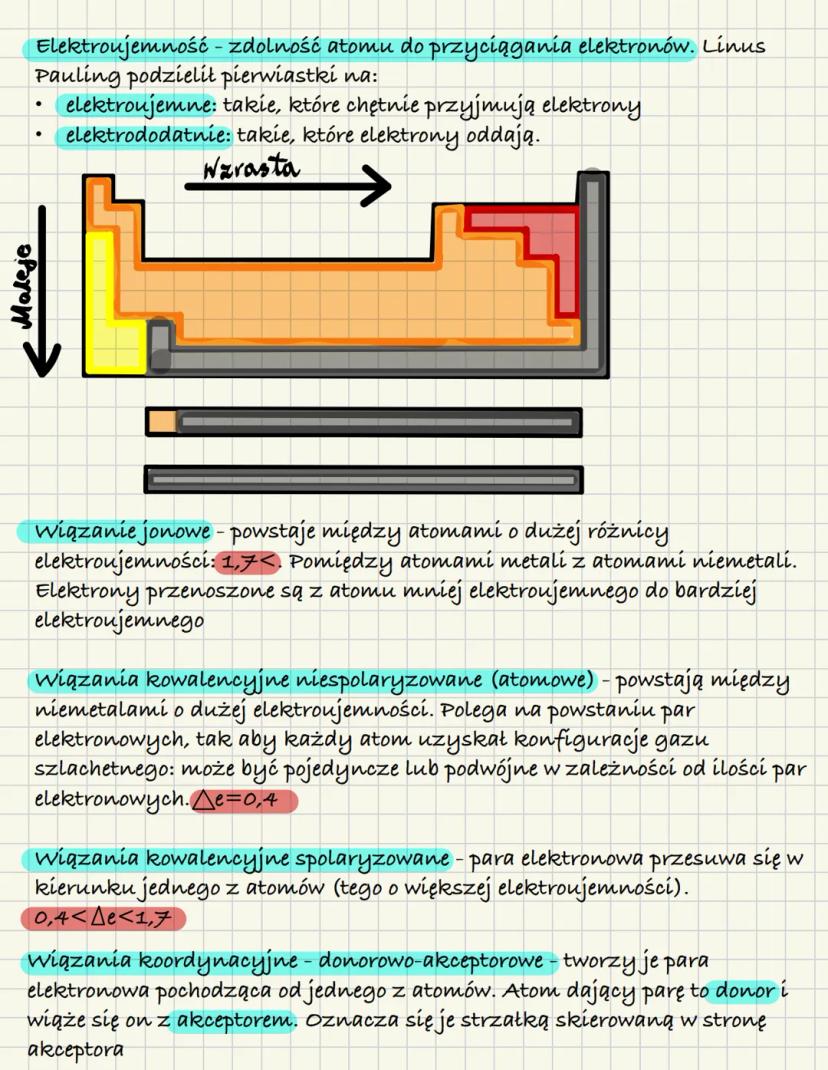
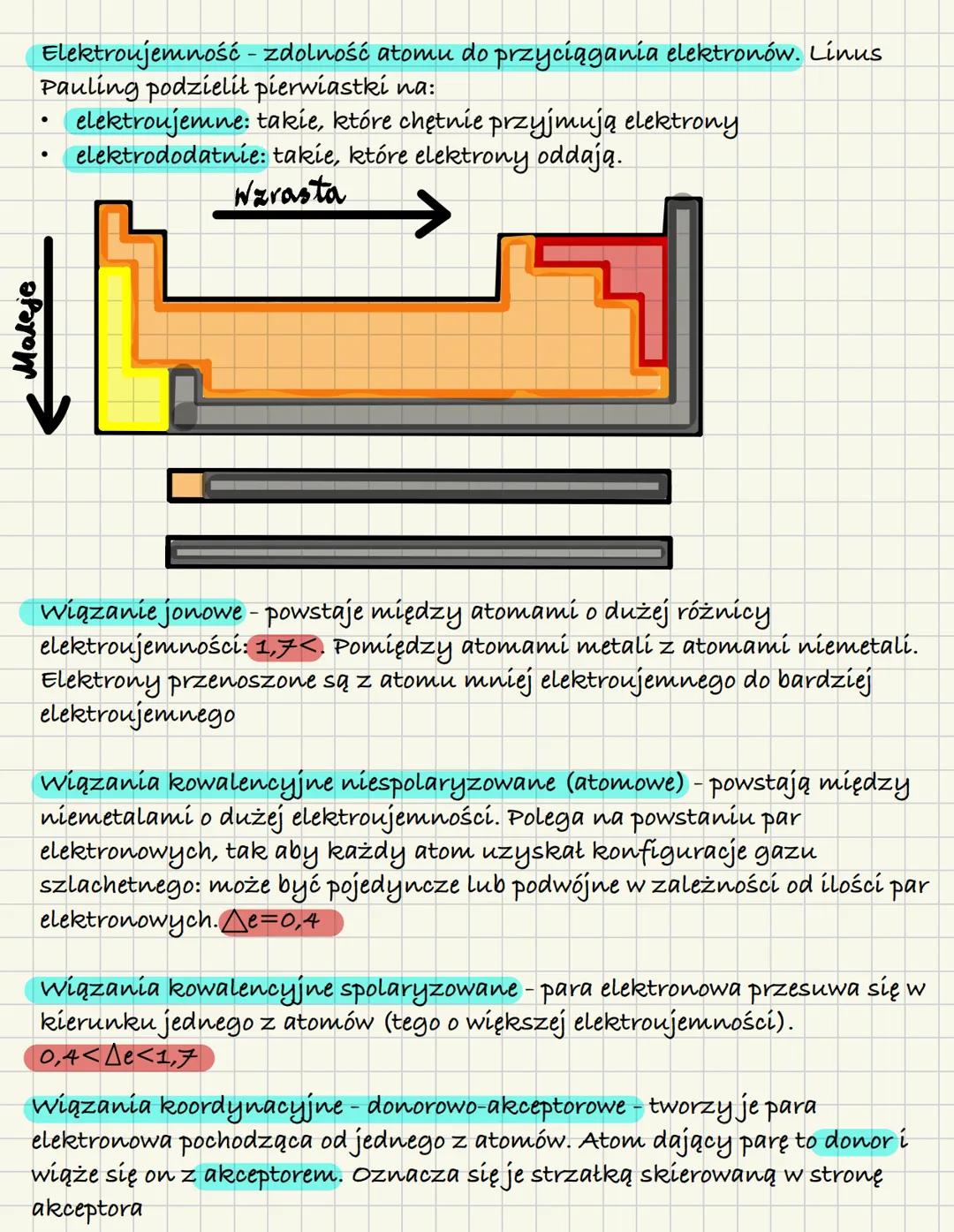
Elektroujemność to "chciwość" atomu na elektrony. Linus Pauling podzielił pierwiastki na elektroujemne (chcą elektrony) i elektrododatnie (oddają elektrony). Ta właściwość decyduje o typie wiązania między atomami.
💡 Wskazówka: W układzie okresowym elektroujemność rośnie w prawo i w górę - fluor jest najbardziej "chciwy"!

Wiązanie jonowe powstaje między metalem a niemetalem, gdy różnica elektroujemności > 1,7. Elektron przeskakuje od jednego atomu do drugiego - powstają jony! Wiązanie kowalencyjne to wspólne "dzielenie się" elektronami między niemetalami.
Gdy elektrony są dzielone równo, mamy wiązanie kowalencyjne niespolaryzowane (Δε < 0,4). Gdy jeden atom bardziej przyciąga elektrony, powstaje wiązanie spolaryzowane (0,4 < Δε < 1,7).
Wiązanie koordynacyjne to specjalny typ - jeden atom daje gotową parę elektronów drugiemu atomowi. Wiązanie metaliczne występuje w metalach, gdzie elektrony tworzą "morze elektronowe".
💡 Pamięć: Wiązania wodorowe to "mostki" między cząsteczkami - dlatego woda ma tak wysoką temperaturę wrzenia!
Reakcje chemiczne dzielą się na syntezy (łączenie), analizy (rozkład) i wymiany (pojedyncze lub podwójne). Reakcje nieodwracalne przebiegają do końca (→), a odwracalne mogą iść w obie strony (⇌).
Równowaga chemiczna to stan, gdy reakcja zachodzi w obu kierunkach z tą samą szybkością. Reguła Le Chateliera mówi, że system zawsze próbuje przeciwstawić się zmianom - zwiększasz temperaturę, reakcja "ucieka" w stronę chłodniejszą!
Mieszaniny jednorodne (roztwory) to takie, gdzie nie widać składników. Mieszaniny niejednorodne to te, gdzie można rozróżnić składniki gołym okiem lub pod mikroskopem.
💡 Przykład: Gdy dodasz cukier do kawy i zamieszasz - powstaje roztwór jednorodny. Olej z wodą to mieszanina niejednorodna!

Roztwory to mieszaniny jednorodne składające się z substancji rozpuszczonej i rozpuszczalnika. Mogą być nienasycone (można dodać więcej substancji), nasycone (maksymalna ilość) lub przesycone (więcej niż maksimum).
Rozpuszczalność to masa substancji, którą można rozpuścić w 100g rozpuszczalnika w danej temperaturze. Stężenie procentowe pokazuje, ile gramów substancji jest w 100g roztworu: Cp = × 100%.
Stężenie molowe to liczba moli substancji w 1 dm³ roztworu: Cm = n/V. Te dwa stężenia można przeliczać wzorem: Cm = (Cp × d)/(M × 100%), gdzie d to gęstość, a M to masa molowa.
💡 Praktycznie: Stężenie procentowe używasz w kuchni (np. 3% ocet), a molowe w laboratorium chemicznym!

Dysocjacja elektrolityczna to rozkład związku na jony pod wpływem wody. Dlatego roztwory soli przewodzą prąd - jony są nośnikami ładunku! Wodne roztwory kwasów, zasad i soli to elektrolity.
Woda jest świetnym rozpuszczalnikiem przez swoją polarną budowę - cząsteczki H₂O "rozbijają" wiązania jonowe i kowalencyjne spolaryzowane. Kwasy wieloprotonowe dysocjują stopniowo - najpierw oddają jeden proton, potem kolejny.
Stopień dysocjacji (α) pokazuje, jaka część elektrolitu rozpadła się na jony: α = n(zdysocjowane)/n(całkowite). Elektrolity mocne mają α > 30%, średnie 5-30%, a słabe < 5%.
💡 Ciekawostka: Kwas solny (HCl) to elektrolit mocny - dysocjuje niemal w 100%, a kwas octowy to elektrolit słaby!


Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
lech
@lechhn
Czas na chemię! To właśnie tu dowiesz się, z czego składa się cały świat wokół ciebie - od atomów w twoim telefonie, po reakcje w twoim organizmie. Przygotuj się na odkrycie tajemnic materii i poznanie praw, które rządzą wszechświatem na... Pokaż więcej

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Zacznijmy od najważniejszego - atom to najmniejsza cząstka pierwiastka, która zachowuje wszystkie jego właściwości. Wyobraź sobie, że to jak najmniejszy kawałek LEGO, z którego zbudowany jest cały świat!
Każdy atom składa się z trzech głównych części. Jądro atomowe zawiera protony (dodatnio naładowane) i neutrony (bez ładunku), które mają masę 1u. Wokół jądra krąży chmura elektronowa - to miejsce, gdzie znajdziesz elektrony (ujemnie naładowane), które są prawie 2000 razy lżejsze!
Izotopy to jak różne wersje tego samego pierwiastka - mają tę samą liczbę protonów, ale różną liczbę neutronów. Odmiany alotropowe to z kolei różne sposoby połączenia atomów tego samego pierwiastka.
💡 Zapamiętaj: p⁺ + n⁰ = A (liczba masowa), a liczba protonów = liczba elektronów w neutralnym atomie!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Stan kwantowy elektronu w atomie opisują cztery liczby kwantowe - to jak adres elektronów w atomie! Główna liczba kwantowa (n) określa energię i tworzy powłoki K, L, M, N. Poboczna liczba kwantowa (l) opisuje kształt orbitali: s, p, d, f.
Magnetyczna liczba kwantowa (m) pokazuje orientację orbitali w przestrzeni. Magnetyczna spinowa liczba kwantowa (ms) to kierunek "wirowania" elektronu wokół własnej osi - może być +1/2 lub -1/2.
Zakaz Pauliego mówi, że w atomie nie mogą być dwa identyczne elektrony - każdy musi mieć unikalny "adres"! Na każdej powłoce może być maksymalnie 2n² elektronów: K=2, L=8, M=18.
💡 Przykład: 13Al ma konfigurację K²L⁸M³ - oznacza to 2 elektrony na powłoce K, 8 na L i 3 na M!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Zjawiska fizyczne to zmiany, które nie tworzą nowych substancji (jak topnienie lodu). Przemiany chemiczne to reakcje, gdzie powstają zupełnie nowe substancje z nowymi właściwościami!
Trzy najważniejsze prawa, które musisz znać: Prawo zachowania masy - w reakcji nic nie ginie, masa substratów = masa produktów. Prawo stałości układu - stosunek mas pierwiastków w związku jest zawsze taki sam.
Prawo Avogadra mówi, że jednakowe objętości gazów w tych samych warunkach zawierają tyle samo cząsteczek. W warunkach normalnych jeden mol gazu zajmuje 22,415 dm³ i zawiera 6,023 × 10²³ cząsteczek.
💡 Do zapamiętania: Liczba Avogadra (6,023 × 10²³) to jak "chemiczna tuzin" - uniwersalna jednostka liczenia cząsteczek!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Układ okresowy to genialna mapa wszystkich pierwiastków! Okresy (poziomo) grupują atomy z tą samą liczbą powłok elektronowych. Grupy (pionowo) zawierają pierwiastki o tej samej liczbie elektronów walencyjnych.
Reguła oktetu i dubletu wyjaśnia, dlaczego atomy się łączą - każdy chce mieć konfigurację najbliższego gazu szlachetnego, bo to najstabilniejszy stan. Sód (Na) oddaje jeden elektron i staje się jak neon!
Elektroujemność to "chciwość" atomu na elektrony. Linus Pauling podzielił pierwiastki na elektroujemne (chcą elektrony) i elektrododatnie (oddają elektrony). Ta właściwość decyduje o typie wiązania między atomami.
💡 Wskazówka: W układzie okresowym elektroujemność rośnie w prawo i w górę - fluor jest najbardziej "chciwy"!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Wiązanie jonowe powstaje między metalem a niemetalem, gdy różnica elektroujemności > 1,7. Elektron przeskakuje od jednego atomu do drugiego - powstają jony! Wiązanie kowalencyjne to wspólne "dzielenie się" elektronami między niemetalami.
Gdy elektrony są dzielone równo, mamy wiązanie kowalencyjne niespolaryzowane (Δε < 0,4). Gdy jeden atom bardziej przyciąga elektrony, powstaje wiązanie spolaryzowane (0,4 < Δε < 1,7).
Wiązanie koordynacyjne to specjalny typ - jeden atom daje gotową parę elektronów drugiemu atomowi. Wiązanie metaliczne występuje w metalach, gdzie elektrony tworzą "morze elektronowe".
💡 Pamięć: Wiązania wodorowe to "mostki" między cząsteczkami - dlatego woda ma tak wysoką temperaturę wrzenia!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Reakcje chemiczne dzielą się na syntezy (łączenie), analizy (rozkład) i wymiany (pojedyncze lub podwójne). Reakcje nieodwracalne przebiegają do końca (→), a odwracalne mogą iść w obie strony (⇌).
Równowaga chemiczna to stan, gdy reakcja zachodzi w obu kierunkach z tą samą szybkością. Reguła Le Chateliera mówi, że system zawsze próbuje przeciwstawić się zmianom - zwiększasz temperaturę, reakcja "ucieka" w stronę chłodniejszą!
Mieszaniny jednorodne (roztwory) to takie, gdzie nie widać składników. Mieszaniny niejednorodne to te, gdzie można rozróżnić składniki gołym okiem lub pod mikroskopem.
💡 Przykład: Gdy dodasz cukier do kawy i zamieszasz - powstaje roztwór jednorodny. Olej z wodą to mieszanina niejednorodna!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Roztwory to mieszaniny jednorodne składające się z substancji rozpuszczonej i rozpuszczalnika. Mogą być nienasycone (można dodać więcej substancji), nasycone (maksymalna ilość) lub przesycone (więcej niż maksimum).
Rozpuszczalność to masa substancji, którą można rozpuścić w 100g rozpuszczalnika w danej temperaturze. Stężenie procentowe pokazuje, ile gramów substancji jest w 100g roztworu: Cp = × 100%.
Stężenie molowe to liczba moli substancji w 1 dm³ roztworu: Cm = n/V. Te dwa stężenia można przeliczać wzorem: Cm = (Cp × d)/(M × 100%), gdzie d to gęstość, a M to masa molowa.
💡 Praktycznie: Stężenie procentowe używasz w kuchni (np. 3% ocet), a molowe w laboratorium chemicznym!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dysocjacja elektrolityczna to rozkład związku na jony pod wpływem wody. Dlatego roztwory soli przewodzą prąd - jony są nośnikami ładunku! Wodne roztwory kwasów, zasad i soli to elektrolity.
Woda jest świetnym rozpuszczalnikiem przez swoją polarną budowę - cząsteczki H₂O "rozbijają" wiązania jonowe i kowalencyjne spolaryzowane. Kwasy wieloprotonowe dysocjują stopniowo - najpierw oddają jeden proton, potem kolejny.
Stopień dysocjacji (α) pokazuje, jaka część elektrolitu rozpadła się na jony: α = n(zdysocjowane)/n(całkowite). Elektrolity mocne mają α > 30%, średnie 5-30%, a słabe < 5%.
💡 Ciekawostka: Kwas solny (HCl) to elektrolit mocny - dysocjuje niemal w 100%, a kwas octowy to elektrolit słaby!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
13
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS