Chrom, mangan, żelazo i miedź to metale przejściowe o niezwykle... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
2,465
•
Zaktualizowano May 14, 2026
•
Ma dzia
@madzia_hphl
Chrom, mangan, żelazo i miedź to metale przejściowe o niezwykle... Pokaż więcej




Chrom to twardy i kruchy metal, który występuje głównie na stopniach utlenienia II, III i VI. Na powietrzu ulega pasywacji - tworzy warstwę ochronną tlenku, która chroni go przed dalszym utlenianiem. Ciekawostką jest, że w konfiguracji elektronowej chromu ([Ar] 4s¹3d⁵) występuje promocja elektronowa z podpowłoki 4s na 3d.
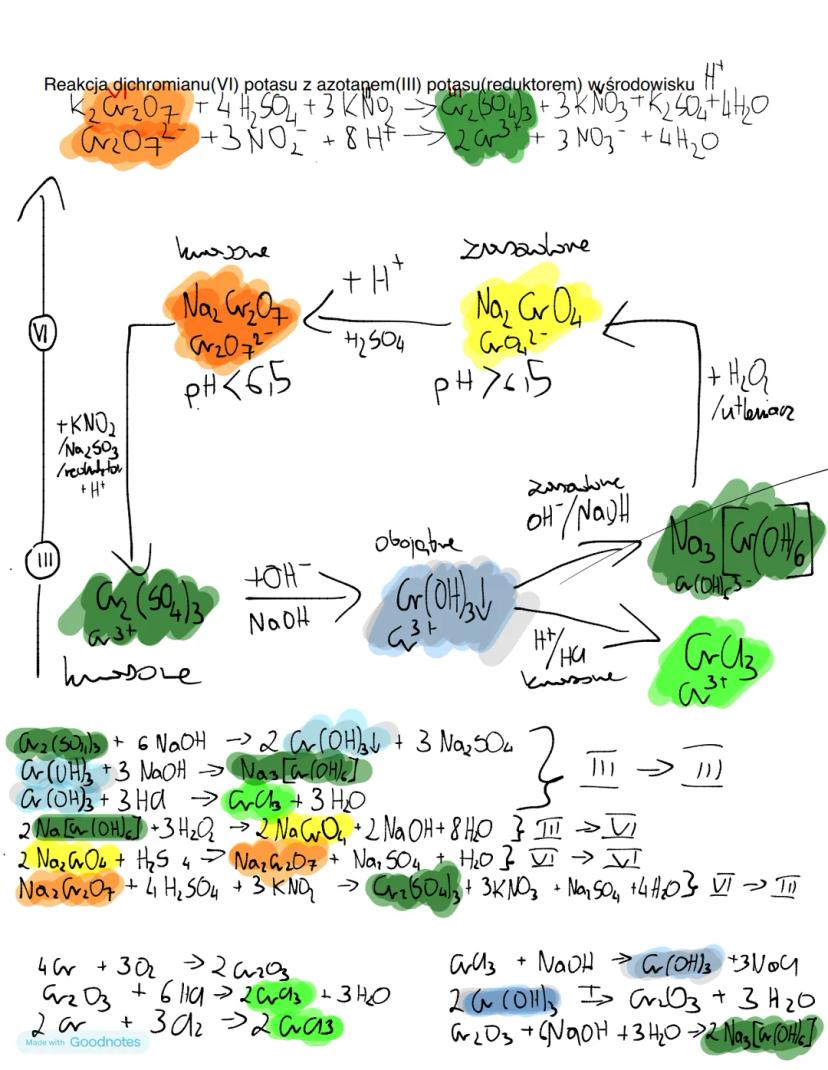
Związki chromu wykazują różny charakter chemiczny zależnie od stopnia utlenienia. Związki Cr(II) mają charakter zasadowy, Cr(III) - amfoteryczny, a Cr(VI) - kwasowy. Wraz ze wzrostem stopnia utlenienia zwiększają się właściwości utleniające i kwasowe związków chromu.
Wodorotlenek chromu(III) Cr(OH)₃ jest doskonałym przykładem związku amfoterycznego:
Warto zapamiętać! W zależności od pH roztworu związki chromu(VI) występują jako jony chromianowe CrO₄²⁻ (żółty roztwór, pH>6,5) lub dichromianowe Cr₂O₇²⁻ (pomarańczowy roztwór, pH<6,5).
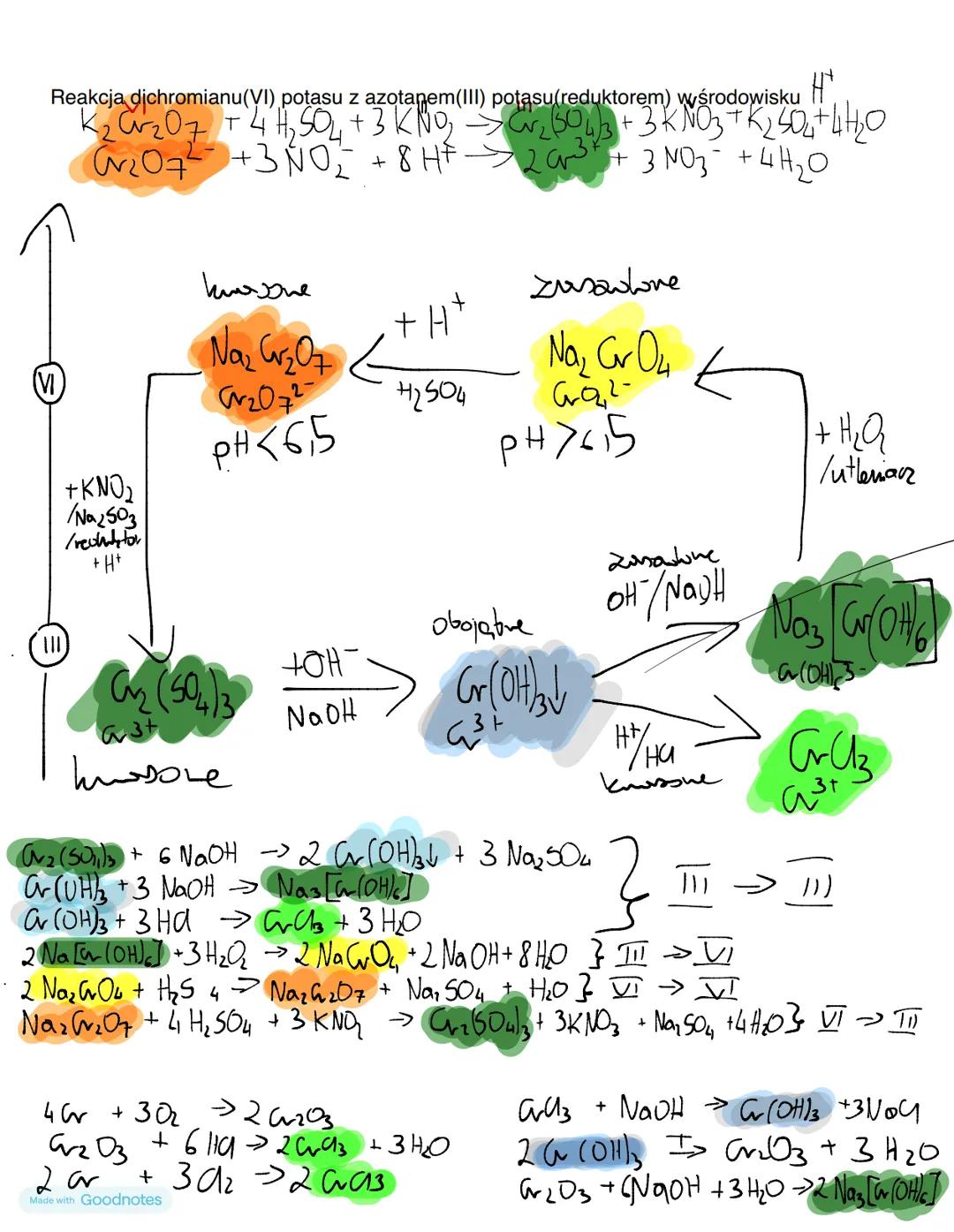
Najważniejsze przemiany związków chromu można przedstawić jako cykl reakcji. Dichromian sodu w środowisku kwasowym (pH<6,5) przechodzi w jon Cr₂O₇²⁻, a w środowisku zasadowym (pH>6,5) w jon CrO₄²⁻. Te przemiany są odwracalne.
Przy działaniu reduktorów (np. Na₂SO₃, KNO₂) w środowisku kwasowym związki chromu(VI) redukują się do związków chromu(III). Przykładowa reakcja:
Siarczany chromu(III) w reakcji z NaOH tworzą wodorotlenek chromu(III), który może dalej reagować zarówno z kwasami (tworząc jony Cr³⁺), jak i z nadmiarem zasad (tworząc hydroksokompleksy). Co ciekawe, w warunkach utleniających związki chromu(III) mogą przejść w związki chromu(VI).
Praktyczna wskazówka! Zmiana barwy roztworu często sygnalizuje zmianę stopnia utlenienia chromu - od zielonej (Cr³⁺) przez żółtą (CrO₄²⁻) do pomarańczowej (Cr₂O₇²⁻). To doskonały wskaźnik wizualny przy analizie chemicznej.
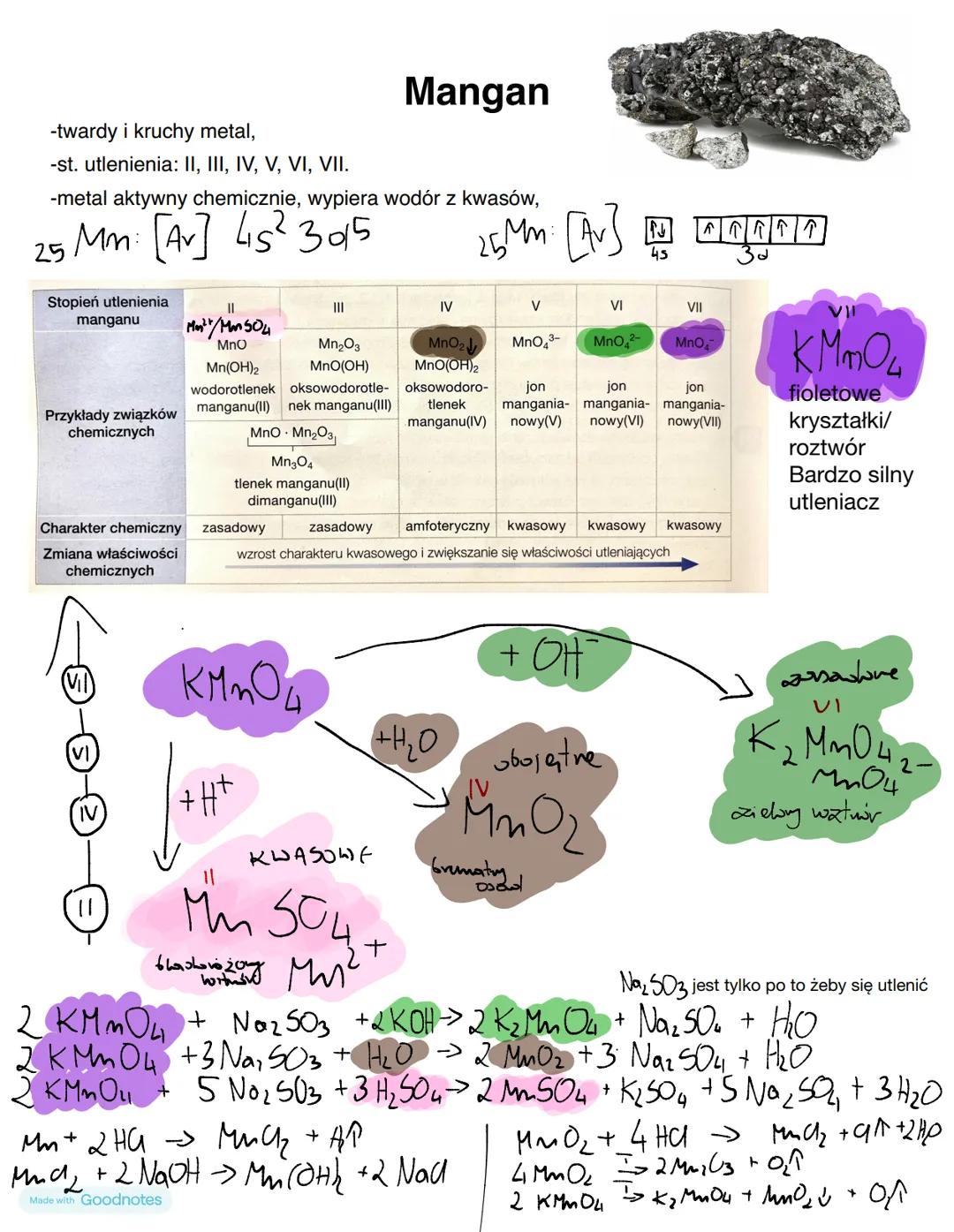
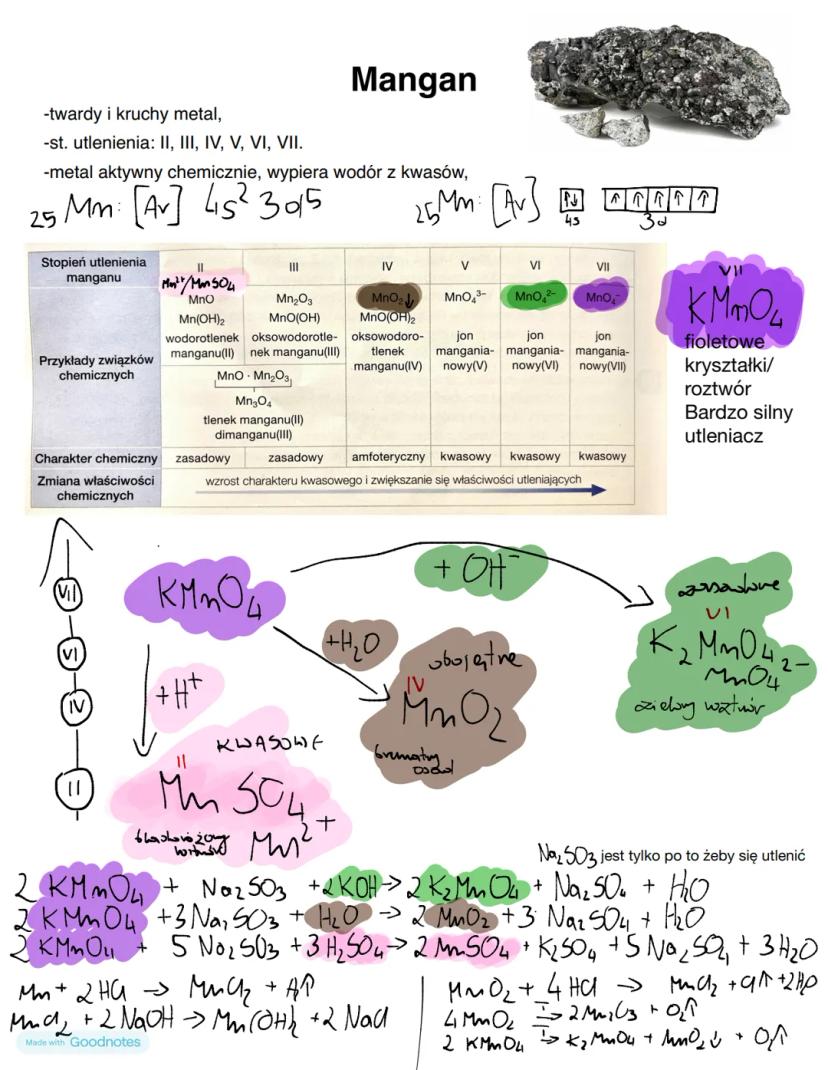
Mangan to twardy i kruchy metal o konfiguracji elektronowej [Ar] 4s²3d⁵. Jest bardzo aktywny chemicznie i może występować na wielu stopniach utlenienia: II, III, IV, V, VI i VII. Ta różnorodność daje mu niezwykłe bogactwo związków chemicznych.
Podobnie jak w przypadku chromu, związki manganu zmieniają swój charakter w zależności od stopnia utlenienia:
Mangan tworzy szereg tlenków i wodorotlenków o różnorodnych właściwościach. Szczególnie ważny jest tlenek manganu(IV) (MnO₂), który może być zarówno utleniaczem, jak i reduktorem. Manganianyjowe jony manganu(VII) (MnO₄⁻) są silnymi utleniaczami i nadają roztworom charakterystyczną fioletową barwę.
Ciekawostka! Nadmanganian potasu (KMnO₄) jest tak silnym utleniaczem, że ma właściwości dezynfekujące i jest używany jako środek antyseptyczny. Jeśli dodasz go do roztworu zawierającego substancje redukujące, zaobserwujesz odbarwienie fioletowego roztworu!

Żelazo to jeden z najważniejszych metali przemysłowych, który występuje głównie na II i III stopniu utlenienia. W zależności od temperatury tworzy cztery odmiany alotropowe, co ma ogromne znaczenie w metalurgii i produkcji stali.
Tlenki i wodorotlenki żelaza (FeO, Fe₂O₃, Fe(OH)₂, Fe(OH)₃) wykazują charakter amfoteryczny, co oznacza, że mogą reagować zarówno z kwasami, jak i zasadami. Żelazo jest dość reaktywne - reaguje z kwasami wypierając wodór , a także bezpośrednio z chlorem .
Ważnym zjawiskiem jest pasywacja żelaza - reakcja ze stężonymi kwasami utleniającymi (HNO₃, H₂SO₄), która prowadzi do utworzenia warstwy ochronnej tlenku FeO na powierzchni metalu. Ta warstwa chroni żelazo przed dalszym utlenianiem i działaniem czynników zewnętrznych.
W praktyce! Zjawisko pasywacji wykorzystuje się w ochronie antykorozyjnej konstrukcji stalowych. Chociaż rdza (tlenek żelaza) może zniszczyć stal, to odpowiednio wytworzona warstwa pasywacyjna może skutecznie chronić metal przed zniszczeniem.
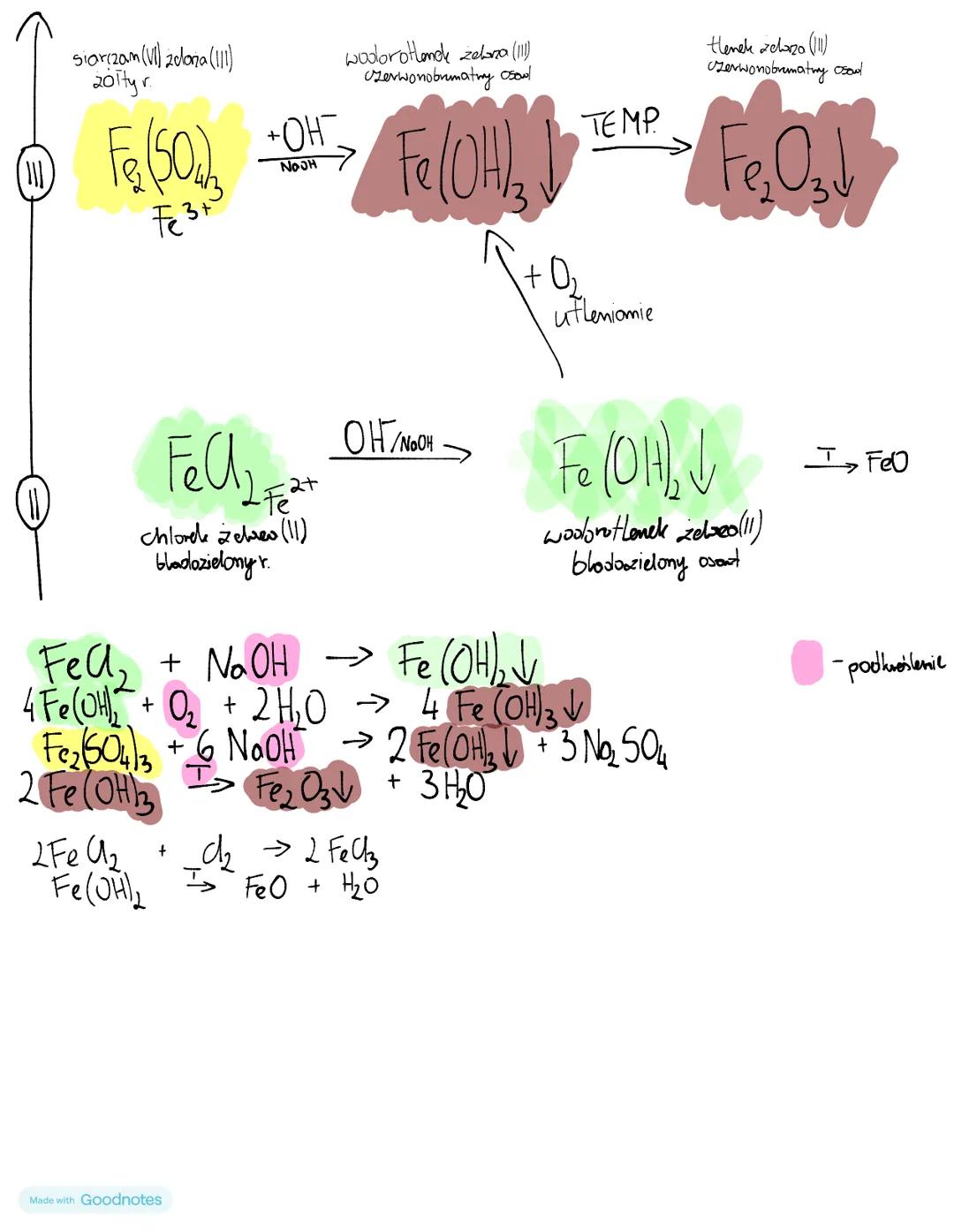
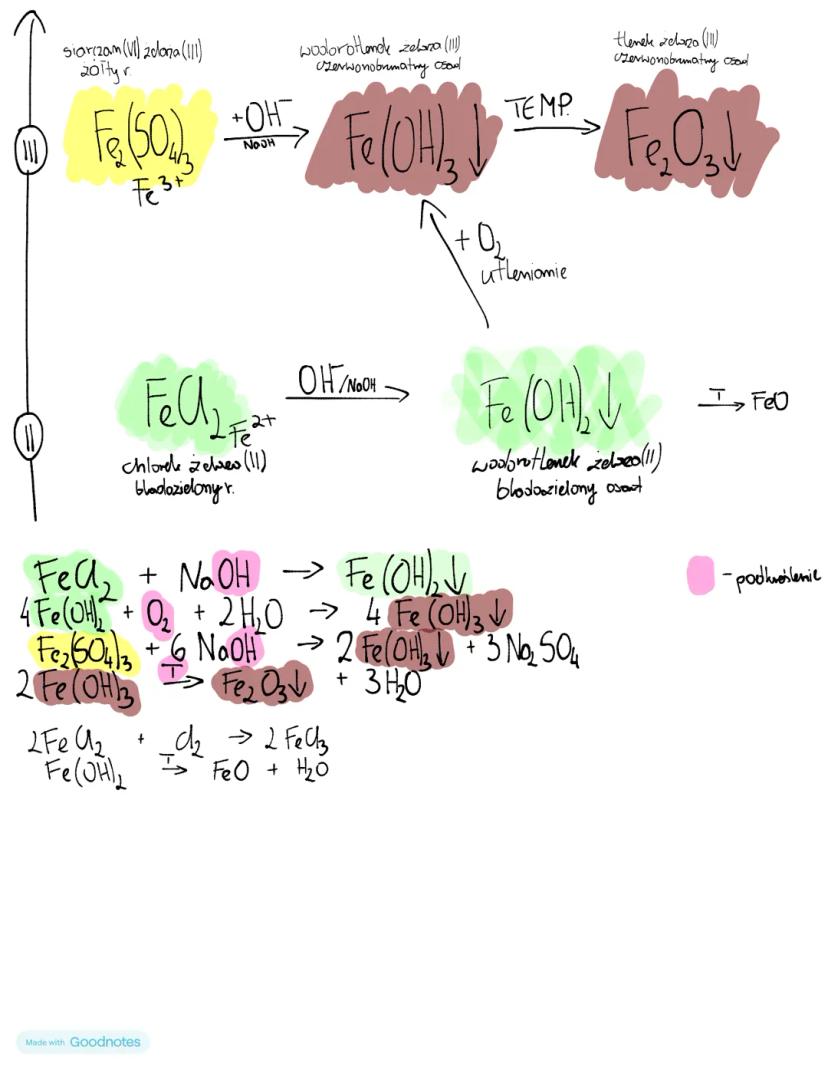
Związki żelaza(II) są zazwyczaj bladozielone, natomiast związki żelaza(III) mają charakterystyczną czerwonobrunatną barwę. Ta różnica kolorów pozwala łatwo rozpoznać stopień utlenienia żelaza w roztworze.
Chlorek żelaza(II) (FeCl₂) reagując z wodorotlenkiem sodu tworzy bladozielony osad wodorotlenku żelaza(II): FeCl₂ + 2NaOH → Fe(OH)₂ + 2NaCl. Wodorotlenek żelaza(II) łatwo utlenia się w powietrzu do wodorotlenku żelaza(III), co możemy zaobserwować jako zmianę barwy osadu z bladozielonej na czerwonobrunatną.
Podobnie siarczan(VI) żelaza(III) reaguje z NaOH tworząc czerwonobrunatny osad wodorotlenku żelaza(III). Po ogrzaniu wodorotlenki żelaza tracą wodę przechodząc w odpowiednie tlenki:
Wskazówka uczniowska! Jeśli na egzaminie pojawi się zadanie z reakcją utleniania-redukcji związków żelaza, zwróć uwagę na zmianę barwy - to podpowiedź, który stopień utlenienia występuje w związku.
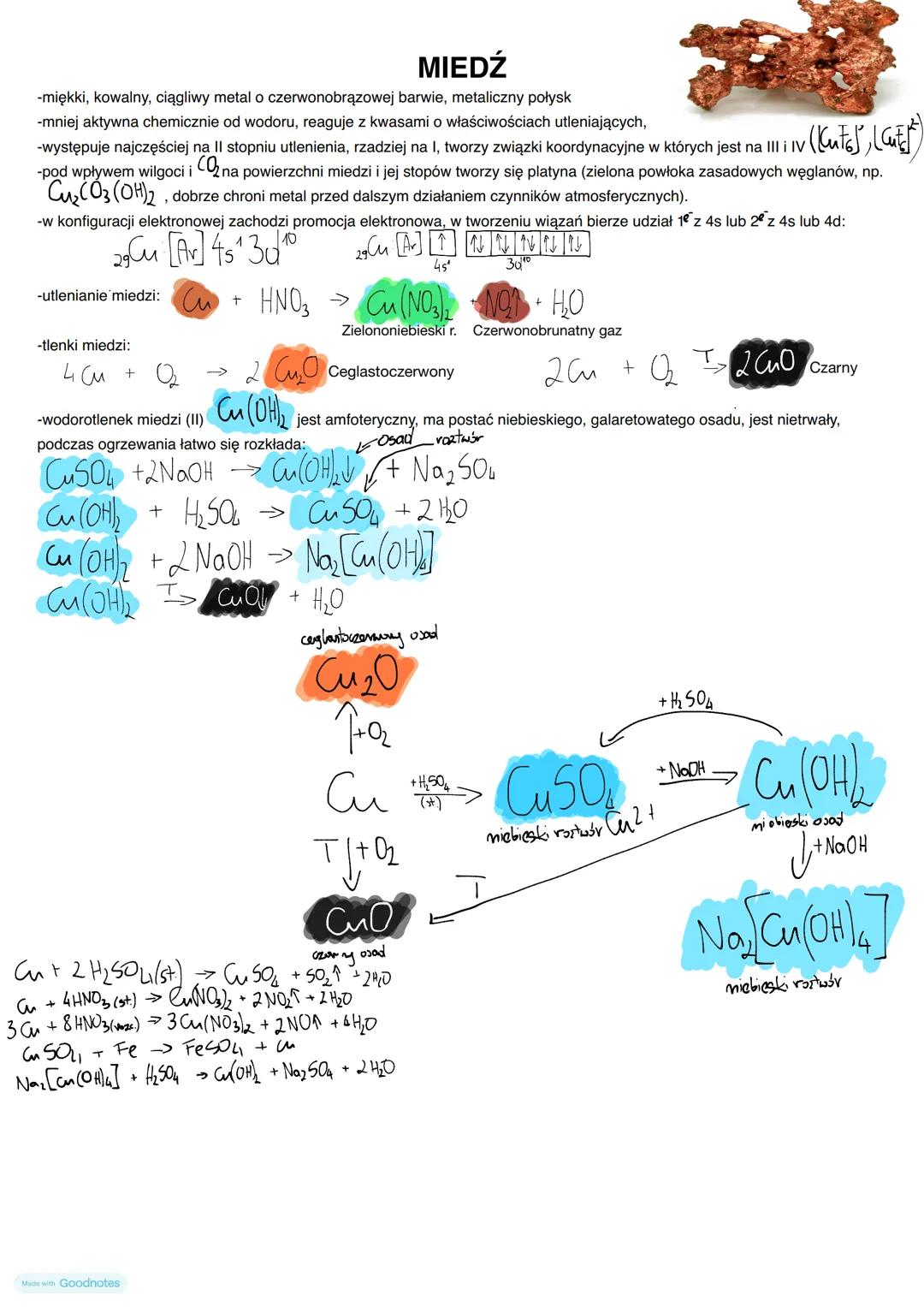
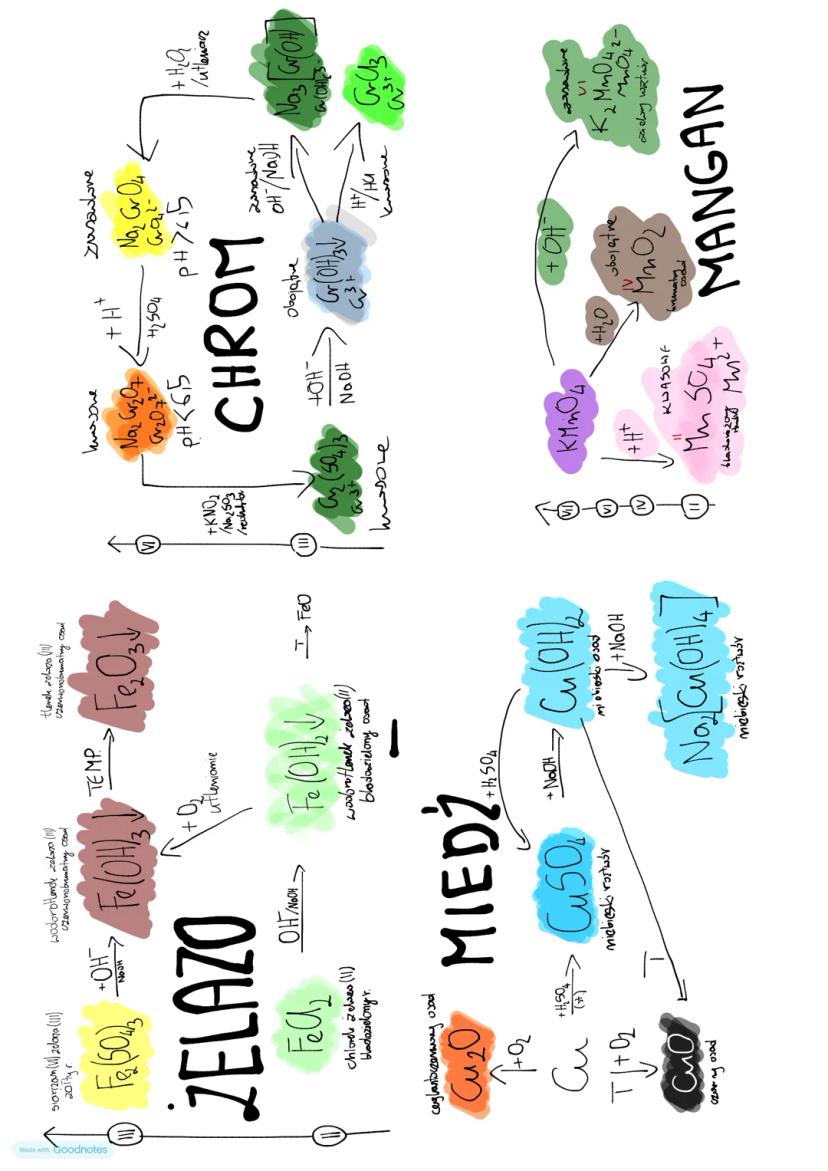
Miedź to miękki, kowalny i ciągliwy metal o charakterystycznej czerwonobrązowej barwie. W przeciwieństwie do wcześniej omawianych metali, jest mniej aktywna chemicznie i nie wypiera wodoru z kwasów nieutleniających. Reaguje natomiast z kwasami o właściwościach utleniających, np. HNO₃.
Miedź występuje najczęściej na II stopniu utlenienia, rzadziej na I. W jej konfiguracji elektronowej ([Ar] 4s¹3d¹⁰) zachodzi promocja elektronowa. Pod wpływem wilgoci i CO₂ na powierzchni miedzi tworzy się patyna - zielona warstwa zasadowych węglanów (np. Cu₂CO₃(OH)₂), która chroni metal przed dalszym działaniem czynników atmosferycznych.
Tlenki miedzi mają różne barwy:
Wodorotlenek miedzi(II) Cu(OH)₂ tworzy niebieski galaretowaty osad i ma charakter amfoteryczny - reaguje zarówno z kwasami (tworząc CuSO₄), jak i z nadmiarem zasad (tworząc kompleks Na₂[Cu(OH)₄]).
Fascynujący fakt! Patyna na miedzi to nie wada, a zaleta! Dzięki niej zabytki wykonane z miedzi i jej stopów (np. Statua Wolności) przetrwały setki lat, mimo narażenia na warunki atmosferyczne.
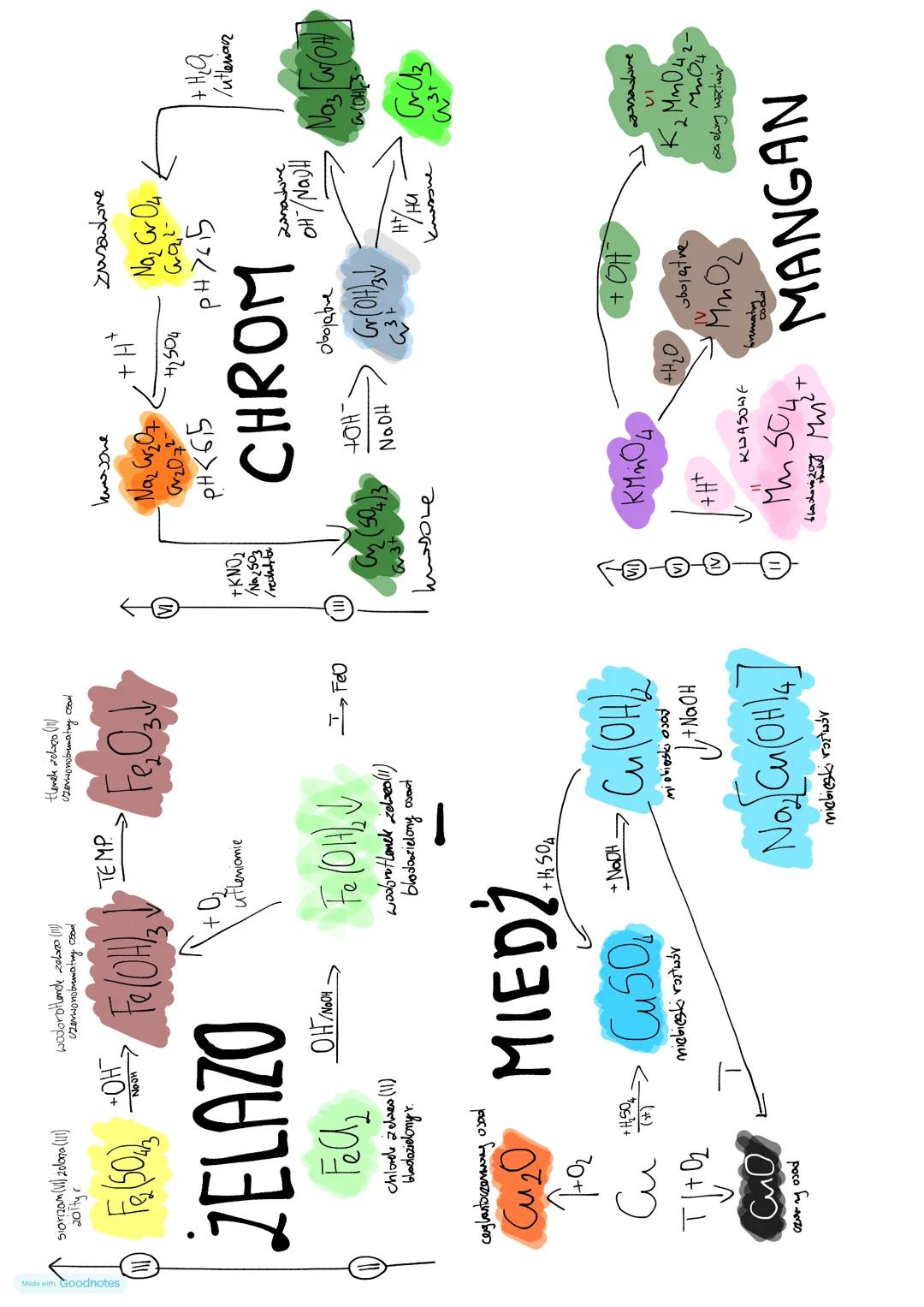
Chrom, mangan, żelazo i miedź to metale przejściowe o podobnych, ale jednocześnie różniących się właściwościach chemicznych. Wszystkie mogą występować na różnych stopniach utlenienia i tworzą związki o barwach charakterystycznych dla danego stopnia utlenienia.
Kluczowe podobieństwa tych metali:
Istotne różnice:
Rada na egzamin! Ucząc się o metalach przejściowych, zwróć uwagę na zależność między stopniem utlenienia, barwą związku i jego charakterem chemicznym. To pomoże ci logicznie przewidzieć przebieg reakcji, nawet jeśli nie pamiętasz wszystkich szczegółów.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Ma dzia
@madzia_hphl
Chrom, mangan, żelazo i miedź to metale przejściowe o niezwykle ważnych właściwościach chemicznych. Każdy z nich wykazuje różne stopnie utlenienia i tworzy związki o zróżnicowanym charakterze chemicznym. Poznanie ich właściwości jest kluczowe do zrozumienia chemii nieorganicznej i procesów redoks.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Chrom to twardy i kruchy metal, który występuje głównie na stopniach utlenienia II, III i VI. Na powietrzu ulega pasywacji - tworzy warstwę ochronną tlenku, która chroni go przed dalszym utlenianiem. Ciekawostką jest, że w konfiguracji elektronowej chromu ([Ar] 4s¹3d⁵) występuje promocja elektronowa z podpowłoki 4s na 3d.
Związki chromu wykazują różny charakter chemiczny zależnie od stopnia utlenienia. Związki Cr(II) mają charakter zasadowy, Cr(III) - amfoteryczny, a Cr(VI) - kwasowy. Wraz ze wzrostem stopnia utlenienia zwiększają się właściwości utleniające i kwasowe związków chromu.
Wodorotlenek chromu(III) Cr(OH)₃ jest doskonałym przykładem związku amfoterycznego:
Warto zapamiętać! W zależności od pH roztworu związki chromu(VI) występują jako jony chromianowe CrO₄²⁻ (żółty roztwór, pH>6,5) lub dichromianowe Cr₂O₇²⁻ (pomarańczowy roztwór, pH<6,5).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Najważniejsze przemiany związków chromu można przedstawić jako cykl reakcji. Dichromian sodu w środowisku kwasowym (pH<6,5) przechodzi w jon Cr₂O₇²⁻, a w środowisku zasadowym (pH>6,5) w jon CrO₄²⁻. Te przemiany są odwracalne.
Przy działaniu reduktorów (np. Na₂SO₃, KNO₂) w środowisku kwasowym związki chromu(VI) redukują się do związków chromu(III). Przykładowa reakcja:
Siarczany chromu(III) w reakcji z NaOH tworzą wodorotlenek chromu(III), który może dalej reagować zarówno z kwasami (tworząc jony Cr³⁺), jak i z nadmiarem zasad (tworząc hydroksokompleksy). Co ciekawe, w warunkach utleniających związki chromu(III) mogą przejść w związki chromu(VI).
Praktyczna wskazówka! Zmiana barwy roztworu często sygnalizuje zmianę stopnia utlenienia chromu - od zielonej (Cr³⁺) przez żółtą (CrO₄²⁻) do pomarańczowej (Cr₂O₇²⁻). To doskonały wskaźnik wizualny przy analizie chemicznej.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Mangan to twardy i kruchy metal o konfiguracji elektronowej [Ar] 4s²3d⁵. Jest bardzo aktywny chemicznie i może występować na wielu stopniach utlenienia: II, III, IV, V, VI i VII. Ta różnorodność daje mu niezwykłe bogactwo związków chemicznych.
Podobnie jak w przypadku chromu, związki manganu zmieniają swój charakter w zależności od stopnia utlenienia:
Mangan tworzy szereg tlenków i wodorotlenków o różnorodnych właściwościach. Szczególnie ważny jest tlenek manganu(IV) (MnO₂), który może być zarówno utleniaczem, jak i reduktorem. Manganianyjowe jony manganu(VII) (MnO₄⁻) są silnymi utleniaczami i nadają roztworom charakterystyczną fioletową barwę.
Ciekawostka! Nadmanganian potasu (KMnO₄) jest tak silnym utleniaczem, że ma właściwości dezynfekujące i jest używany jako środek antyseptyczny. Jeśli dodasz go do roztworu zawierającego substancje redukujące, zaobserwujesz odbarwienie fioletowego roztworu!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Żelazo to jeden z najważniejszych metali przemysłowych, który występuje głównie na II i III stopniu utlenienia. W zależności od temperatury tworzy cztery odmiany alotropowe, co ma ogromne znaczenie w metalurgii i produkcji stali.
Tlenki i wodorotlenki żelaza (FeO, Fe₂O₃, Fe(OH)₂, Fe(OH)₃) wykazują charakter amfoteryczny, co oznacza, że mogą reagować zarówno z kwasami, jak i zasadami. Żelazo jest dość reaktywne - reaguje z kwasami wypierając wodór , a także bezpośrednio z chlorem .
Ważnym zjawiskiem jest pasywacja żelaza - reakcja ze stężonymi kwasami utleniającymi (HNO₃, H₂SO₄), która prowadzi do utworzenia warstwy ochronnej tlenku FeO na powierzchni metalu. Ta warstwa chroni żelazo przed dalszym utlenianiem i działaniem czynników zewnętrznych.
W praktyce! Zjawisko pasywacji wykorzystuje się w ochronie antykorozyjnej konstrukcji stalowych. Chociaż rdza (tlenek żelaza) może zniszczyć stal, to odpowiednio wytworzona warstwa pasywacyjna może skutecznie chronić metal przed zniszczeniem.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Związki żelaza(II) są zazwyczaj bladozielone, natomiast związki żelaza(III) mają charakterystyczną czerwonobrunatną barwę. Ta różnica kolorów pozwala łatwo rozpoznać stopień utlenienia żelaza w roztworze.
Chlorek żelaza(II) (FeCl₂) reagując z wodorotlenkiem sodu tworzy bladozielony osad wodorotlenku żelaza(II): FeCl₂ + 2NaOH → Fe(OH)₂ + 2NaCl. Wodorotlenek żelaza(II) łatwo utlenia się w powietrzu do wodorotlenku żelaza(III), co możemy zaobserwować jako zmianę barwy osadu z bladozielonej na czerwonobrunatną.
Podobnie siarczan(VI) żelaza(III) reaguje z NaOH tworząc czerwonobrunatny osad wodorotlenku żelaza(III). Po ogrzaniu wodorotlenki żelaza tracą wodę przechodząc w odpowiednie tlenki:
Wskazówka uczniowska! Jeśli na egzaminie pojawi się zadanie z reakcją utleniania-redukcji związków żelaza, zwróć uwagę na zmianę barwy - to podpowiedź, który stopień utlenienia występuje w związku.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Miedź to miękki, kowalny i ciągliwy metal o charakterystycznej czerwonobrązowej barwie. W przeciwieństwie do wcześniej omawianych metali, jest mniej aktywna chemicznie i nie wypiera wodoru z kwasów nieutleniających. Reaguje natomiast z kwasami o właściwościach utleniających, np. HNO₃.
Miedź występuje najczęściej na II stopniu utlenienia, rzadziej na I. W jej konfiguracji elektronowej ([Ar] 4s¹3d¹⁰) zachodzi promocja elektronowa. Pod wpływem wilgoci i CO₂ na powierzchni miedzi tworzy się patyna - zielona warstwa zasadowych węglanów (np. Cu₂CO₃(OH)₂), która chroni metal przed dalszym działaniem czynników atmosferycznych.
Tlenki miedzi mają różne barwy:
Wodorotlenek miedzi(II) Cu(OH)₂ tworzy niebieski galaretowaty osad i ma charakter amfoteryczny - reaguje zarówno z kwasami (tworząc CuSO₄), jak i z nadmiarem zasad (tworząc kompleks Na₂[Cu(OH)₄]).
Fascynujący fakt! Patyna na miedzi to nie wada, a zaleta! Dzięki niej zabytki wykonane z miedzi i jej stopów (np. Statua Wolności) przetrwały setki lat, mimo narażenia na warunki atmosferyczne.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Chrom, mangan, żelazo i miedź to metale przejściowe o podobnych, ale jednocześnie różniących się właściwościach chemicznych. Wszystkie mogą występować na różnych stopniach utlenienia i tworzą związki o barwach charakterystycznych dla danego stopnia utlenienia.
Kluczowe podobieństwa tych metali:
Istotne różnice:
Rada na egzamin! Ucząc się o metalach przejściowych, zwróć uwagę na zależność między stopniem utlenienia, barwą związku i jego charakterem chemicznym. To pomoże ci logicznie przewidzieć przebieg reakcji, nawet jeśli nie pamiętasz wszystkich szczegółów.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
27
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS