Chemia węglowodanów to fascynujący dział chemii organicznej, który pomoże Ci... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
1,513
•
Zaktualizowano May 25, 2026
•
Chemia węglowodanów to fascynujący dział chemii organicznej, który pomoże Ci... Pokaż więcej







Węglowodany możemy podzielić na trzy główne grupy: cukry proste (jak glukoza i fruktoza), cukry złożone (np. sacharoza, skrobia) oraz pochodne węglowodanów. To podstawowe składniki naszej diety i struktury organizmów.
Cukry proste dzielą się na heksozy (6 atomów węgla) oraz pentozy (5 atomów węgla). Najpopularniejsze z nich - glukoza i fruktoza - mają ten sam wzór sumaryczny C₆H₁₂O₆, ale różnią się budową. Glukoza należy do grupy aldoz (zawiera grupę aldehydową), a fruktoza to ketoza (zawiera grupę ketonową).
Naturalnie występujące cukry należą do szeregu D, co możemy określić sprawdzając po której stronie ostatniego atomu węgla znajduje się grupa OH. To ciekawa prawidłowość przyrody - z kolei naturalne aminokwasy należą do szeregu L.
Ciekawostka! Wzór Fishera to płaskie przedstawienie cząsteczki cukru, podczas gdy wzór Hawortha pokazuje jego rzeczywistą, przestrzenną strukturę. Warto nauczyć się obu tych sposobów zapisu - przydadzą Ci się na sprawdzianach!

Glukoza i fruktoza są względem siebie metamerami - różnią się rodzajem grupy funkcyjnej, co wpływa na ich właściwości chemiczne. Możesz spotkać glukozę powstającą podczas fotosyntezy lub w wyniku hydrolizy skrobi.
W roztworach wodnych monosacharydy występują w równowadze różnych form. Zjawisko to nazywamy mutarotacją - przechodzeniem pomiędzy anomerami α i β. Możesz łatwo zapamiętać różnicę: anomer β przypomina motylka (OH na górze), a anomer α - rybkę (OH na dole).
Monosacharydy wchodzą w różne reakcje chemiczne. W reakcji redukcji glukoza i fruktoza przekształcają się w sorbitol , substancję stosowaną jako słodzik. Z kolei w reakcjach utleniania glukoza może tworzyć różne kwasy, w zależności od użytego utleniacza.
Wskazówka! Za pomocą wody bromowej w obecności NaHCO₃ możesz łatwo odróżnić aldozy od ketoz - aldozy dają pozytywny wynik próby (odbarwienie roztworu), a ketozy zazwyczaj nie reagują (choć fruktoza daje pozytywny wynik, bo przekształca się w glukozę).

W procesie utleniania glukozy możemy otrzymać różne produkty w zależności od użytego utleniacza. Silne utleniacze jak stężony kwas azotowy(V) powodują powstanie kwasu glikarowego .
Przy zastosowaniu słabszych utleniaczy, jak woda bromowa, powstaje kwas glukonowy . Ta reakcja jest podstawą ważnej metody analitycznej pozwalającej odróżnić aldozy od ketoz.
Próba z wodą bromową w obecności NaHCO₃ daje pozytywny wynik dla aldoz - następuje odbarwienie roztworu i wydzielają się pęcherzyki bezbarwnego gazu (CO₂). Jeśli badana substancja to ketoza - wynik próby będzie negatywny, reakcja nie zachodzi.
Ważne! Fruktoza (ketoza) może dać pozytywny wynik próby, ponieważ w środowisku zasadowym przekształca się w glukozę, która ma właściwości redukujące. To może być podchwytliwe pytanie na sprawdzianie!

Disacharydy to cukry zbudowane z dwóch cząsteczek monosacharydów połączonych wiązaniem glikozydowym. Najpopularniejsze z nich to: sacharoza , laktoza , celobioza i maltoza .
Sacharoza (cukier stołowy) ma wiązanie 1,2-O-glikozydowe i nie posiada właściwości redukujących, co oznacza, że nie reaguje w próbach Trommera i Tollensa. Dopiero po hydrolizie, gdy rozpadnie się na glukozę i fruktozę, próba da wynik pozytywny.
Laktoza (cukier mleczny) ma wiązanie β-1,4-O-glikozydowe i wykazuje właściwości redukujące, podobnie jak celobioza i maltoza. To oznacza, że te disacharydy mogą reagować z odczynnikiem Trommera i Tollensa, dając charakterystyczne produkty.
Zapamiętaj! Wśród popularnych disacharydów tylko sacharoza nie ma właściwości redukujących. Wszystkie inne - laktoza, celobioza i maltoza - są cukrami redukującymi. To ważna cecha rozróżniająca, często sprawdzana na testach!

Wszystkie disacharydy ulegają hydrolizie - w odpowiednich warunkach (kwas, wysoka temperatura lub enzymy) rozpadają się na monosacharydy. Na przykład: sacharoza → α-glukoza + β-fruktoza, maltoza → α-glukoza + β-glukoza.
Disacharydy tworzą szafirowe kompleksy z Cu(OH)₂ w temperaturze pokojowej. Te kompleksy są dobrze rozpuszczalne w wodzie dzięki obecności wielu grup hydroksylowych sąsiadujących ze sobą w cząsteczkach cukrów.
W ciekawym doświadczeniu z Cu(OH)₂ i różnymi cukrami (glukoza, fruktoza, maltoza, sacharoza) wszystkie roztwory zmieniły barwę na szafirową w temperaturze pokojowej. Jednak po ogrzaniu, w probówkach z glukozą, fruktozą i maltozą powstał ceglastoczerwony osad Cu₂O, a w probówce z sacharozą - czarny osad CuO.
Zrozum dlaczego! Ceglastoczerwony osad Cu₂O świadczy o właściwościach redukujących cukru. Czarny osad CuO w przypadku sacharozy oznacza, że ten disacharyd nie ma właściwości redukujących - następuje tylko rozkład Cu(OH)₂ pod wpływem temperatury.
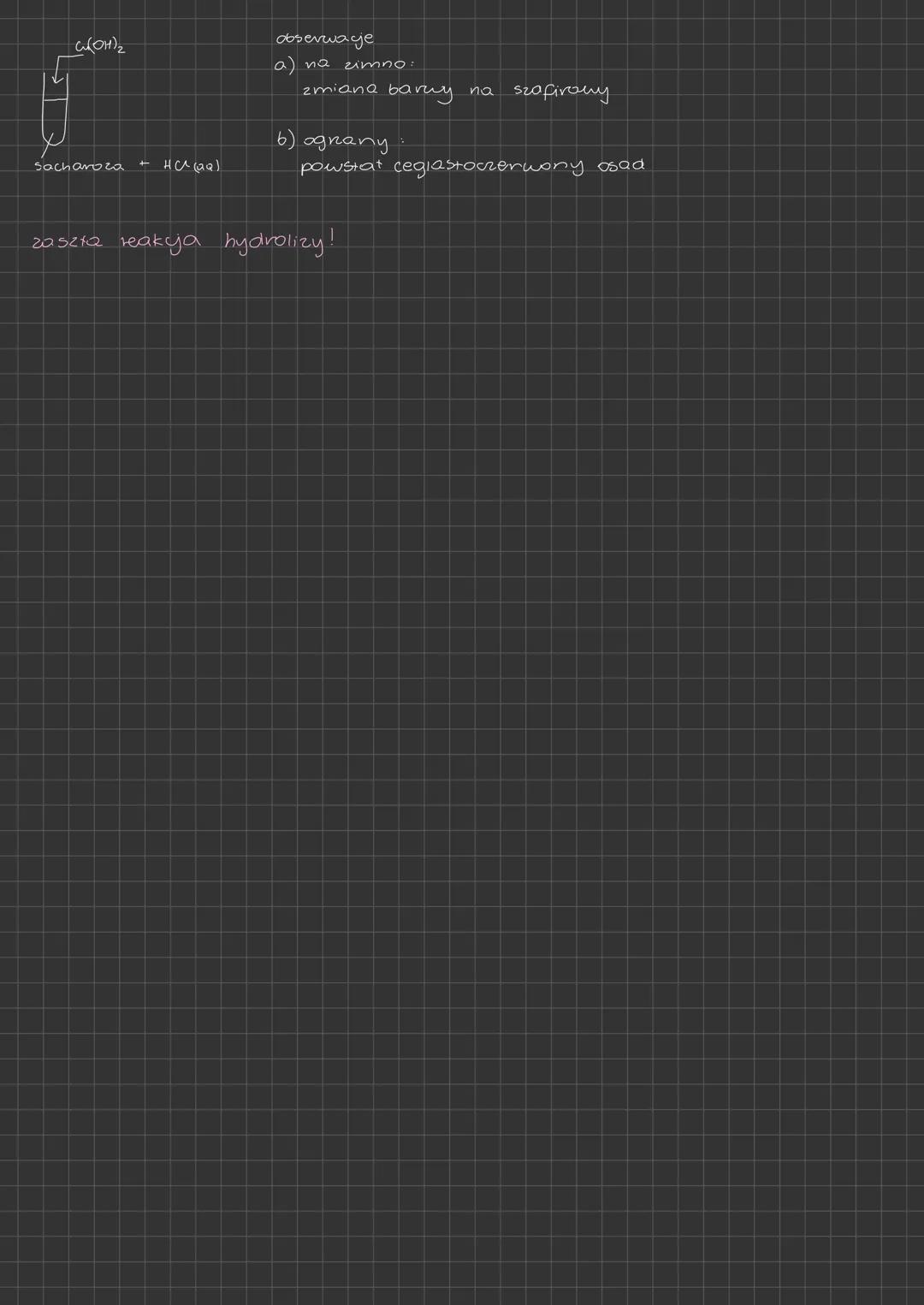
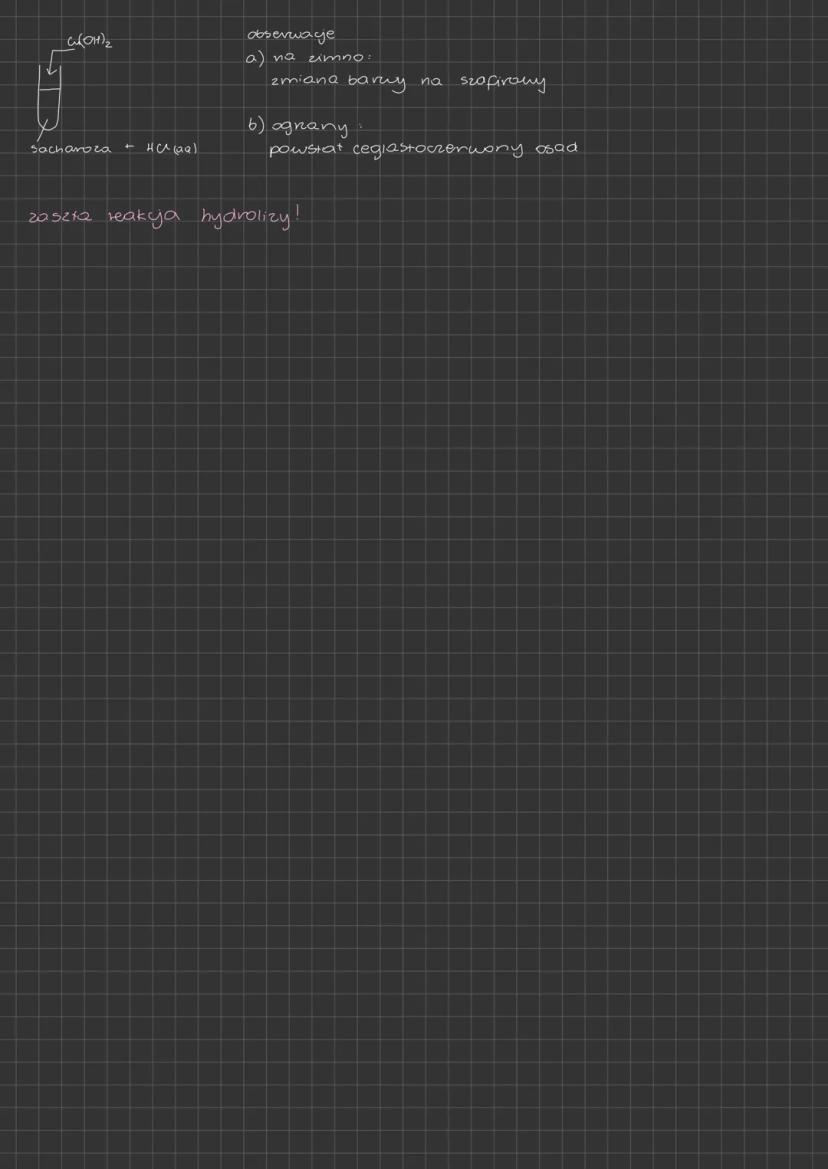
Sacharoza (C₁₂H₂₂O₁₁) zachowuje się inaczej niż pozostałe disacharydy w reakcjach redoks. Jej cząsteczka ma budowę, która uniemożliwia jej bezpośrednie właściwości redukujące.
W temperaturze pokojowej sacharoza z Cu(OH)₂ daje szafirowe zabarwienie roztworu, co jest charakterystyczne dla związków posiadających wiele grup hydroksylowych. Ten efekt obserwujemy dla wszystkich cukrów.
Po ogrzaniu mieszaniny sacharozy z Cu(OH)₂ początkowo powstaje czarny osad CuO. Jednak, jeśli w środowisku jest woda i wysoka temperatura, sacharoza ulega hydrolizie do glukozy i fruktozy, które są cukrami redukującymi. Wtedy możemy zaobserwować ceglastoczerwony osad Cu₂O.
Praktyczna rada! Na egzaminie możesz dostać pytanie o wynik próby z Cu(OH)₂ dla sacharozy po dłuższym ogrzewaniu. Pamiętaj, że początkowo powstaje czarny osad (CuO), ale jeśli reakcja trwa dłużej, może pojawić się ceglastoczerwony osad (Cu₂O) w wyniku hydrolizy sacharozy.

Polisacharydy to długie łańcuchy cukrowe składające się z wielu jednostek monosacharydów. Najważniejsze przykłady to skrobia (magazynuje energię w roślinach), celuloza (buduje ściany komórkowe roślin), chityna (pancerze owadów), glikogen (zapas energii u zwierząt) i inne, jak heparyna czy kwas hialuronowy.
Polisacharydy generalnie nie wykazują właściwości redukujących w próbach Trommera i Tollensa. W przypadku skrobi wynika to z faktu, że jej łańcuchy są bardzo długie, a potencjalna grupa redukująca (na końcu łańcucha) stanowi zbyt mały procent całości, by dać zauważalną reakcję.
Hydrolizie polisacharydów można zapisać ogólnym równaniem: (C₆H₁₀O₅)ₙ + nH₂O → nC₆H₁₂O₆. Po hydrolizie skrobi otrzymujemy glukozę, która jest cukrem redukującym, dlatego daje pozytywny wynik prób Trommera i Tollensa.
Ciekawostka chemiczna! Skrobia daje charakterystyczną granatową barwę z jodem (próba jodowa). To wynik tworzenia kompleksów jodu z helikalną strukturą amylozy. Barwa ta zanika po podgrzaniu, gdyż następuje rozwinięcie helis, ale powraca po ochłodzeniu. Skrobia to mieszanina amylozy (20%, nierozgałęzione łańcuchy) i amylopektyny (80%, rozgałęzione łańcuchy).
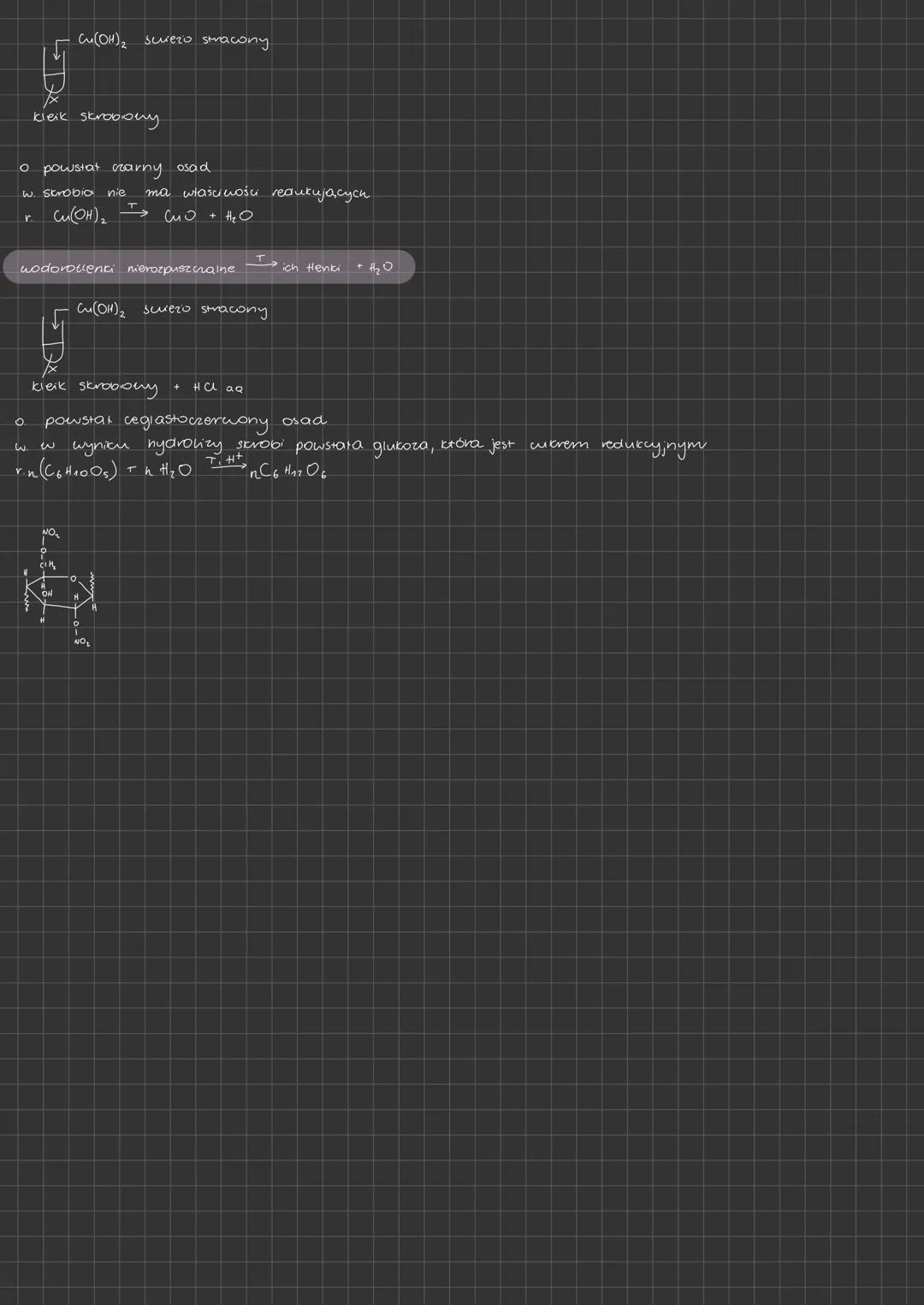
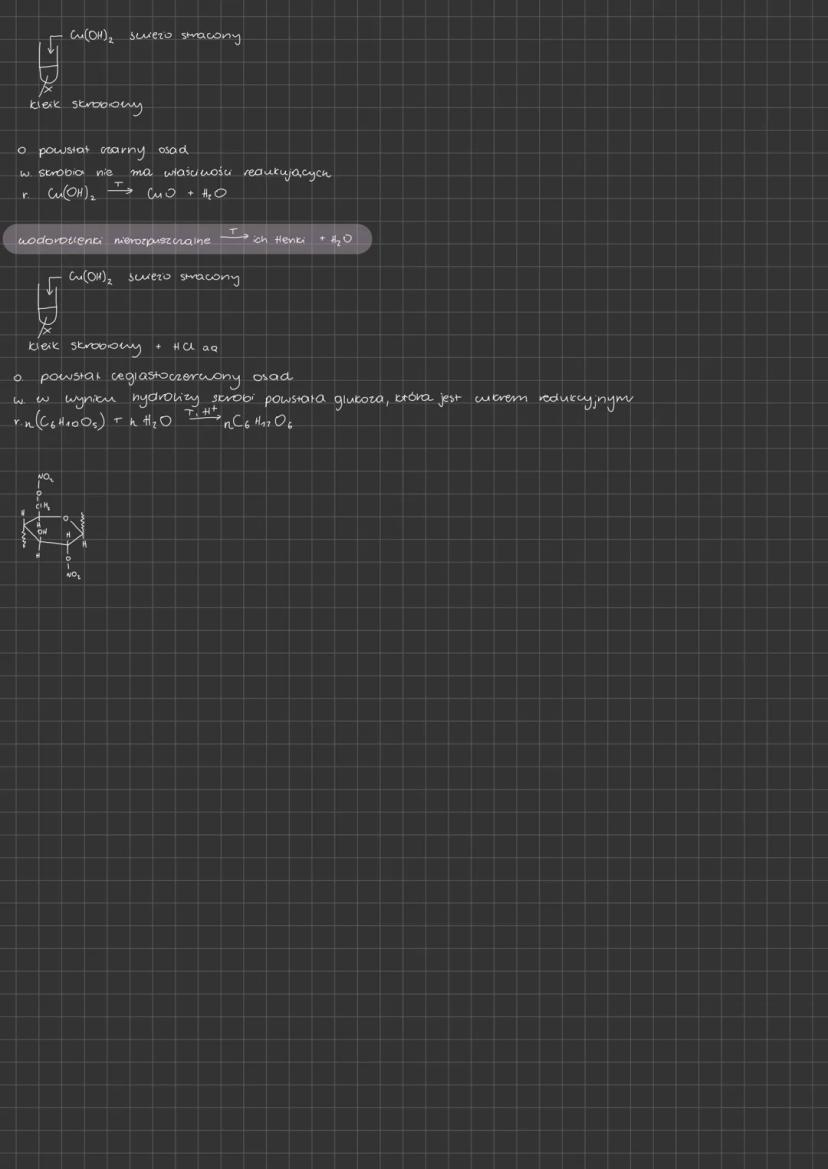
Reakcje identyfikacyjne skrobi pomagają zrozumieć jej właściwości chemiczne i odróżnić ją od innych polisacharydów. Dwa najważniejsze testy to próba z Cu(OH)₂ oraz próba jodowa.
W teście z wodorotlenkiem miedzi(II) i kleikiem skrobiowym, po ogrzaniu powstaje czarny osad CuO. Wynika to z rozkładu Cu(OH)₂ do CuO i wody pod wpływem temperatury. Skrobia nie ma właściwości redukujących, więc nie może zredukować Cu(II) do Cu(I).
Jeśli jednak wcześniej przeprowadzimy hydrolizę skrobi (np. dodając HCl), a następnie wykonamy próbę z Cu(OH)₂ i ogrzejemy, to powstanie ceglastoczerwony osad Cu₂O. To dowód, że w wyniku hydrolizy skrobi powstała glukoza, która jest cukrem redukującym: n(C₆H₁₀O₅) + nH₂O → nC₆H₁₂O₆.
Na egzaminie! Pamiętaj o różnicy między bezpośrednią reakcją skrobi (czarny osad CuO) a reakcją produktów jej hydrolizy (ceglastoczerwony osad Cu₂O). To częsty temat zadań obliczeniowych i problemów na sprawdzianach z chemii organicznej.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Chemia węglowodanów to fascynujący dział chemii organicznej, który pomoże Ci zrozumieć, jak zbudowane są cukry - jedne z najważniejszych związków w przyrodzie. Cukry dostarczają nam energii, budują struktury komórkowe i uczestniczą w wielu procesach życiowych.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Węglowodany możemy podzielić na trzy główne grupy: cukry proste (jak glukoza i fruktoza), cukry złożone (np. sacharoza, skrobia) oraz pochodne węglowodanów. To podstawowe składniki naszej diety i struktury organizmów.
Cukry proste dzielą się na heksozy (6 atomów węgla) oraz pentozy (5 atomów węgla). Najpopularniejsze z nich - glukoza i fruktoza - mają ten sam wzór sumaryczny C₆H₁₂O₆, ale różnią się budową. Glukoza należy do grupy aldoz (zawiera grupę aldehydową), a fruktoza to ketoza (zawiera grupę ketonową).
Naturalnie występujące cukry należą do szeregu D, co możemy określić sprawdzając po której stronie ostatniego atomu węgla znajduje się grupa OH. To ciekawa prawidłowość przyrody - z kolei naturalne aminokwasy należą do szeregu L.
Ciekawostka! Wzór Fishera to płaskie przedstawienie cząsteczki cukru, podczas gdy wzór Hawortha pokazuje jego rzeczywistą, przestrzenną strukturę. Warto nauczyć się obu tych sposobów zapisu - przydadzą Ci się na sprawdzianach!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Glukoza i fruktoza są względem siebie metamerami - różnią się rodzajem grupy funkcyjnej, co wpływa na ich właściwości chemiczne. Możesz spotkać glukozę powstającą podczas fotosyntezy lub w wyniku hydrolizy skrobi.
W roztworach wodnych monosacharydy występują w równowadze różnych form. Zjawisko to nazywamy mutarotacją - przechodzeniem pomiędzy anomerami α i β. Możesz łatwo zapamiętać różnicę: anomer β przypomina motylka (OH na górze), a anomer α - rybkę (OH na dole).
Monosacharydy wchodzą w różne reakcje chemiczne. W reakcji redukcji glukoza i fruktoza przekształcają się w sorbitol , substancję stosowaną jako słodzik. Z kolei w reakcjach utleniania glukoza może tworzyć różne kwasy, w zależności od użytego utleniacza.
Wskazówka! Za pomocą wody bromowej w obecności NaHCO₃ możesz łatwo odróżnić aldozy od ketoz - aldozy dają pozytywny wynik próby (odbarwienie roztworu), a ketozy zazwyczaj nie reagują (choć fruktoza daje pozytywny wynik, bo przekształca się w glukozę).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
W procesie utleniania glukozy możemy otrzymać różne produkty w zależności od użytego utleniacza. Silne utleniacze jak stężony kwas azotowy(V) powodują powstanie kwasu glikarowego .
Przy zastosowaniu słabszych utleniaczy, jak woda bromowa, powstaje kwas glukonowy . Ta reakcja jest podstawą ważnej metody analitycznej pozwalającej odróżnić aldozy od ketoz.
Próba z wodą bromową w obecności NaHCO₃ daje pozytywny wynik dla aldoz - następuje odbarwienie roztworu i wydzielają się pęcherzyki bezbarwnego gazu (CO₂). Jeśli badana substancja to ketoza - wynik próby będzie negatywny, reakcja nie zachodzi.
Ważne! Fruktoza (ketoza) może dać pozytywny wynik próby, ponieważ w środowisku zasadowym przekształca się w glukozę, która ma właściwości redukujące. To może być podchwytliwe pytanie na sprawdzianie!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Disacharydy to cukry zbudowane z dwóch cząsteczek monosacharydów połączonych wiązaniem glikozydowym. Najpopularniejsze z nich to: sacharoza , laktoza , celobioza i maltoza .
Sacharoza (cukier stołowy) ma wiązanie 1,2-O-glikozydowe i nie posiada właściwości redukujących, co oznacza, że nie reaguje w próbach Trommera i Tollensa. Dopiero po hydrolizie, gdy rozpadnie się na glukozę i fruktozę, próba da wynik pozytywny.
Laktoza (cukier mleczny) ma wiązanie β-1,4-O-glikozydowe i wykazuje właściwości redukujące, podobnie jak celobioza i maltoza. To oznacza, że te disacharydy mogą reagować z odczynnikiem Trommera i Tollensa, dając charakterystyczne produkty.
Zapamiętaj! Wśród popularnych disacharydów tylko sacharoza nie ma właściwości redukujących. Wszystkie inne - laktoza, celobioza i maltoza - są cukrami redukującymi. To ważna cecha rozróżniająca, często sprawdzana na testach!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Wszystkie disacharydy ulegają hydrolizie - w odpowiednich warunkach (kwas, wysoka temperatura lub enzymy) rozpadają się na monosacharydy. Na przykład: sacharoza → α-glukoza + β-fruktoza, maltoza → α-glukoza + β-glukoza.
Disacharydy tworzą szafirowe kompleksy z Cu(OH)₂ w temperaturze pokojowej. Te kompleksy są dobrze rozpuszczalne w wodzie dzięki obecności wielu grup hydroksylowych sąsiadujących ze sobą w cząsteczkach cukrów.
W ciekawym doświadczeniu z Cu(OH)₂ i różnymi cukrami (glukoza, fruktoza, maltoza, sacharoza) wszystkie roztwory zmieniły barwę na szafirową w temperaturze pokojowej. Jednak po ogrzaniu, w probówkach z glukozą, fruktozą i maltozą powstał ceglastoczerwony osad Cu₂O, a w probówce z sacharozą - czarny osad CuO.
Zrozum dlaczego! Ceglastoczerwony osad Cu₂O świadczy o właściwościach redukujących cukru. Czarny osad CuO w przypadku sacharozy oznacza, że ten disacharyd nie ma właściwości redukujących - następuje tylko rozkład Cu(OH)₂ pod wpływem temperatury.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Sacharoza (C₁₂H₂₂O₁₁) zachowuje się inaczej niż pozostałe disacharydy w reakcjach redoks. Jej cząsteczka ma budowę, która uniemożliwia jej bezpośrednie właściwości redukujące.
W temperaturze pokojowej sacharoza z Cu(OH)₂ daje szafirowe zabarwienie roztworu, co jest charakterystyczne dla związków posiadających wiele grup hydroksylowych. Ten efekt obserwujemy dla wszystkich cukrów.
Po ogrzaniu mieszaniny sacharozy z Cu(OH)₂ początkowo powstaje czarny osad CuO. Jednak, jeśli w środowisku jest woda i wysoka temperatura, sacharoza ulega hydrolizie do glukozy i fruktozy, które są cukrami redukującymi. Wtedy możemy zaobserwować ceglastoczerwony osad Cu₂O.
Praktyczna rada! Na egzaminie możesz dostać pytanie o wynik próby z Cu(OH)₂ dla sacharozy po dłuższym ogrzewaniu. Pamiętaj, że początkowo powstaje czarny osad (CuO), ale jeśli reakcja trwa dłużej, może pojawić się ceglastoczerwony osad (Cu₂O) w wyniku hydrolizy sacharozy.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Polisacharydy to długie łańcuchy cukrowe składające się z wielu jednostek monosacharydów. Najważniejsze przykłady to skrobia (magazynuje energię w roślinach), celuloza (buduje ściany komórkowe roślin), chityna (pancerze owadów), glikogen (zapas energii u zwierząt) i inne, jak heparyna czy kwas hialuronowy.
Polisacharydy generalnie nie wykazują właściwości redukujących w próbach Trommera i Tollensa. W przypadku skrobi wynika to z faktu, że jej łańcuchy są bardzo długie, a potencjalna grupa redukująca (na końcu łańcucha) stanowi zbyt mały procent całości, by dać zauważalną reakcję.
Hydrolizie polisacharydów można zapisać ogólnym równaniem: (C₆H₁₀O₅)ₙ + nH₂O → nC₆H₁₂O₆. Po hydrolizie skrobi otrzymujemy glukozę, która jest cukrem redukującym, dlatego daje pozytywny wynik prób Trommera i Tollensa.
Ciekawostka chemiczna! Skrobia daje charakterystyczną granatową barwę z jodem (próba jodowa). To wynik tworzenia kompleksów jodu z helikalną strukturą amylozy. Barwa ta zanika po podgrzaniu, gdyż następuje rozwinięcie helis, ale powraca po ochłodzeniu. Skrobia to mieszanina amylozy (20%, nierozgałęzione łańcuchy) i amylopektyny (80%, rozgałęzione łańcuchy).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Reakcje identyfikacyjne skrobi pomagają zrozumieć jej właściwości chemiczne i odróżnić ją od innych polisacharydów. Dwa najważniejsze testy to próba z Cu(OH)₂ oraz próba jodowa.
W teście z wodorotlenkiem miedzi(II) i kleikiem skrobiowym, po ogrzaniu powstaje czarny osad CuO. Wynika to z rozkładu Cu(OH)₂ do CuO i wody pod wpływem temperatury. Skrobia nie ma właściwości redukujących, więc nie może zredukować Cu(II) do Cu(I).
Jeśli jednak wcześniej przeprowadzimy hydrolizę skrobi (np. dodając HCl), a następnie wykonamy próbę z Cu(OH)₂ i ogrzejemy, to powstanie ceglastoczerwony osad Cu₂O. To dowód, że w wyniku hydrolizy skrobi powstała glukoza, która jest cukrem redukującym: n(C₆H₁₀O₅) + nH₂O → nC₆H₁₂O₆.
Na egzaminie! Pamiętaj o różnicy między bezpośrednią reakcją skrobi (czarny osad CuO) a reakcją produktów jej hydrolizy (ceglastoczerwony osad Cu₂O). To częsty temat zadań obliczeniowych i problemów na sprawdzianach z chemii organicznej.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
30
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS