Fluorowcopochodne węglowodorów to związki organiczne, w których atomy wodoru zostały... Pokaż więcej
Wprowadzenie do Fluorowcopochodnych Węglowodorów








Budowa i charakterystyka fluorowcopochodnych
Fluorowcopochodne węglowodorów składają się z dwóch kluczowych elementów: grupy węglowodorowej (R) oraz grupy funkcyjnej w postaci atomu fluorowca (X). Te związki nazywane są też halogenkami i mają ogólny wzór R-X.
Atomy fluorowców są jednowartościowe, co oznacza, że mogą tworzyć tylko jedno wiązanie kowalencyjne. Mogą one zastępować atomy wodoru w różnych pozycjach cząsteczki węglowodoru, tworząc związki o odmiennych właściwościach.
⚡ Warto zapamiętać! Im więcej atomów fluorowca w cząsteczce, tym bardziej zmieniają się właściwości związku w porównaniu do wyjściowego węglowodoru.
Przykłady takich związków to: chlorometan (CH₃Cl), gdzie jeden atom wodoru metanu został zastąpiony chlorem, czy tetrachlorometan (CCl₄), gdzie wszystkie cztery atomy wodoru zostały zastąpione chlorem.

Nazewnictwo fluorowcopochodnych
Fluorowcopochodne węglowodorów dzielą się na dwie główne grupy: halogenki alkilowe (pochodne węglowodorów alifatycznych) i halogenki arylowe (pochodne węglowodorów aromatycznych).
W przypadku halogenków alkilowych atom fluorowca zastępuje atom wodoru w prostym łańcuchu węglowym. Przykłady to: chloroeten , 1-bromopropan czy dichlorodifluorometan (CF₂Cl₂).
Halogenki arylowe to związki zawierające pierścień benzenowy, w którym atom wodoru został zastąpiony atomem fluorowca. Można je nazywać na dwa sposoby, np. bromometylobenzen lub bromofenylometan.
🔑 Kluczowa różnica: Fluorowcopochodne alifatyczne mają proste lub rozgałęzione łańcuchy węglowe, podczas gdy aromatyczne zawierają pierścień benzenowy lub inny układ aromatyczny.

Właściwości fluorowcopochodnych
Właściwości fluorowcopochodnych zależą od ich masy cząsteczkowej - im większa masa, tym wyższa temperatura wrzenia. Najczęściej są to niepalne ciecze, nierozpuszczalne w wodzie, choć istnieją wyjątki - niektóre lżejsze związki występują jako gazy (np. CH₃F, CH₃Cl, CH₃Br).
Fluorowcopochodne łatwo rozpuszczają się w niepolarnych rozpuszczalnikach. Wykazują wysoką reaktywność chemiczną ze względu na spolaryzowane wiązanie C-X , co prowadzi do tego, że związki te są polarne i mają niezerowy moment dipolowy.
⚠️ Uwaga! Wiązanie C-X jest spolaryzowane, z ładunkiem δ+ na atomie węgla i δ- na atomie fluorowca, co sprawia, że atom węgla może być atakowany przez czynniki nukleofilowe.
Przykłady fluorowcopochodnych aromatycznych to 4-chlorotoluen i 1,6-dichloronaftalen, które zachowują specyficzne właściwości związków aromatycznych, jednocześnie zyskując nowe właściwości dzięki obecności atomów fluorowców.

Metody otrzymywania fluorowcopochodnych (I)
Fluorowcopochodne można otrzymywać na kilka sposobów. Jednym z nich jest reakcja substytucji, w której atom wodoru zostaje zastąpiony atomem fluorowca:
- W węglowodorach nasyconych: CH₄ + Cl₂ → CH₃Cl + HCl
- W węglowodorach aromatycznych: benzen + Br₂ → bromobenzen + HBr (w obecności katalizatora FeBr₃)
Inną metodą jest substytucja grupy hydroksylowej w cząsteczce alkoholu atomem fluorowca: CH₃CH₂OH + HCl → CH₃CH₂Cl + H₂O
🧪 Ciekawostka praktyczna: Reakcje addycji fluorowca lub fluorowcowodoru do alkenów i alkinów są powszechnie wykorzystywane w przemyśle do produkcji różnych związków organicznych.
Fluorowcopochodne można także uzyskać poprzez addycję fluorowca lub fluorowcowodoru do węglowodorów nienasyconych:
- Z alkenów: CH₂=CH₂ + Cl₂ → CH₂Cl-CH₂Cl
- Z alkinów: CH≡CH + HBr → CH₂=CHBr

Metody otrzymywania fluorowcopochodnych (II)
Substytucja rodnikowa to kolejna ważna metoda, w której bezpośrednio wprowadza się atomy chloru lub bromu do cząsteczki alkanu. Proces zachodzi w temperaturze 25-35°C przy obecności światła:
CH₃-CH₂-CH₃ + Cl₂ → CH₃-CH₂-CH₂Cl (45%) + CH₃-CHCl-CH₃ (55%)
Substytucja nukleofilowa zachodzi, gdy mocna zasada reaguje z fluorowcopochodną w środowisku alkoholowym: CH₃-CH₂-Cl + KOH → CH₃-CH₂-OH + KCl
💡 Wskazówka! Pamiętaj, że w reakcji fluorowcopochodnych z amoniakiem powstają aminy - związki organiczne zawierające grupę aminową .
Interesującym przykładem jest reakcja fluorowcopochodnych z amoniakiem, prowadząca do otrzymania amin: CH₃-CH₂-CH₂Cl + NH₃ → CH₃-CH₂-CH₂NH₂ + HCl

Reakcja Wurtza i eliminacji
Reakcja Wurtza to metoda łączenia dwóch cząsteczek fluorowcopochodnych przy użyciu sodu, prowadząca do otrzymania dłuższych łańcuchów węglowych:
2CH₃Cl + 2Na → CH₃-CH₃ + 2NaCl (etan) 2CH₃CH₂Cl + 2Na → CH₃-CH₂-CH₂-CH₃ + 2NaCl (butan)
Jeśli w reakcji uczestniczą różne fluorowcopochodne, otrzymujemy mieszaninę alkanów o różnej długości łańcucha.
Reakcja eliminacji polega na oderwaniu prostszej cząsteczki od substratu, co prowadzi do powstania wiązania wielokrotnego. Jest to ważna metoda otrzymywania alkenów:
CH₃-CH₂Cl + KOH → CH₂=CH₂ + KCl + H₂O
📝 Na sprawdzian: W przypadku halogenków alkenów o dłuższym łańcuchu węglowym mogą powstawać mieszaniny różnych alkenów, zależnie od miejsca eliminacji.
W przypadku fluorowcopochodnych o dłuższych łańcuchach, eliminacja może prowadzić do powstania różnych izomerów, np.: CH₃-CH₂-CHBr-CH₃ + KOH → CH₃-CH=CH-CH₃ + CH₃-CH₂-CH=CH₂

Związki magnezoorganiczne
Związki magnezoorganiczne (odczynniki Grignarda) o wzorze RMgX otrzymuje się w reakcji halogenków alkilowych z metalicznym magnezem:
CH₃-CH₂Cl + Mg → CH₃-CH₂MgCl (chlorek etylomagnezowy)
Reakcję tę prowadzi się w bezwodnym rozpuszczalniku, ponieważ woda rozkłada produkty! Odczynniki Grignarda są niezwykle użyteczne w syntezie organicznej.
Rozkład związków magnezoorganicznych w wodzie prowadzi do powstania węglowodorów:
CH₃-CH₂MgCl + H₂O → CH₃-CH₃ + MgCl(OH)
⚠️ Uwaga praktyczna: Związki magnezoorganiczne są wrażliwe na wodę i powietrze - podczas pracy z nimi zawsze trzeba stosować atmosferę gazu obojętnego (np. argonu).
Związki magnezoorganiczne znajdują szerokie zastosowanie w syntezie organicznej jako silne nukleofile i zasady, umożliwiając tworzenie nowych wiązań węgiel-węgiel.
Fluorowcopochodne węglowodorów aromatycznych
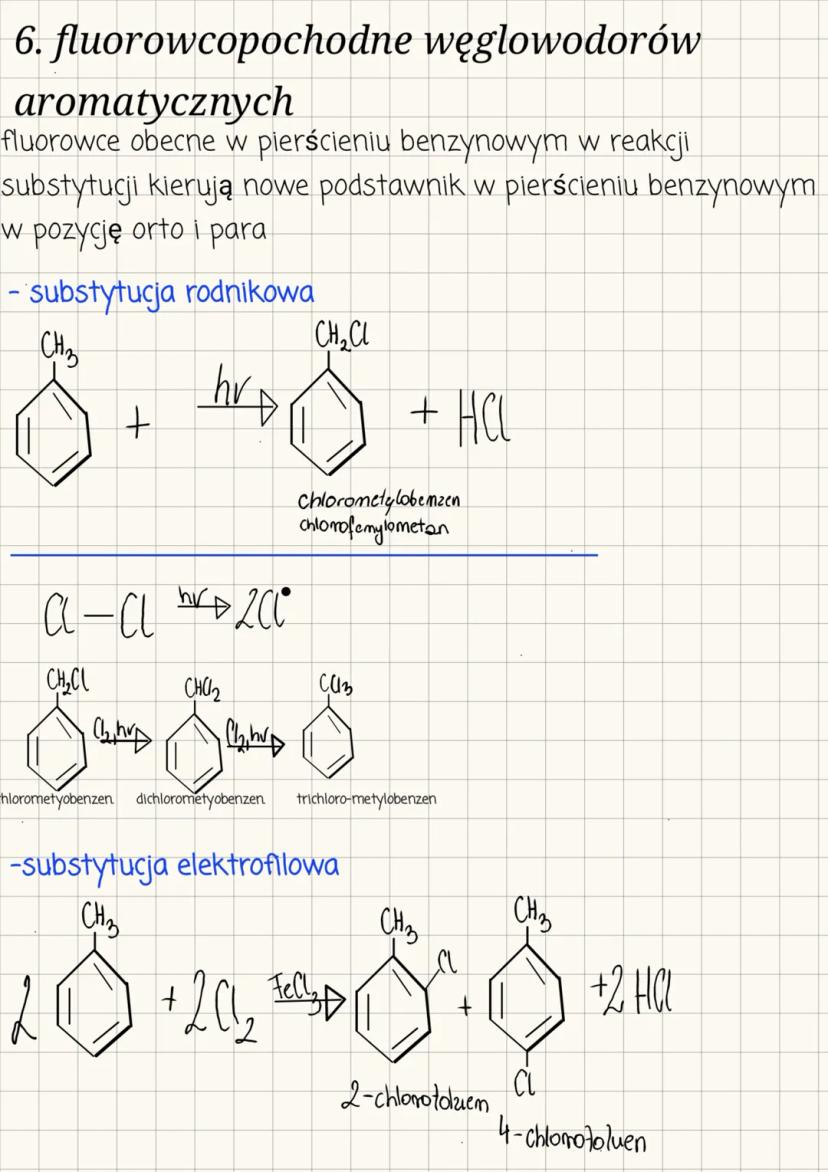
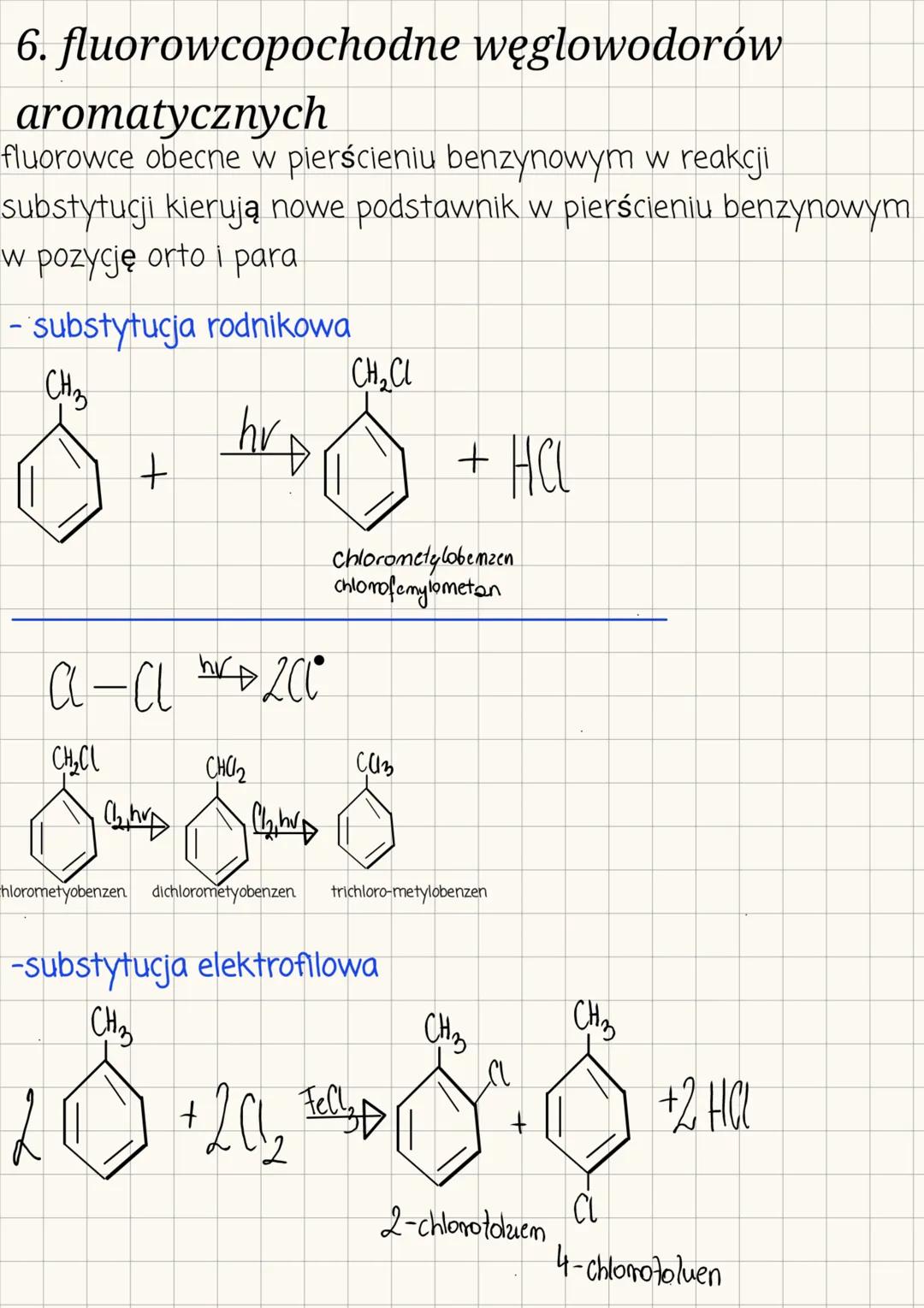
Fluorowce obecne w pierścieniu benzenowym kierują nowe podstawniki w pozycje orto i para. Istnieją dwie główne metody wprowadzania podstawników halogenowych:
-
Substytucja rodnikowa - umożliwia podstawienie atomów wodoru w grupie metylowej, np.: Toluen + Cl₂ → Chlorometylbenzen + HCl
Proces ten może być kontynuowany, prowadząc do dichlorometylobenzenu i trichlorometylobenzenu.
-
Substytucja elektrofilowa - wprowadza atom fluorowca bezpośrednio do pierścienia aromatycznego: Toluen + Cl₂ → 2-chlorotoluen + 4-chlorotoluen + HCl (z katalizatorem FeCl₃)
🧠 Zapamiętaj: Kierunek podstawienia w pierścieniu aromatycznym zależy od charakteru obecnego już podstawnika - grupy aktywujące kierują w pozycje orto i para, a dezaktywujące w pozycję meta.
Fluorowcopochodne aromatyczne wykazują inną reaktywność niż alifatyczne, co wynika z obecności układu aromatycznego, który zmienia właściwości elektronowe całej cząsteczki.
Reakcje fluorowcopochodnych aromatycznych
Fluorowcopochodne aromatyczne mogą ulegać różnym reakcjom, w tym reakcji z zasadami i kwasami:
-
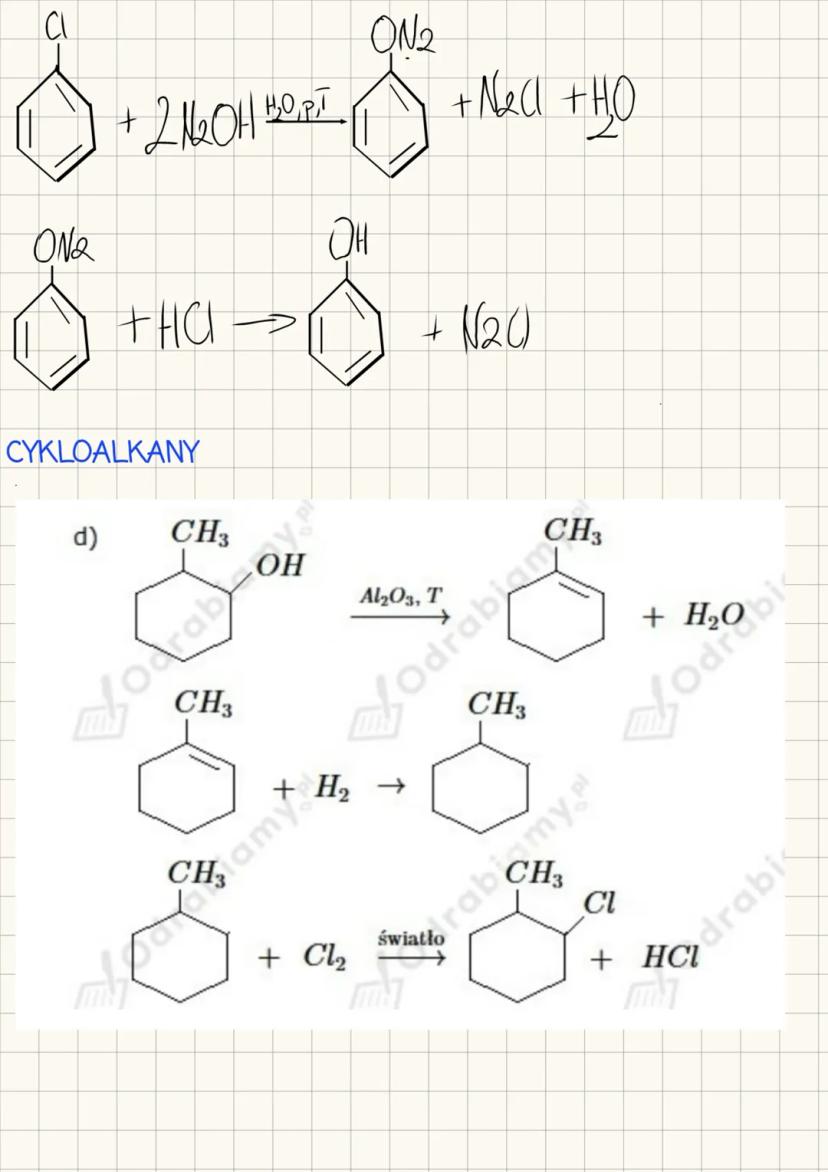
Reakcja z NaOH: Chlorobenzen + 2NaOH → Fenol + NaCl + H₂O (w podwyższonej temperaturze i ciśnieniu)
-
Reakcja z HCl: Diazopochodna + HCl → Pochodna chlorowa + N₂
Związki cykloalkanowe z podstawnikami halogenowymi również wykazują interesujące właściwości i reaktywność:
- Dehydratacja alkoholi cyklicznych: Cykliczny alkohol + Al₂O₃ → Cykloalken + H₂O (w podwyższonej temperaturze)
🔬 Warto wiedzieć: Podstawienie atomu fluorowca w pierścieniu aromatycznym znacząco zmienia jego reaktywność, co ma duże znaczenie w syntezie leków i innych związków biologicznie czynnych.
Halogenowanie cykloalkanów przebiega podobnie jak w przypadku alkanów prostołańcuchowych: Cykloalkan + Cl₂ → Chlorocykloalkan + HCl (w obecności światła)
Polimeryzacja fluorowcopochodnych
Polimeryzacja fluorowcopochodnych ma ogromne znaczenie przemysłowe. Dwa najważniejsze przykłady to:
-
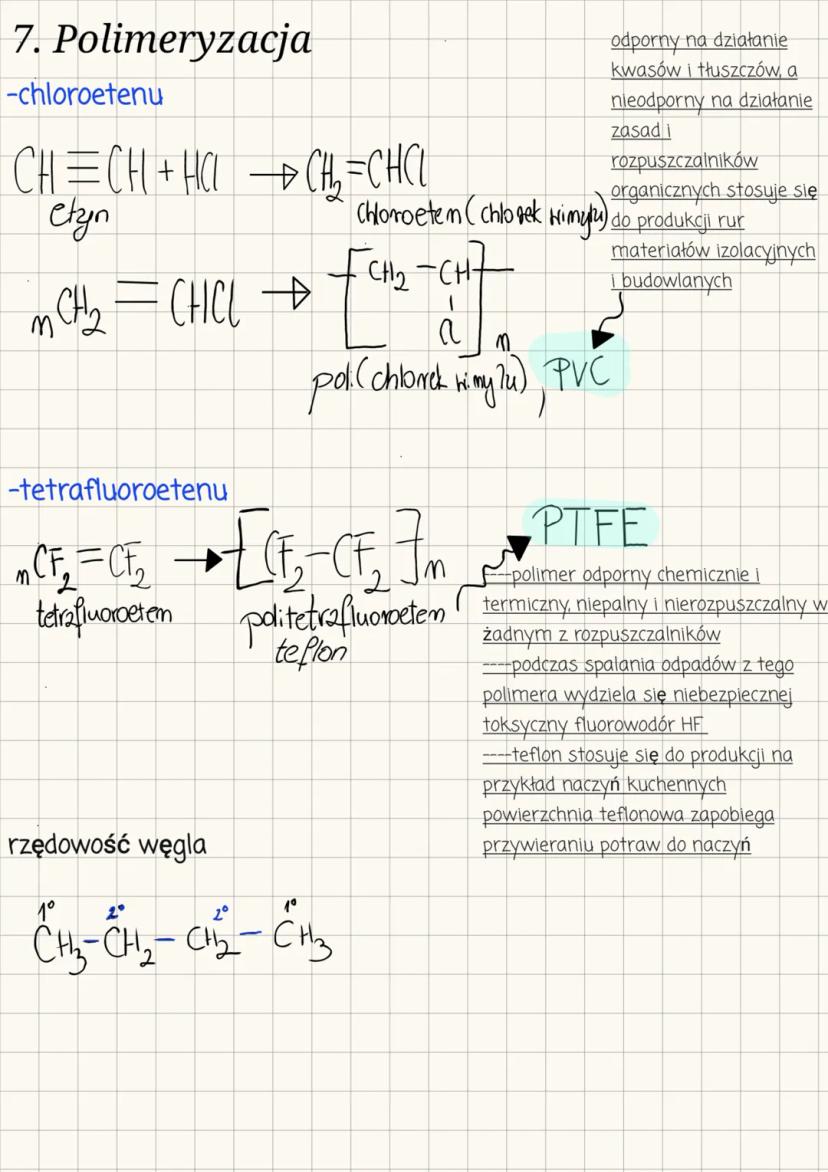
Polimeryzacja chloroetenu (chlorku winylu): nCH₂=CHCl → ₙ Powstały poli(chlorek winylu) (PVC) jest odporny na działanie kwasów i tłuszczów, ale nieodporny na zasady i rozpuszczalniki organiczne. Stosuje się go do produkcji rur, materiałów izolacyjnych i budowlanych.
-
Polimeryzacja tetrafluoroetenu: nCF₂=CF₂ → ₙ Powstały politetrafluoroetylen (PTFE, teflon) jest wyjątkowo odporny chemicznie i termicznie, niepalny i nierozpuszczalny w rozpuszczalnikach.
⚠️ Ostrzeżenie! Podczas spalania teflonu wydziela się niebezpieczny, toksyczny fluorowodór (HF), dlatego odpady tego polimeru muszą być odpowiednio utylizowane.
Teflon jest powszechnie stosowany do produkcji naczyń kuchennych, gdyż jego powierzchnia zapobiega przywieraniu potraw. Jest to jeden z najbardziej wszechstronnych polimerów wykorzystywanych w życiu codziennym dzięki swoim unikalnym właściwościom.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: chemia organiczna
9Węglowodory nienasycone - alkeny
Notatka chemia rozszerzona- alkeny, chemia organiczna
Chemia organiczna w pigułce
Chemia organiczna, notatki do matury, BEZ alkanów/ alkenów/ alkinów
Zatrucie i Właściwości Benzenu
Odkryj kluczowe informacje na temat benzenu, jego właściwości fizycznych i chemicznych, objawów zatrucia oraz reakcji chemicznych. Materiał obejmuje mechanizmy reakcji, takie jak bromowanie, nitrowanie i alkilowanie, a także skutki zdrowotne związane z narażeniem na benzen. Idealne dla studentów chemii i biologii.
Charakterystyczne Reakcje Chemii Organicznej
Odkryj kluczowe reakcje charakterystyczne w chemii organicznej, w tym reakcje biuretowe, ksantoproteinowe oraz próby Trommera i Tollensa. Zrozum, jak różne grupy funkcyjne, takie jak aminokwasy, cukry i fenole, reagują w różnych warunkach. Idealne dla studentów chemii poszukujących praktycznych informacji o reakcjach organicznych.
Chemia Benzenowa
Zgłębiaj chemię benzenową i jej reakcje. Dowiedz się o mechanizmach substytucji elektrofilowej, właściwościach benzenowych i toluenu, a także o reakcjach nitrowania, sulfonowania i alkilowania. Idealne dla studentów chemii, którzy chcą zrozumieć aromatyczne węglowodory i ich zastosowania.
Reakcje Chemiczne: Kluczowe Procesy
Kompleksowy przegląd najważniejszych reakcji chemicznych w chemii organicznej i nieorganicznej. Obejmuje reakcje amin, amidów, kwasów karboksylowych, hydrolizę, reakcje metali oraz doświadczenia takie jak próba Trommera i reakcja biuretowa. Idealne dla studentów przygotowujących się do egzaminów.
Aromatyczne Węglowodory: Benzen
Zgłębiaj właściwości benzenu, jego strukturę oraz mechanizmy reakcji, w tym substytucję i nitrowanie. Dowiedz się, jak benzen spełnia regułę Hückla i jakie cechy definiują węglowodory aromatyczne. Idealne dla studentów chemii.
Właściwości i Nazewnictwo Alkanów
Zgłębiaj właściwości fizyczne i chemiczne alkanów, ich nazewnictwo oraz metody syntezy. Notatka zawiera szczegółowe informacje o reakcjach spalania, charakterystyce węglowodorów nasyconych oraz przykłady zadań. Idealna dla studentów chemii organicznej.
Chemia związków węgla
Notatka z 1 tematu chemii organicznej - węgiel 6C i jego związki chemiczne na podstawie podr. Nowej Ery dla rozszerzenia
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Wprowadzenie do Fluorowcopochodnych Węglowodorów
Fluorowcopochodne węglowodorów to związki organiczne, w których atomy wodoru zostały zastąpione atomami fluorowców (F, Cl, Br, I). Charakteryzują się specyficznymi właściwościami chemicznymi i fizycznymi, które decydują o ich wszechstronnym zastosowaniu w przemyśle i życiu codziennym.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa i charakterystyka fluorowcopochodnych
Fluorowcopochodne węglowodorów składają się z dwóch kluczowych elementów: grupy węglowodorowej (R) oraz grupy funkcyjnej w postaci atomu fluorowca (X). Te związki nazywane są też halogenkami i mają ogólny wzór R-X.
Atomy fluorowców są jednowartościowe, co oznacza, że mogą tworzyć tylko jedno wiązanie kowalencyjne. Mogą one zastępować atomy wodoru w różnych pozycjach cząsteczki węglowodoru, tworząc związki o odmiennych właściwościach.
⚡ Warto zapamiętać! Im więcej atomów fluorowca w cząsteczce, tym bardziej zmieniają się właściwości związku w porównaniu do wyjściowego węglowodoru.
Przykłady takich związków to: chlorometan (CH₃Cl), gdzie jeden atom wodoru metanu został zastąpiony chlorem, czy tetrachlorometan (CCl₄), gdzie wszystkie cztery atomy wodoru zostały zastąpione chlorem.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo fluorowcopochodnych
Fluorowcopochodne węglowodorów dzielą się na dwie główne grupy: halogenki alkilowe (pochodne węglowodorów alifatycznych) i halogenki arylowe (pochodne węglowodorów aromatycznych).
W przypadku halogenków alkilowych atom fluorowca zastępuje atom wodoru w prostym łańcuchu węglowym. Przykłady to: chloroeten , 1-bromopropan czy dichlorodifluorometan (CF₂Cl₂).
Halogenki arylowe to związki zawierające pierścień benzenowy, w którym atom wodoru został zastąpiony atomem fluorowca. Można je nazywać na dwa sposoby, np. bromometylobenzen lub bromofenylometan.
🔑 Kluczowa różnica: Fluorowcopochodne alifatyczne mają proste lub rozgałęzione łańcuchy węglowe, podczas gdy aromatyczne zawierają pierścień benzenowy lub inny układ aromatyczny.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości fluorowcopochodnych
Właściwości fluorowcopochodnych zależą od ich masy cząsteczkowej - im większa masa, tym wyższa temperatura wrzenia. Najczęściej są to niepalne ciecze, nierozpuszczalne w wodzie, choć istnieją wyjątki - niektóre lżejsze związki występują jako gazy (np. CH₃F, CH₃Cl, CH₃Br).
Fluorowcopochodne łatwo rozpuszczają się w niepolarnych rozpuszczalnikach. Wykazują wysoką reaktywność chemiczną ze względu na spolaryzowane wiązanie C-X , co prowadzi do tego, że związki te są polarne i mają niezerowy moment dipolowy.
⚠️ Uwaga! Wiązanie C-X jest spolaryzowane, z ładunkiem δ+ na atomie węgla i δ- na atomie fluorowca, co sprawia, że atom węgla może być atakowany przez czynniki nukleofilowe.
Przykłady fluorowcopochodnych aromatycznych to 4-chlorotoluen i 1,6-dichloronaftalen, które zachowują specyficzne właściwości związków aromatycznych, jednocześnie zyskując nowe właściwości dzięki obecności atomów fluorowców.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Metody otrzymywania fluorowcopochodnych (I)
Fluorowcopochodne można otrzymywać na kilka sposobów. Jednym z nich jest reakcja substytucji, w której atom wodoru zostaje zastąpiony atomem fluorowca:
- W węglowodorach nasyconych: CH₄ + Cl₂ → CH₃Cl + HCl
- W węglowodorach aromatycznych: benzen + Br₂ → bromobenzen + HBr (w obecności katalizatora FeBr₃)
Inną metodą jest substytucja grupy hydroksylowej w cząsteczce alkoholu atomem fluorowca: CH₃CH₂OH + HCl → CH₃CH₂Cl + H₂O
🧪 Ciekawostka praktyczna: Reakcje addycji fluorowca lub fluorowcowodoru do alkenów i alkinów są powszechnie wykorzystywane w przemyśle do produkcji różnych związków organicznych.
Fluorowcopochodne można także uzyskać poprzez addycję fluorowca lub fluorowcowodoru do węglowodorów nienasyconych:
- Z alkenów: CH₂=CH₂ + Cl₂ → CH₂Cl-CH₂Cl
- Z alkinów: CH≡CH + HBr → CH₂=CHBr

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Metody otrzymywania fluorowcopochodnych (II)
Substytucja rodnikowa to kolejna ważna metoda, w której bezpośrednio wprowadza się atomy chloru lub bromu do cząsteczki alkanu. Proces zachodzi w temperaturze 25-35°C przy obecności światła:
CH₃-CH₂-CH₃ + Cl₂ → CH₃-CH₂-CH₂Cl (45%) + CH₃-CHCl-CH₃ (55%)
Substytucja nukleofilowa zachodzi, gdy mocna zasada reaguje z fluorowcopochodną w środowisku alkoholowym: CH₃-CH₂-Cl + KOH → CH₃-CH₂-OH + KCl
💡 Wskazówka! Pamiętaj, że w reakcji fluorowcopochodnych z amoniakiem powstają aminy - związki organiczne zawierające grupę aminową .
Interesującym przykładem jest reakcja fluorowcopochodnych z amoniakiem, prowadząca do otrzymania amin: CH₃-CH₂-CH₂Cl + NH₃ → CH₃-CH₂-CH₂NH₂ + HCl

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcja Wurtza i eliminacji
Reakcja Wurtza to metoda łączenia dwóch cząsteczek fluorowcopochodnych przy użyciu sodu, prowadząca do otrzymania dłuższych łańcuchów węglowych:
2CH₃Cl + 2Na → CH₃-CH₃ + 2NaCl (etan) 2CH₃CH₂Cl + 2Na → CH₃-CH₂-CH₂-CH₃ + 2NaCl (butan)
Jeśli w reakcji uczestniczą różne fluorowcopochodne, otrzymujemy mieszaninę alkanów o różnej długości łańcucha.
Reakcja eliminacji polega na oderwaniu prostszej cząsteczki od substratu, co prowadzi do powstania wiązania wielokrotnego. Jest to ważna metoda otrzymywania alkenów:
CH₃-CH₂Cl + KOH → CH₂=CH₂ + KCl + H₂O
📝 Na sprawdzian: W przypadku halogenków alkenów o dłuższym łańcuchu węglowym mogą powstawać mieszaniny różnych alkenów, zależnie od miejsca eliminacji.
W przypadku fluorowcopochodnych o dłuższych łańcuchach, eliminacja może prowadzić do powstania różnych izomerów, np.: CH₃-CH₂-CHBr-CH₃ + KOH → CH₃-CH=CH-CH₃ + CH₃-CH₂-CH=CH₂

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Związki magnezoorganiczne
Związki magnezoorganiczne (odczynniki Grignarda) o wzorze RMgX otrzymuje się w reakcji halogenków alkilowych z metalicznym magnezem:
CH₃-CH₂Cl + Mg → CH₃-CH₂MgCl (chlorek etylomagnezowy)
Reakcję tę prowadzi się w bezwodnym rozpuszczalniku, ponieważ woda rozkłada produkty! Odczynniki Grignarda są niezwykle użyteczne w syntezie organicznej.
Rozkład związków magnezoorganicznych w wodzie prowadzi do powstania węglowodorów:
CH₃-CH₂MgCl + H₂O → CH₃-CH₃ + MgCl(OH)
⚠️ Uwaga praktyczna: Związki magnezoorganiczne są wrażliwe na wodę i powietrze - podczas pracy z nimi zawsze trzeba stosować atmosferę gazu obojętnego (np. argonu).
Związki magnezoorganiczne znajdują szerokie zastosowanie w syntezie organicznej jako silne nukleofile i zasady, umożliwiając tworzenie nowych wiązań węgiel-węgiel.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Fluorowcopochodne węglowodorów aromatycznych
Fluorowce obecne w pierścieniu benzenowym kierują nowe podstawniki w pozycje orto i para. Istnieją dwie główne metody wprowadzania podstawników halogenowych:
-
Substytucja rodnikowa - umożliwia podstawienie atomów wodoru w grupie metylowej, np.: Toluen + Cl₂ → Chlorometylbenzen + HCl
Proces ten może być kontynuowany, prowadząc do dichlorometylobenzenu i trichlorometylobenzenu.
-
Substytucja elektrofilowa - wprowadza atom fluorowca bezpośrednio do pierścienia aromatycznego: Toluen + Cl₂ → 2-chlorotoluen + 4-chlorotoluen + HCl (z katalizatorem FeCl₃)
🧠 Zapamiętaj: Kierunek podstawienia w pierścieniu aromatycznym zależy od charakteru obecnego już podstawnika - grupy aktywujące kierują w pozycje orto i para, a dezaktywujące w pozycję meta.
Fluorowcopochodne aromatyczne wykazują inną reaktywność niż alifatyczne, co wynika z obecności układu aromatycznego, który zmienia właściwości elektronowe całej cząsteczki.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
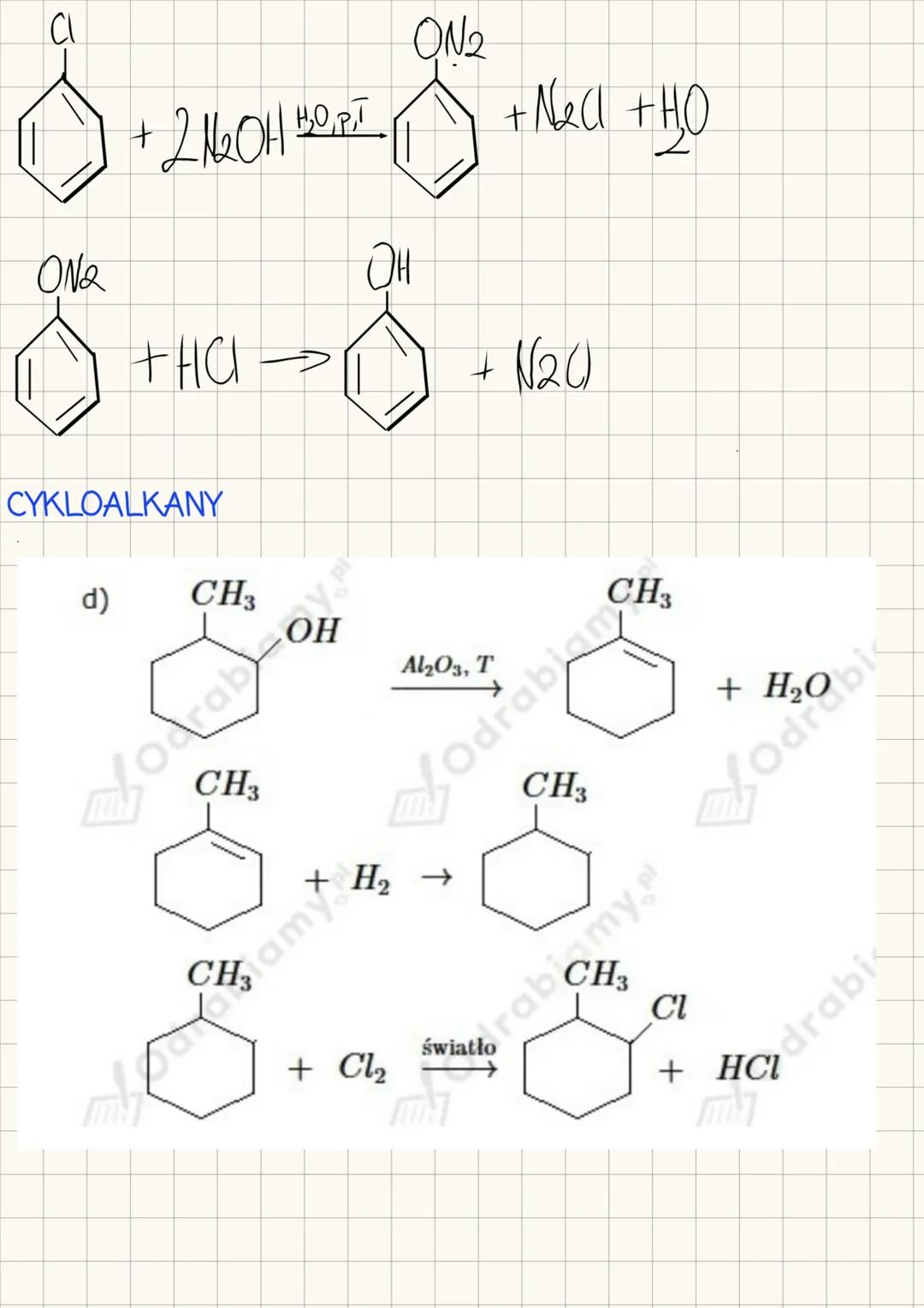
Reakcje fluorowcopochodnych aromatycznych
Fluorowcopochodne aromatyczne mogą ulegać różnym reakcjom, w tym reakcji z zasadami i kwasami:
-
Reakcja z NaOH: Chlorobenzen + 2NaOH → Fenol + NaCl + H₂O (w podwyższonej temperaturze i ciśnieniu)
-
Reakcja z HCl: Diazopochodna + HCl → Pochodna chlorowa + N₂
Związki cykloalkanowe z podstawnikami halogenowymi również wykazują interesujące właściwości i reaktywność:
- Dehydratacja alkoholi cyklicznych: Cykliczny alkohol + Al₂O₃ → Cykloalken + H₂O (w podwyższonej temperaturze)
🔬 Warto wiedzieć: Podstawienie atomu fluorowca w pierścieniu aromatycznym znacząco zmienia jego reaktywność, co ma duże znaczenie w syntezie leków i innych związków biologicznie czynnych.
Halogenowanie cykloalkanów przebiega podobnie jak w przypadku alkanów prostołańcuchowych: Cykloalkan + Cl₂ → Chlorocykloalkan + HCl (w obecności światła)

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
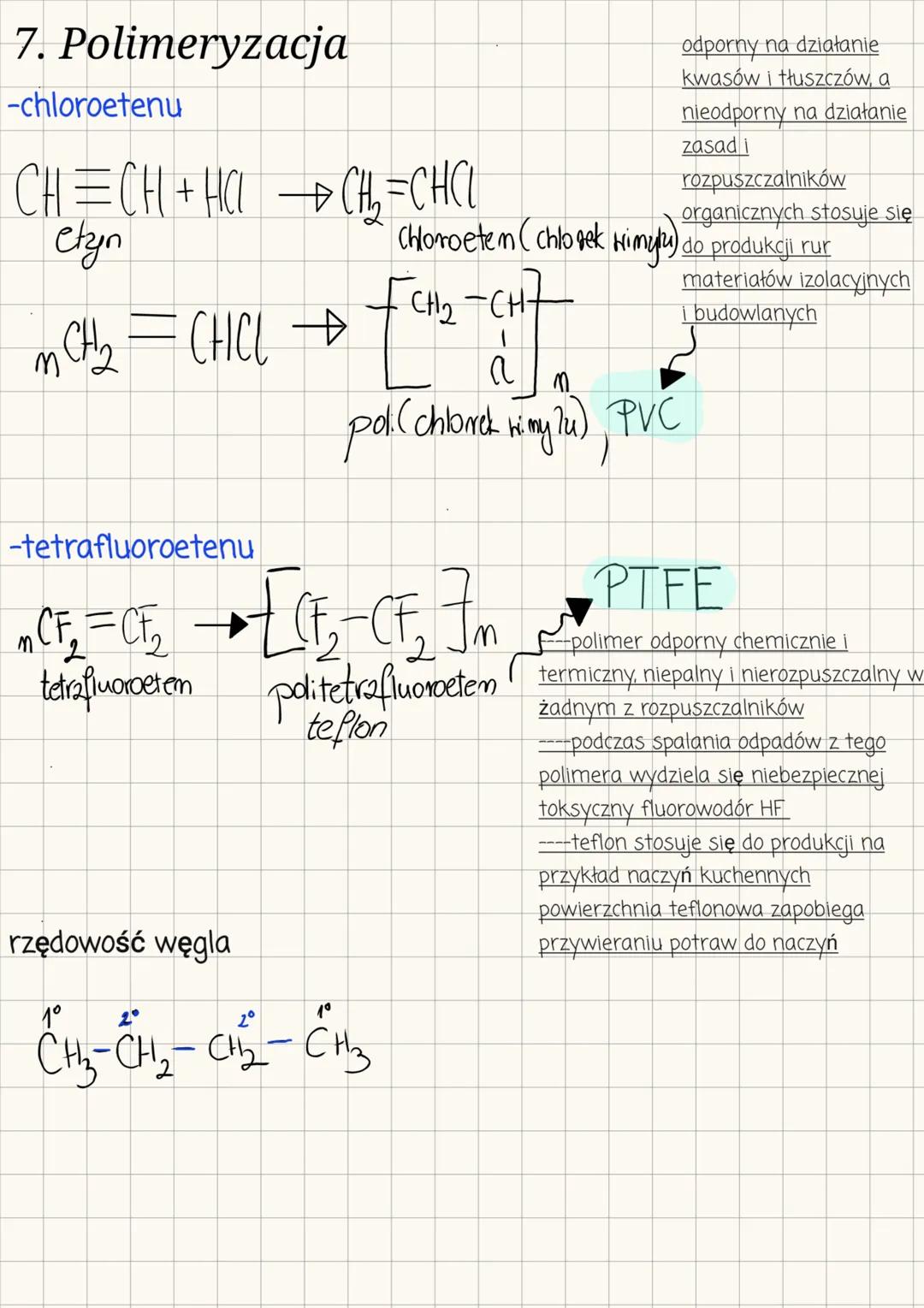
Polimeryzacja fluorowcopochodnych
Polimeryzacja fluorowcopochodnych ma ogromne znaczenie przemysłowe. Dwa najważniejsze przykłady to:
-
Polimeryzacja chloroetenu (chlorku winylu): nCH₂=CHCl → ₙ Powstały poli(chlorek winylu) (PVC) jest odporny na działanie kwasów i tłuszczów, ale nieodporny na zasady i rozpuszczalniki organiczne. Stosuje się go do produkcji rur, materiałów izolacyjnych i budowlanych.
-
Polimeryzacja tetrafluoroetenu: nCF₂=CF₂ → ₙ Powstały politetrafluoroetylen (PTFE, teflon) jest wyjątkowo odporny chemicznie i termicznie, niepalny i nierozpuszczalny w rozpuszczalnikach.
⚠️ Ostrzeżenie! Podczas spalania teflonu wydziela się niebezpieczny, toksyczny fluorowodór (HF), dlatego odpady tego polimeru muszą być odpowiednio utylizowane.
Teflon jest powszechnie stosowany do produkcji naczyń kuchennych, gdyż jego powierzchnia zapobiega przywieraniu potraw. Jest to jeden z najbardziej wszechstronnych polimerów wykorzystywanych w życiu codziennym dzięki swoim unikalnym właściwościom.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: chemia organiczna
9Węglowodory nienasycone - alkeny
Notatka chemia rozszerzona- alkeny, chemia organiczna
Chemia organiczna w pigułce
Chemia organiczna, notatki do matury, BEZ alkanów/ alkenów/ alkinów
Zatrucie i Właściwości Benzenu
Odkryj kluczowe informacje na temat benzenu, jego właściwości fizycznych i chemicznych, objawów zatrucia oraz reakcji chemicznych. Materiał obejmuje mechanizmy reakcji, takie jak bromowanie, nitrowanie i alkilowanie, a także skutki zdrowotne związane z narażeniem na benzen. Idealne dla studentów chemii i biologii.
Charakterystyczne Reakcje Chemii Organicznej
Odkryj kluczowe reakcje charakterystyczne w chemii organicznej, w tym reakcje biuretowe, ksantoproteinowe oraz próby Trommera i Tollensa. Zrozum, jak różne grupy funkcyjne, takie jak aminokwasy, cukry i fenole, reagują w różnych warunkach. Idealne dla studentów chemii poszukujących praktycznych informacji o reakcjach organicznych.
Chemia Benzenowa
Zgłębiaj chemię benzenową i jej reakcje. Dowiedz się o mechanizmach substytucji elektrofilowej, właściwościach benzenowych i toluenu, a także o reakcjach nitrowania, sulfonowania i alkilowania. Idealne dla studentów chemii, którzy chcą zrozumieć aromatyczne węglowodory i ich zastosowania.
Reakcje Chemiczne: Kluczowe Procesy
Kompleksowy przegląd najważniejszych reakcji chemicznych w chemii organicznej i nieorganicznej. Obejmuje reakcje amin, amidów, kwasów karboksylowych, hydrolizę, reakcje metali oraz doświadczenia takie jak próba Trommera i reakcja biuretowa. Idealne dla studentów przygotowujących się do egzaminów.
Aromatyczne Węglowodory: Benzen
Zgłębiaj właściwości benzenu, jego strukturę oraz mechanizmy reakcji, w tym substytucję i nitrowanie. Dowiedz się, jak benzen spełnia regułę Hückla i jakie cechy definiują węglowodory aromatyczne. Idealne dla studentów chemii.
Właściwości i Nazewnictwo Alkanów
Zgłębiaj właściwości fizyczne i chemiczne alkanów, ich nazewnictwo oraz metody syntezy. Notatka zawiera szczegółowe informacje o reakcjach spalania, charakterystyce węglowodorów nasyconych oraz przykłady zadań. Idealna dla studentów chemii organicznej.
Chemia związków węgla
Notatka z 1 tematu chemii organicznej - węgiel 6C i jego związki chemiczne na podstawie podr. Nowej Ery dla rozszerzenia
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.