Hybrydyzacja to kluczowy proces w chemii, który pomaga zrozumieć kształt... Pokaż więcej
Hybrydyzacja: Typy i Kształty Cząsteczek



Podstawy hybrydyzacji
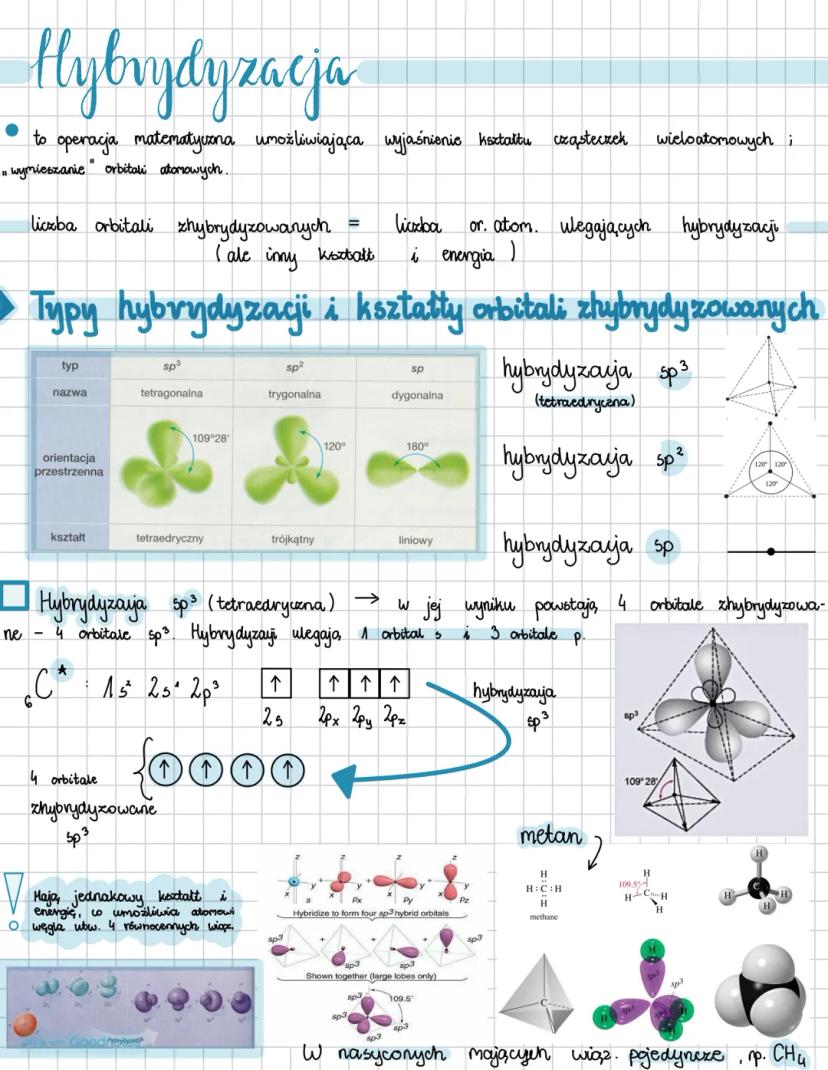
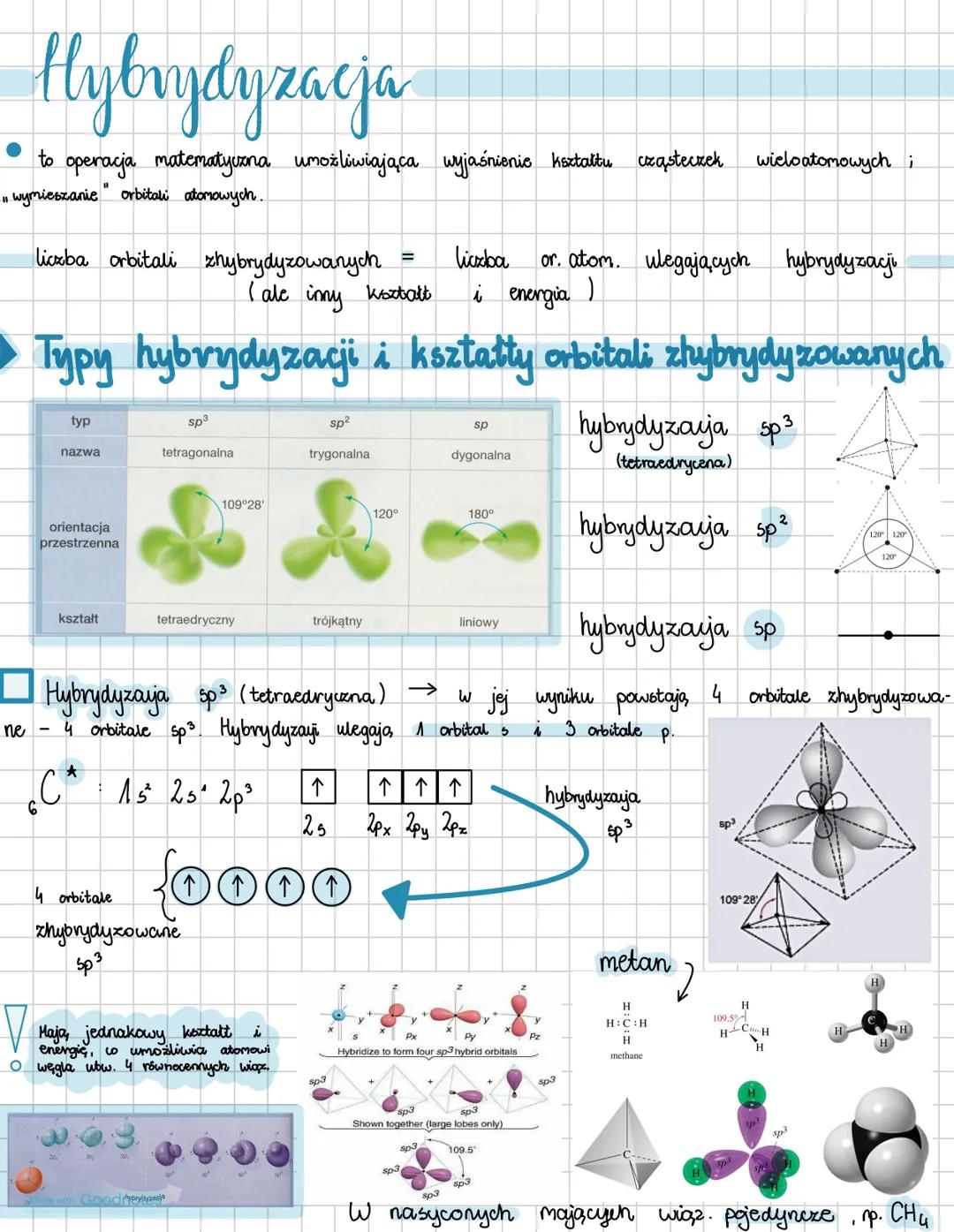
Hybrydyzacja to operacja matematyczna umożliwiająca wyjaśnienie kształtów cząsteczek wieloatomowych poprzez "wymieszanie" orbitali atomowych. Liczba orbitali zhybrydyzowanych zawsze równa się liczbie orbitali atomowych, które ulegają hybrydyzacji.
Istnieją trzy główne typy hybrydyzacji: sp³ (tetragonalna), sp² (trygonalna) i sp (dygonalna). Każdy typ charakteryzuje się inną orientacją przestrzenną i kształtem. W hybrydyzacji sp³ orbitale są ułożone pod kątem 109°28' tworząc kształt tetraedryczny, w sp² pod kątem 120° dając kształt trójkątny, a w sp pod kątem 180° co daje układ liniowy.
Hybrydyzacja sp³ zachodzi gdy 1 orbital s i 3 orbitale p mieszają się, tworząc 4 równocenne orbitale sp³. Dzięki temu atom węgla może utworzyć 4 równocenne wiązania, jak na przykład w cząsteczce metanu (CH₄).
Ciekawostka: Hybrydyzacja sp³ występuje w nasyconych związkach organicznych, które mają tylko wiązania pojedyncze, co wyjaśnia charakterystyczną strukturę przestrzenną alkanów!
Hybrydyzacja sp² i sp
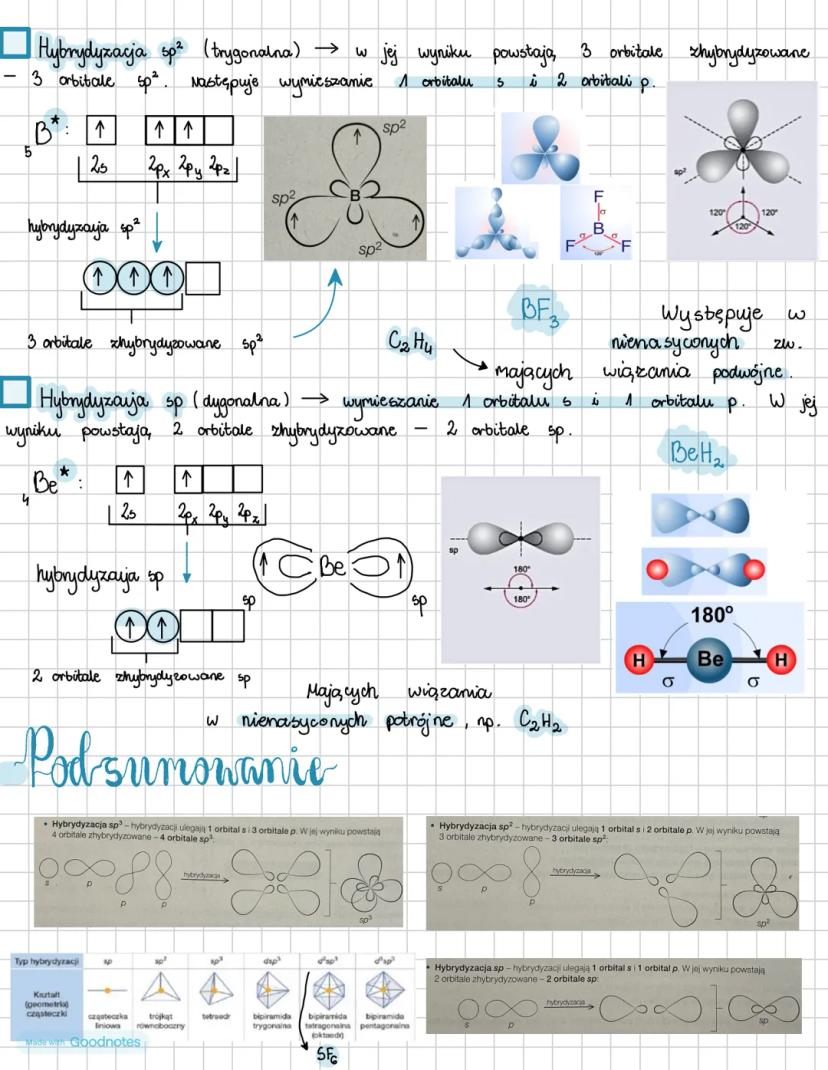
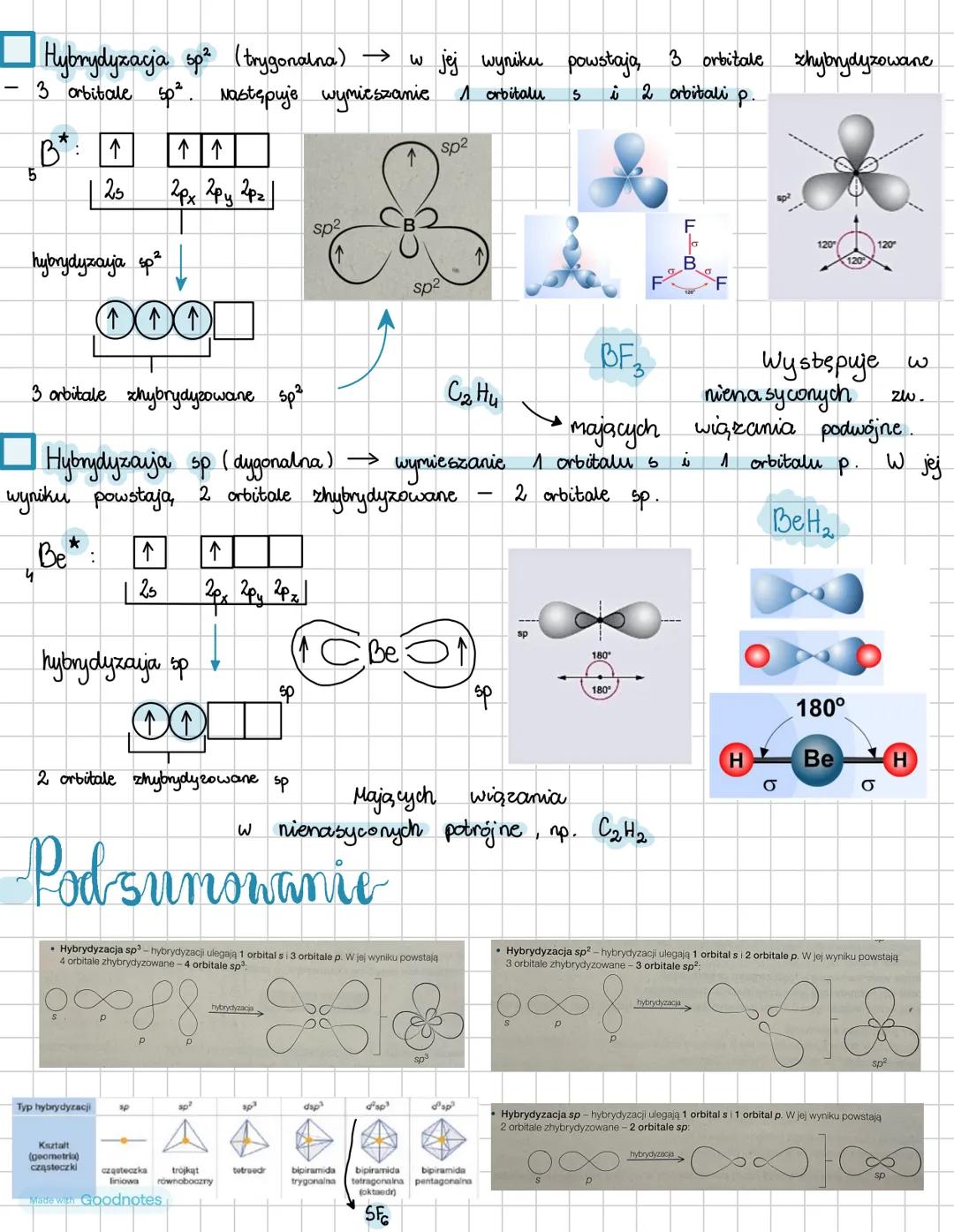
Hybrydyzacja sp² powstaje, gdy wymieszaniu ulega 1 orbital s i 2 orbitale p. W wyniku tego procesu tworzą się 3 orbitale zhybrydyzowane sp² ułożone w jednej płaszczyźnie pod kątem 120° względem siebie. Ten typ hybrydyzacji występuje w związkach nienasyconych mających wiązania podwójne, na przykład w BF₃.
Hybrydyzacja sp to wymieszanie 1 orbitalu s i 1 orbitalu p. Efektem są 2 orbitale zhybrydyzowane sp ułożone liniowo pod kątem 180°. Ten rodzaj hybrydyzacji znajdziemy w związkach z wiązaniami potrójnymi, takich jak acetylen (C₂H₂).
Różne typy hybrydyzacji odpowiadają różnym kształtom cząsteczek. Orbitale sp dają cząsteczki liniowe, sp² - trójkątne, sp³ - tetraedryczne, a przy udziale orbitali d możemy uzyskać bardziej złożone struktury jak bipiramidy czy oktaedry.
Wskazówka: Zapamiętaj prostą regułę - liczba w indeksie górnym (sp, sp², sp³) wskazuje, ile orbitali p uczestniczy w hybrydyzacji!
Geometria cząsteczek
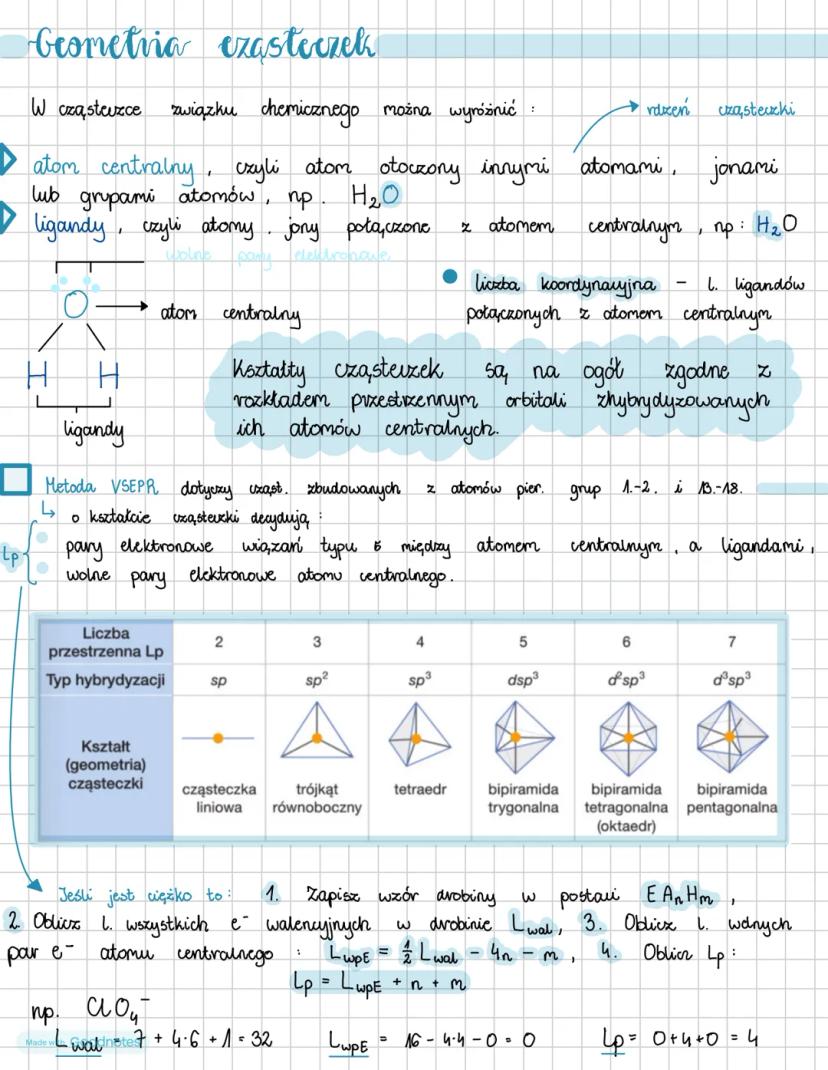
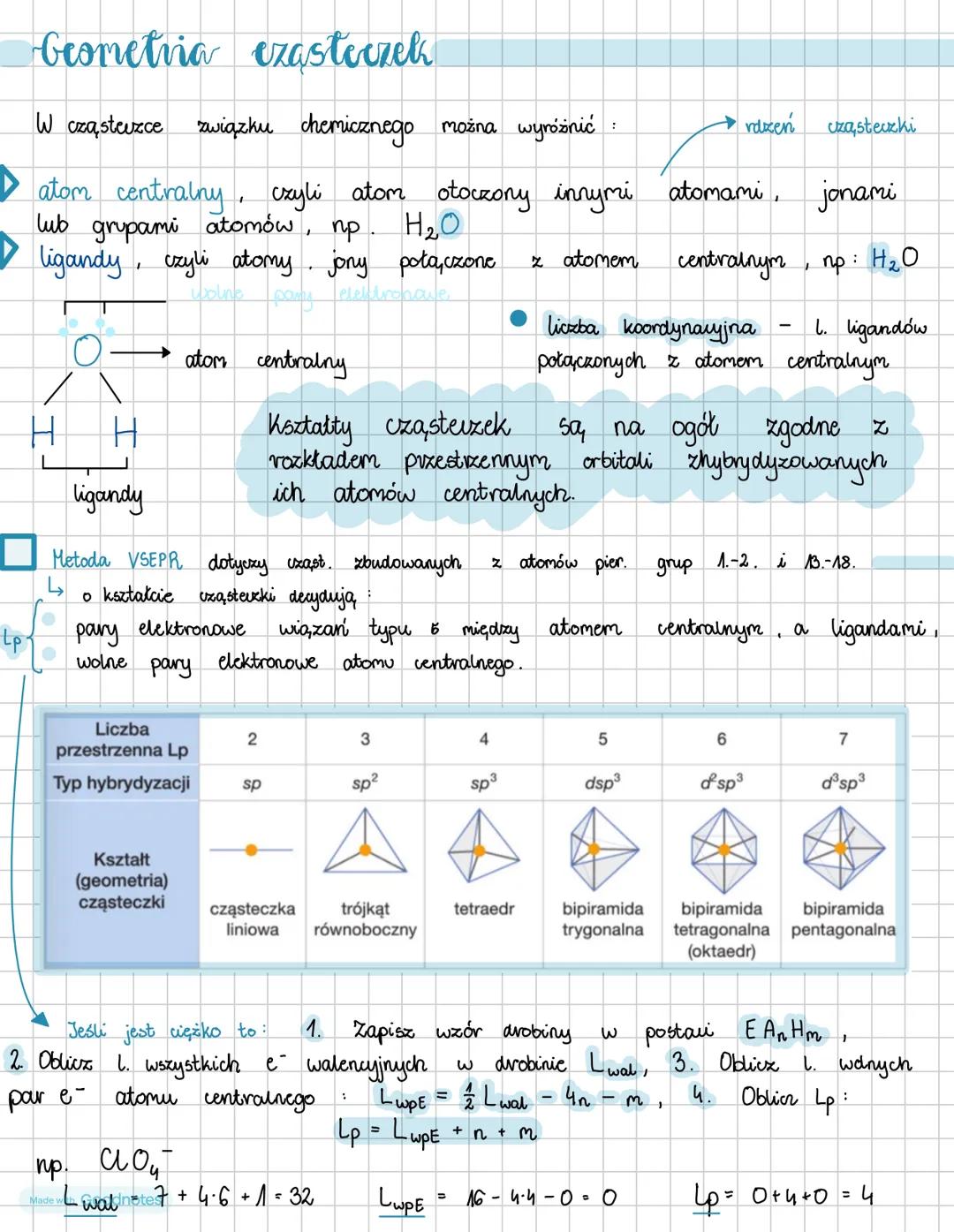
W każdej cząsteczce związku chemicznego możemy wyróżnić atom centralny (otoczony innymi atomami) oraz ligandy (atomy lub grupy atomów połączone z atomem centralnym). Na przykład w wodzie (H₂O) tlenem jest atom centralny, a wodory to ligandy.
Kształty cząsteczek najczęściej są zgodne z rozkładem przestrzennym orbitali zhybrydyzowanych ich atomów centralnych. O geometrii cząsteczki decydują pary elektronowe wiązań oraz wolne pary elektronowe atomu centralnego.
Metoda VSEPR pomaga przewidzieć kształt cząsteczek zbudowanych z atomów pierwiastków grup 1.-2. i 13.-18. ukłądu okresowego. Zgodnie z tą metodą, typ hybrydyzacji zależy od liczby przestrzennej par elektronowych (Lp).
Jeśli masz trudności z określeniem geometrii, możesz użyć prostego wzoru:
- Oblicz liczbę wszystkich elektronów walencyjnych
- Oblicz liczbę wolnych par elektronowych: Lwpe = - 4n - m
- Oblicz liczbę par elektronowych: Lp = Lwpe + n + m
Pomocna wskazówka: Liczba koordynacyjna to po prostu liczba ligandów połączonych z atomem centralnym. To kluczowy parametr przy określaniu geometrii!

Wpływ wolnych par elektronowych na geometrię
Wolne pary elektronowe atomu centralnego mogą znacząco zmieniać geometrię cząsteczki. Odpychanie między różnymi parami elektronowymi ma różną siłę, która rośnie w następującej kolejności:
- odpychanie między parami wiążącymi
- odpychanie między parą wiążącą a wolną parą
- odpychanie między wolnymi parami elektronowymi
To właśnie różna siła odpychania między parami elektronowymi powoduje, że rzeczywisty kształt cząsteczki może odbiegać od idealnej geometrii wynikającej z typu hybrydyzacji.
Na przykład, cząsteczka z hybrydyzacją sp³ i czterema ligandami tworzy tetraedr (np. CH₄). Jednak gdy mamy trzy ligandy i jedną wolną parę elektronową, powstaje kształt piramidy trygonalnej (NH₃). A przy dwóch ligandach i dwóch wolnych parach, cząsteczka staje się kątowa jak w przypadku wody (H₂O).
Zapamiętaj: Im więcej wolnych par elektronowych na atomie centralnym, tym bardziej rzeczywisty kształt cząsteczki będzie odbiegał od idealnego kształtu wynikającego z samej hybrydyzacji!

Przykłady określania geometrii cząsteczek
Przeanalizujmy kilka przykładów określania hybrydyzacji i geometrii cząsteczek:
CO₂: Lp = 2 + 0 = 2, więc hybrydyzacja sp. Cząsteczka jest liniowa: O=C=O.
H₂S: Lp = 2 + 2 = 4, hybrydyzacja sp³. Ze względu na dwie wolne pary elektronów na atomie siarki, cząsteczka ma kształt kątowy: H-S-H.
NCl₃: Lp = 3 + 1 = 4, hybrydyzacja sp³. Azot ma jedną wolną parę elektronów, więc cząsteczka ma kształt piramidy trygonalnej.
HCHO: Lp = 3 + 0 = 3, hybrydyzacja sp². Cząsteczka ma kształt trójkąta równobocznego.
NH₄⁺: Lp = 4 + 0 = 4, hybrydyzacja sp³. Jon amonowy ma kształt tetraedru, gdyż azot nie ma wolnych par elektronowych.
Praktyczna wskazówka: Aby szybko określić hybrydyzację, oblicz sumę ligandów i wolnych par elektronowych na atomie centralnym. Ta suma wskazuje na typ hybrydyzacji: 2 = sp, 3 = sp², 4 = sp³.
Więcej przykładów hybrydyzacji
Zobaczmy więcej przykładów określania hybrydyzacji i geometrii cząsteczek:
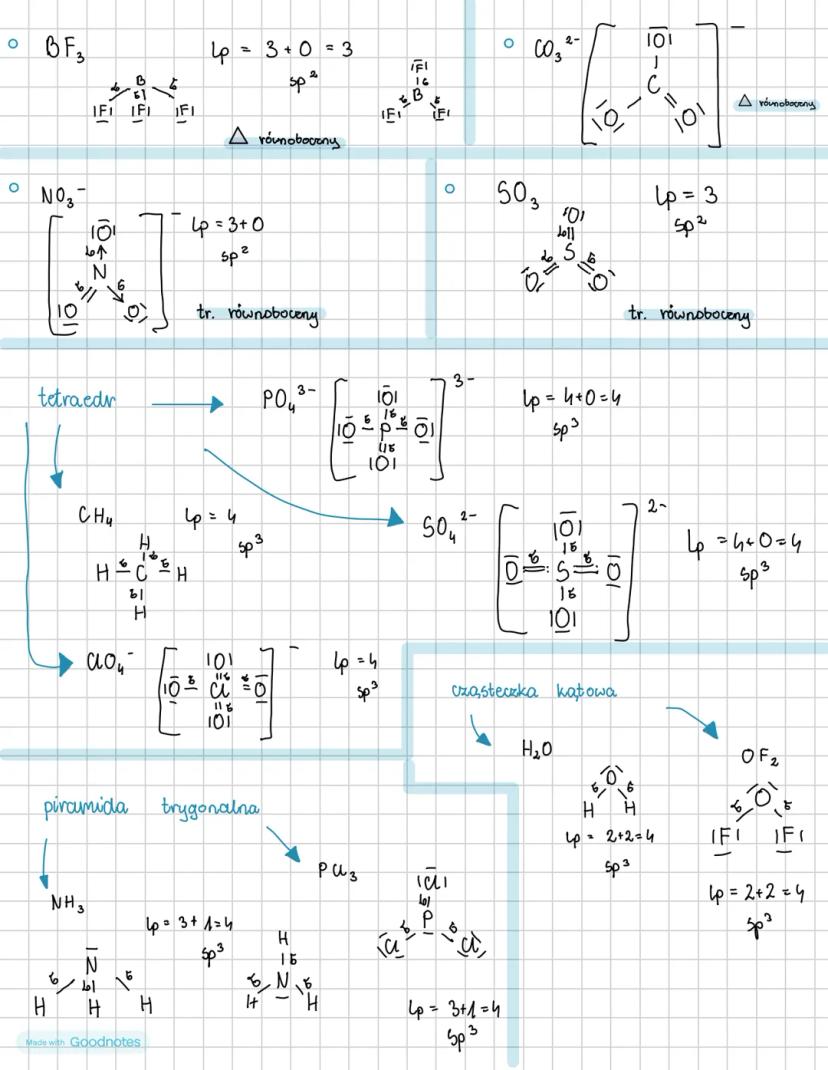
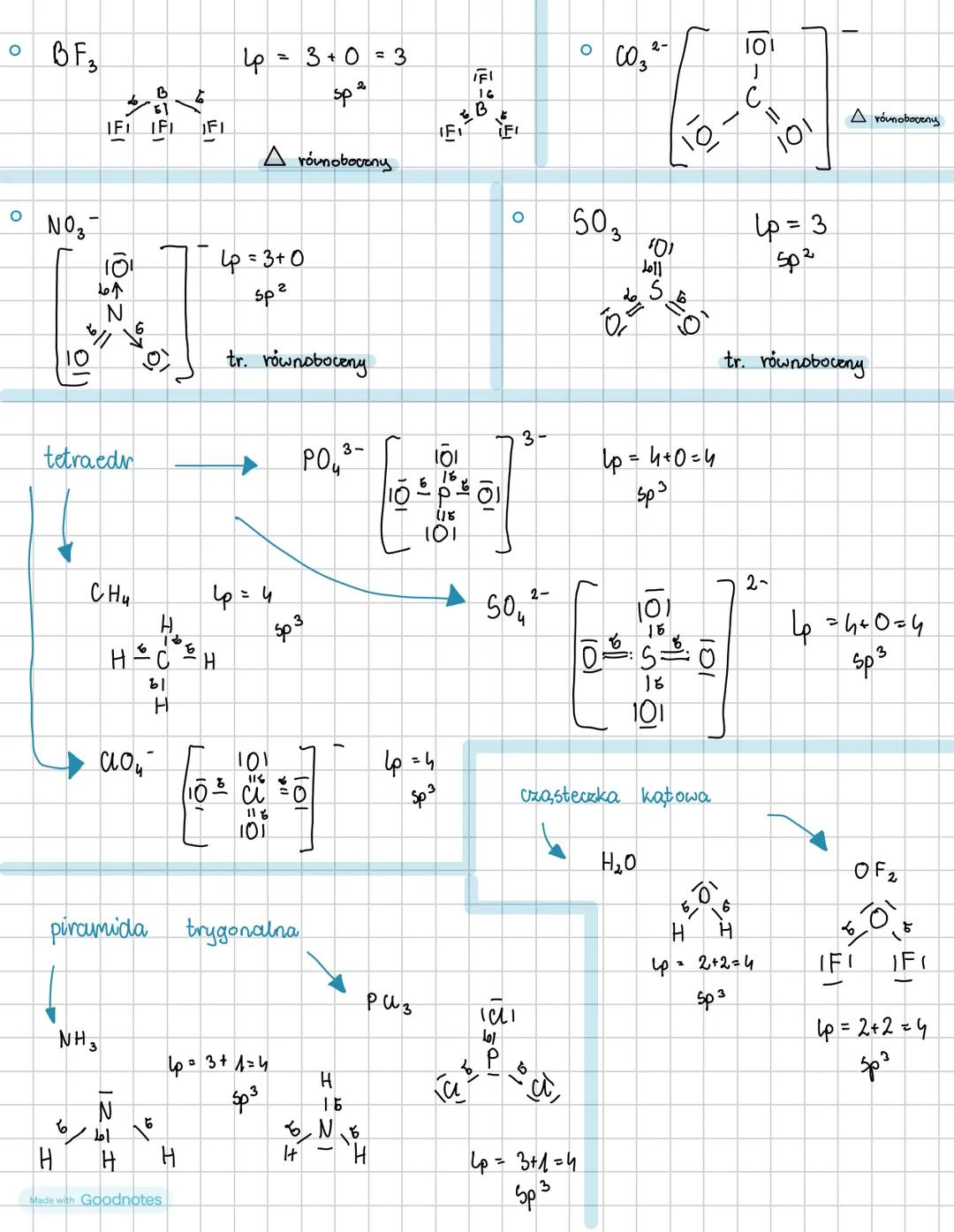
BF₃: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Wszystkie atomy leżą w jednej płaszczyźnie.
NO₃⁻: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Jon azotanowy jest płaski.
CH₄: Lp = 4 + 0 = 4, hybrydyzacja sp³, kształt tetraedru. Każdy kąt H-C-H wynosi 109°28'.
CO₃²⁻: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Jon węglanowy jest płaski.
H₂O: Lp = 2 + 2 = 4, hybrydyzacja sp³, cząsteczka kątowa. Dwie wolne pary elektronów na atomie tlenu zmieniają idealny kształt tetraedru na kątowy.
NH₃: Lp = 3 + 1 = 4, hybrydyzacja sp³, kształt piramidy trygonalnej. Jedna wolna para elektronów na atomie azotu.
Ważne: Płaskie cząsteczki powstają zawsze przy hybrydyzacji sp i sp², natomiast przy sp³ cząsteczka jest przestrzenna (tetraedr) lub może być kątowa (gdy są wolne pary elektronowe).

Zaawansowane przykłady i wskazówki
Pamiętaj, że cząsteczki mogą być płaskie lub przestrzenne. Zawsze płaskie są cząsteczki z hybrydyzacją sp i sp². Przy hybrydyzacji sp³ cząsteczki mają kształt tetraedru lub piramidy, czyli są przestrzenne.
SF₆: Lp = 4 + 1 = 5, hybrydyzacja sp³d. Kształt bipiramidy trygonalnej.
Dla bromu (Br) z konfiguracją elektronową [Ar] 4s² 3d¹⁰ 4p⁵, będziemy mieli jeden niesparowany elektron na orbitalu 4p.
BeH₂: Dla atomu berylu (1s² 2s²) po promocji mamy konfigurację 1s² 2s¹ 2p¹, co prowadzi do hybrydyzacji sp. Cząsteczka ma kształt liniowy.
Pamiętaj o praktycznym zastosowaniu poznanych reguł:
- Lp = 2 → hybrydyzacja sp → kształt liniowy
- Lp = 3 → hybrydyzacja sp² → kształt trójkątny
- Lp = 4 → hybrydyzacja sp³ → kształt tetraedryczny
- Lp = 5 → hybrydyzacja sp³d → kształt bipiramidy trygonalnej
- Lp = 6 → hybrydyzacja sp³d² → kształt oktaedru
Ważna wskazówka przed egzaminem: Podczas określania hybrydyzacji, zawsze najpierw policz liczbę par elektronowych, a następnie sprawdź, ile z nich to wolne pary. Dopiero wtedy możesz prawidłowo określić rzeczywisty kształt cząsteczki!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: hybrydyzacja
9Typy Hybrydyzacji Orbitali
Zrozumienie hybrydyzacji orbitali: szczegółowe omówienie typów sp, sp², sp³, ich kształtów cząsteczek oraz przykłady zastosowania. Idealne dla studentów chemii, którzy chcą zgłębić temat hybrydyzacji i jej wpływu na strukturę cząsteczek.
Hybrydyzacja
Hybrydyzacja – Proste Wytłumaczenie od Zera chemia rozszerzona
Typy hybrydyzacji i kształty orbitali zhybrydyzowanych
Temat o hybrydyzacji i kształtów cząsteczek chemia rozszerzona klasa 1
Hybrydyzacja i Wiązania Chemiczne
Zrozumienie hybrydyzacji i różnych typów wiązań chemicznych, w tym kowalencyjnych, jonowych i koordynacyjnych. Dowiedz się, jak obliczać liczbę przestrzenną oraz moment dipolowy cząsteczek. Materiał obejmuje również właściwości wody i znaczenie wiązań wodorowych. Idealne dla studentów chemii na poziomie średnim i wyższym.
Hybrydyzacja i Wiązania
Zrozumienie hybrydyzacji i rodzajów wiązań chemicznych, w tym wiązań kowalencyjnych i koordynacyjnych. Materiał obejmuje kluczowe koncepcje, takie jak geometria cząsteczek, polarność oraz elektroujemność. Idealne przygotowanie do matury z chemii.
Rodzaje Hybrydyzacji
Zrozumienie hybrydyzacji atomów: rodzaje hybrydyzacji (sp, sp², sp³) oraz ich wpływ na kształt cząsteczek. Dowiedz się, jak określić typ hybrydyzacji na podstawie liczby wiązań sigma i par elektronowych. Idealne dla studentów chemii, którzy chcą zgłębić temat wiązań chemicznych i struktury cząsteczek.
Typy Hybrydyzacji Orbitali
Zrozumienie hybrydyzacji orbitali atomowych: typy (sp, sp², sp³), geometria cząsteczek oraz ich zastosowanie w chemii. Dowiedz się, jak hybrydyzacja wpływa na kształt i właściwości związków chemicznych. Idealne dla studentów chemii i osób przygotowujących się do egzaminów.
Hybrydyzacja i Kształt Cząsteczek
Zrozumienie hybrydyzacji orbitali atomowych oraz kształtów cząsteczek w chemii. Materiał omawia różne typy wiązań chemicznych, w tym wiązania sigma i pi, oraz zastosowanie metody VSEPR do analizy geometrii cząsteczek. Idealne dla uczniów chemii na poziomie rozszerzonym.
Hybrydyzacja Orbitali Atomowych
Zrozumienie hybrydyzacji orbitali atomowych, w tym koncepcji Linusa Paulinga, redystrybucji energii orbitali oraz ich roli w tworzeniu wiązań chemicznych. Dowiedz się, jak konfiguracja elektronowa wpływa na powstawanie wiązań kowalencyjnych i geometrie cząsteczek, takich jak metan i BF3. Typ notatki: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Hybrydyzacja: Typy i Kształty Cząsteczek
Hybrydyzacja to kluczowy proces w chemii, który pomaga zrozumieć kształt cząsteczek i sposób tworzenia wiązań chemicznych. To matematyczna operacja "mieszania" orbitali atomowych, która tłumaczy dlaczego cząsteczki przyjmują określone kształty w przestrzeni.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Podstawy hybrydyzacji
Hybrydyzacja to operacja matematyczna umożliwiająca wyjaśnienie kształtów cząsteczek wieloatomowych poprzez "wymieszanie" orbitali atomowych. Liczba orbitali zhybrydyzowanych zawsze równa się liczbie orbitali atomowych, które ulegają hybrydyzacji.
Istnieją trzy główne typy hybrydyzacji: sp³ (tetragonalna), sp² (trygonalna) i sp (dygonalna). Każdy typ charakteryzuje się inną orientacją przestrzenną i kształtem. W hybrydyzacji sp³ orbitale są ułożone pod kątem 109°28' tworząc kształt tetraedryczny, w sp² pod kątem 120° dając kształt trójkątny, a w sp pod kątem 180° co daje układ liniowy.
Hybrydyzacja sp³ zachodzi gdy 1 orbital s i 3 orbitale p mieszają się, tworząc 4 równocenne orbitale sp³. Dzięki temu atom węgla może utworzyć 4 równocenne wiązania, jak na przykład w cząsteczce metanu (CH₄).
Ciekawostka: Hybrydyzacja sp³ występuje w nasyconych związkach organicznych, które mają tylko wiązania pojedyncze, co wyjaśnia charakterystyczną strukturę przestrzenną alkanów!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Hybrydyzacja sp² i sp
Hybrydyzacja sp² powstaje, gdy wymieszaniu ulega 1 orbital s i 2 orbitale p. W wyniku tego procesu tworzą się 3 orbitale zhybrydyzowane sp² ułożone w jednej płaszczyźnie pod kątem 120° względem siebie. Ten typ hybrydyzacji występuje w związkach nienasyconych mających wiązania podwójne, na przykład w BF₃.
Hybrydyzacja sp to wymieszanie 1 orbitalu s i 1 orbitalu p. Efektem są 2 orbitale zhybrydyzowane sp ułożone liniowo pod kątem 180°. Ten rodzaj hybrydyzacji znajdziemy w związkach z wiązaniami potrójnymi, takich jak acetylen (C₂H₂).
Różne typy hybrydyzacji odpowiadają różnym kształtom cząsteczek. Orbitale sp dają cząsteczki liniowe, sp² - trójkątne, sp³ - tetraedryczne, a przy udziale orbitali d możemy uzyskać bardziej złożone struktury jak bipiramidy czy oktaedry.
Wskazówka: Zapamiętaj prostą regułę - liczba w indeksie górnym (sp, sp², sp³) wskazuje, ile orbitali p uczestniczy w hybrydyzacji!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Geometria cząsteczek
W każdej cząsteczce związku chemicznego możemy wyróżnić atom centralny (otoczony innymi atomami) oraz ligandy (atomy lub grupy atomów połączone z atomem centralnym). Na przykład w wodzie (H₂O) tlenem jest atom centralny, a wodory to ligandy.
Kształty cząsteczek najczęściej są zgodne z rozkładem przestrzennym orbitali zhybrydyzowanych ich atomów centralnych. O geometrii cząsteczki decydują pary elektronowe wiązań oraz wolne pary elektronowe atomu centralnego.
Metoda VSEPR pomaga przewidzieć kształt cząsteczek zbudowanych z atomów pierwiastków grup 1.-2. i 13.-18. ukłądu okresowego. Zgodnie z tą metodą, typ hybrydyzacji zależy od liczby przestrzennej par elektronowych (Lp).
Jeśli masz trudności z określeniem geometrii, możesz użyć prostego wzoru:
- Oblicz liczbę wszystkich elektronów walencyjnych
- Oblicz liczbę wolnych par elektronowych: Lwpe = - 4n - m
- Oblicz liczbę par elektronowych: Lp = Lwpe + n + m
Pomocna wskazówka: Liczba koordynacyjna to po prostu liczba ligandów połączonych z atomem centralnym. To kluczowy parametr przy określaniu geometrii!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wpływ wolnych par elektronowych na geometrię
Wolne pary elektronowe atomu centralnego mogą znacząco zmieniać geometrię cząsteczki. Odpychanie między różnymi parami elektronowymi ma różną siłę, która rośnie w następującej kolejności:
- odpychanie między parami wiążącymi
- odpychanie między parą wiążącą a wolną parą
- odpychanie między wolnymi parami elektronowymi
To właśnie różna siła odpychania między parami elektronowymi powoduje, że rzeczywisty kształt cząsteczki może odbiegać od idealnej geometrii wynikającej z typu hybrydyzacji.
Na przykład, cząsteczka z hybrydyzacją sp³ i czterema ligandami tworzy tetraedr (np. CH₄). Jednak gdy mamy trzy ligandy i jedną wolną parę elektronową, powstaje kształt piramidy trygonalnej (NH₃). A przy dwóch ligandach i dwóch wolnych parach, cząsteczka staje się kątowa jak w przypadku wody (H₂O).
Zapamiętaj: Im więcej wolnych par elektronowych na atomie centralnym, tym bardziej rzeczywisty kształt cząsteczki będzie odbiegał od idealnego kształtu wynikającego z samej hybrydyzacji!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Przykłady określania geometrii cząsteczek
Przeanalizujmy kilka przykładów określania hybrydyzacji i geometrii cząsteczek:
CO₂: Lp = 2 + 0 = 2, więc hybrydyzacja sp. Cząsteczka jest liniowa: O=C=O.
H₂S: Lp = 2 + 2 = 4, hybrydyzacja sp³. Ze względu na dwie wolne pary elektronów na atomie siarki, cząsteczka ma kształt kątowy: H-S-H.
NCl₃: Lp = 3 + 1 = 4, hybrydyzacja sp³. Azot ma jedną wolną parę elektronów, więc cząsteczka ma kształt piramidy trygonalnej.
HCHO: Lp = 3 + 0 = 3, hybrydyzacja sp². Cząsteczka ma kształt trójkąta równobocznego.
NH₄⁺: Lp = 4 + 0 = 4, hybrydyzacja sp³. Jon amonowy ma kształt tetraedru, gdyż azot nie ma wolnych par elektronowych.
Praktyczna wskazówka: Aby szybko określić hybrydyzację, oblicz sumę ligandów i wolnych par elektronowych na atomie centralnym. Ta suma wskazuje na typ hybrydyzacji: 2 = sp, 3 = sp², 4 = sp³.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Więcej przykładów hybrydyzacji
Zobaczmy więcej przykładów określania hybrydyzacji i geometrii cząsteczek:
BF₃: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Wszystkie atomy leżą w jednej płaszczyźnie.
NO₃⁻: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Jon azotanowy jest płaski.
CH₄: Lp = 4 + 0 = 4, hybrydyzacja sp³, kształt tetraedru. Każdy kąt H-C-H wynosi 109°28'.
CO₃²⁻: Lp = 3 + 0 = 3, hybrydyzacja sp², kształt trójkąta równobocznego. Jon węglanowy jest płaski.
H₂O: Lp = 2 + 2 = 4, hybrydyzacja sp³, cząsteczka kątowa. Dwie wolne pary elektronów na atomie tlenu zmieniają idealny kształt tetraedru na kątowy.
NH₃: Lp = 3 + 1 = 4, hybrydyzacja sp³, kształt piramidy trygonalnej. Jedna wolna para elektronów na atomie azotu.
Ważne: Płaskie cząsteczki powstają zawsze przy hybrydyzacji sp i sp², natomiast przy sp³ cząsteczka jest przestrzenna (tetraedr) lub może być kątowa (gdy są wolne pary elektronowe).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zaawansowane przykłady i wskazówki
Pamiętaj, że cząsteczki mogą być płaskie lub przestrzenne. Zawsze płaskie są cząsteczki z hybrydyzacją sp i sp². Przy hybrydyzacji sp³ cząsteczki mają kształt tetraedru lub piramidy, czyli są przestrzenne.
SF₆: Lp = 4 + 1 = 5, hybrydyzacja sp³d. Kształt bipiramidy trygonalnej.
Dla bromu (Br) z konfiguracją elektronową [Ar] 4s² 3d¹⁰ 4p⁵, będziemy mieli jeden niesparowany elektron na orbitalu 4p.
BeH₂: Dla atomu berylu (1s² 2s²) po promocji mamy konfigurację 1s² 2s¹ 2p¹, co prowadzi do hybrydyzacji sp. Cząsteczka ma kształt liniowy.
Pamiętaj o praktycznym zastosowaniu poznanych reguł:
- Lp = 2 → hybrydyzacja sp → kształt liniowy
- Lp = 3 → hybrydyzacja sp² → kształt trójkątny
- Lp = 4 → hybrydyzacja sp³ → kształt tetraedryczny
- Lp = 5 → hybrydyzacja sp³d → kształt bipiramidy trygonalnej
- Lp = 6 → hybrydyzacja sp³d² → kształt oktaedru
Ważna wskazówka przed egzaminem: Podczas określania hybrydyzacji, zawsze najpierw policz liczbę par elektronowych, a następnie sprawdź, ile z nich to wolne pary. Dopiero wtedy możesz prawidłowo określić rzeczywisty kształt cząsteczki!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: hybrydyzacja
9Typy Hybrydyzacji Orbitali
Zrozumienie hybrydyzacji orbitali: szczegółowe omówienie typów sp, sp², sp³, ich kształtów cząsteczek oraz przykłady zastosowania. Idealne dla studentów chemii, którzy chcą zgłębić temat hybrydyzacji i jej wpływu na strukturę cząsteczek.
Hybrydyzacja
Hybrydyzacja – Proste Wytłumaczenie od Zera chemia rozszerzona
Typy hybrydyzacji i kształty orbitali zhybrydyzowanych
Temat o hybrydyzacji i kształtów cząsteczek chemia rozszerzona klasa 1
Hybrydyzacja i Wiązania Chemiczne
Zrozumienie hybrydyzacji i różnych typów wiązań chemicznych, w tym kowalencyjnych, jonowych i koordynacyjnych. Dowiedz się, jak obliczać liczbę przestrzenną oraz moment dipolowy cząsteczek. Materiał obejmuje również właściwości wody i znaczenie wiązań wodorowych. Idealne dla studentów chemii na poziomie średnim i wyższym.
Hybrydyzacja i Wiązania
Zrozumienie hybrydyzacji i rodzajów wiązań chemicznych, w tym wiązań kowalencyjnych i koordynacyjnych. Materiał obejmuje kluczowe koncepcje, takie jak geometria cząsteczek, polarność oraz elektroujemność. Idealne przygotowanie do matury z chemii.
Rodzaje Hybrydyzacji
Zrozumienie hybrydyzacji atomów: rodzaje hybrydyzacji (sp, sp², sp³) oraz ich wpływ na kształt cząsteczek. Dowiedz się, jak określić typ hybrydyzacji na podstawie liczby wiązań sigma i par elektronowych. Idealne dla studentów chemii, którzy chcą zgłębić temat wiązań chemicznych i struktury cząsteczek.
Typy Hybrydyzacji Orbitali
Zrozumienie hybrydyzacji orbitali atomowych: typy (sp, sp², sp³), geometria cząsteczek oraz ich zastosowanie w chemii. Dowiedz się, jak hybrydyzacja wpływa na kształt i właściwości związków chemicznych. Idealne dla studentów chemii i osób przygotowujących się do egzaminów.
Hybrydyzacja i Kształt Cząsteczek
Zrozumienie hybrydyzacji orbitali atomowych oraz kształtów cząsteczek w chemii. Materiał omawia różne typy wiązań chemicznych, w tym wiązania sigma i pi, oraz zastosowanie metody VSEPR do analizy geometrii cząsteczek. Idealne dla uczniów chemii na poziomie rozszerzonym.
Hybrydyzacja Orbitali Atomowych
Zrozumienie hybrydyzacji orbitali atomowych, w tym koncepcji Linusa Paulinga, redystrybucji energii orbitali oraz ich roli w tworzeniu wiązań chemicznych. Dowiedz się, jak konfiguracja elektronowa wpływa na powstawanie wiązań kowalencyjnych i geometrie cząsteczek, takich jak metan i BF3. Typ notatki: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.