Kwasy karboksylowe to niezwykle ważna grupa związków organicznych, które spotykasz... Pokaż więcej
Kwasy Karboksylowe – Nowe Informacje i Zastosowania



Budowa i nomenklatura kwasów karboksylowych
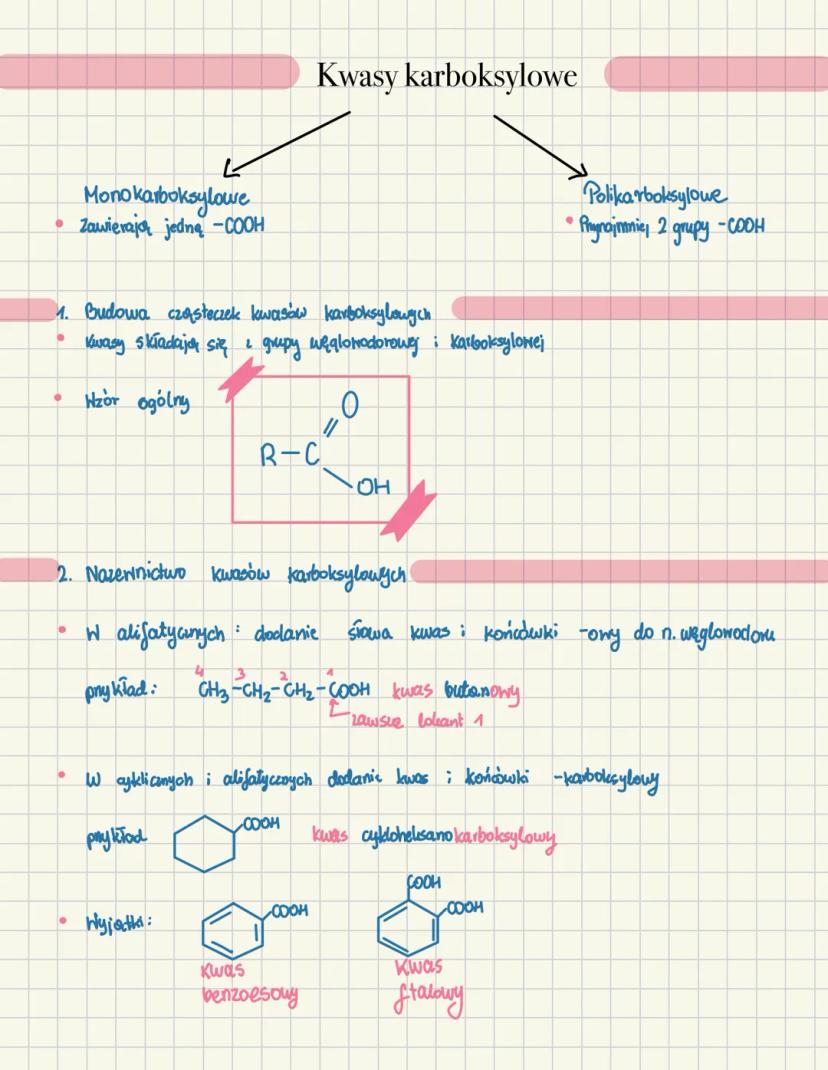
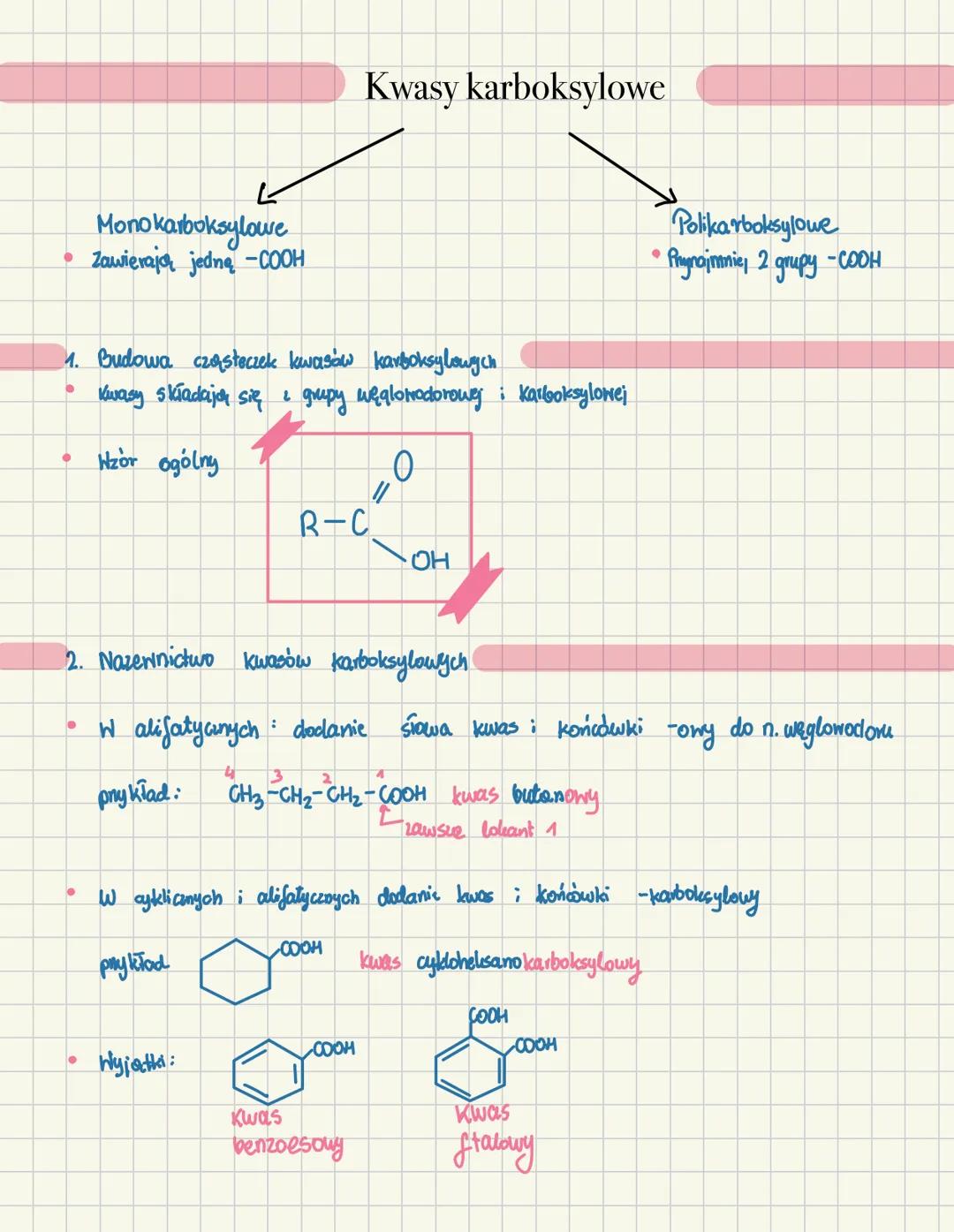
Kwasy karboksylowe dzielą się na monokarboksylowe i polikarboksylowe . Ich cząsteczka składa się z części węglowodorowej i grupy karboksylowej o wzorze ogólnym R-COH.
Nazewnictwo tych związków jest dość proste, gdy się je zrozumie. Dla kwasów alifatycznych dodajemy słowo "kwas" i końcówkę "-owy" do nazwy węglowodoru . W przypadku związków cyklicznych lub aromatycznych dodajemy "kwas" i końcówkę "-karboksylowy" (np. kwas cykloheksanokarboksylowy).
Niektóre kwasy mają też powszechnie używane nazwy zwyczajowe, jak kwas benzoesowy czy kwas ftalowy, które warto zapamiętać.
💡 Wskazówka: Grupę karboksylową zawsze numerujemy jako pozycję 1 w łańcuchu. To znacznie ułatwia nazywanie tych związków!
Szereg homologiczny i izomeria szkieletowa
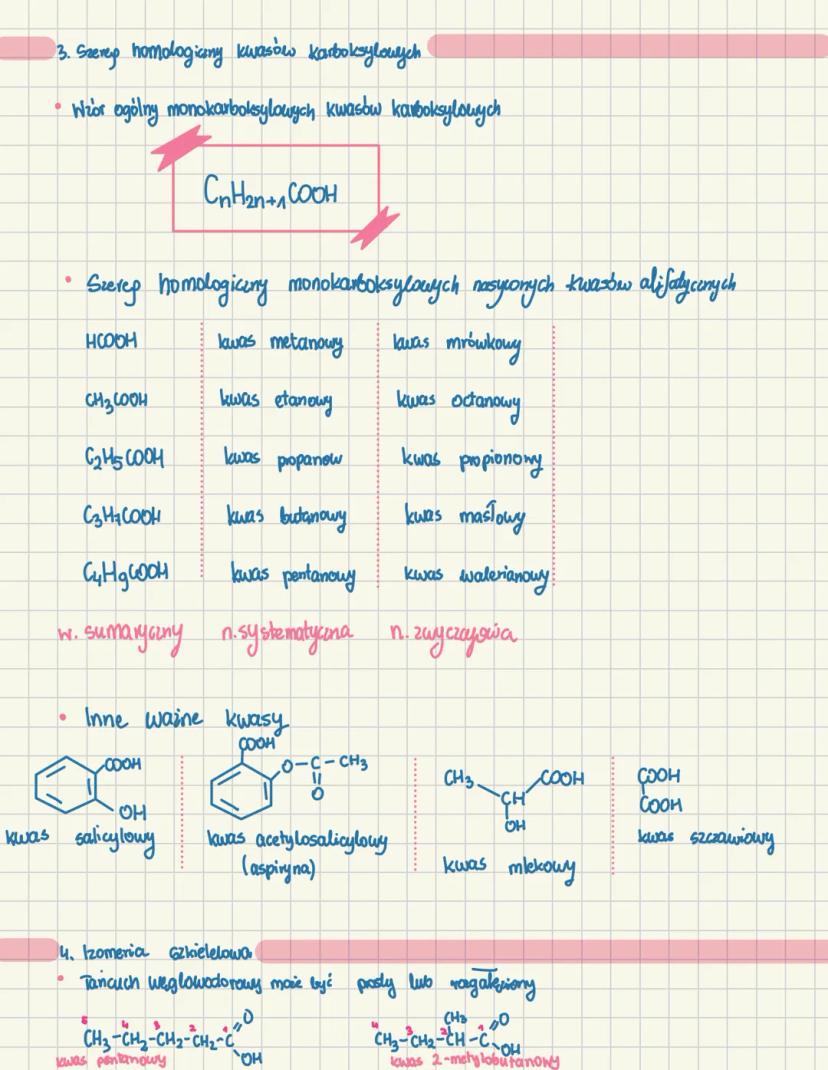
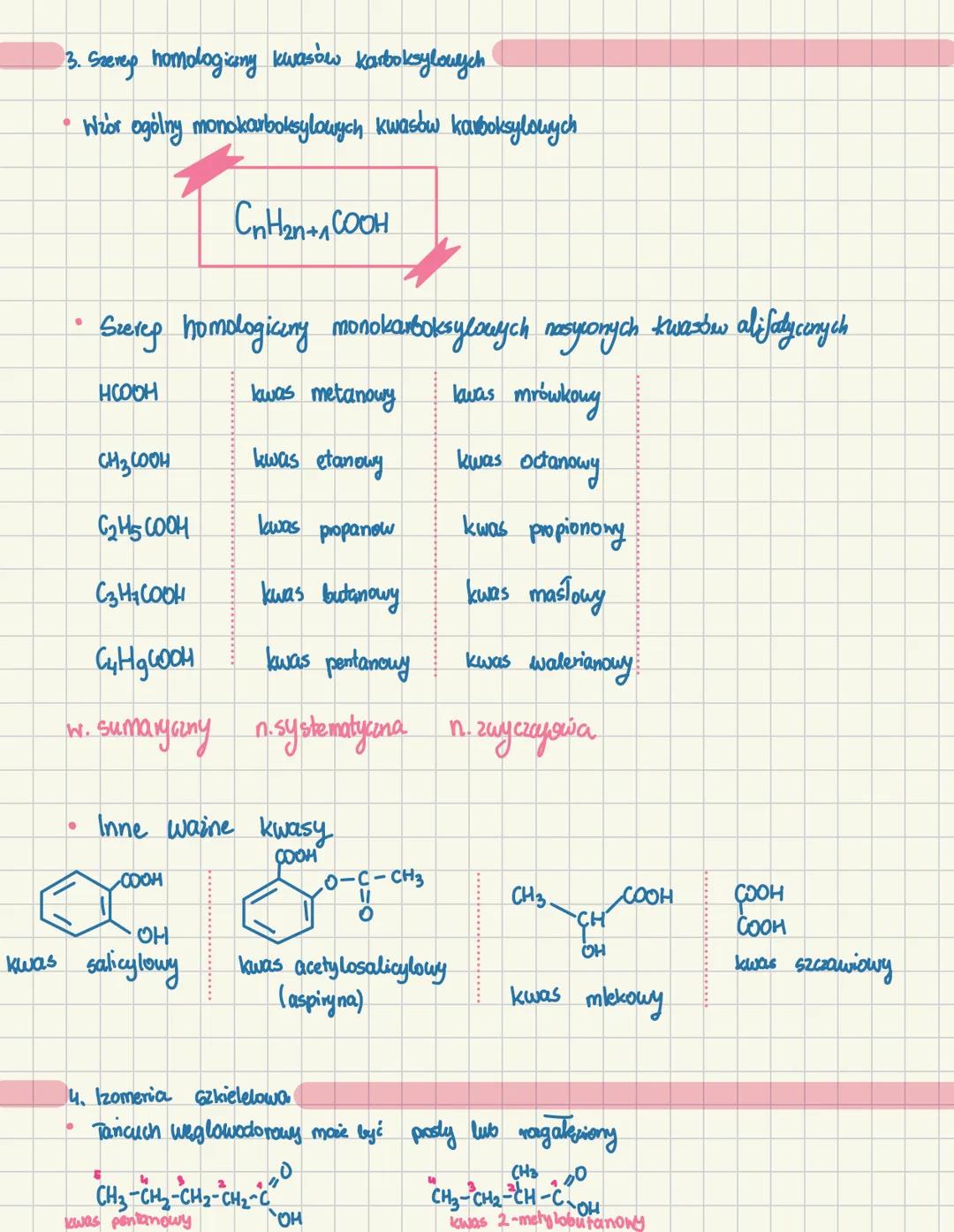
Nasycone monokarboksylowe kwasy alifatyczne tworzą szereg homologiczny o wzorze ogólnym CₙH₂ₙ₊₁COOH. Zaczynając od najprostszego kwasu metanowego (mrówkowego) HCOOH, każdy kolejny członek ma o jedną grupę -CH₂- więcej.
Wśród ważnych przedstawicieli warto zapamiętać:
- kwas metanowy (mrówkowy) - HCOOH
- kwas etanowy (octowy) - CH₃COOH
- kwas propanowy (propionowy) - C₂H₅COOH
- kwas butanowy (masłowy) - C₃H₇COOH
- kwas pentanowy (walerianowy) - C₄H₉COOH
W chemii organicznej znajdziesz też ważne kwasy zawierające dodatkowe grupy funkcyjne, takie jak kwas salicylowy, kwas acetylosalicylowy (aspiryna), kwas szczawiowy czy kwas mlekowy.
Izomeria szkieletowa kwasów karboksylowych polega na różnych układach atomów w łańcuchu węglowym. Na przykład kwas pentanowy (C₅H₁₀O₂) ma izomery takie jak kwas 2-metylobutanowy o tym samym wzorze sumarycznym, ale innym ułożeniu atomów.
📝 Ważne: Pamiętaj, że mimo różnej budowy, izomery mają zawsze ten sam wzór sumaryczny. To klucz do zrozumienia izomerii w chemii organicznej!
Rodzaje izomerii kwasów karboksylowych
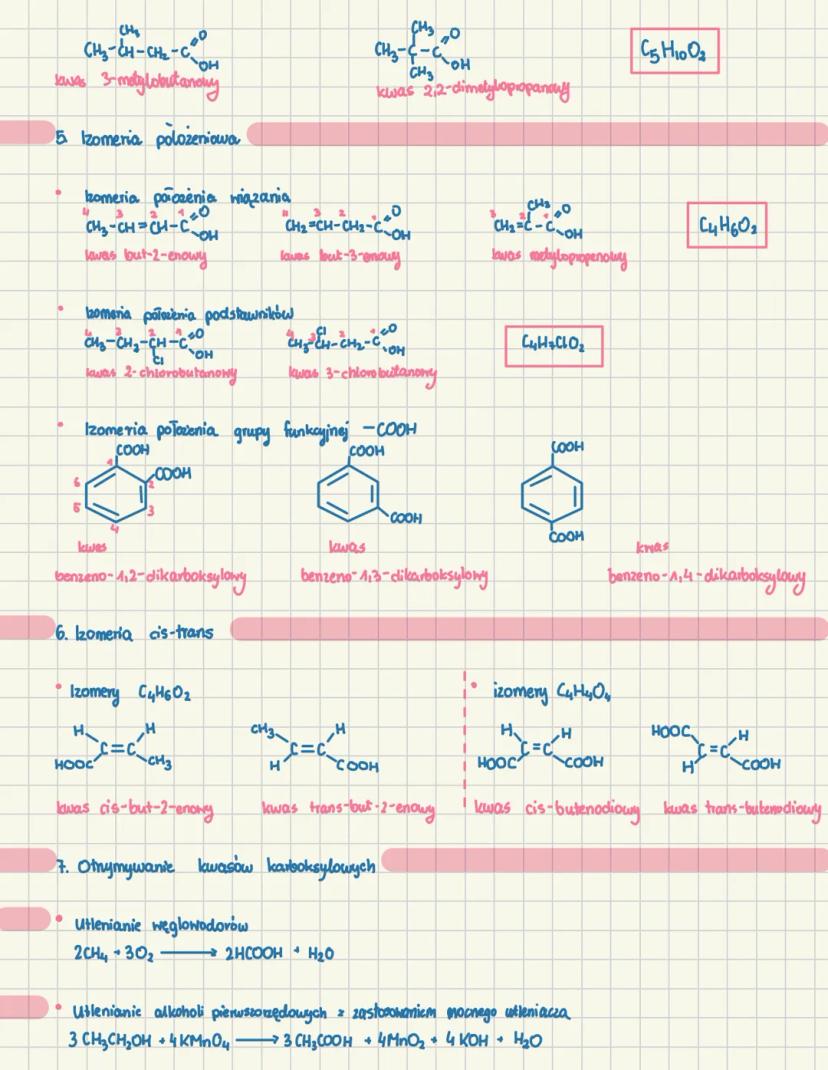
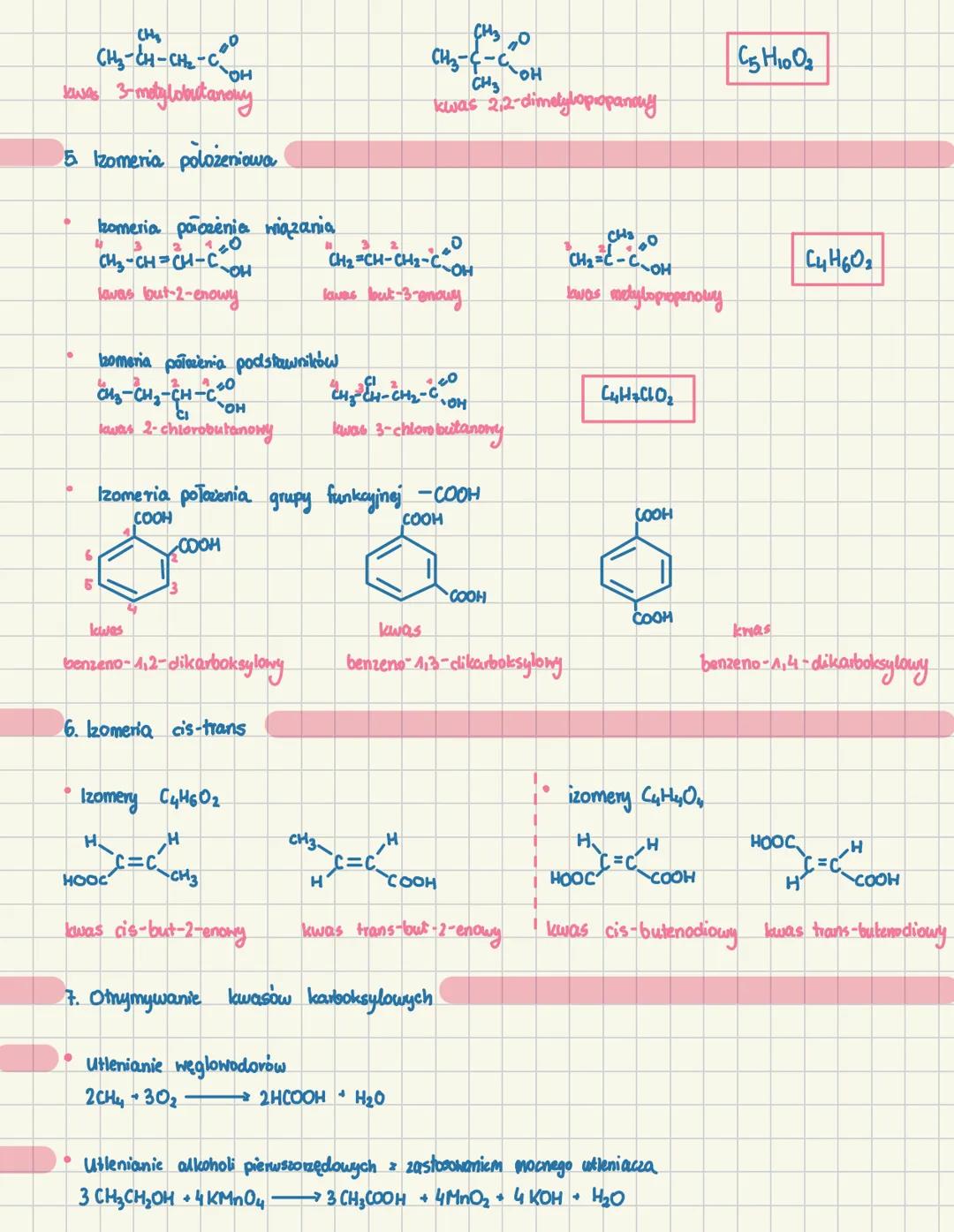
Kwasy karboksylowe wykazują różne rodzaje izomerii, co znacząco wpływa na ich właściwości. Izomeria położeniowa może dotyczyć położenia wiązania podwójnego w cząsteczce. Na przykład kwas but-2-enowy i kwas but-3-enowy (C₄H₆O₂) różnią się położeniem wiązania podwójnego w łańcuchu.
Izomeria położenia podstawników to kolejny typ - np. kwas 2-chlorobutanowy i kwas 3-chlorobutanowy (C₄H₇ClO₂) różnią się położeniem atomu chloru. W przypadku kwasów dikarboksylowych możemy mieć izomerię położenia grup -COOH, jak w kwasach benzenodikarboksylowych.
Szczególnie interesująca jest izomeria cis-trans, występująca przy wiązaniu podwójnym. Kwas cis-but-2-enowy i kwas trans-but-2-enowy mają te same grupy, ale inaczej rozmieszczone w przestrzeni względem wiązania podwójnego.
Kwasy karboksylowe można otrzymać na kilka sposobów:
- Przez utlenianie węglowodorów
- Przez utlenianie alkoholi pierwszorzędowych (z użyciem KMnO₄)
- Przez utlenianie aldehydów (próby Tollensa lub Trommera)
🧪 Eksperyment: Próba Tollensa (powstawanie lustra srebrowego) jest świetnym sposobem na odróżnienie aldehydów od ketonów - tylko aldehydy dają pozytywny wynik!

Otrzymywanie kwasów i ich dysocjacja
Kwasy karboksylowe można otrzymać różnymi metodami. W przypadku kwasu mrówkowego (HCOOH) stosuje się reakcję tlenku węgla z wodorotlenkiem sodu, a następnie reakcję z kwasem siarkowym. Można też przeprowadzić hydrolizę mrówczanu metylu.
Kwas octowy (CH₃COOH) otrzymujemy przez utlenianie aldehydu octowego lub przez fermentację octową alkoholu etylowego. Ta ostatnia metoda jest stosowana w produkcji octu spożywczego.
Dysocjacja elektrolityczna to kluczowa właściwość kwasów karboksylowych. Zachodzi ona dzięki polaryzacji wiązania C-O w grupie karboksylowej, co osłabia wiązanie O-H. W wyniku dysocjacji powstaje jon wodorowy (H⁺) i reszta kwasowa (np. HCOO⁻ lub CH₃COO⁻).
Równania dysocjacji można zapisać:
- HCOOH → HCOO⁻ + H⁺
- CH₃COOH → CH₃COO⁻ + H⁺
💡 Ciekawostka: Kwasy karboksylowe są znacznie słabsze od kwasów nieorganicznych (jak HCl czy H₂SO₄), ale dzięki temu znajdują szersze zastosowanie w produktach spożywczych i kosmetycznych.

Asocjacja i reakcje kwasów karboksylowych
Asocjacja to proces łączenia się cząsteczek kwasów karboksylowych w większe zespoły poprzez wiązania wodorowe. Ten proces wpływa na ich właściwości fizyczne - wraz z wydłużeniem łańcucha węglowego zmienia się stan skupienia (z ciekłego na stały), zmniejsza się lotność i rozpuszczalność w wodzie.
Polarność wiązań w grupie karbonylowej i hydroksylowej sprzyja tworzeniu wiązań wodorowych między cząsteczkami kwasu. Pojedyncza cząsteczka może utworzyć nawet 12 wiązań wodorowych!
Kwasy karboksylowe wchodzą w liczne reakcje chemiczne:
- Z metalami aktywnymi
- Z tlenkami metali
- Z wodorotlenkami metali
- Z solami słabszych kwasów
Mogą również ulegać reakcjom fluorowcowania czy addycji wodoru do wiązania podwójnego .
🔍 Wskazówka praktyczna: Reakcje kwasów z wodorotlenkami (zobojętnianie) są podstawą miareczkowania, którym możesz określić stężenie kwasu lub zasady w roztworze.
Moc kwasów karboksylowych
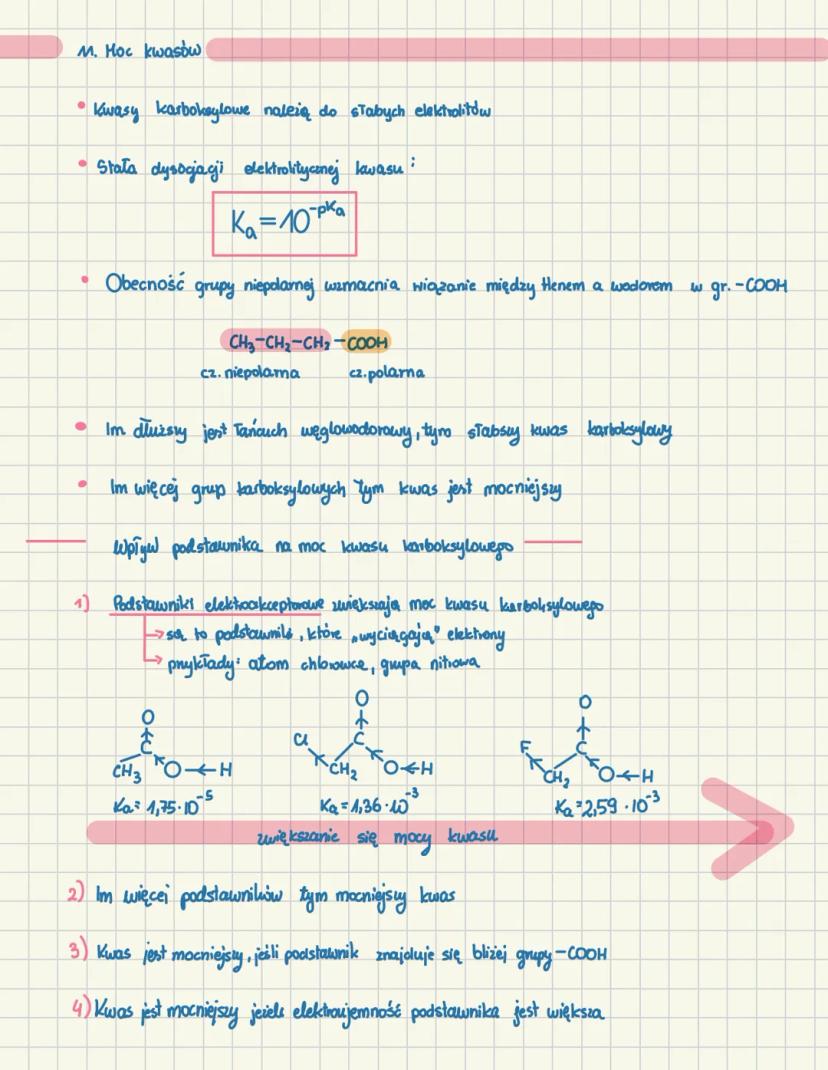
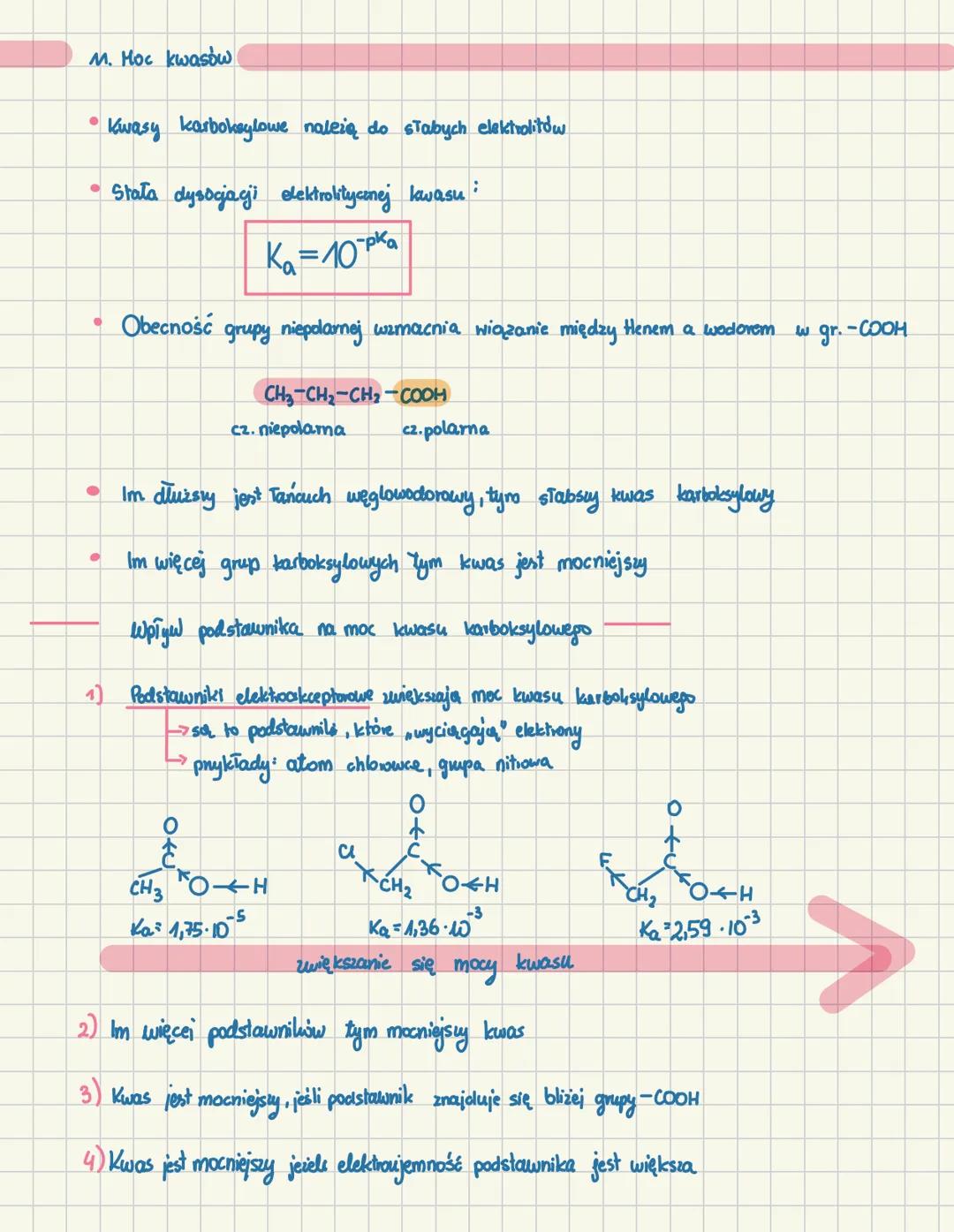
Kwasy karboksylowe należą do słabych elektrolitów, co oznacza, że dysocjują tylko częściowo w roztworze wodnym. Moc kwasu wyrażamy za pomocą stałej dysocjacji Ka lub wartości pKa .
Czynniki wpływające na moc kwasu:
- Długość łańcucha węglowodorowego - im dłuższy łańcuch niepolarny, tym słabszy kwas.
- Liczba grup karboksylowych - im więcej grup -COOH, tym kwas jest mocniejszy.
- Podstawniki elektroakceptorowe (wyciągające elektrony, np. atomy chlorowców, grupa nitrowa) zwiększają moc kwasu.
- Pozycja podstawnika - kwas jest mocniejszy, gdy podstawnik znajduje się bliżej grupy -COOH.
- Elektrujemność podstawnika - im większa, tym kwas mocniejszy.
Natomiast podstawniki elektrodonorowe (dostarczające elektrony, np. grupy alkilowe, grupa hydroksylowa) zmniejszają moc kwasów karboksylowych.
⚠️ Pamiętaj: Moc kwasu może być kluczowa dla przebiegu reakcji! Mocniejszy kwas będzie lepszym katalizatorem w wielu reakcjach i będzie łatwiej oddawał proton w reakcjach z zasadami.

Specyficzne właściwości i reakcje
Podstawniki elektroakceptorowe (EA) zwiększają moc kwasów, gdy:
- Znajdują się bliżej grupy -COOH w cząsteczce
- Jest ich więcej w cząsteczce
- Mają większą elektrujemność
Sole kwasów karboksylowych mają odczyn zasadowy. Podczas hydrolizy soli, np. CH₃COONa, powstaje słaby kwas i mocna zasada: CH₃COO⁻ + H₂O ⇌ CH₃COOH + OH⁻
Kwas metanowy (mrówkowy) wyróżnia się spośród innych kwasów karboksylowych, ponieważ posiada dwie grupy funkcyjne: karboksylową -COOH i aldehydową H-C=O. Ta unikalna budowa nadaje mu właściwości redukujące, których nie mają wyższe kwasy.
Ważną reakcją kwasów karboksylowych jest dekarboksylacja (odłączenie CO₂): R-COOH → R-H + CO₂
Inne kwasy karboksylowe można redukować według schematu: R-COOH → R-CHO → R-CH₂OH (kwas karboksylowy → aldehyd → alkohol)
🧪 Zastosowanie: Dekarboksylacja jest ważna w biochemii - wiele przemian metabolicznych w organizmie opiera się na tej reakcji, np. podczas cyklu Krebsa.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Gazy i tlenki. Powietrze i inne gazy.
Notatki do sprawdzianu z chemii dla klasy 7 z działu Powietrze i inne gazy (lub w innych podręcznikach Gazy i tlenki). Obejmuje tematy: Powietrze, gazy szlachetne, tlenek węgla IV, wodór, azot, zanieczyszczenia powietrza.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Kwasy Karboksylowe – Nowe Informacje i Zastosowania
Kwasy karboksylowe to niezwykle ważna grupa związków organicznych, które spotykasz każdego dnia - w occie, cytrusach czy niektórych lekach. Charakteryzują się obecnością grupy karboksylowej -COOH, która nadaje im ich szczególne właściwości. Zrozumienie ich budowy i reakcji jest kluczowe zarówno w... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa i nomenklatura kwasów karboksylowych
Kwasy karboksylowe dzielą się na monokarboksylowe i polikarboksylowe . Ich cząsteczka składa się z części węglowodorowej i grupy karboksylowej o wzorze ogólnym R-COH.
Nazewnictwo tych związków jest dość proste, gdy się je zrozumie. Dla kwasów alifatycznych dodajemy słowo "kwas" i końcówkę "-owy" do nazwy węglowodoru . W przypadku związków cyklicznych lub aromatycznych dodajemy "kwas" i końcówkę "-karboksylowy" (np. kwas cykloheksanokarboksylowy).
Niektóre kwasy mają też powszechnie używane nazwy zwyczajowe, jak kwas benzoesowy czy kwas ftalowy, które warto zapamiętać.
💡 Wskazówka: Grupę karboksylową zawsze numerujemy jako pozycję 1 w łańcuchu. To znacznie ułatwia nazywanie tych związków!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Szereg homologiczny i izomeria szkieletowa
Nasycone monokarboksylowe kwasy alifatyczne tworzą szereg homologiczny o wzorze ogólnym CₙH₂ₙ₊₁COOH. Zaczynając od najprostszego kwasu metanowego (mrówkowego) HCOOH, każdy kolejny członek ma o jedną grupę -CH₂- więcej.
Wśród ważnych przedstawicieli warto zapamiętać:
- kwas metanowy (mrówkowy) - HCOOH
- kwas etanowy (octowy) - CH₃COOH
- kwas propanowy (propionowy) - C₂H₅COOH
- kwas butanowy (masłowy) - C₃H₇COOH
- kwas pentanowy (walerianowy) - C₄H₉COOH
W chemii organicznej znajdziesz też ważne kwasy zawierające dodatkowe grupy funkcyjne, takie jak kwas salicylowy, kwas acetylosalicylowy (aspiryna), kwas szczawiowy czy kwas mlekowy.
Izomeria szkieletowa kwasów karboksylowych polega na różnych układach atomów w łańcuchu węglowym. Na przykład kwas pentanowy (C₅H₁₀O₂) ma izomery takie jak kwas 2-metylobutanowy o tym samym wzorze sumarycznym, ale innym ułożeniu atomów.
📝 Ważne: Pamiętaj, że mimo różnej budowy, izomery mają zawsze ten sam wzór sumaryczny. To klucz do zrozumienia izomerii w chemii organicznej!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Rodzaje izomerii kwasów karboksylowych
Kwasy karboksylowe wykazują różne rodzaje izomerii, co znacząco wpływa na ich właściwości. Izomeria położeniowa może dotyczyć położenia wiązania podwójnego w cząsteczce. Na przykład kwas but-2-enowy i kwas but-3-enowy (C₄H₆O₂) różnią się położeniem wiązania podwójnego w łańcuchu.
Izomeria położenia podstawników to kolejny typ - np. kwas 2-chlorobutanowy i kwas 3-chlorobutanowy (C₄H₇ClO₂) różnią się położeniem atomu chloru. W przypadku kwasów dikarboksylowych możemy mieć izomerię położenia grup -COOH, jak w kwasach benzenodikarboksylowych.
Szczególnie interesująca jest izomeria cis-trans, występująca przy wiązaniu podwójnym. Kwas cis-but-2-enowy i kwas trans-but-2-enowy mają te same grupy, ale inaczej rozmieszczone w przestrzeni względem wiązania podwójnego.
Kwasy karboksylowe można otrzymać na kilka sposobów:
- Przez utlenianie węglowodorów
- Przez utlenianie alkoholi pierwszorzędowych (z użyciem KMnO₄)
- Przez utlenianie aldehydów (próby Tollensa lub Trommera)
🧪 Eksperyment: Próba Tollensa (powstawanie lustra srebrowego) jest świetnym sposobem na odróżnienie aldehydów od ketonów - tylko aldehydy dają pozytywny wynik!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie kwasów i ich dysocjacja
Kwasy karboksylowe można otrzymać różnymi metodami. W przypadku kwasu mrówkowego (HCOOH) stosuje się reakcję tlenku węgla z wodorotlenkiem sodu, a następnie reakcję z kwasem siarkowym. Można też przeprowadzić hydrolizę mrówczanu metylu.
Kwas octowy (CH₃COOH) otrzymujemy przez utlenianie aldehydu octowego lub przez fermentację octową alkoholu etylowego. Ta ostatnia metoda jest stosowana w produkcji octu spożywczego.
Dysocjacja elektrolityczna to kluczowa właściwość kwasów karboksylowych. Zachodzi ona dzięki polaryzacji wiązania C-O w grupie karboksylowej, co osłabia wiązanie O-H. W wyniku dysocjacji powstaje jon wodorowy (H⁺) i reszta kwasowa (np. HCOO⁻ lub CH₃COO⁻).
Równania dysocjacji można zapisać:
- HCOOH → HCOO⁻ + H⁺
- CH₃COOH → CH₃COO⁻ + H⁺
💡 Ciekawostka: Kwasy karboksylowe są znacznie słabsze od kwasów nieorganicznych (jak HCl czy H₂SO₄), ale dzięki temu znajdują szersze zastosowanie w produktach spożywczych i kosmetycznych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Asocjacja i reakcje kwasów karboksylowych
Asocjacja to proces łączenia się cząsteczek kwasów karboksylowych w większe zespoły poprzez wiązania wodorowe. Ten proces wpływa na ich właściwości fizyczne - wraz z wydłużeniem łańcucha węglowego zmienia się stan skupienia (z ciekłego na stały), zmniejsza się lotność i rozpuszczalność w wodzie.
Polarność wiązań w grupie karbonylowej i hydroksylowej sprzyja tworzeniu wiązań wodorowych między cząsteczkami kwasu. Pojedyncza cząsteczka może utworzyć nawet 12 wiązań wodorowych!
Kwasy karboksylowe wchodzą w liczne reakcje chemiczne:
- Z metalami aktywnymi
- Z tlenkami metali
- Z wodorotlenkami metali
- Z solami słabszych kwasów
Mogą również ulegać reakcjom fluorowcowania czy addycji wodoru do wiązania podwójnego .
🔍 Wskazówka praktyczna: Reakcje kwasów z wodorotlenkami (zobojętnianie) są podstawą miareczkowania, którym możesz określić stężenie kwasu lub zasady w roztworze.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Moc kwasów karboksylowych
Kwasy karboksylowe należą do słabych elektrolitów, co oznacza, że dysocjują tylko częściowo w roztworze wodnym. Moc kwasu wyrażamy za pomocą stałej dysocjacji Ka lub wartości pKa .
Czynniki wpływające na moc kwasu:
- Długość łańcucha węglowodorowego - im dłuższy łańcuch niepolarny, tym słabszy kwas.
- Liczba grup karboksylowych - im więcej grup -COOH, tym kwas jest mocniejszy.
- Podstawniki elektroakceptorowe (wyciągające elektrony, np. atomy chlorowców, grupa nitrowa) zwiększają moc kwasu.
- Pozycja podstawnika - kwas jest mocniejszy, gdy podstawnik znajduje się bliżej grupy -COOH.
- Elektrujemność podstawnika - im większa, tym kwas mocniejszy.
Natomiast podstawniki elektrodonorowe (dostarczające elektrony, np. grupy alkilowe, grupa hydroksylowa) zmniejszają moc kwasów karboksylowych.
⚠️ Pamiętaj: Moc kwasu może być kluczowa dla przebiegu reakcji! Mocniejszy kwas będzie lepszym katalizatorem w wielu reakcjach i będzie łatwiej oddawał proton w reakcjach z zasadami.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Specyficzne właściwości i reakcje
Podstawniki elektroakceptorowe (EA) zwiększają moc kwasów, gdy:
- Znajdują się bliżej grupy -COOH w cząsteczce
- Jest ich więcej w cząsteczce
- Mają większą elektrujemność
Sole kwasów karboksylowych mają odczyn zasadowy. Podczas hydrolizy soli, np. CH₃COONa, powstaje słaby kwas i mocna zasada: CH₃COO⁻ + H₂O ⇌ CH₃COOH + OH⁻
Kwas metanowy (mrówkowy) wyróżnia się spośród innych kwasów karboksylowych, ponieważ posiada dwie grupy funkcyjne: karboksylową -COOH i aldehydową H-C=O. Ta unikalna budowa nadaje mu właściwości redukujące, których nie mają wyższe kwasy.
Ważną reakcją kwasów karboksylowych jest dekarboksylacja (odłączenie CO₂): R-COOH → R-H + CO₂
Inne kwasy karboksylowe można redukować według schematu: R-COOH → R-CHO → R-CH₂OH (kwas karboksylowy → aldehyd → alkohol)
🧪 Zastosowanie: Dekarboksylacja jest ważna w biochemii - wiele przemian metabolicznych w organizmie opiera się na tej reakcji, np. podczas cyklu Krebsa.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Pierwiaski bloku d chrom mangan miedź żelazo
Chrom mangan miedź żelazo doświadczenia właściwości tych pierwiastków
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Gazy i tlenki. Powietrze i inne gazy.
Notatki do sprawdzianu z chemii dla klasy 7 z działu Powietrze i inne gazy (lub w innych podręcznikach Gazy i tlenki). Obejmuje tematy: Powietrze, gazy szlachetne, tlenek węgla IV, wodór, azot, zanieczyszczenia powietrza.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.