Metale bloku d to fascynująca grupa pierwiastków, które posiadają elektrony... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
4,594
•
Zaktualizowano May 11, 2026
•
Anna Migała
@annamigala.7381
Metale bloku d to fascynująca grupa pierwiastków, które posiadają elektrony... Pokaż więcej









Metale bloku d charakteryzują się posiadaniem elektronów walencyjnych na dwóch różnych powłokach: 4s oraz 3d. To sprawia, że mają ciekawe właściwości chemiczne i zmienne stopnie utlenienia.
Miedź i chrom stanowią wyjątki w tej grupie - mają tylko jeden elektron na podpowłoce 4s, co wpływa na ich odmienne zachowanie chemiczne w porównaniu z innymi metalami tego bloku.
Warto wiedzieć! Właśnie ta specyficzna konfiguracja elektronowa odpowiada za zmienne właściwości chemiczne i fizyczne metali przejściowych, które wykorzystujemy w różnych dziedzinach życia - od biżuterii po przemysł ciężki.

Mangan (Mn) to metal o konfiguracji elektronowej [Ar] 4s² 3d⁵. Występuje głównie w stopniach utlenienia II, IV, VI i VII, co czyni go wszechstronnym pierwiastkiem w reakcjach chemicznych.
Jest dość aktywny chemicznie, ale na powietrzu ulega powolnej pasywacji. Reaguje z fluorowcami, siarką i kwasami nieutleniającymi, np. HCl, wypierając wodór: Mn + 2HCl → MnCl₂ + H₂
Mangan to drugi po żelazie najbardziej rozpowszechniony metal przejściowy. Ma wysoką temperaturę topnienia, srebrzystą barwę z różowym połyskiem oraz jest twardy i kruchy. W przyrodzie występuje głównie jako braunsztyn (MnO₂), z którego otrzymuje się czysty mangan w procesie aluminotermii: 3MnO₂ + 4Al → 2Al₂O₃ + 3Mn
Ciekawostka! Mangan jest niezbędnym mikroelementem dla roślin i zwierząt - bierze udział w procesach enzymatycznych i wspiera prawidłowy rozwój organizmu.

Mangan tworzy szereg tlenków o różnym charakterze chemicznym, zależnym od stopnia utlenienia:
Sole manganu(II), jak MnCl₂, mają charakterystyczną bladoróżową barwę. Manganiany(VI) jak K₂MnO₄ są zielone, a manganiany(VII) jak KMnO₄ mają fioletową barwę.
Wodorotlenek manganu(II) - Mn(OH)₂ - to biały osad, który można otrzymać w reakcji: MnCl₂ + 2KOH → Mn(OH)₂ + 2KCl
Wodorotlenek manganu(II) jest związkiem nietrwałym i na powietrzu utlenia się do braunsztynu: 2Mn(OH)₂ + O₂ → 2MnO(OH)₂
Zapamiętaj! Zmiana barwy w związkach manganu jest doskonałym wskaźnikiem jego stopnia utlenienia - od bladoróżowej (Mn²⁺), przez zieloną (Mn⁶⁺), po fioletową (Mn⁷⁺).
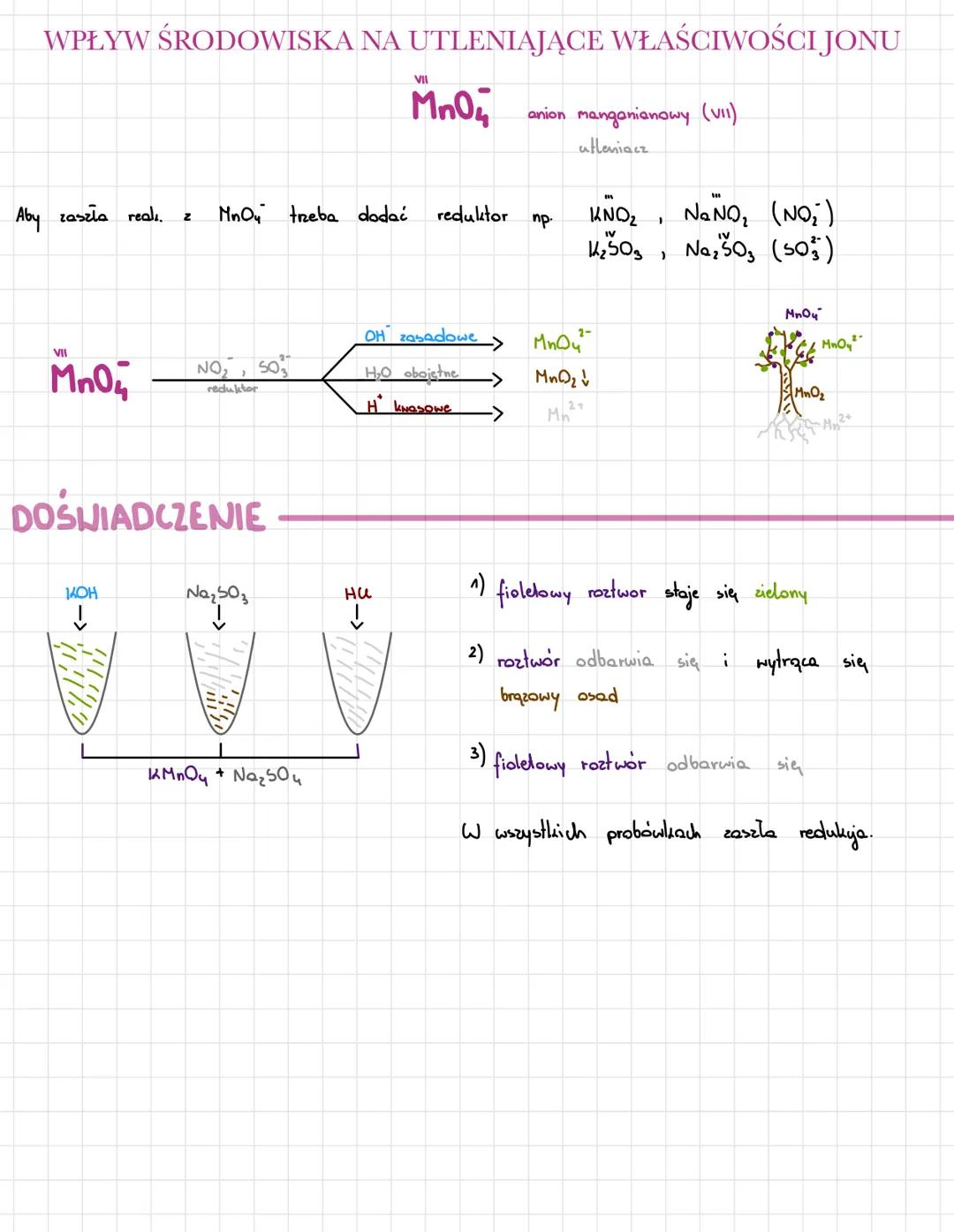
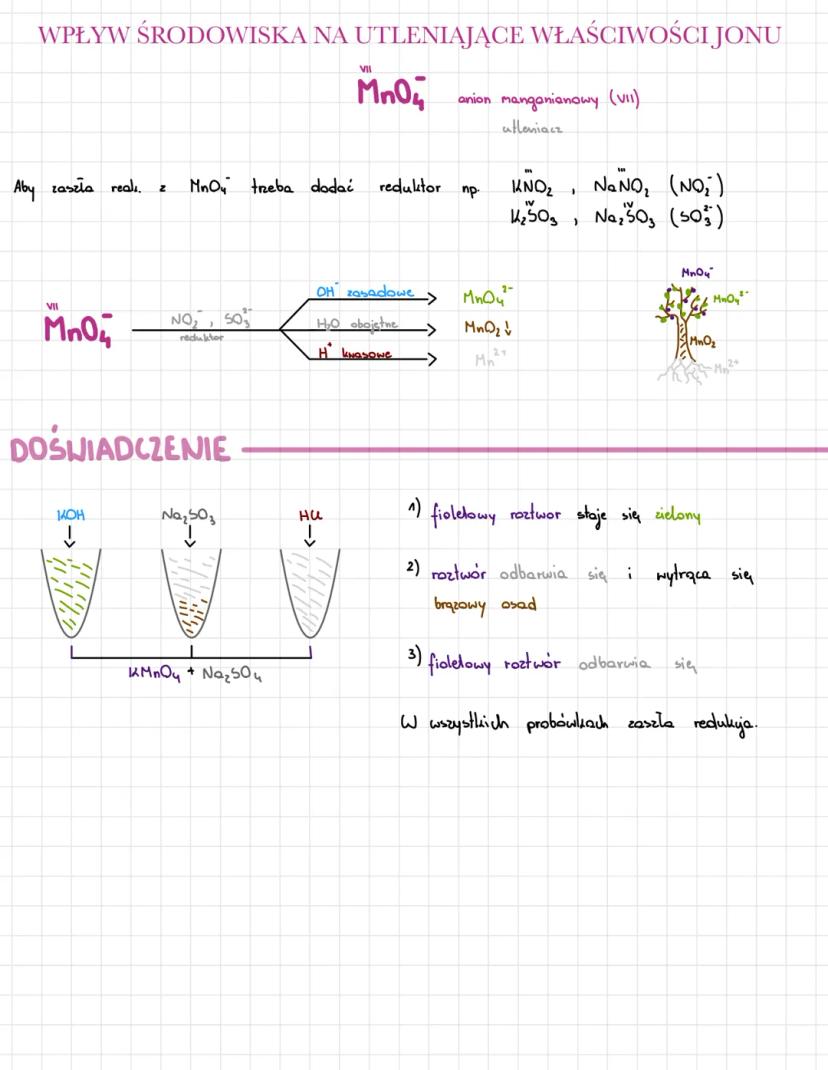
Anion manganianowy(VII) (MnO₄⁻) jest silnym utleniaczem, którego właściwości zależą od środowiska. Aby zaszła reakcja z MnO₄⁻, trzeba dodać reduktor, np. NO₂⁻ lub SO₃²⁻.
W zależności od pH środowiska, MnO₄⁻ redukuje się do różnych form:
W doświadczeniach z KMnO₄ i Na₂SO₃ obserwujemy:
Eksperymentuj! Próbując dodać KMnO₄ do różnych roztworów o odmiennym pH, możesz łatwo zaobserwować te zmiany kolorów i nauczyć się rozpoznawać środowisko reakcji.

Chrom (Cr) ma konfigurację elektronową [Ar] 4s¹ 3d⁵, gdzie najwyższą energię mają elektrony 3d⁵, a najniższą 4s¹. To twardy, srebrzysto-biały metal odporny na korozję.
W związkach chrom występuje najczęściej na II, III i VI stopniu utlenienia. Jego tlenki mają różny charakter chemiczny:
Chrom ulega pasywacji na powietrzu, pokrywając się warstwą tlenku chromu(III). Nie reaguje z wodą, ale z kwasem solnym reaguje, wypierając wodór: Cr + 2HCl → CrCl₂ + H₂
Wodorotlenki chromu również mają różny charakter:
Zastosowanie! Dzięki odporności na korozję, chrom jest szeroko stosowany do galwanicznego pokrywania innych metali, nadając im połysk i odporność na czynniki zewnętrzne - dlatego tak wiele elementów w naszym otoczeniu jest "chromowanych".
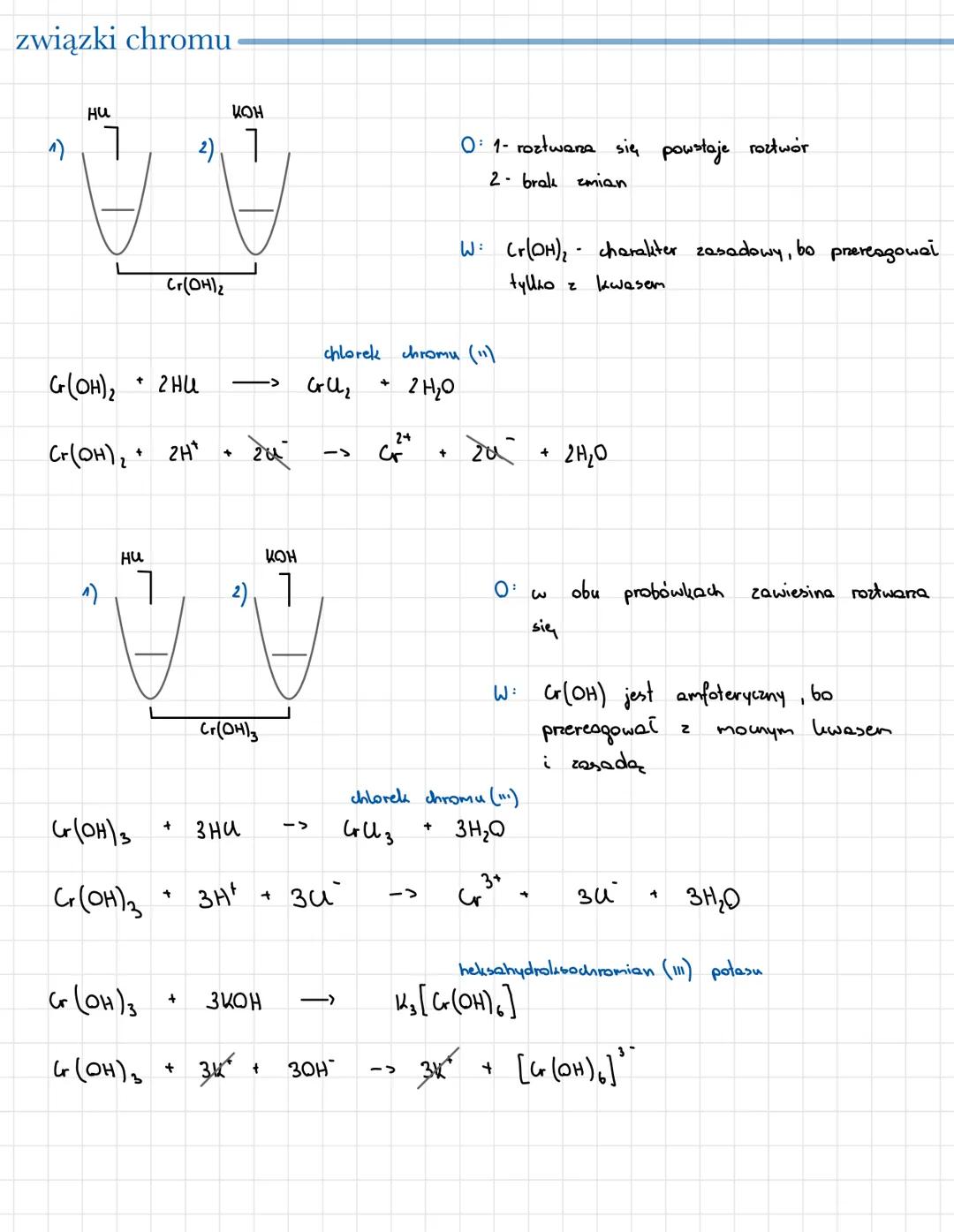
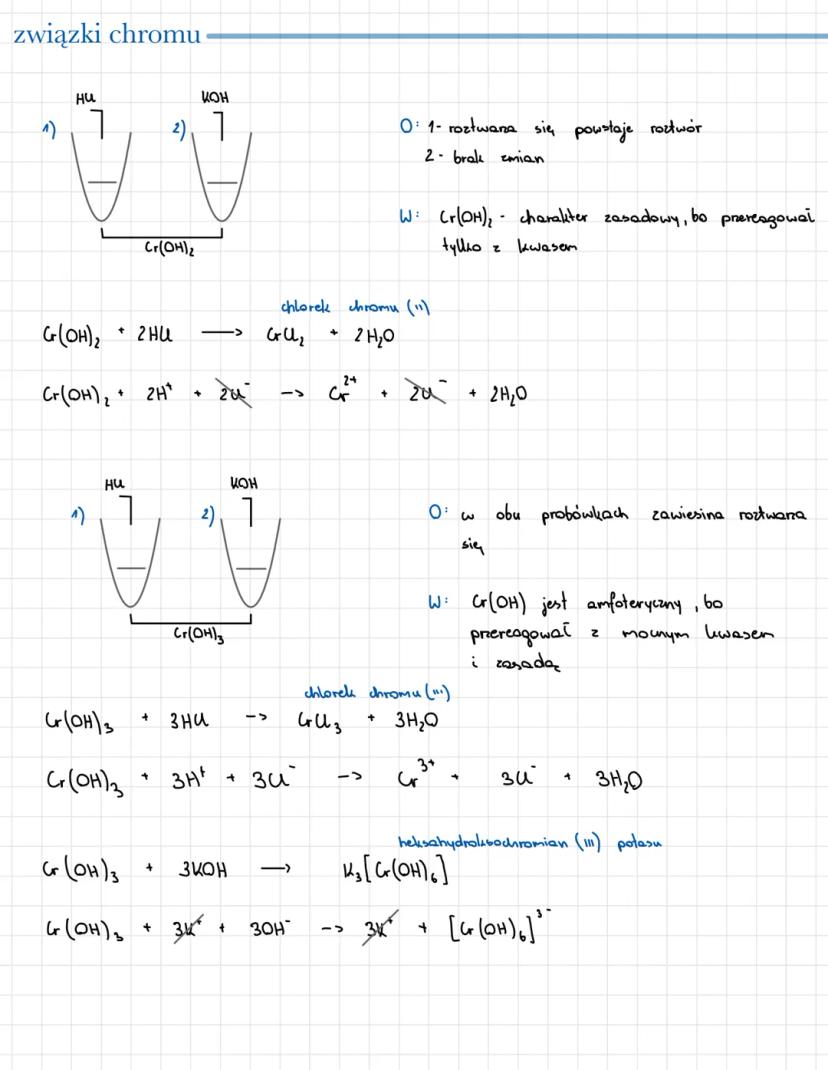
Wodorotlenek chromu(II) (Cr(OH)₂) ma charakter zasadowy - reaguje z kwasami, ale nie z zasadami. W reakcji z kwasem solnym tworzy chlorek chromu(II): Cr(OH)₂ + 2HCl → CrCl₂ + 2H₂O
Wodorotlenek chromu(III) (Cr(OH)₃) wykazuje charakter amfoteryczny - reaguje zarówno z kwasami, jak i zasadami. W reakcji z kwasem solnym tworzy chlorek chromu(III): Cr(OH)₃ + 3HCl → CrCl₃ + 3H₂O
W reakcji z wodorotlenkiem potasu tworzy heksahydroksochromian(III) potasu: Cr(OH)₃ + 3KOH → K₃[Cr(OH)₆]
Te różne zachowania wodorotlenków chromu możesz łatwo zaobserwować w probówkach:
Eksperyment! Dodając HCl i KOH do zawiesin Cr(OH)₂ i Cr(OH)₃, możesz samodzielnie sprawdzić ich charakter chemiczny i zaobserwować zachodzące reakcje.

W solach chromu na II i III stopniu utlenienia (np. CrCl₂, CrCl₃) pierwiastek ten występuje jako jon prosty (Cr²⁺, Cr³⁺). CrCl₂ działa jako reduktor, natomiast CrCl₃ może pełnić rolę zarówno reduktora, jak i utleniacza.
Na VI stopniu utlenienia chrom w solach występuje w postaci jonu złożonego:
Efektownym doświadczeniem jest tzw. "wulkan" z dichromianu(VI) amonu. Po zainicjowaniu reakcji (zapaleniem zapałki) pomarańczowe kryształki zamieniają się w zielony proszek, zwiększając objętość, a reakcji towarzyszą iskry. Zachodzi wtedy rozklad: (NH₄)₂Cr₂O₇ → Cr₂O₃ + N₂ + 4H₂O
Uwaga! "Wulkan chromiany" to spektakularne, ale niebezpieczne doświadczenie - zawsze obserwuj je tylko pod nadzorem nauczyciela, gdyż związki chromu(VI) są toksyczne!

Jony chromianowe (VI) i dichromianowe (VI) wykazują różną trwałość w zależności od pH środowiska:
Dichromian(VI) potasu (K₂Cr₂O₇) o pomarańczowej barwie:
Reakcja: Cr₂O₇²⁻ + 2OH⁻ → 2CrO₄²⁻ + H₂O
Chromian(VI) potasu (K₂CrO₄) o żółtej barwie:
Reakcja: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O
Praktyczna wskazówka! Ta właściwość jonów chromu pozwala wykorzystywać je jako wskaźniki pH - zapamiętaj, że żółty kolor wskazuje na środowisko zasadowe, a pomarańczowy na kwasowe.

Dichromian(VI) potasu (K₂Cr₂O₇) jest silnym utleniaczem, co można zaobserwować w reakcji z etanolem w obecności kwasu siarkowego.
Po dodaniu etanolu do roztworu K₂Cr₂O₇ w środowisku kwasowym (H₂SO₄) obserwujemy zmianę koloru z pomarańczowego na zielony. Jest to reakcja egzotermiczna, w której:
Równanie reakcji: K₂Cr₂O₇ + 3CH₃CH₂OH + 8H₂SO₄ → 2Cr₂(SO₄)₃ + 3CH₃COOH + 2K₂SO₄ + 11H₂O
W procesie tym zachodzą następujące półreakcje:
Wskazówka praktyczna! Ta reakcja jest podstawą chemicznego wykrywania alkoholu w wydychanym powietrzu - zmiana barwy z pomarańczowej na zieloną świadczy o obecności etanolu.

Żelazo to srebrzysty, miękki metal o wysokiej temperaturze topnienia i właściwościach ferromagnetycznych. Jest kowalny i ciężki. Czyste żelazo jest odporne na działanie wody i powietrza, jednak żelazo techniczne łatwo ulega korozji.
W przyrodzie występuje w różnych związkach:
Żelazo tworzy związki głównie na II i III stopniu utlenienia. Trwalsza jest konfiguracja Fe³⁺ (3d⁵), ponieważ jest korzystniejsza energetycznie. Związki żelaza(III) mają charakterystyczną brązową barwę, a związki żelaza(II) - bladozieloną.
Z chlorem żelazo tworzy chlorek żelaza(III): 2Fe + 3Cl₂ → 2FeCl₃
Z kwasami reaguje różnie:
Ciekawostka metalurgiczna! Choć żelazo jest jednym z najpowszechniejszych metali na Ziemi, czyste żelazo prawie nie występuje w przyrodzie - większość wydobywamy jako rudy żelaza i przetwarzamy w wielkich piecach.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Anna Migała
@annamigala.7381
Metale bloku d to fascynująca grupa pierwiastków, które posiadają elektrony walencyjne na dwóch różnych powłokach: 4s i 3d. Wyróżniają się zmiennymi stopniami utlenienia i szeregiem ciekawych właściwości chemicznych. W tym opracowaniu przyjrzymy się szczegółowo manganowi, chromowi i żelazu.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Metale bloku d charakteryzują się posiadaniem elektronów walencyjnych na dwóch różnych powłokach: 4s oraz 3d. To sprawia, że mają ciekawe właściwości chemiczne i zmienne stopnie utlenienia.
Miedź i chrom stanowią wyjątki w tej grupie - mają tylko jeden elektron na podpowłoce 4s, co wpływa na ich odmienne zachowanie chemiczne w porównaniu z innymi metalami tego bloku.
Warto wiedzieć! Właśnie ta specyficzna konfiguracja elektronowa odpowiada za zmienne właściwości chemiczne i fizyczne metali przejściowych, które wykorzystujemy w różnych dziedzinach życia - od biżuterii po przemysł ciężki.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Mangan (Mn) to metal o konfiguracji elektronowej [Ar] 4s² 3d⁵. Występuje głównie w stopniach utlenienia II, IV, VI i VII, co czyni go wszechstronnym pierwiastkiem w reakcjach chemicznych.
Jest dość aktywny chemicznie, ale na powietrzu ulega powolnej pasywacji. Reaguje z fluorowcami, siarką i kwasami nieutleniającymi, np. HCl, wypierając wodór: Mn + 2HCl → MnCl₂ + H₂
Mangan to drugi po żelazie najbardziej rozpowszechniony metal przejściowy. Ma wysoką temperaturę topnienia, srebrzystą barwę z różowym połyskiem oraz jest twardy i kruchy. W przyrodzie występuje głównie jako braunsztyn (MnO₂), z którego otrzymuje się czysty mangan w procesie aluminotermii: 3MnO₂ + 4Al → 2Al₂O₃ + 3Mn
Ciekawostka! Mangan jest niezbędnym mikroelementem dla roślin i zwierząt - bierze udział w procesach enzymatycznych i wspiera prawidłowy rozwój organizmu.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Mangan tworzy szereg tlenków o różnym charakterze chemicznym, zależnym od stopnia utlenienia:
Sole manganu(II), jak MnCl₂, mają charakterystyczną bladoróżową barwę. Manganiany(VI) jak K₂MnO₄ są zielone, a manganiany(VII) jak KMnO₄ mają fioletową barwę.
Wodorotlenek manganu(II) - Mn(OH)₂ - to biały osad, który można otrzymać w reakcji: MnCl₂ + 2KOH → Mn(OH)₂ + 2KCl
Wodorotlenek manganu(II) jest związkiem nietrwałym i na powietrzu utlenia się do braunsztynu: 2Mn(OH)₂ + O₂ → 2MnO(OH)₂
Zapamiętaj! Zmiana barwy w związkach manganu jest doskonałym wskaźnikiem jego stopnia utlenienia - od bladoróżowej (Mn²⁺), przez zieloną (Mn⁶⁺), po fioletową (Mn⁷⁺).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Anion manganianowy(VII) (MnO₄⁻) jest silnym utleniaczem, którego właściwości zależą od środowiska. Aby zaszła reakcja z MnO₄⁻, trzeba dodać reduktor, np. NO₂⁻ lub SO₃²⁻.
W zależności od pH środowiska, MnO₄⁻ redukuje się do różnych form:
W doświadczeniach z KMnO₄ i Na₂SO₃ obserwujemy:
Eksperymentuj! Próbując dodać KMnO₄ do różnych roztworów o odmiennym pH, możesz łatwo zaobserwować te zmiany kolorów i nauczyć się rozpoznawać środowisko reakcji.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Chrom (Cr) ma konfigurację elektronową [Ar] 4s¹ 3d⁵, gdzie najwyższą energię mają elektrony 3d⁵, a najniższą 4s¹. To twardy, srebrzysto-biały metal odporny na korozję.
W związkach chrom występuje najczęściej na II, III i VI stopniu utlenienia. Jego tlenki mają różny charakter chemiczny:
Chrom ulega pasywacji na powietrzu, pokrywając się warstwą tlenku chromu(III). Nie reaguje z wodą, ale z kwasem solnym reaguje, wypierając wodór: Cr + 2HCl → CrCl₂ + H₂
Wodorotlenki chromu również mają różny charakter:
Zastosowanie! Dzięki odporności na korozję, chrom jest szeroko stosowany do galwanicznego pokrywania innych metali, nadając im połysk i odporność na czynniki zewnętrzne - dlatego tak wiele elementów w naszym otoczeniu jest "chromowanych".

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Wodorotlenek chromu(II) (Cr(OH)₂) ma charakter zasadowy - reaguje z kwasami, ale nie z zasadami. W reakcji z kwasem solnym tworzy chlorek chromu(II): Cr(OH)₂ + 2HCl → CrCl₂ + 2H₂O
Wodorotlenek chromu(III) (Cr(OH)₃) wykazuje charakter amfoteryczny - reaguje zarówno z kwasami, jak i zasadami. W reakcji z kwasem solnym tworzy chlorek chromu(III): Cr(OH)₃ + 3HCl → CrCl₃ + 3H₂O
W reakcji z wodorotlenkiem potasu tworzy heksahydroksochromian(III) potasu: Cr(OH)₃ + 3KOH → K₃[Cr(OH)₆]
Te różne zachowania wodorotlenków chromu możesz łatwo zaobserwować w probówkach:
Eksperyment! Dodając HCl i KOH do zawiesin Cr(OH)₂ i Cr(OH)₃, możesz samodzielnie sprawdzić ich charakter chemiczny i zaobserwować zachodzące reakcje.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
W solach chromu na II i III stopniu utlenienia (np. CrCl₂, CrCl₃) pierwiastek ten występuje jako jon prosty (Cr²⁺, Cr³⁺). CrCl₂ działa jako reduktor, natomiast CrCl₃ może pełnić rolę zarówno reduktora, jak i utleniacza.
Na VI stopniu utlenienia chrom w solach występuje w postaci jonu złożonego:
Efektownym doświadczeniem jest tzw. "wulkan" z dichromianu(VI) amonu. Po zainicjowaniu reakcji (zapaleniem zapałki) pomarańczowe kryształki zamieniają się w zielony proszek, zwiększając objętość, a reakcji towarzyszą iskry. Zachodzi wtedy rozklad: (NH₄)₂Cr₂O₇ → Cr₂O₃ + N₂ + 4H₂O
Uwaga! "Wulkan chromiany" to spektakularne, ale niebezpieczne doświadczenie - zawsze obserwuj je tylko pod nadzorem nauczyciela, gdyż związki chromu(VI) są toksyczne!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Jony chromianowe (VI) i dichromianowe (VI) wykazują różną trwałość w zależności od pH środowiska:
Dichromian(VI) potasu (K₂Cr₂O₇) o pomarańczowej barwie:
Reakcja: Cr₂O₇²⁻ + 2OH⁻ → 2CrO₄²⁻ + H₂O
Chromian(VI) potasu (K₂CrO₄) o żółtej barwie:
Reakcja: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O
Praktyczna wskazówka! Ta właściwość jonów chromu pozwala wykorzystywać je jako wskaźniki pH - zapamiętaj, że żółty kolor wskazuje na środowisko zasadowe, a pomarańczowy na kwasowe.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dichromian(VI) potasu (K₂Cr₂O₇) jest silnym utleniaczem, co można zaobserwować w reakcji z etanolem w obecności kwasu siarkowego.
Po dodaniu etanolu do roztworu K₂Cr₂O₇ w środowisku kwasowym (H₂SO₄) obserwujemy zmianę koloru z pomarańczowego na zielony. Jest to reakcja egzotermiczna, w której:
Równanie reakcji: K₂Cr₂O₇ + 3CH₃CH₂OH + 8H₂SO₄ → 2Cr₂(SO₄)₃ + 3CH₃COOH + 2K₂SO₄ + 11H₂O
W procesie tym zachodzą następujące półreakcje:
Wskazówka praktyczna! Ta reakcja jest podstawą chemicznego wykrywania alkoholu w wydychanym powietrzu - zmiana barwy z pomarańczowej na zieloną świadczy o obecności etanolu.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Żelazo to srebrzysty, miękki metal o wysokiej temperaturze topnienia i właściwościach ferromagnetycznych. Jest kowalny i ciężki. Czyste żelazo jest odporne na działanie wody i powietrza, jednak żelazo techniczne łatwo ulega korozji.
W przyrodzie występuje w różnych związkach:
Żelazo tworzy związki głównie na II i III stopniu utlenienia. Trwalsza jest konfiguracja Fe³⁺ (3d⁵), ponieważ jest korzystniejsza energetycznie. Związki żelaza(III) mają charakterystyczną brązową barwę, a związki żelaza(II) - bladozieloną.
Z chlorem żelazo tworzy chlorek żelaza(III): 2Fe + 3Cl₂ → 2FeCl₃
Z kwasami reaguje różnie:
Ciekawostka metalurgiczna! Choć żelazo jest jednym z najpowszechniejszych metali na Ziemi, czyste żelazo prawie nie występuje w przyrodzie - większość wydobywamy jako rudy żelaza i przetwarzamy w wielkich piecach.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
101
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS