Czas na poznanie chemii metali przejściowych! Chrom, mangan, żelazo i... Pokaż więcej
Pierwiastki bloku d: właściwości chromu, manganu, miedzi i żelaza






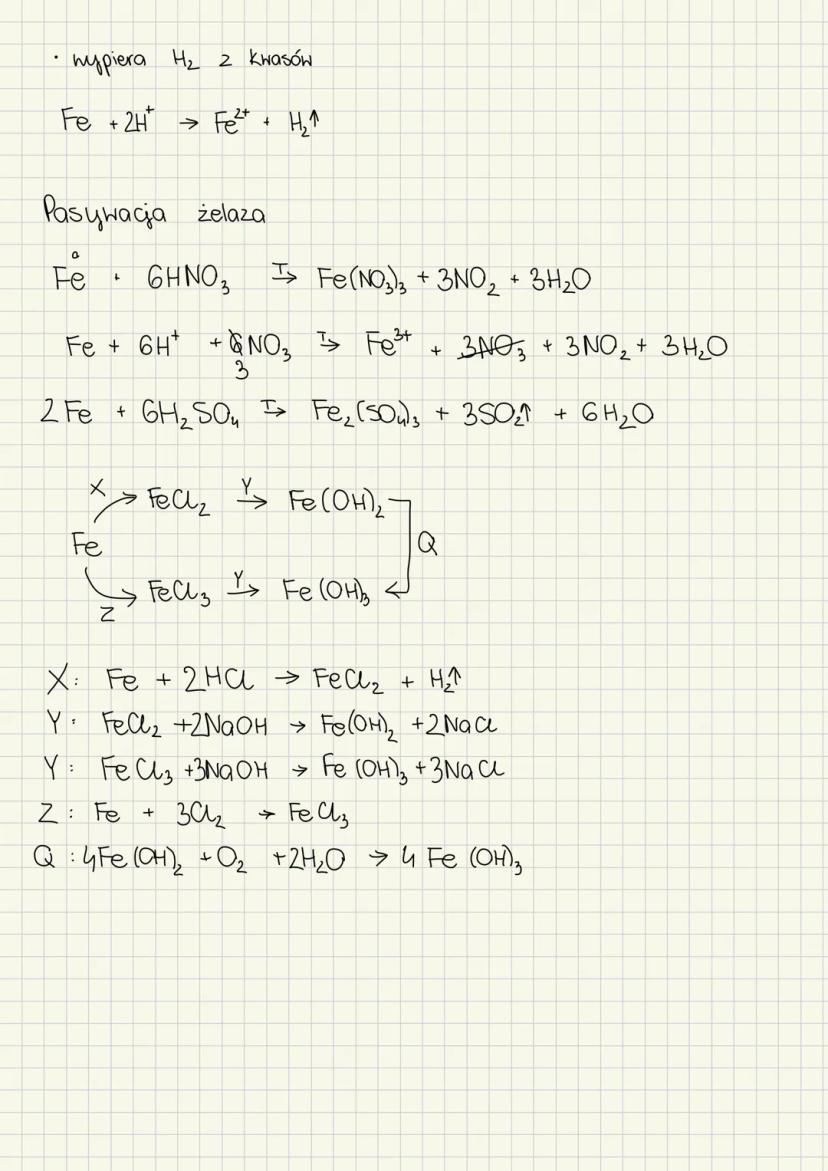


![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_1.webp&w=2048&q=75)
Chrom i jego związki
Chrom ma konfigurację elektronową [Ar] 4s¹ 3d⁵ i na powietrzu ulega pasywacji - czyli pokrywa się ochronną warstwą. To dlatego chromowane przedmioty nie rdzewieją!
Najważniejsze stopnie utlenienia chromu to +2, +3 i +6. W stopniu +2 mamy CrO i Cr(OH)₂ (zasadowe), w stopniu +3 - Cr₂O₃ i Cr(OH)₃ (amfoteryczne), a w stopniu +6 - CrO₃ (kwasowy).
Wodorotlenek chromu(III) możesz otrzymać dodając zasadę do jonów Cr³⁺. Wytrąci się szaroniebieskie osad: Cr³⁺ + 3OH⁻ → Cr(OH)₃↓. Ten związek zachowuje się amfoteryczne - rozpuszcza się zarówno w kwasach jak i zasadach, dając zielone roztwory.
Pamiętaj: Cr(OH)₃ + OH⁻ → [Cr(OH)₄]⁻ (w zasadzie) i Cr(OH)₃ + 3H⁺ → Cr³⁺ + 3H₂O (w kwasie)
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_2.webp&w=2048&q=75)
Reakcje utleniania i redukcji chromu
Utlenianie Cr³⁺ do Cr⁶⁺ robisz wodą utlenioną w środowisku zasadowym. Roztwór zmienia barwę z zielonej na żółtą - powstają jony chromianowe(VI): 2[Cr(OH)₄]⁻ + 3H₂O₂ + 2OH⁻ → 2CrO₄²⁻ + 8H₂O.
W środowisku kwasowym jony chromianowe przekształcają się w dichromianowe: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O. Reakcja jest odwracalna - w zasadzie znów powstają chromianowe.
Redukcja dichromianów w kwasach daje spektakularną zmianę barwy z pomarańczowej na zieloną. Przykład: Cr₂O₇²⁻ + 3SO₃²⁻ + 8H⁺ → 2Cr³⁺ + 4H₂O + 3SO₄²⁻.
Ciekawostka: Metaliczny chrom otrzymujesz w procesie aluminotermii: 2Al + Cr₂O₃ → 2Cr + Al₂O₃
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_3.webp&w=2048&q=75)
Mangan - mistrz wielu stopni utlenienia
Mangan [Ar] 4s² 3d⁵ występuje w stopniach utlenienia od +2 do +7. Im wyższy stopień, tym silniejsze właściwości utleniające - MnO₄⁻ to jeden z najsilniejszych utleniaczy!
W stopniu +2 masz MnO i Mn(OH)₂ (zasadowe), w +4 - MnO₂ (amfoteryczny), a w +7 - KMnO₄ .
Reakcje manganianu(VII) zależą od pH środowiska. W kwasach: 2MnO₄⁻ + 5SO₃²⁻ + 6H⁺ → 2Mn²⁺ + 5SO₄²⁻ + 3H₂O. W obojętnych powstaje MnO₂, a w zasadowych MnO₄²⁻.
Uwaga: Mangan reaguje z kwasami tylko utleniającymi (HNO₃, H₂SO₄ stężony), nie z HCl czy rozcieńczonym H₂SO₄
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_4.webp&w=2048&q=75)
Właściwości związków manganu
Rozkład termiczny KMnO₄ przebiega według: 2KMnO₄ → K₂MnO₄ + MnO₂ + O₂. To źródło tlenu w laboratorium!
Tlenki manganu mają różne właściwości: MnO (zasadowy), MnO₂ (amfoteryczny), Mn₂O₇ (kwasowy). MnO₂ możesz utleniać do manganianów: MnO₂ + KNO₃ + K₂CO₃ → K₂MnO₄ + KNO₂ + CO₂.
Metaliczny mangan rozpuszcza się w kwasach nieutleniających: Mn + 2HCl → MnCl₂ + H₂↑. Z kwasami utleniającymi daje wyższe stopnie utlenienia.
Wodorotlenek Mn(OH)₂ na powietrzu utlenia się do wyższych stopni utlenienia, podobnie jak u żelaza.
Praktyczne zastosowanie: Aluminotermia manganu: 3MnO₂ + 4Al → 3Mn + 2Al₂O₃
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_5.webp&w=2048&q=75)
Schemat przemian manganu
Ta strona pokazuje wzajemne przemiany związków manganu w zależności od warunków reakcji. Możesz przechodzić między różnymi stopniami utlenienia używając odpowiednich utleniaczy i reduktorów.
Kluczowe przemiany: Mn(OH)₂ utlenia się tlenem do MnO₂, który z KNO₃ i K₂CO₃ daje manganiany(VI). Manganiany(VII) możesz redukować do różnych produktów zależnie od pH.
Wskazówka: Naucz się tego schematu - pomoże ci zrozumieć wszystkie reakcje manganu!
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_6.webp&w=2048&q=75)
Żelazo - podstawowe reakcje i związki
Żelazo [Ar] 4s² 3d⁶ wypiera wodór z większości kwasów, ale HNO₃ i stężony H₂SO₄ powodują jego pasywację - pokrycie ochronną warstwą tlenków.
Podstawowa reakcja: Fe + 2HCl → FeCl₂ + H₂↑. Z chlorem: 2Fe + 3Cl₂ → 2FeCl₃. Spalanie w tlenie daje charakterystyczny magnetyt: 3Fe + 2O₂ → Fe₃O₄.
Tlenki żelaza: FeO (zasadowy), Fe₂O₃ (amfoteryczny), Fe₃O₄ (mieszany - FeO·Fe₂O₃, to słynny magnetyt).
Wodorotlenki otrzymujesz dodając NaOH do soli: Fe²⁺ + 2OH⁻ → Fe(OH)₂↓ (zielony osad) i Fe³⁺ + 3OH⁻ → Fe(OH)₃↓ (brązowy osad). Fe(OH)₂ na powietrzu utlenia się do Fe(OH)₃.
Ważne: Fe(OH)₂ początkowo jest zielony, ale szybko brązowieje przez utlenianie tlenem z powietrza
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_7.webp&w=2048&q=75)
Pasywacja żelaza i reakcje z kwasami
Pasywacja żelaza to kluczowe zjawisko. Z kwasami utleniającymi: Fe + 6HNO₃ → Fe(NO₃)₃ + 3NO₂ + 3H₂O oraz 2Fe + 6H₂SO₄ → Fe₂(SO₄)₃ + 3SO₂ + 6H₂O.
Zwykłe reakcje z kwasami nieuleniającymi: Fe + 2HCl → FeCl₂ + H₂↑. Potem możesz otrzymać wodorotlenki: FeCl₂ + 2NaOH → Fe(OH)₂ + 2NaCl.
Utlenianie Fe(OH)₂ na powietrzu: 4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃. To dlatego świeży osad zielony szybko brązowieje.
Spalanie żelaza w chlorze daje od razu Fe³⁺: 2Fe + 3Cl₂ → 2FeCl₃.
Pamiętaj: Żelazo z kwasami nieuleniającymi daje Fe²⁺, a z utleniającymi Fe³⁺
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_8.webp&w=2048&q=75)
Przemiany związków żelaza
Ta strona pokazuje wzajemne przemiany między różnymi związkami żelaza. Możesz przechodzić między Fe²⁺ i Fe³⁺ używając odpowiednich utleniaczy lub reduktorów.
Rozkład termiczny: Fe(OH)₂ → FeO + H₂O i 2Fe(OH)₃ → Fe₂O₃ + 3H₂O. Magnetyt Fe₃O₄ ma właściwości amfoteryczne.
Wszystkie wodorotlenki żelaza są amfoteryczne - rozpuszczają się zarówno w kwasach jak i silnych zasadach.
Wskazówka: Ten schemat pomoże ci zrozumieć, jak różne związki żelaza się przekształcają
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_9.webp&w=2048&q=75)
Miedź - szlachetny metal o ciekawych właściwościach
Miedź [Ar] 4s¹ 3d¹⁰ nie wypiera wodoru z kwasów nieuleniających - to dlatego nie reaguje z HCl. Charakterystyczna reakcja dysproporcjonowania: 2Cu⁺ → Cu + Cu²⁺.
Z kwasami uleniającymi daje spektakularne reakcje. Z HNO₃ stężonym: 3Cu + 8HNO₃ → 3Cu(NO₃)₂ + 2NO₂↑ (brunatny gaz) + 4H₂O. Z rozcieńczonym HNO₃ powstaje NO (bezbarwny, ale brunatnieje na powietrzu).
Tlenki miedzi: Cu₂O i CuO (oba zasadowe). Spalanie: 4Cu + O₂ → 2Cu₂O i 2Cu + O₂ → 2CuO.
Wodorotlenek Cu(OH)₂ otrzymujesz z soli: CuSO₄ + 2NaOH → Cu(OH)₂↓ + Na₂SO₄. Wytrąca się niebieski galaretowaty osad.
Obserwacja: Miedź z kwasami nie daje H₂, tylko tlenki gazowe (NO₂, NO, SO₂)
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_10.webp&w=2048&q=75)
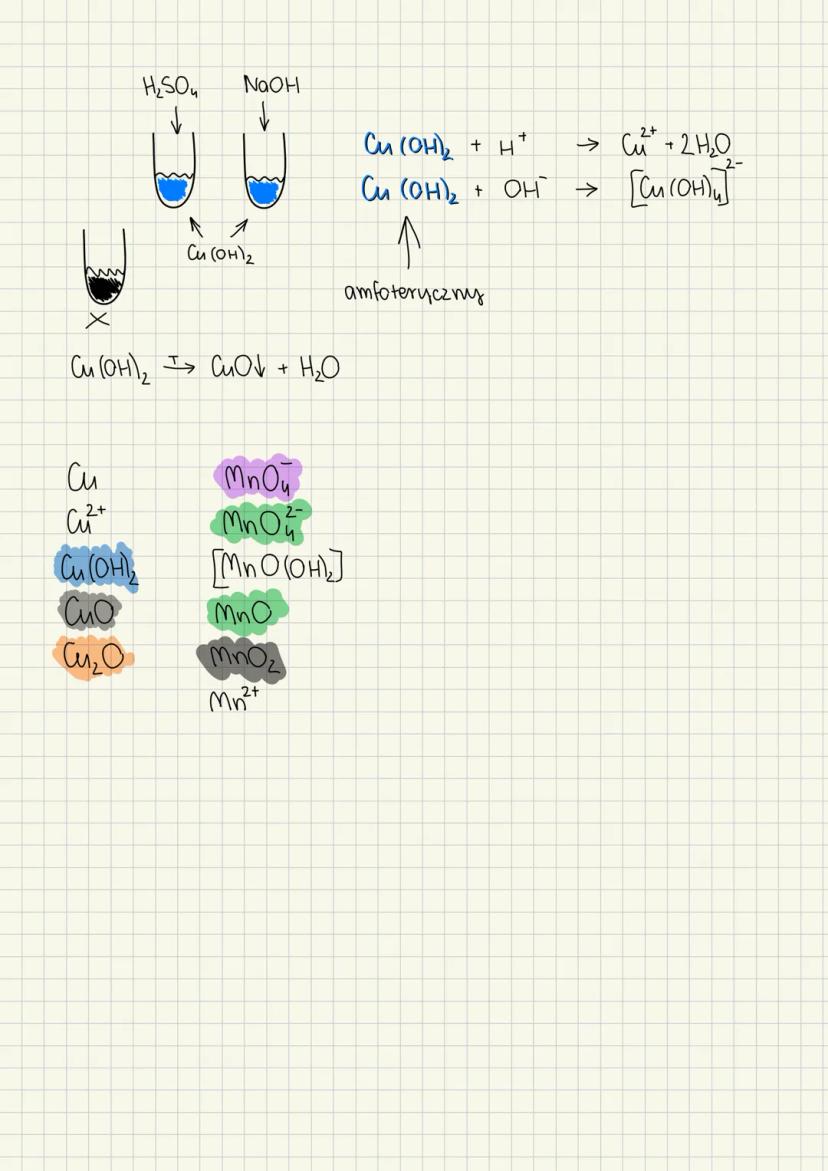
Właściwości amfoteryczne wodorotlenku miedzi
Wodorotlenek Cu(OH)₂ jest amfoteryczny - rozpuszcza się w kwasach i zasadach. W kwasach: Cu(OH)₂ + 2H⁺ → Cu²⁺ + 2H₂O. W silnych zasadach: Cu(OH)₂ + 2OH⁻ → [Cu(OH)₄]²⁻.
Rozkład termiczny: Cu(OH)₂ → CuO + H₂O. Niebieski osad zmienia się w czarny tlenek.
Porównanie z manganem: oba metale tworzą związki w różnych stopniach utlenienia z charakterystycznymi kolorami i właściwościami kwasowo-zasadowymi.
Najważniejsze stopnie utlenienia: Cu⁺ , Cu²⁺ (niebieski/zielony). Sole Cu²⁺ dają charakterystyczne niebieskie lub zielone roztwory.
Kluczowa cecha: Związki Cu²⁺ mają charakterystyczny niebieski kolor - łatwo je rozpoznać!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Gazy i tlenki. Powietrze i inne gazy.
Notatki do sprawdzianu z chemii dla klasy 7 z działu Powietrze i inne gazy (lub w innych podręcznikach Gazy i tlenki). Obejmuje tematy: Powietrze, gazy szlachetne, tlenek węgla IV, wodór, azot, zanieczyszczenia powietrza.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Pierwiastki bloku d: właściwości chromu, manganu, miedzi i żelaza
Czas na poznanie chemii metali przejściowych! Chrom, mangan, żelazo i miedź to elementy, które spotkasz nie tylko na maturze, ale też w codziennym życiu - od nierdzewnej stali po kolorowe związki.
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_1.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Chrom i jego związki
Chrom ma konfigurację elektronową [Ar] 4s¹ 3d⁵ i na powietrzu ulega pasywacji - czyli pokrywa się ochronną warstwą. To dlatego chromowane przedmioty nie rdzewieją!
Najważniejsze stopnie utlenienia chromu to +2, +3 i +6. W stopniu +2 mamy CrO i Cr(OH)₂ (zasadowe), w stopniu +3 - Cr₂O₃ i Cr(OH)₃ (amfoteryczne), a w stopniu +6 - CrO₃ (kwasowy).
Wodorotlenek chromu(III) możesz otrzymać dodając zasadę do jonów Cr³⁺. Wytrąci się szaroniebieskie osad: Cr³⁺ + 3OH⁻ → Cr(OH)₃↓. Ten związek zachowuje się amfoteryczne - rozpuszcza się zarówno w kwasach jak i zasadach, dając zielone roztwory.
Pamiętaj: Cr(OH)₃ + OH⁻ → [Cr(OH)₄]⁻ (w zasadzie) i Cr(OH)₃ + 3H⁺ → Cr³⁺ + 3H₂O (w kwasie)
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_2.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje utleniania i redukcji chromu
Utlenianie Cr³⁺ do Cr⁶⁺ robisz wodą utlenioną w środowisku zasadowym. Roztwór zmienia barwę z zielonej na żółtą - powstają jony chromianowe(VI): 2[Cr(OH)₄]⁻ + 3H₂O₂ + 2OH⁻ → 2CrO₄²⁻ + 8H₂O.
W środowisku kwasowym jony chromianowe przekształcają się w dichromianowe: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O. Reakcja jest odwracalna - w zasadzie znów powstają chromianowe.
Redukcja dichromianów w kwasach daje spektakularną zmianę barwy z pomarańczowej na zieloną. Przykład: Cr₂O₇²⁻ + 3SO₃²⁻ + 8H⁺ → 2Cr³⁺ + 4H₂O + 3SO₄²⁻.
Ciekawostka: Metaliczny chrom otrzymujesz w procesie aluminotermii: 2Al + Cr₂O₃ → 2Cr + Al₂O₃
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_3.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Mangan - mistrz wielu stopni utlenienia
Mangan [Ar] 4s² 3d⁵ występuje w stopniach utlenienia od +2 do +7. Im wyższy stopień, tym silniejsze właściwości utleniające - MnO₄⁻ to jeden z najsilniejszych utleniaczy!
W stopniu +2 masz MnO i Mn(OH)₂ (zasadowe), w +4 - MnO₂ (amfoteryczny), a w +7 - KMnO₄ .
Reakcje manganianu(VII) zależą od pH środowiska. W kwasach: 2MnO₄⁻ + 5SO₃²⁻ + 6H⁺ → 2Mn²⁺ + 5SO₄²⁻ + 3H₂O. W obojętnych powstaje MnO₂, a w zasadowych MnO₄²⁻.
Uwaga: Mangan reaguje z kwasami tylko utleniającymi (HNO₃, H₂SO₄ stężony), nie z HCl czy rozcieńczonym H₂SO₄
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_4.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości związków manganu
Rozkład termiczny KMnO₄ przebiega według: 2KMnO₄ → K₂MnO₄ + MnO₂ + O₂. To źródło tlenu w laboratorium!
Tlenki manganu mają różne właściwości: MnO (zasadowy), MnO₂ (amfoteryczny), Mn₂O₇ (kwasowy). MnO₂ możesz utleniać do manganianów: MnO₂ + KNO₃ + K₂CO₃ → K₂MnO₄ + KNO₂ + CO₂.
Metaliczny mangan rozpuszcza się w kwasach nieutleniających: Mn + 2HCl → MnCl₂ + H₂↑. Z kwasami utleniającymi daje wyższe stopnie utlenienia.
Wodorotlenek Mn(OH)₂ na powietrzu utlenia się do wyższych stopni utlenienia, podobnie jak u żelaza.
Praktyczne zastosowanie: Aluminotermia manganu: 3MnO₂ + 4Al → 3Mn + 2Al₂O₃
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_5.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Schemat przemian manganu
Ta strona pokazuje wzajemne przemiany związków manganu w zależności od warunków reakcji. Możesz przechodzić między różnymi stopniami utlenienia używając odpowiednich utleniaczy i reduktorów.
Kluczowe przemiany: Mn(OH)₂ utlenia się tlenem do MnO₂, który z KNO₃ i K₂CO₃ daje manganiany(VI). Manganiany(VII) możesz redukować do różnych produktów zależnie od pH.
Wskazówka: Naucz się tego schematu - pomoże ci zrozumieć wszystkie reakcje manganu!
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_6.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Żelazo - podstawowe reakcje i związki
Żelazo [Ar] 4s² 3d⁶ wypiera wodór z większości kwasów, ale HNO₃ i stężony H₂SO₄ powodują jego pasywację - pokrycie ochronną warstwą tlenków.
Podstawowa reakcja: Fe + 2HCl → FeCl₂ + H₂↑. Z chlorem: 2Fe + 3Cl₂ → 2FeCl₃. Spalanie w tlenie daje charakterystyczny magnetyt: 3Fe + 2O₂ → Fe₃O₄.
Tlenki żelaza: FeO (zasadowy), Fe₂O₃ (amfoteryczny), Fe₃O₄ (mieszany - FeO·Fe₂O₃, to słynny magnetyt).
Wodorotlenki otrzymujesz dodając NaOH do soli: Fe²⁺ + 2OH⁻ → Fe(OH)₂↓ (zielony osad) i Fe³⁺ + 3OH⁻ → Fe(OH)₃↓ (brązowy osad). Fe(OH)₂ na powietrzu utlenia się do Fe(OH)₃.
Ważne: Fe(OH)₂ początkowo jest zielony, ale szybko brązowieje przez utlenianie tlenem z powietrza
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_7.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Pasywacja żelaza i reakcje z kwasami
Pasywacja żelaza to kluczowe zjawisko. Z kwasami utleniającymi: Fe + 6HNO₃ → Fe(NO₃)₃ + 3NO₂ + 3H₂O oraz 2Fe + 6H₂SO₄ → Fe₂(SO₄)₃ + 3SO₂ + 6H₂O.
Zwykłe reakcje z kwasami nieuleniającymi: Fe + 2HCl → FeCl₂ + H₂↑. Potem możesz otrzymać wodorotlenki: FeCl₂ + 2NaOH → Fe(OH)₂ + 2NaCl.
Utlenianie Fe(OH)₂ na powietrzu: 4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃. To dlatego świeży osad zielony szybko brązowieje.
Spalanie żelaza w chlorze daje od razu Fe³⁺: 2Fe + 3Cl₂ → 2FeCl₃.
Pamiętaj: Żelazo z kwasami nieuleniającymi daje Fe²⁺, a z utleniającymi Fe³⁺
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_8.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Przemiany związków żelaza
Ta strona pokazuje wzajemne przemiany między różnymi związkami żelaza. Możesz przechodzić między Fe²⁺ i Fe³⁺ używając odpowiednich utleniaczy lub reduktorów.
Rozkład termiczny: Fe(OH)₂ → FeO + H₂O i 2Fe(OH)₃ → Fe₂O₃ + 3H₂O. Magnetyt Fe₃O₄ ma właściwości amfoteryczne.
Wszystkie wodorotlenki żelaza są amfoteryczne - rozpuszczają się zarówno w kwasach jak i silnych zasadach.
Wskazówka: Ten schemat pomoże ci zrozumieć, jak różne związki żelaza się przekształcają
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_9.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Miedź - szlachetny metal o ciekawych właściwościach
Miedź [Ar] 4s¹ 3d¹⁰ nie wypiera wodoru z kwasów nieuleniających - to dlatego nie reaguje z HCl. Charakterystyczna reakcja dysproporcjonowania: 2Cu⁺ → Cu + Cu²⁺.
Z kwasami uleniającymi daje spektakularne reakcje. Z HNO₃ stężonym: 3Cu + 8HNO₃ → 3Cu(NO₃)₂ + 2NO₂↑ (brunatny gaz) + 4H₂O. Z rozcieńczonym HNO₃ powstaje NO (bezbarwny, ale brunatnieje na powietrzu).
Tlenki miedzi: Cu₂O i CuO (oba zasadowe). Spalanie: 4Cu + O₂ → 2Cu₂O i 2Cu + O₂ → 2CuO.
Wodorotlenek Cu(OH)₂ otrzymujesz z soli: CuSO₄ + 2NaOH → Cu(OH)₂↓ + Na₂SO₄. Wytrąca się niebieski galaretowaty osad.
Obserwacja: Miedź z kwasami nie daje H₂, tylko tlenki gazowe (NO₂, NO, SO₂)
![# Cr
Cr [Ar] 4s¹ 3d⁵
- na powietnu ulega pasywacji
Henki i wodorotlenki chromu
CrO
Cr(OH)₂
H+
Cr²+
fon
chomu (11)
rasadony
Cr₂O₃](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F01967da2-0e5c-7e4b-a279-c829b5ac5e9f_image_page_10.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości amfoteryczne wodorotlenku miedzi
Wodorotlenek Cu(OH)₂ jest amfoteryczny - rozpuszcza się w kwasach i zasadach. W kwasach: Cu(OH)₂ + 2H⁺ → Cu²⁺ + 2H₂O. W silnych zasadach: Cu(OH)₂ + 2OH⁻ → [Cu(OH)₄]²⁻.
Rozkład termiczny: Cu(OH)₂ → CuO + H₂O. Niebieski osad zmienia się w czarny tlenek.
Porównanie z manganem: oba metale tworzą związki w różnych stopniach utlenienia z charakterystycznymi kolorami i właściwościami kwasowo-zasadowymi.
Najważniejsze stopnie utlenienia: Cu⁺ , Cu²⁺ (niebieski/zielony). Sole Cu²⁺ dają charakterystyczne niebieskie lub zielone roztwory.
Kluczowa cecha: Związki Cu²⁺ mają charakterystyczny niebieski kolor - łatwo je rozpoznać!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: właściwości materii
9alkohole i fenole
podstawa
Hydroksykwasy
Prezentacja na temat hydroksykwasów
Węglowodory aromatyczne
Wszystko co najważniejsze o węglowodorach aromatycznych
Benzen
Benzen - charakterystyka, reakcje, zastosowanie
Stężenie procentowe i molowe
Notata
Kwasy karboksylowe rozszerzenie
Kwasy karboksylowe z zakresy rozszerzonego na podstawie podręcznika nowej ery
Benzen - Węglowodory Aromatyczne
Notatki chemia rozszerzona: benzen, metylobenzen i izomeria
Aldehydy, ketony, kwasy karboksylowe, estry
Notatka z chemii nowa era. 3 klasa poziom podstawowy
Gazy i tlenki. Powietrze i inne gazy.
Notatki do sprawdzianu z chemii dla klasy 7 z działu Powietrze i inne gazy (lub w innych podręcznikach Gazy i tlenki). Obejmuje tematy: Powietrze, gazy szlachetne, tlenek węgla IV, wodór, azot, zanieczyszczenia powietrza.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.