Metale przejściowe takie jak chrom, miedź, żelazo i cynk odgrywają... Pokaż więcej
Pierwiastki Bloku D: Przegląd i Charakterystyka


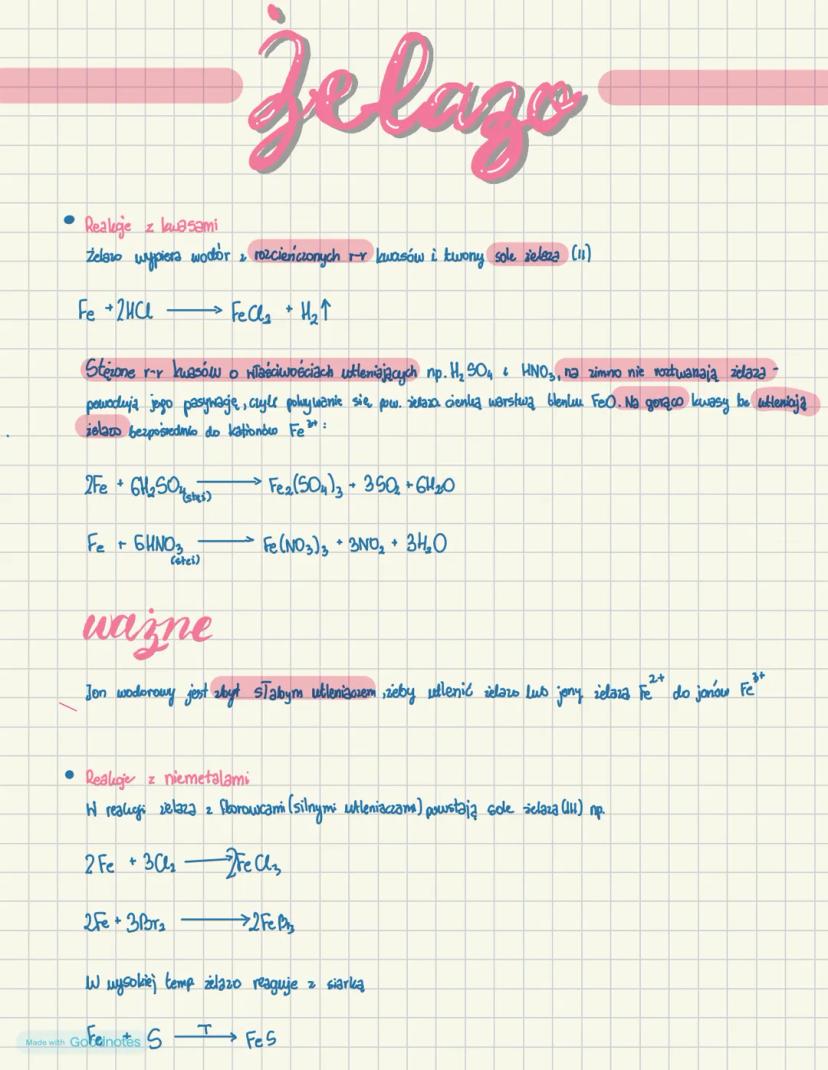






Właściwości i reakcje chromu
Chrom to metal, który w powietrzu ulega pasywacji - pokrywa się warstwą tlenku chromu(III), co chroni go przed dalszym utlenianiem i korozją:
4Cr + 3O₂ → 2Cr₂O₃
W reakcji z kwasem solnym chrom zachowuje się różnie w zależności od warunków. W warunkach beztlenowych powstaje chlorek chromu(II), a w warunkach tlenowych - chlorek chromu(III):
- Beztlenowo: Cr + 2HCl → CrCl₂ + H₂↑
- Tlenowo: Cr + 6HCl + O₂ → 2CrCl₃ + H₂↑
Warto zapamiętać! Bezwodny chlorek chromu(II) jest bezbarwny, ale po uwodnieniu przybiera charakterystyczną niebieską barwę.
Chrom reaguje również z innymi rozcieńczonymi kwasami, jak np. kwas siarkowy(VI), tworząc odpowiednie sole i uwalniając wodór.
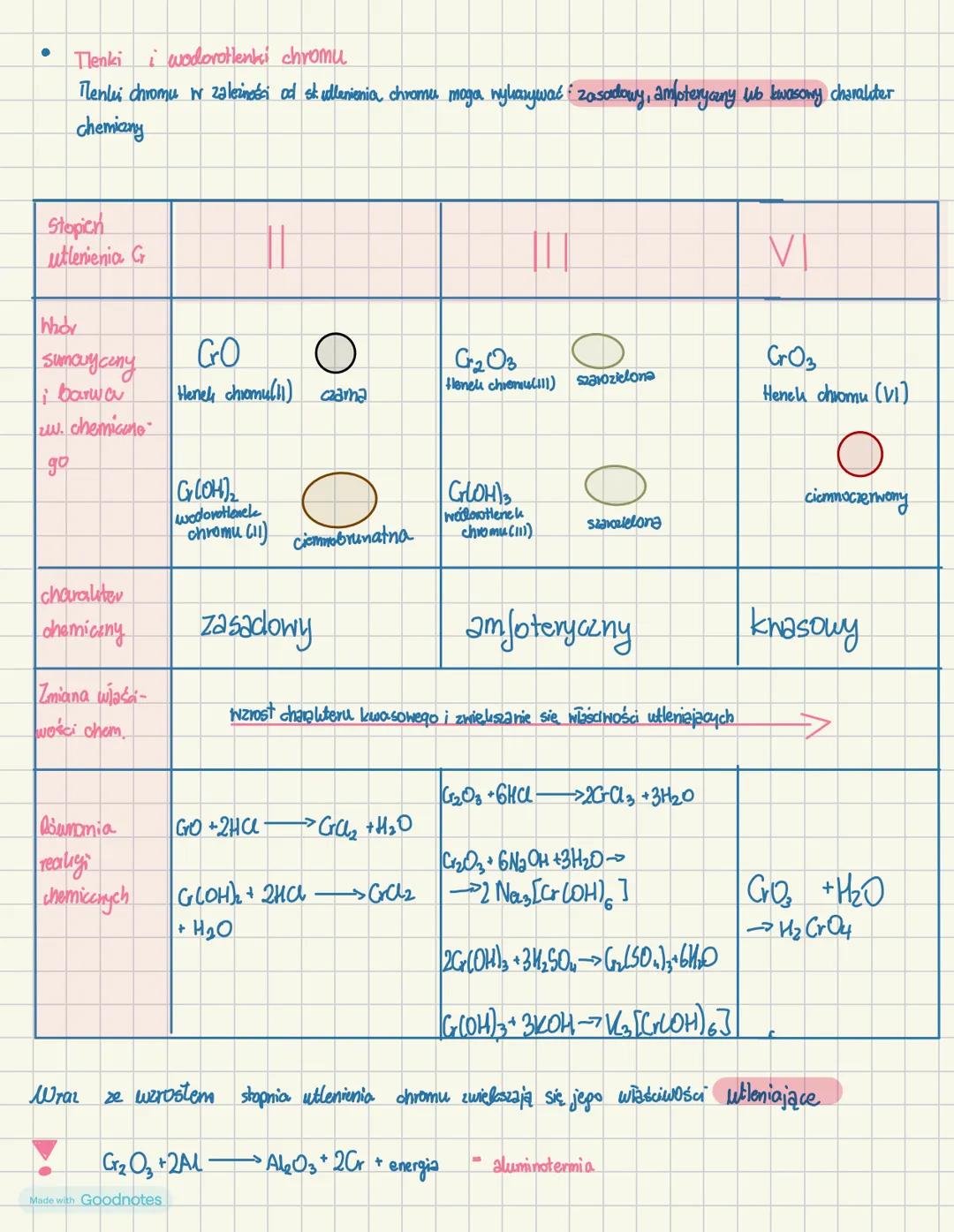
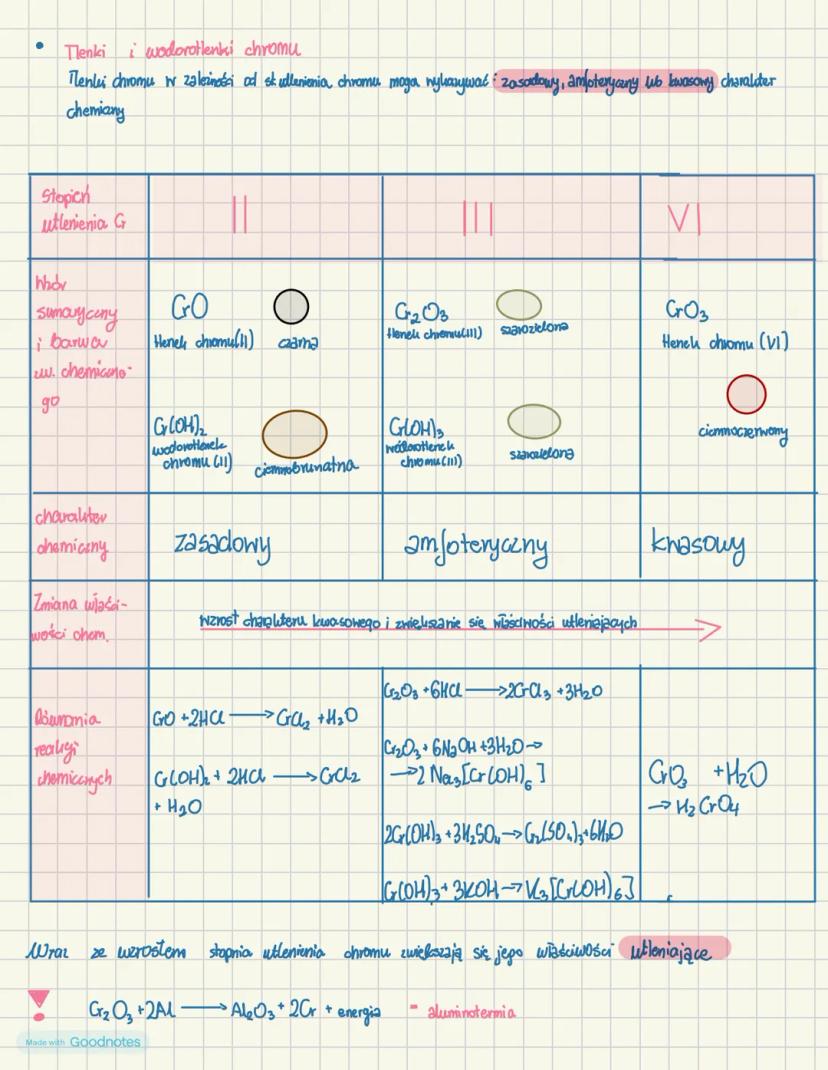
Tlenki i wodorotlenki chromu
Charakter chemiczny związków chromu zmienia się wraz ze wzrostem stopnia utlenienia:
| Stopień utlenienia | Tlenek | Wodorotlenek | Charakter chemiczny |
|---|---|---|---|
| II | CrO (ciemnoczerwony) | Cr(OH)₂ | zasadowy |
| III | Cr₂O₃ (zielony) | Cr(OH)₃ | amfoteryczny |
| VI | CrO₃ | - | kwasowy |
Wraz ze wzrostem stopnia utlenienia chromu zwiększa się charakter kwasowy jego związków oraz ich właściwości utleniające. Związki chromu reagują zarówno z kwasami, jak i zasadami, zgodnie z ich charakterem chemicznym.
Tlenek chromu(III) może być zredukowany w procesie aluminotermii: Cr₂O₃ + 2Al → Al₂O₃ + 2Cr + energia
Ciekawostka: Aluminotermia to reakcja silnie egzotermiczna, która wykorzystywana jest w metalurgii do otrzymywania metali z ich tlenków.
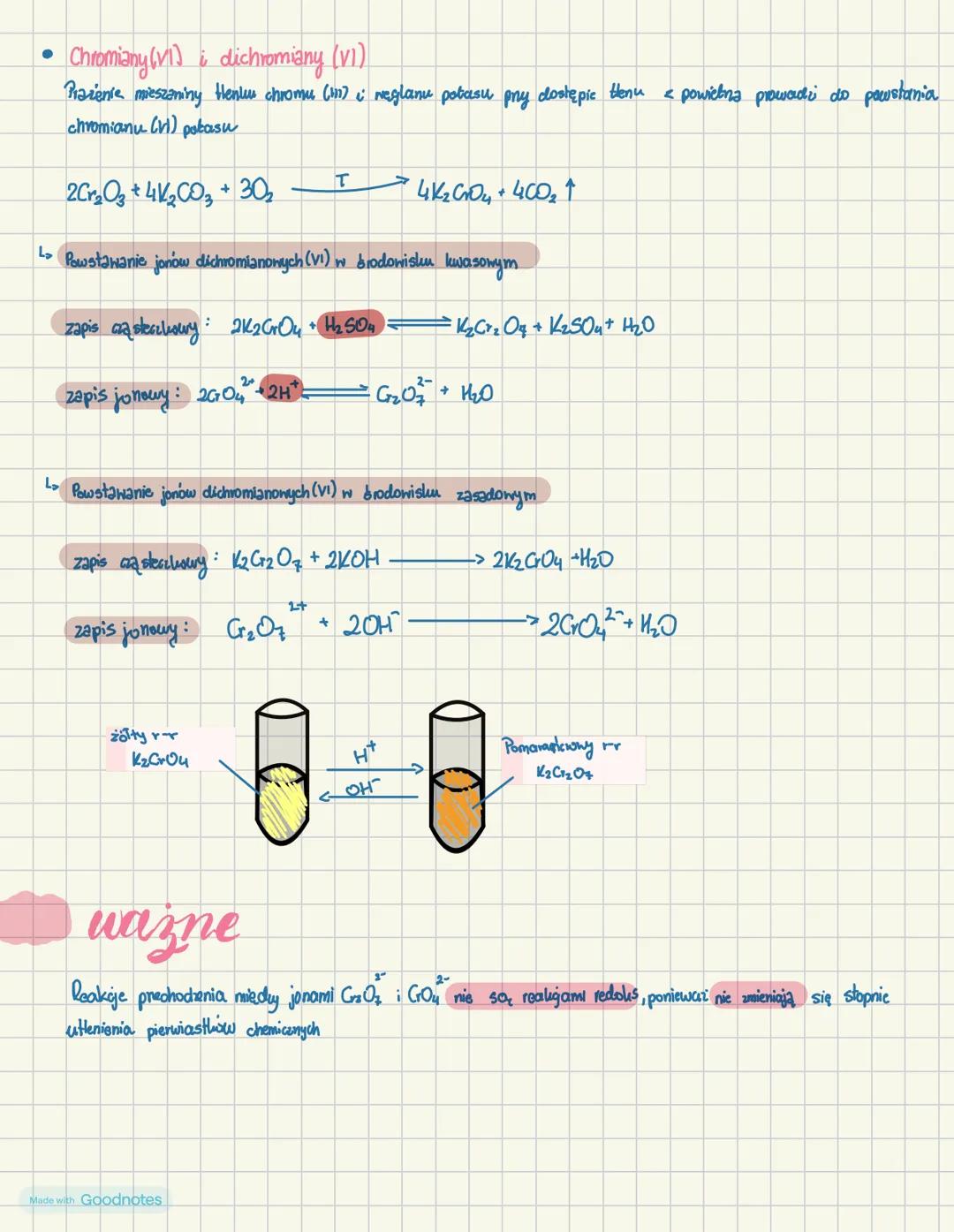
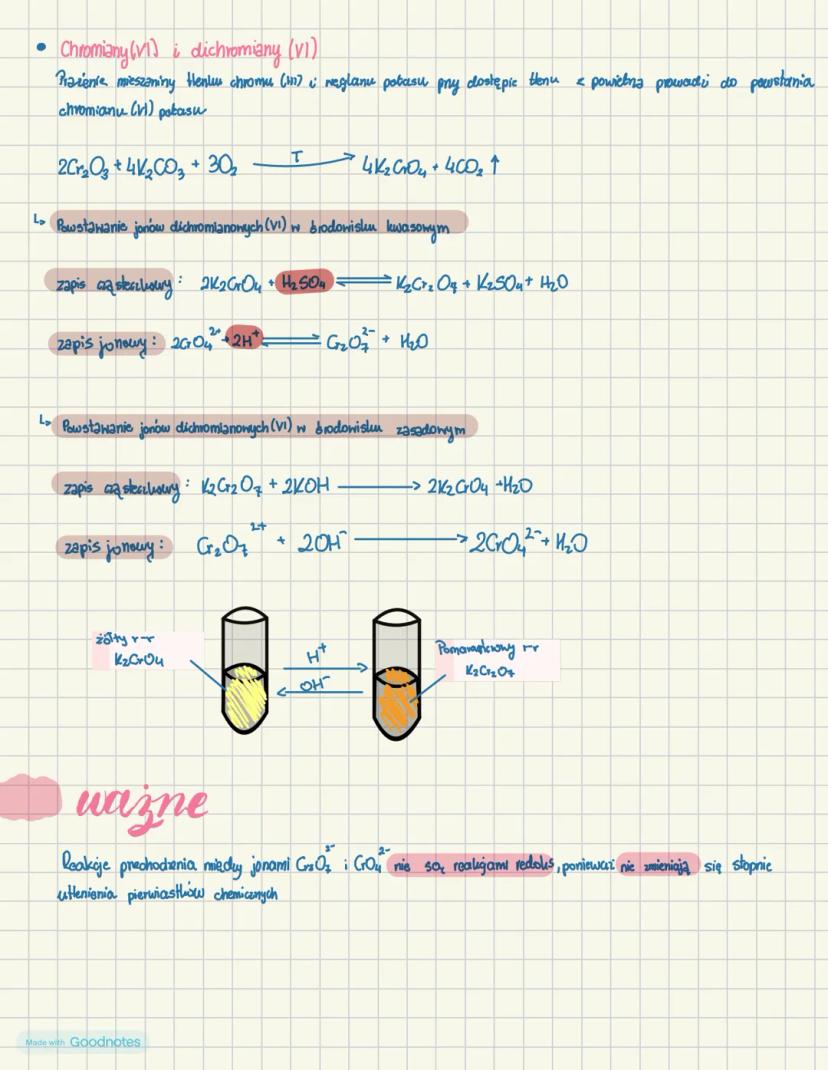
Chromiany i dichromiany
Jony chromianowe i dichromianowe to ważne formy występowania chromu na VI stopniu utlenienia. Chromiany można otrzymać przez prażenie tlenku chromu(III) z wodorotlenkiem potasu w obecności tlenu:
2Cr₂O₃ + 4K₂CO₃ + 3O₂ → 4K₂CrO₄ + 4CO₂↑
Te związki mogą przechodzić między sobą w zależności od pH środowiska:
-
W środowisku kwasowym chromiany przekształcają się w dichromiany: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O
-
W środowisku zasadowym dichromiany przekształcają się w chromiany: Cr₂O₇²⁻ + 2OH⁻ → 2CrO₄²⁻ + H₂O
Zapamiętaj! Chromiany mają żółtą barwę, a dichromiany pomarańczową. Te przemiany nie są reakcjami redoks, ponieważ stopień utlenienia chromu nie zmienia się .

Właściwości redukująco-utleniające związków chromu
Związki chromu wykazują różne właściwości redoks w zależności od stopnia utlenienia:
- Chrom(II) działa jako reduktor
- Chrom(VI) działa jako utleniacz
- Chrom(III) może pełnić obie funkcje, w zależności od warunków
Dichromiany są szczególnie silnymi utleniaczami w środowisku kwaśnym, redukując się do jonów Cr³⁺ o ciemnogranatowej lub ciemnozielonej barwie. Typowym przykładem jest utlenianie jonów żelaza(II):
Cr₂O₇²⁻ + 6Fe²⁺ + 14H⁺ → 2Cr³⁺ + 6Fe³⁺ + 7H₂O
W równaniu tym zachodzą dwa półprocesy:
- Redukcja: Cr₂O₇²⁻ + 14H⁺ + 6e⁻ → 2Cr³⁺ + 7H₂O
- Utlenianie: 6Fe²⁺ → 6Fe³⁺ + 6e⁻
Na sprawdzianie! Dichromiany mogą utleniać również związki nieorganiczne, jak np. jony siarczanowe(IV) do siarczanowych(VI), co jest ważną reakcją w analizie chemicznej.
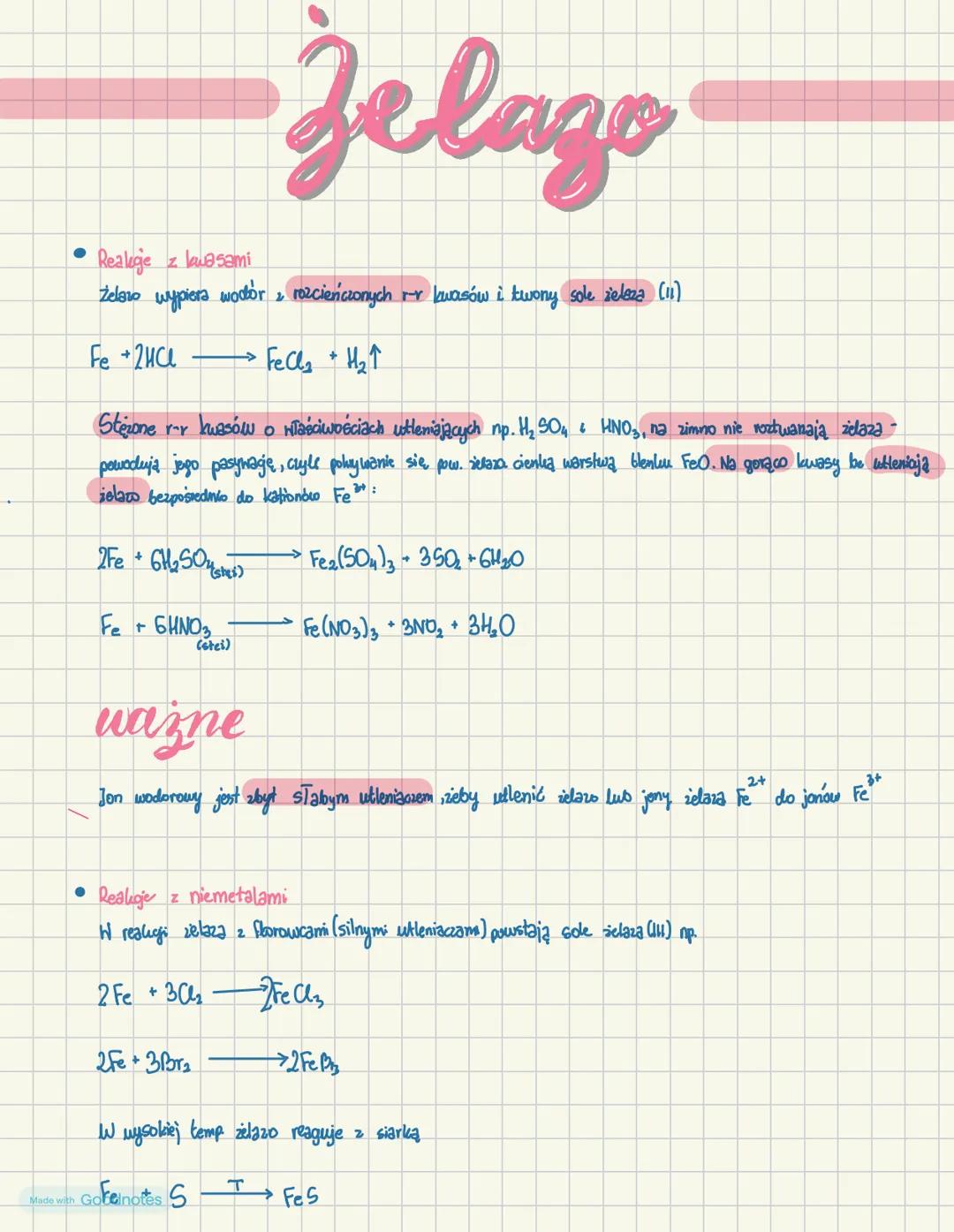
Żelazo - reakcje z kwasami i niemetalami
Żelazo wypiera wodór z rozcieńczonych kwasów, tworząc sole żelaza(II):
Fe + 2HCl → FeCl₂ + H₂↑
Z kolei stężone kwasy utleniające (H₂SO₄, HNO₃) powodują na zimno pasywację żelaza - pokrywanie powierzchni metalu warstwą tlenku FeO. Na gorąco te same kwasy utleniają żelazo do jonów Fe³⁺:
2Fe + 6H₂SO₄ → Fe₂(SO₄)₃ + 3SO₂ + 6H₂O
Żelazo reaguje z silnymi utleniaczami, jak fluorowce, tworząc sole żelaza(III):
2Fe + 3Cl₂ → 2FeCl₃
W wysokiej temperaturze żelazo reaguje również z siarką:
Fe + S → FeS
Ważne: Jon wodorowy jest zbyt słabym utleniaczem, aby utlenić żelazo lub jony Fe²⁺ do jonów Fe³⁺ - dlatego w reakcji z kwasami nieutleniającymi powstają sole żelaza(II).

Żelazo - reakcje z tlenem i wodą
Rozdrobnione żelazo spala się w tlenie, tworząc magnetyt (Fe₃O₄) - tlenek o mieszanym charakterze żelaza(II,III):
3Fe + 2O₂ → Fe₃O₄
W podwyższonych temperaturach żelazo reaguje również z parą wodną:
3Fe + 4H₂O → Fe₃O₄ + 4H₂↑
Wodorotlenki żelaza są słabo rozpuszczalne w wodzie i otrzymuje się je w reakcjach strącania:
- Fe²⁺ + 2OH⁻ → Fe(OH)₂↓
- Fe³⁺ + 3OH⁻ → Fe(OH)₃↓ (brunatny osad)
Świeżo strącony wodorotlenek żelaza(II) ulega utlenieniu tlenem rozpuszczonym w wodzie:
4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃
Na laboratorium: Reakcja utleniania Fe(OH)₂ do Fe(OH)₃ zachodzi szybciej w obecności nadtlenku wodoru, co można zaobserwować jako zmianę barwy osadu z białozielonej na brunatną.

Miedź - reakcje z kwasami i niemetalami
Miedź jest mniej aktywna chemicznie niż wodór, więc nie wypiera go z kwasów nieutleniających. Rozpuszcza się jednak w kwasach utleniających:
Cu + 2H₂SO₄(stęż.) → CuSO₄ + SO₂ + 2H₂O Cu + 4HNO₃ → Cu(NO₃)₂ + 2NO₂ + 2H₂O
Miedź reaguje z fluorowcami jako silnymi utleniaczami, tworząc sole miedzi(II):
Cu + Cl₂ → CuCl₂
W reakcji z siarką zachowanie miedzi zależy od warunków:
- z parami siarki powstaje Cu₂S (siarczek miedzi(I))
- z ciekłą siarką w temperaturze powyżej 346,85°C powstaje CuS (siarczek miedzi(II))
Miedź reaguje z tlenem, pokrywając się warstwą tlenku miedzi(I) o ceglastoczerwonej barwie:
4Cu + O₂ → 2Cu₂O
Podobnie jak miedź! Srebro również reaguje tylko z kwasami utleniającymi, co wynika z jego pozycji w szeregu aktywności metali.

Miedź - tlenki i wodorotlenek
W podwyższonej temperaturze miedź reaguje z tlenem, tworząc czarny tlenek miedzi(II):
2Cu + O₂ → 2CuO
Tlenek miedzi(II) jest utleniaczem, który może utleniać alkohole do aldehydów:
CH₃CH₂OH + CuO → CH₃CHO + Cu + H₂O
Pojawienie się ceglastoczerwonego osadu tlenku miedzi(I) jest pozytywnym wynikiem próby Trommera, służącej do wykrywania właściwości redukujących aldehydów i cukrów:
2Cu(OH)₂ + CH₃CHO + OH⁻ → Cu₂O + CH₃COO⁻ + 3H₂O
Wodorotlenek miedzi(II) otrzymuje się w reakcji strącania:
Cu²⁺ + 2OH⁻ → Cu(OH)₂↓
Jest on nietrwały i podczas ogrzewania rozkłada się:
Cu(OH)₂ → CuO + H₂O
Ciekawostka laboratoryjna: Próba Trommera jest jedną z podstawowych metod identyfikacji aldehydów i cukrów redukujących w analizie organicznej.

Miedź - reakcje wodorotlenku
Wodorotlenek miedzi(II) w reakcji z kwasami tworzy sole miedzi(II):
Cu(OH)₂ + H₂SO₄ → CuSO₄ + 2H₂O
Świeżo strącony wodorotlenek miedzi(II) rozpuszcza się w stężonych i mocnych zasadach, tworząc granatowe tetrahydroksokompleksy:
Cu(OH)₂ + 2OH⁻ → [Cu(OH)₄]²⁻
Wodorotlenek miedzi reaguje również z amoniakiem, tworząc intensywnie niebieskie kompleksy aminowe:
Cu(OH)₂ + 4NH₃ → [Cu(NH₃)₄]²⁺ + 2OH⁻
Zjawisko z codziennego życia: Patyna - jasnozielona warstwa [Cu(OH)₂CO₃] pokrywająca powierzchnię wyrobów z miedzi i jej stopów - chroni głębsze warstwy metalu przed korozją. Możesz ją zobaczyć na starych miedzianych dachach i pomnikach.

Cynk - metal o właściwościach amfoterycznych
Cynk jest metalem o właściwościach amfoterycznych, co oznacza, że reaguje zarówno z kwasami, jak i z zasadami.
W reakcji z kwasami nieutleniającymi cynk rozpuszcza się, tworząc sole cynku i uwalniając wodór:
Zn + 2HCl → ZnCl₂ + H₂↑
Cynk rozpuszcza się również w gorących roztworach mocnych zasad, tworząc tetrahydroksocynkany:
Zn + 2OH⁻ + 2H₂O → [Zn(OH)₄]²⁻ + H₂↑
Na powietrzu cynk pokrywa się cienką warstwą tlenku cynku, co powoduje, że jego powierzchnia traci połysk:
2Zn + O₂ → 2ZnO
Wodorotlenek cynku można otrzymać w reakcji strącania:
Zn²⁺ + 2OH⁻ → Zn(OH)₂↓
Kluczowa właściwość: Wodorotlenek cynku jest trudno rozpuszczalny w wodzie i wykazuje charakter amfoteryczny - reaguje zarówno z kwasami, jak i z zasadami, tworząc rozpuszczalne kompleksy.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Reakcje redoks
9Ogniwa Galwaniczne i Redoks
Zrozumienie ogniw galwanicznych, reakcji redoks oraz stopni utlenienia pierwiastków. Dowiedz się o korozji metali, metodach ochrony oraz zastosowaniach ogniw Daniella. Idealne dla uczniów chemii i studentów przygotowujących się do egzaminów.
Reguły Stopni Utlenienia
Zrozumienie stopni utlenienia pierwiastków chemicznych oraz ich roli w reakcjach redoks. Notatka obejmuje definicje, kluczowe zasady ustalania stopni utlenienia, przykłady oraz wyjaśnienia dotyczące utleniaczy i reduktorów. Idealna dla uczniów chemii.
Właściwości Metali D-Block
Zgłębiaj właściwości i reakcje metali bloku D, takich jak mangan, chrom, żelazo, miedź i cynk. Dowiedz się o ich związkach, amfoterycznych tlenkach oraz doświadczeniach laboratoryjnych. Idealne dla studentów chemii, którzy chcą zrozumieć chemiczne zachowanie metali i ich zastosowania.
Reakcje Pierwiastków Bloku D
Odkryj szczegółowe reakcje chemiczne i właściwości pierwiastków bloku d, w tym mangan, chrom i miedź. Zawiera informacje o stanach utlenienia, reakcjach redoks oraz kolorach związków chemicznych. Idealne dla uczniów przygotowujących się do egzaminów z chemii. Typ: Podsumowanie.
Chemia Bloku D: Metale
Zgłębiaj charakterystykę metali bloku D, w tym srebra, cynku, żelaza i manganu. Dowiedz się o reakcjach chemicznych, stanach utlenienia oraz właściwościach amfoterycznych. Idealne materiały do nauki dla studentów chemii.
Elektrochemia: Zasady i Reakcje
Kompleksowe notatki z elektrochemii obejmujące kluczowe zagadnienia, takie jak reakcje redoks, prawo Faradaya, procesy elektrolizy oraz właściwości elektrolitów. Idealne dla uczniów przygotowujących się do egzaminów z chemii na poziomie rozszerzonym.
Reakcje Redoks: Przykłady i Zasady
Zrozumienie reakcji redoks, w tym reakcji dysproporcjonowania i synproporcjonowania. Przykłady reakcji chemicznych, obliczanie stopni utlenienia oraz bilans elektronowy. Idealne dla studentów chemii, którzy chcą zgłębić temat utleniania i redukcji.
Redoks
Notatka do na nauki reakcji utleniania i redukcji do matury/na sprawdzian/ na karkówkę
Reakcje Redoks i Utlenianie
Zrozumienie reakcji utleniania-redukcji, półogniw oraz bilansowania równań chemicznych. Obejmuje kluczowe pojęcia, takie jak stopnie utlenienia, elektrody, oraz przykłady reakcji redoks. Idealne materiały do nauki przed sprawdzianem.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Pierwiastki Bloku D: Przegląd i Charakterystyka
Metale przejściowe takie jak chrom, miedź, żelazo i cynk odgrywają ważną rolę w chemii i naszym codziennym życiu. Każdy z nich posiada charakterystyczne właściwości i reakcje chemiczne, które decydują o ich zastosowaniach. Poznanie tych właściwości pomoże ci zrozumieć zachowanie metali... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości i reakcje chromu
Chrom to metal, który w powietrzu ulega pasywacji - pokrywa się warstwą tlenku chromu(III), co chroni go przed dalszym utlenianiem i korozją:
4Cr + 3O₂ → 2Cr₂O₃
W reakcji z kwasem solnym chrom zachowuje się różnie w zależności od warunków. W warunkach beztlenowych powstaje chlorek chromu(II), a w warunkach tlenowych - chlorek chromu(III):
- Beztlenowo: Cr + 2HCl → CrCl₂ + H₂↑
- Tlenowo: Cr + 6HCl + O₂ → 2CrCl₃ + H₂↑
Warto zapamiętać! Bezwodny chlorek chromu(II) jest bezbarwny, ale po uwodnieniu przybiera charakterystyczną niebieską barwę.
Chrom reaguje również z innymi rozcieńczonymi kwasami, jak np. kwas siarkowy(VI), tworząc odpowiednie sole i uwalniając wodór.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Tlenki i wodorotlenki chromu
Charakter chemiczny związków chromu zmienia się wraz ze wzrostem stopnia utlenienia:
| Stopień utlenienia | Tlenek | Wodorotlenek | Charakter chemiczny |
|---|---|---|---|
| II | CrO (ciemnoczerwony) | Cr(OH)₂ | zasadowy |
| III | Cr₂O₃ (zielony) | Cr(OH)₃ | amfoteryczny |
| VI | CrO₃ | - | kwasowy |
Wraz ze wzrostem stopnia utlenienia chromu zwiększa się charakter kwasowy jego związków oraz ich właściwości utleniające. Związki chromu reagują zarówno z kwasami, jak i zasadami, zgodnie z ich charakterem chemicznym.
Tlenek chromu(III) może być zredukowany w procesie aluminotermii: Cr₂O₃ + 2Al → Al₂O₃ + 2Cr + energia
Ciekawostka: Aluminotermia to reakcja silnie egzotermiczna, która wykorzystywana jest w metalurgii do otrzymywania metali z ich tlenków.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Chromiany i dichromiany
Jony chromianowe i dichromianowe to ważne formy występowania chromu na VI stopniu utlenienia. Chromiany można otrzymać przez prażenie tlenku chromu(III) z wodorotlenkiem potasu w obecności tlenu:
2Cr₂O₃ + 4K₂CO₃ + 3O₂ → 4K₂CrO₄ + 4CO₂↑
Te związki mogą przechodzić między sobą w zależności od pH środowiska:
-
W środowisku kwasowym chromiany przekształcają się w dichromiany: 2CrO₄²⁻ + 2H⁺ → Cr₂O₇²⁻ + H₂O
-
W środowisku zasadowym dichromiany przekształcają się w chromiany: Cr₂O₇²⁻ + 2OH⁻ → 2CrO₄²⁻ + H₂O
Zapamiętaj! Chromiany mają żółtą barwę, a dichromiany pomarańczową. Te przemiany nie są reakcjami redoks, ponieważ stopień utlenienia chromu nie zmienia się .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości redukująco-utleniające związków chromu
Związki chromu wykazują różne właściwości redoks w zależności od stopnia utlenienia:
- Chrom(II) działa jako reduktor
- Chrom(VI) działa jako utleniacz
- Chrom(III) może pełnić obie funkcje, w zależności od warunków
Dichromiany są szczególnie silnymi utleniaczami w środowisku kwaśnym, redukując się do jonów Cr³⁺ o ciemnogranatowej lub ciemnozielonej barwie. Typowym przykładem jest utlenianie jonów żelaza(II):
Cr₂O₇²⁻ + 6Fe²⁺ + 14H⁺ → 2Cr³⁺ + 6Fe³⁺ + 7H₂O
W równaniu tym zachodzą dwa półprocesy:
- Redukcja: Cr₂O₇²⁻ + 14H⁺ + 6e⁻ → 2Cr³⁺ + 7H₂O
- Utlenianie: 6Fe²⁺ → 6Fe³⁺ + 6e⁻
Na sprawdzianie! Dichromiany mogą utleniać również związki nieorganiczne, jak np. jony siarczanowe(IV) do siarczanowych(VI), co jest ważną reakcją w analizie chemicznej.
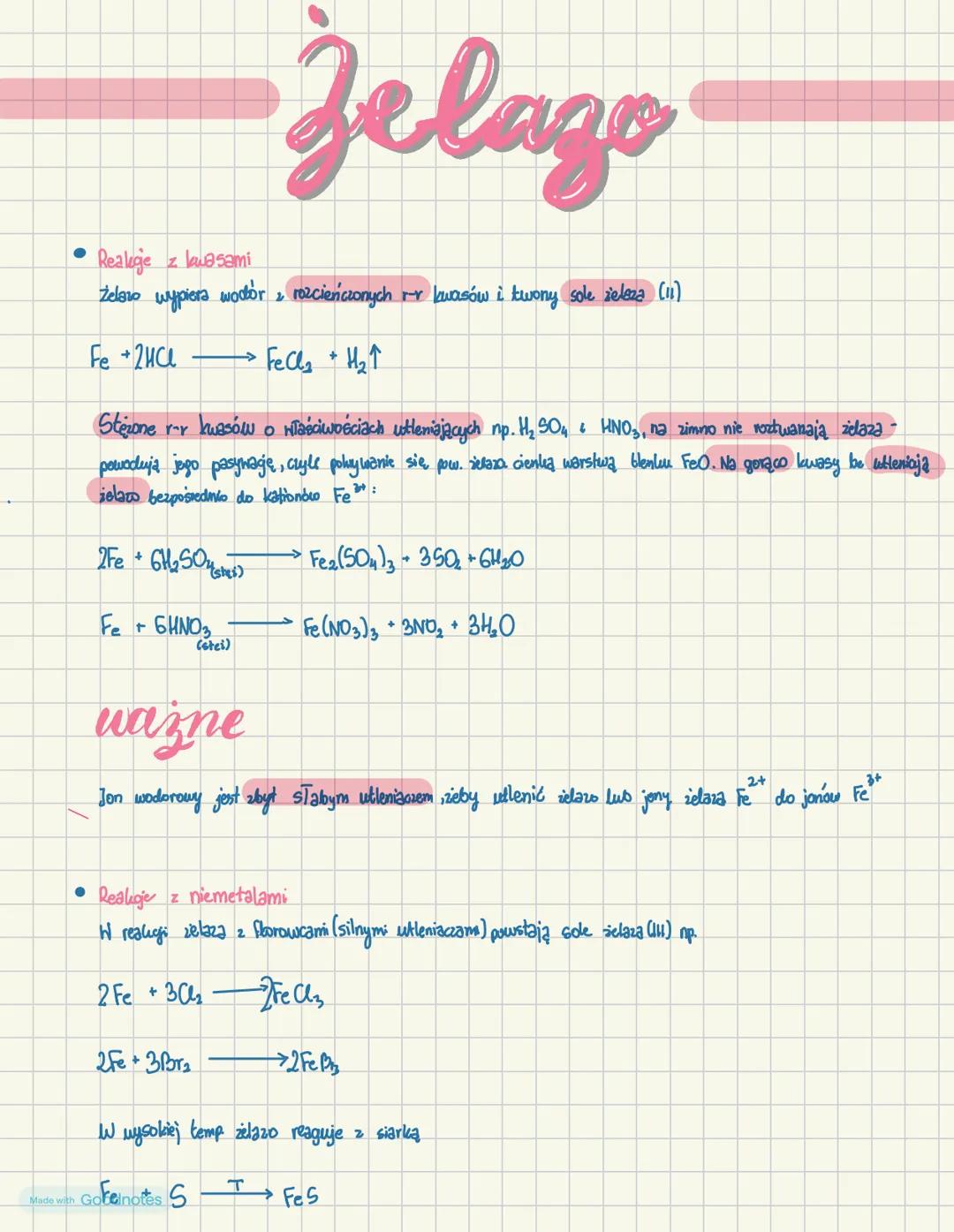
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Żelazo - reakcje z kwasami i niemetalami
Żelazo wypiera wodór z rozcieńczonych kwasów, tworząc sole żelaza(II):
Fe + 2HCl → FeCl₂ + H₂↑
Z kolei stężone kwasy utleniające (H₂SO₄, HNO₃) powodują na zimno pasywację żelaza - pokrywanie powierzchni metalu warstwą tlenku FeO. Na gorąco te same kwasy utleniają żelazo do jonów Fe³⁺:
2Fe + 6H₂SO₄ → Fe₂(SO₄)₃ + 3SO₂ + 6H₂O
Żelazo reaguje z silnymi utleniaczami, jak fluorowce, tworząc sole żelaza(III):
2Fe + 3Cl₂ → 2FeCl₃
W wysokiej temperaturze żelazo reaguje również z siarką:
Fe + S → FeS
Ważne: Jon wodorowy jest zbyt słabym utleniaczem, aby utlenić żelazo lub jony Fe²⁺ do jonów Fe³⁺ - dlatego w reakcji z kwasami nieutleniającymi powstają sole żelaza(II).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Żelazo - reakcje z tlenem i wodą
Rozdrobnione żelazo spala się w tlenie, tworząc magnetyt (Fe₃O₄) - tlenek o mieszanym charakterze żelaza(II,III):
3Fe + 2O₂ → Fe₃O₄
W podwyższonych temperaturach żelazo reaguje również z parą wodną:
3Fe + 4H₂O → Fe₃O₄ + 4H₂↑
Wodorotlenki żelaza są słabo rozpuszczalne w wodzie i otrzymuje się je w reakcjach strącania:
- Fe²⁺ + 2OH⁻ → Fe(OH)₂↓
- Fe³⁺ + 3OH⁻ → Fe(OH)₃↓ (brunatny osad)
Świeżo strącony wodorotlenek żelaza(II) ulega utlenieniu tlenem rozpuszczonym w wodzie:
4Fe(OH)₂ + O₂ + 2H₂O → 4Fe(OH)₃
Na laboratorium: Reakcja utleniania Fe(OH)₂ do Fe(OH)₃ zachodzi szybciej w obecności nadtlenku wodoru, co można zaobserwować jako zmianę barwy osadu z białozielonej na brunatną.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Miedź - reakcje z kwasami i niemetalami
Miedź jest mniej aktywna chemicznie niż wodór, więc nie wypiera go z kwasów nieutleniających. Rozpuszcza się jednak w kwasach utleniających:
Cu + 2H₂SO₄(stęż.) → CuSO₄ + SO₂ + 2H₂O Cu + 4HNO₃ → Cu(NO₃)₂ + 2NO₂ + 2H₂O
Miedź reaguje z fluorowcami jako silnymi utleniaczami, tworząc sole miedzi(II):
Cu + Cl₂ → CuCl₂
W reakcji z siarką zachowanie miedzi zależy od warunków:
- z parami siarki powstaje Cu₂S (siarczek miedzi(I))
- z ciekłą siarką w temperaturze powyżej 346,85°C powstaje CuS (siarczek miedzi(II))
Miedź reaguje z tlenem, pokrywając się warstwą tlenku miedzi(I) o ceglastoczerwonej barwie:
4Cu + O₂ → 2Cu₂O
Podobnie jak miedź! Srebro również reaguje tylko z kwasami utleniającymi, co wynika z jego pozycji w szeregu aktywności metali.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Miedź - tlenki i wodorotlenek
W podwyższonej temperaturze miedź reaguje z tlenem, tworząc czarny tlenek miedzi(II):
2Cu + O₂ → 2CuO
Tlenek miedzi(II) jest utleniaczem, który może utleniać alkohole do aldehydów:
CH₃CH₂OH + CuO → CH₃CHO + Cu + H₂O
Pojawienie się ceglastoczerwonego osadu tlenku miedzi(I) jest pozytywnym wynikiem próby Trommera, służącej do wykrywania właściwości redukujących aldehydów i cukrów:
2Cu(OH)₂ + CH₃CHO + OH⁻ → Cu₂O + CH₃COO⁻ + 3H₂O
Wodorotlenek miedzi(II) otrzymuje się w reakcji strącania:
Cu²⁺ + 2OH⁻ → Cu(OH)₂↓
Jest on nietrwały i podczas ogrzewania rozkłada się:
Cu(OH)₂ → CuO + H₂O
Ciekawostka laboratoryjna: Próba Trommera jest jedną z podstawowych metod identyfikacji aldehydów i cukrów redukujących w analizie organicznej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Miedź - reakcje wodorotlenku
Wodorotlenek miedzi(II) w reakcji z kwasami tworzy sole miedzi(II):
Cu(OH)₂ + H₂SO₄ → CuSO₄ + 2H₂O
Świeżo strącony wodorotlenek miedzi(II) rozpuszcza się w stężonych i mocnych zasadach, tworząc granatowe tetrahydroksokompleksy:
Cu(OH)₂ + 2OH⁻ → [Cu(OH)₄]²⁻
Wodorotlenek miedzi reaguje również z amoniakiem, tworząc intensywnie niebieskie kompleksy aminowe:
Cu(OH)₂ + 4NH₃ → [Cu(NH₃)₄]²⁺ + 2OH⁻
Zjawisko z codziennego życia: Patyna - jasnozielona warstwa [Cu(OH)₂CO₃] pokrywająca powierzchnię wyrobów z miedzi i jej stopów - chroni głębsze warstwy metalu przed korozją. Możesz ją zobaczyć na starych miedzianych dachach i pomnikach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Cynk - metal o właściwościach amfoterycznych
Cynk jest metalem o właściwościach amfoterycznych, co oznacza, że reaguje zarówno z kwasami, jak i z zasadami.
W reakcji z kwasami nieutleniającymi cynk rozpuszcza się, tworząc sole cynku i uwalniając wodór:
Zn + 2HCl → ZnCl₂ + H₂↑
Cynk rozpuszcza się również w gorących roztworach mocnych zasad, tworząc tetrahydroksocynkany:
Zn + 2OH⁻ + 2H₂O → [Zn(OH)₄]²⁻ + H₂↑
Na powietrzu cynk pokrywa się cienką warstwą tlenku cynku, co powoduje, że jego powierzchnia traci połysk:
2Zn + O₂ → 2ZnO
Wodorotlenek cynku można otrzymać w reakcji strącania:
Zn²⁺ + 2OH⁻ → Zn(OH)₂↓
Kluczowa właściwość: Wodorotlenek cynku jest trudno rozpuszczalny w wodzie i wykazuje charakter amfoteryczny - reaguje zarówno z kwasami, jak i z zasadami, tworząc rozpuszczalne kompleksy.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Reakcje redoks
9Ogniwa Galwaniczne i Redoks
Zrozumienie ogniw galwanicznych, reakcji redoks oraz stopni utlenienia pierwiastków. Dowiedz się o korozji metali, metodach ochrony oraz zastosowaniach ogniw Daniella. Idealne dla uczniów chemii i studentów przygotowujących się do egzaminów.
Reguły Stopni Utlenienia
Zrozumienie stopni utlenienia pierwiastków chemicznych oraz ich roli w reakcjach redoks. Notatka obejmuje definicje, kluczowe zasady ustalania stopni utlenienia, przykłady oraz wyjaśnienia dotyczące utleniaczy i reduktorów. Idealna dla uczniów chemii.
Właściwości Metali D-Block
Zgłębiaj właściwości i reakcje metali bloku D, takich jak mangan, chrom, żelazo, miedź i cynk. Dowiedz się o ich związkach, amfoterycznych tlenkach oraz doświadczeniach laboratoryjnych. Idealne dla studentów chemii, którzy chcą zrozumieć chemiczne zachowanie metali i ich zastosowania.
Reakcje Pierwiastków Bloku D
Odkryj szczegółowe reakcje chemiczne i właściwości pierwiastków bloku d, w tym mangan, chrom i miedź. Zawiera informacje o stanach utlenienia, reakcjach redoks oraz kolorach związków chemicznych. Idealne dla uczniów przygotowujących się do egzaminów z chemii. Typ: Podsumowanie.
Chemia Bloku D: Metale
Zgłębiaj charakterystykę metali bloku D, w tym srebra, cynku, żelaza i manganu. Dowiedz się o reakcjach chemicznych, stanach utlenienia oraz właściwościach amfoterycznych. Idealne materiały do nauki dla studentów chemii.
Elektrochemia: Zasady i Reakcje
Kompleksowe notatki z elektrochemii obejmujące kluczowe zagadnienia, takie jak reakcje redoks, prawo Faradaya, procesy elektrolizy oraz właściwości elektrolitów. Idealne dla uczniów przygotowujących się do egzaminów z chemii na poziomie rozszerzonym.
Reakcje Redoks: Przykłady i Zasady
Zrozumienie reakcji redoks, w tym reakcji dysproporcjonowania i synproporcjonowania. Przykłady reakcji chemicznych, obliczanie stopni utlenienia oraz bilans elektronowy. Idealne dla studentów chemii, którzy chcą zgłębić temat utleniania i redukcji.
Redoks
Notatka do na nauki reakcji utleniania i redukcji do matury/na sprawdzian/ na karkówkę
Reakcje Redoks i Utlenianie
Zrozumienie reakcji utleniania-redukcji, półogniw oraz bilansowania równań chemicznych. Obejmuje kluczowe pojęcia, takie jak stopnie utlenienia, elektrody, oraz przykłady reakcji redoks. Idealne materiały do nauki przed sprawdzianem.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.