Niemetale to fascynująca grupa pierwiastków, która obejmuje węgiel, krzem, azot,... Pokaż więcej
Niemetale z Bloku P - Charakterystyka i Właściwości





![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_1.webp&w=2048&q=75)
Niemetale - pierwiastki bloku p
Niemetale to grupa pierwiastków o wyjątkowych właściwościach chemicznych. Znajdziesz je w prawej części układu okresowego, głównie w bloku p.
Te pierwiastki różnią się znacznie od metali - są zazwyczaj słabymi przewodnikami ciepła i elektryczności. Wiele z nich występuje w postaci gazów w temperaturze pokojowej.
💡 Pamiętaj: Niemetale często tworzą związki kowalencyjne i mają tendencję do przyjmowania elektronów w reakcjach chemicznych.
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_2.webp&w=2048&q=75)
Węgiel i krzem - podstawy życia i technologii
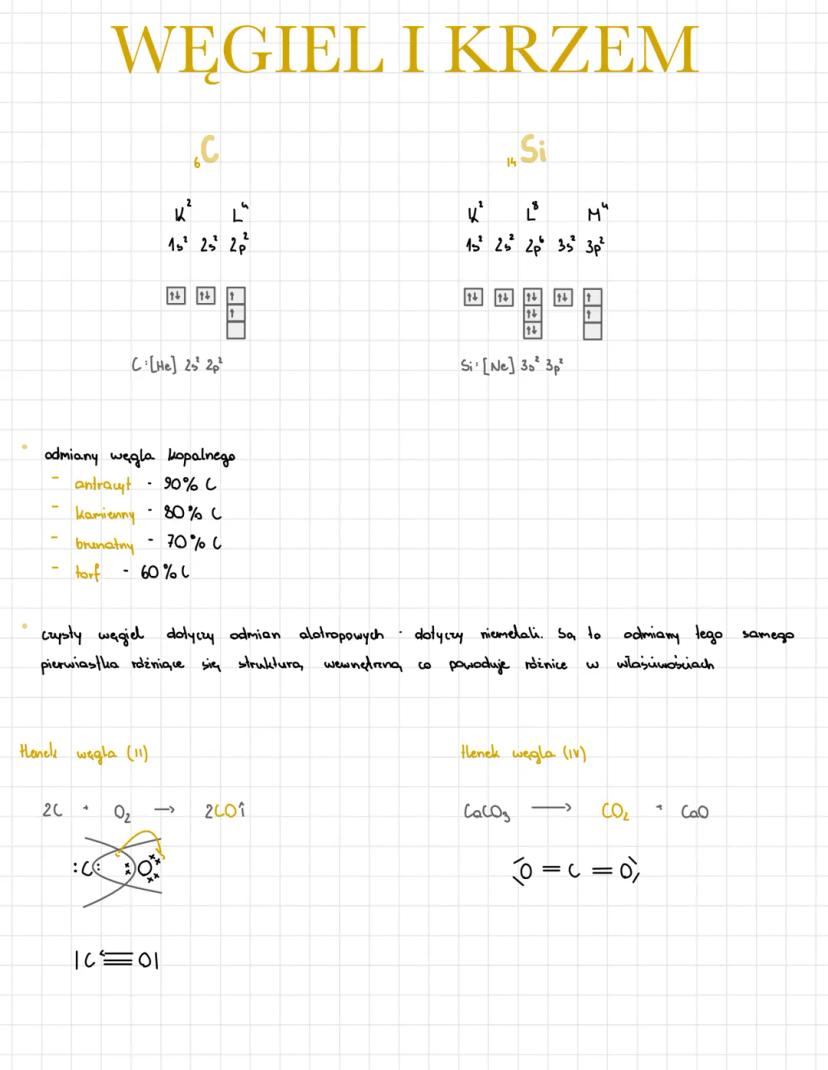
Węgiel (C) i krzem (Si) to pierwiastki z tej samej grupy, ale o różnych właściwościach. Węgiel ma konfigurację elektronową [He] 2s² 2p², a krzem [Ne] 3s² 3p².
Odmiany węgla kopalnego różnią się zawartością czystego węgla: antracyt (90%), węgiel kamienny (80%), brunatny (70%) i torf (60%). Czyste formy węgla to odmiany alotropowe - ten sam pierwiastek o różnej strukturze wewnętrznej.
Węgiel tworzy dwa ważne tlenki. Tlenek węgla(II) CO powstaje z reakcji 2C + O₂ → 2CO i ma potrójne wiązanie. Tlenek węgla(IV) CO₂ można otrzymać z węglanu wapnia: CaCO₃ → CO₂ + CaO.
💡 Ciekawostka: Różne odmiany alotropowe tego samego pierwiastka mogą mieć całkowicie inne właściwości!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_3.webp&w=2048&q=75)
Doświadczenia z kwasami
W laboratorium możesz łatwo otrzymać dwa różne kwasy używając podobnych związków.
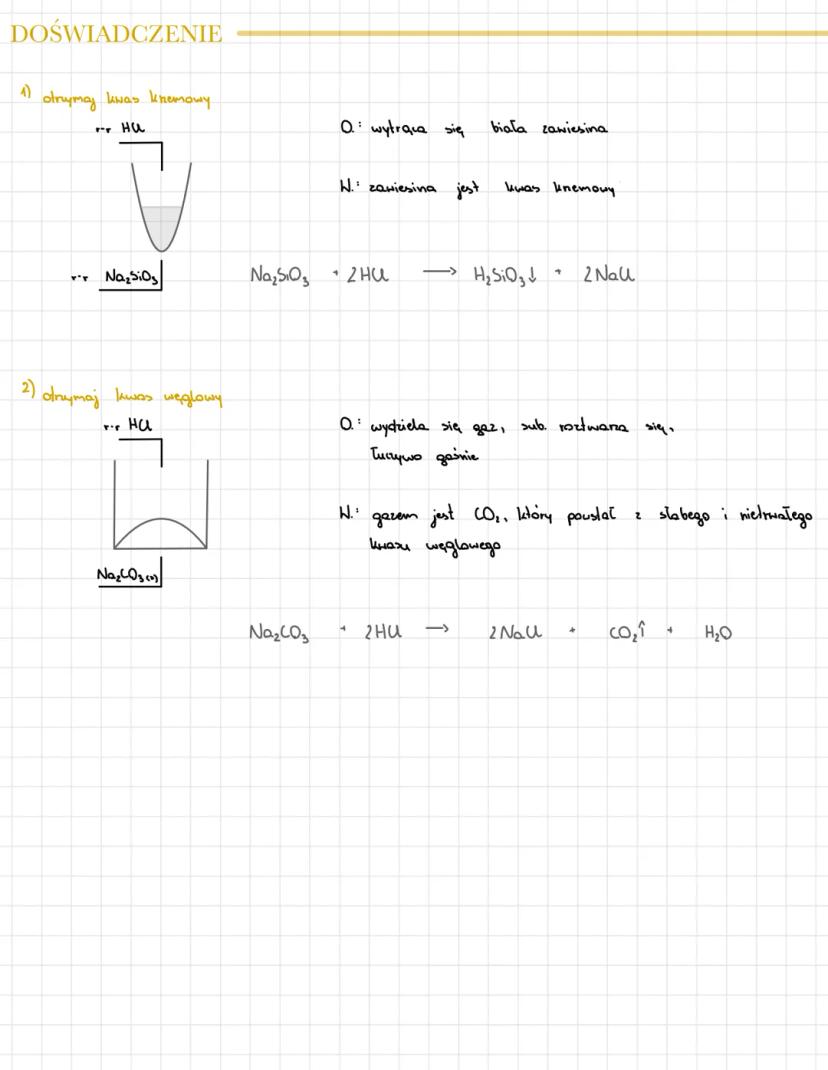
Otrzymywanie kwasu krzemowego: Gdy dodasz HCl do krzemianu sodu Na₂SiO₃, powstaje biała zawiesina kwasu krzemowego: Na₂SiO₃ + 2HCl → H₂SiO₃↓ + 2NaCl.
Otrzymywanie kwasu węglowego: Z węglanem sodu Na₂CO₃ reakcja przebiega inaczej - wydziela się gaz CO₂: Na₂CO₃ + 2HCl → 2NaCl + CO₂↑ + H₂O.
💡 Obserwacja: Zwróć uwagę na różnice - jeden kwas wypada jako osad, drugi rozkłada się do gazu!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_4.webp&w=2048&q=75)
Azot - podstawa życia
Azot (N) ma konfigurację [He] 2s² 2p³ i może występować w stopniach utlenienia od -III do +V. To główny składnik powietrza (78%) i kluczowy element białek w naszym organizmie.
W stanie wolnym azot występuje jako N₂ z potrójnym wiązaniem, co czyni go bardzo stabilnym. Ten bezbarwny, bezwonny gaz jest lżejszy od powietrza i słabo rozpuszcza się w wodzie.
Amoniak NH₃ to lżejszy gaz o charakterystycznym zapachu, który doskonale rozpuszcza się w wodzie. Powstaje w syntezie: N₂ + 3H₂ → 2NH₃. Ma budowę dipola z parą elektronów niebiorących udziału w wiązaniu.
💡 Ważne: Azot w temperaturze pokojowej jest mało reaktywny, ale podwyższenie temperatury czy ciśnienia zmienia to radykalnie!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_5.webp&w=2048&q=75)
Związki azotu w akcji
Woda amoniakalna to słaby roztwór zasadowy powstający z reakcji NH₃ + H₂O → NH₄⁺ + OH⁻. Powstaje kation amonowy i jony wodorotlenkowe nadające odczyn zasadowy.
Spektakularną reakcję zobaczysz, gdy amoniak spotka chlorowodór: NH₃(g) + HCl(g) → NH₄Cl(s). Powstaje biały dym - to układy koloidalne chlorku amonu.
Tlenki azotu mają różne właściwości: NO to obojętny biały gaz, a NO₂ to kwasowy brunatny gaz. Gdy NO₂ reaguje z wodą, zachodzi dysproporcjonowanie: 2NO₂ + H₂O → HNO₂ + HNO₃.
💡 Pamiętaj: Kwas azotowy(V) HNO₃ to mocny kwas silnie utleniający, a jego sole to saletry!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_6.webp&w=2048&q=75)
Fosfor - pierwiastek o dwóch twarzach
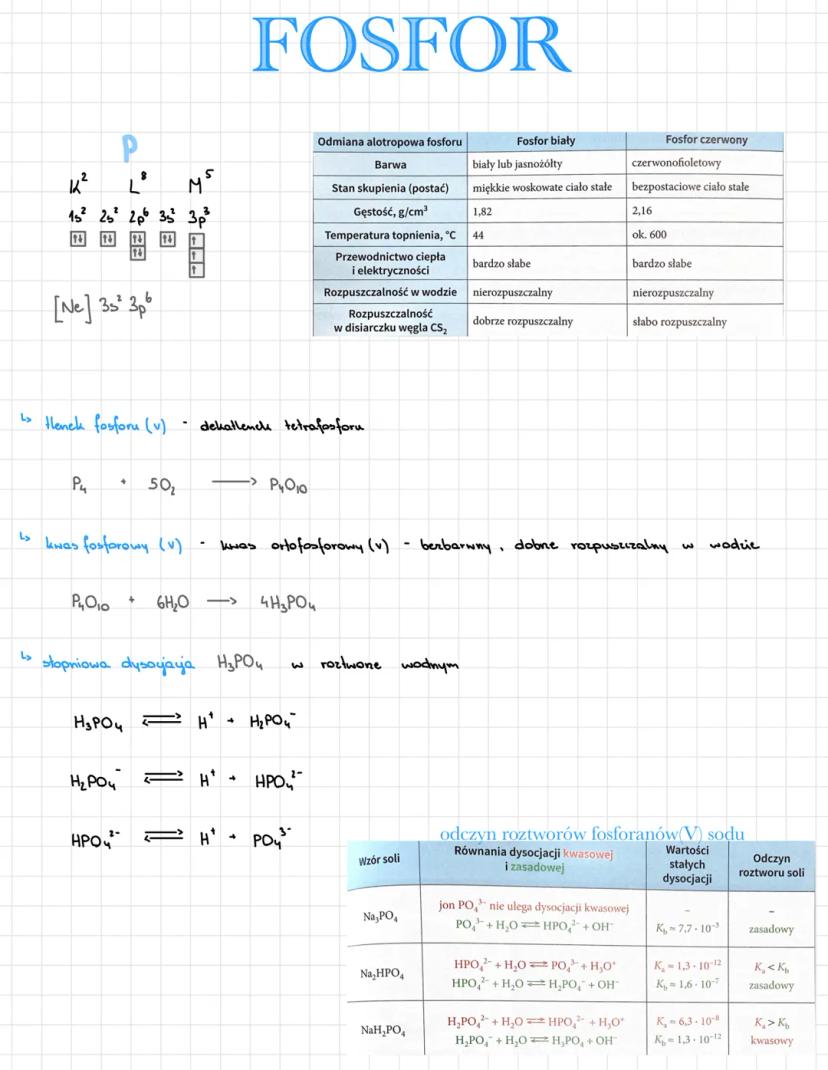
Fosfor (P) z konfiguracją [Ne] 3s² 3p³ występuje w dwóch głównych odmianach alotropowych o dramatycznie różnych właściwościach.
Fosfor biały to miękkie, woskowate ciało stałe o temperaturze topnienia 44°C, dobrze rozpuszczalne w disiarczku węgla. Fosfor czerwony jest twardszy, topi się około 600°C i słabo rozpuszcza się w CS₂.
Kwas fosforowy(V) H₃PO₄ powstaje z tlenku: P₄O₁₀ + 6H₂O → 4H₃PO₄. Ten trójprotonowy kwas dysocjuje stopniowo w trzech etapach, co wpływa na odczyn jego soli.
Sole fosforanu sodu mają różne odczyny: Na₃PO₄ (zasadowy), Na₂HPO₄ (zasadowy), NaH₂PO₄ (kwasowy) - zależy to od przewagi dysocjacji kwasowej lub zasadowej.
💡 Bezpieczeństwo: Fosfor biały jest bardzo toksyczny i łatwopalny - dlatego przechowuje się go pod wodą!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_7.webp&w=2048&q=75)
Praktyczne zastosowania fosforu
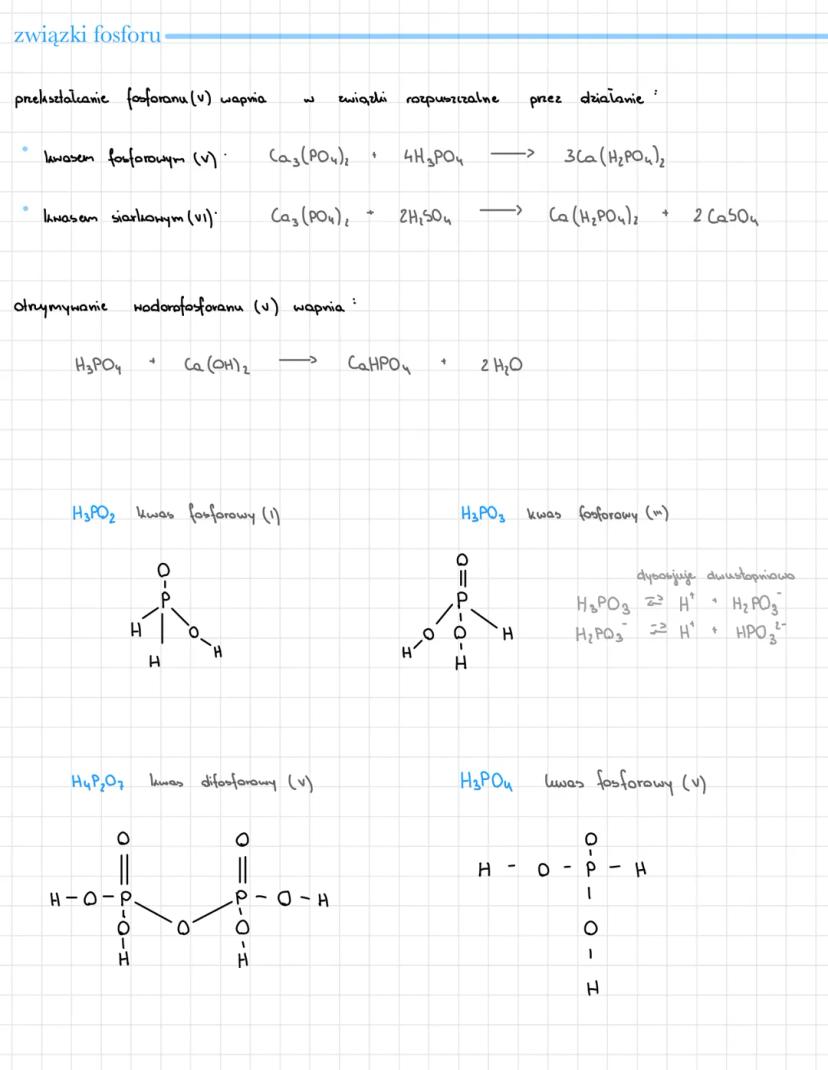
W rolnictwie fosforany są kluczowymi nawozami, ale naturalny fosforan(V) wapnia Ca₃(PO₄)₂ jest słabo rozpuszczalny. Trzeba go przekształcić w związki dostępne dla roślin.
Możesz to zrobić kwasem fosforowym: Ca₃(PO₄)₂ + 4H₃PO₄ → 3Ca(H₂PO₄)₂ lub kwasem siarkowym: Ca₃(PO₄)₂ + 2H₂SO₄ → Ca(H₂PO₄)₂ + 2CaSO₄.
Fosfor tworzy różne kwasy o różnych stopniach utlenienia: H₃PO₂ (kwas fosforowy(I)), H₃PO₃ , H₄P₂O₇ (kwas difosforowy(V)) i H₃PO₄ (kwas fosforowy(V)).
💡 Ciekawostka: Kwas fosforowy(III) ma tylko dwa protony zdolne do dysocjacji, mimo trzech atomów wodoru we wzorze!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_8.webp&w=2048&q=75)
Siarka - żółty niemetal o wielu obliczach
Siarka (S) to żółty niemetal z konfiguracją [Ne] 3s² 3p⁴, występujący w odmianach alotropowych: rombowej i jednoskośnej. Obie formy mają molekuły S₈ i podobne właściwości chemiczne.
Siarka jest mniej aktywna niż fluorowce, ale reaguje z metalami tworząc siarczki: Cu + S → Cu₂S, Fe + S → FeS. W wysokiej temperaturze łączy się z wodorem: H₂ + S → H₂S.
Siarkowodór H₂S to nietrwały, słaby kwas o nieprzyjemnym zapachu. Dobrze rozpuszcza się w wodzie, ale ulega rozkładowi. Możesz go wydzielić z siarczków działając kwasem: 2H⁺ + S²⁻ → H₂S↑.
💡 Uwaga: Siarkowodór jest bardzo toksyczny - nawet małe stężenia są niebezpieczne!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_9.webp&w=2048&q=75)
Tlenki i kwasy siarki
Gdy siarka spala się w powietrzu, powstaje tlenek siarki(IV): S + O₂ → SO₂. Ten gaz tworzy z wodą niestały kwas siarkowy(IV): H₂SO₃ ⇌ H₂O + SO₂.
Kwas siarkowy(VI) H₂SO₄ to mocny, silnie utleniający kwas o właściwościach higroskopijnych i żrących. W kontakcie z cukrem powoduje spektakularną reakcję - białe kryształki brązowieją i powstaje czarna masa węglowa.
Mechanizm działania: kwas siarkowy "usuwa" wodę z sacharozy , pozostawiając czysty węgiel. To proces odwodnienia, nie spalania!
Przemysłowo H₂SO₄ otrzymuje się w procesie kontaktowym: S + O₂ → SO₂, potem 2SO₂ + O₂ → 2SO₃, i na koniec SO₃ + H₂O → H₂SO₄.
💡 Eksperyment: Reakcja kwasu siarkowego z cukrem to klasyczna demonstracja odwodnania - nigdy nie próbuj tego w domu!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_10.webp&w=2048&q=75)
Fluorowce - chemiczni agresorzy
Fluorowce to najbardziej reaktywna grupa niemetali, występująca w cząsteczkach dwuatomowych. Są słabo rozpuszczalne w wodzie, ale mają silne właściwości utleniające.
Aktywność chemiczna maleje w dół grupy: F₂ > Cl₂ > Br₂ > I₂, ale moc ich kwasów rośnie: HF < HCl < HBr < HI. To pozorny paradoks wynikający z różnych mechanizmów.
Fluor F₂ (żółty gaz) występuje tylko w stopniu -1 i reaguje z wodorem wybuchowo. Chlor Cl₂ ma stopnie od -1 do +7. Brom Br₂ to brunatno-czerwona ciecz, a jod I₂ - stalowo-czarne ciało stałe sublimujące do fioletowego gazu.
💡 Pamiętaj: Im większy atom fluorowca, tym słabiej utlenia, ale tym mocniejszy kwas tworzy z wodorem!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Element
9Pierwiastki Bloku P
Odkryj właściwości i reakcje pierwiastków bloku P, w tym azot, fosfor, siarkę, węgiel oraz ich związki chemiczne. Zawiera informacje o kwasach, tlenkach, allotropach oraz eksperymentach chemicznych. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Chemia Bloku S
Zgłębiaj właściwości chemiczne pierwiastków bloku S, ich reakcje, otrzymywanie wodorotlenków oraz zastosowania w laboratoriach. Dowiedz się o charakterystyce metali alkalicznych i ziem alkalicznych, a także o ich wpływie na środowisko. Idealne dla uczniów i studentów chemii.
Układ Okresowy Pierwiastków
Zrozumienie układu okresowego pierwiastków chemicznych, ich symboli, liczby atomowej oraz mas atomowych. Materiał obejmuje kluczowe koncepcje chemii ogólnej, w tym strukturę materii i klasyfikację pierwiastków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Właściwości Wodoru i Helu
Odkryj kluczowe informacje o wodoru i helu, ich właściwościach fizycznych i chemicznych, a także metody ich otrzymywania. Notatka obejmuje przygotowanie wodorków, reakcje chemiczne oraz zastosowania tych pierwiastków w przemyśle. Idealna dla studentów chemii na poziomie nieorganicznym.
Właściwości Borowców
Zgłębiaj właściwości chemiczne i fizyczne borowców, ich zastosowanie w metalurgii oraz wytwarzaniu materiałów. Dowiedz się o najważniejszych minerałach, procesach pasywacji oraz roli boru, glinu i talu w przemyśle. Idealne dla studentów chemii i inżynierii materiałowej.
Wartościowość Pierwiastków
Odkryj zasady wartościowości pierwiastków chemicznych, w tym ich stany utlenienia i właściwości. Ta notatka zawiera kluczowe informacje o grupach pierwiastków oraz ich charakterystyce, co ułatwi naukę i zapamiętywanie. Idealna dla uczniów chemii, którzy chcą zrozumieć podstawowe koncepcje związane z wartościowością.
Właściwości metali alkalicznych
Zgłębiaj właściwości chemiczne metali alkalicznych, ich reakcje z wodą, kwasami oraz metody otrzymywania wodorotlenków. Notatka obejmuje kluczowe informacje o litowcach, ich konfiguracji elektronowej oraz zastosowaniach w przemyśle. Idealna dla studentów chemii.
Chemia: Budowa Atomów
Zrozumienie budowy atomów i ich właściwości chemicznych. Materiał obejmuje zagadnienia takie jak masa atomowa, konfiguracja elektronowa, izotopy oraz obliczanie mas cząsteczkowych. Idealne dla uczniów przygotowujących się do sprawdzianów z chemii.
Podstawowe pierwiastki chemiczne
Zrozumienie podstawowych pierwiastków chemicznych oraz ich symboli. Materiał obejmuje kluczowe informacje o pierwiastkach takich jak wodór, tlen, żelazo, srebro i wiele innych. Idealne dla uczniów klasy 7, którzy chcą zgłębić chemię. Typ: prezentacja.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Niemetale z Bloku P - Charakterystyka i Właściwości
Niemetale to fascynująca grupa pierwiastków, która obejmuje węgiel, krzem, azot, fosfor, siarkę i fluorowce. Te pierwiastki mają unikalne właściwości i tworzą związki, które spotykasz codziennie - od dwutlenku węgla w napojach gazowanych po chlor w wodzie z kranu.
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_1.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Niemetale - pierwiastki bloku p
Niemetale to grupa pierwiastków o wyjątkowych właściwościach chemicznych. Znajdziesz je w prawej części układu okresowego, głównie w bloku p.
Te pierwiastki różnią się znacznie od metali - są zazwyczaj słabymi przewodnikami ciepła i elektryczności. Wiele z nich występuje w postaci gazów w temperaturze pokojowej.
💡 Pamiętaj: Niemetale często tworzą związki kowalencyjne i mają tendencję do przyjmowania elektronów w reakcjach chemicznych.
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_2.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Węgiel i krzem - podstawy życia i technologii
Węgiel (C) i krzem (Si) to pierwiastki z tej samej grupy, ale o różnych właściwościach. Węgiel ma konfigurację elektronową [He] 2s² 2p², a krzem [Ne] 3s² 3p².
Odmiany węgla kopalnego różnią się zawartością czystego węgla: antracyt (90%), węgiel kamienny (80%), brunatny (70%) i torf (60%). Czyste formy węgla to odmiany alotropowe - ten sam pierwiastek o różnej strukturze wewnętrznej.
Węgiel tworzy dwa ważne tlenki. Tlenek węgla(II) CO powstaje z reakcji 2C + O₂ → 2CO i ma potrójne wiązanie. Tlenek węgla(IV) CO₂ można otrzymać z węglanu wapnia: CaCO₃ → CO₂ + CaO.
💡 Ciekawostka: Różne odmiany alotropowe tego samego pierwiastka mogą mieć całkowicie inne właściwości!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_3.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Doświadczenia z kwasami
W laboratorium możesz łatwo otrzymać dwa różne kwasy używając podobnych związków.
Otrzymywanie kwasu krzemowego: Gdy dodasz HCl do krzemianu sodu Na₂SiO₃, powstaje biała zawiesina kwasu krzemowego: Na₂SiO₃ + 2HCl → H₂SiO₃↓ + 2NaCl.
Otrzymywanie kwasu węglowego: Z węglanem sodu Na₂CO₃ reakcja przebiega inaczej - wydziela się gaz CO₂: Na₂CO₃ + 2HCl → 2NaCl + CO₂↑ + H₂O.
💡 Obserwacja: Zwróć uwagę na różnice - jeden kwas wypada jako osad, drugi rozkłada się do gazu!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_4.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Azot - podstawa życia
Azot (N) ma konfigurację [He] 2s² 2p³ i może występować w stopniach utlenienia od -III do +V. To główny składnik powietrza (78%) i kluczowy element białek w naszym organizmie.
W stanie wolnym azot występuje jako N₂ z potrójnym wiązaniem, co czyni go bardzo stabilnym. Ten bezbarwny, bezwonny gaz jest lżejszy od powietrza i słabo rozpuszcza się w wodzie.
Amoniak NH₃ to lżejszy gaz o charakterystycznym zapachu, który doskonale rozpuszcza się w wodzie. Powstaje w syntezie: N₂ + 3H₂ → 2NH₃. Ma budowę dipola z parą elektronów niebiorących udziału w wiązaniu.
💡 Ważne: Azot w temperaturze pokojowej jest mało reaktywny, ale podwyższenie temperatury czy ciśnienia zmienia to radykalnie!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_5.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Związki azotu w akcji
Woda amoniakalna to słaby roztwór zasadowy powstający z reakcji NH₃ + H₂O → NH₄⁺ + OH⁻. Powstaje kation amonowy i jony wodorotlenkowe nadające odczyn zasadowy.
Spektakularną reakcję zobaczysz, gdy amoniak spotka chlorowodór: NH₃(g) + HCl(g) → NH₄Cl(s). Powstaje biały dym - to układy koloidalne chlorku amonu.
Tlenki azotu mają różne właściwości: NO to obojętny biały gaz, a NO₂ to kwasowy brunatny gaz. Gdy NO₂ reaguje z wodą, zachodzi dysproporcjonowanie: 2NO₂ + H₂O → HNO₂ + HNO₃.
💡 Pamiętaj: Kwas azotowy(V) HNO₃ to mocny kwas silnie utleniający, a jego sole to saletry!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_6.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Fosfor - pierwiastek o dwóch twarzach
Fosfor (P) z konfiguracją [Ne] 3s² 3p³ występuje w dwóch głównych odmianach alotropowych o dramatycznie różnych właściwościach.
Fosfor biały to miękkie, woskowate ciało stałe o temperaturze topnienia 44°C, dobrze rozpuszczalne w disiarczku węgla. Fosfor czerwony jest twardszy, topi się około 600°C i słabo rozpuszcza się w CS₂.
Kwas fosforowy(V) H₃PO₄ powstaje z tlenku: P₄O₁₀ + 6H₂O → 4H₃PO₄. Ten trójprotonowy kwas dysocjuje stopniowo w trzech etapach, co wpływa na odczyn jego soli.
Sole fosforanu sodu mają różne odczyny: Na₃PO₄ (zasadowy), Na₂HPO₄ (zasadowy), NaH₂PO₄ (kwasowy) - zależy to od przewagi dysocjacji kwasowej lub zasadowej.
💡 Bezpieczeństwo: Fosfor biały jest bardzo toksyczny i łatwopalny - dlatego przechowuje się go pod wodą!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_7.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Praktyczne zastosowania fosforu
W rolnictwie fosforany są kluczowymi nawozami, ale naturalny fosforan(V) wapnia Ca₃(PO₄)₂ jest słabo rozpuszczalny. Trzeba go przekształcić w związki dostępne dla roślin.
Możesz to zrobić kwasem fosforowym: Ca₃(PO₄)₂ + 4H₃PO₄ → 3Ca(H₂PO₄)₂ lub kwasem siarkowym: Ca₃(PO₄)₂ + 2H₂SO₄ → Ca(H₂PO₄)₂ + 2CaSO₄.
Fosfor tworzy różne kwasy o różnych stopniach utlenienia: H₃PO₂ (kwas fosforowy(I)), H₃PO₃ , H₄P₂O₇ (kwas difosforowy(V)) i H₃PO₄ (kwas fosforowy(V)).
💡 Ciekawostka: Kwas fosforowy(III) ma tylko dwa protony zdolne do dysocjacji, mimo trzech atomów wodoru we wzorze!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_8.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Siarka - żółty niemetal o wielu obliczach
Siarka (S) to żółty niemetal z konfiguracją [Ne] 3s² 3p⁴, występujący w odmianach alotropowych: rombowej i jednoskośnej. Obie formy mają molekuły S₈ i podobne właściwości chemiczne.
Siarka jest mniej aktywna niż fluorowce, ale reaguje z metalami tworząc siarczki: Cu + S → Cu₂S, Fe + S → FeS. W wysokiej temperaturze łączy się z wodorem: H₂ + S → H₂S.
Siarkowodór H₂S to nietrwały, słaby kwas o nieprzyjemnym zapachu. Dobrze rozpuszcza się w wodzie, ale ulega rozkładowi. Możesz go wydzielić z siarczków działając kwasem: 2H⁺ + S²⁻ → H₂S↑.
💡 Uwaga: Siarkowodór jest bardzo toksyczny - nawet małe stężenia są niebezpieczne!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_9.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
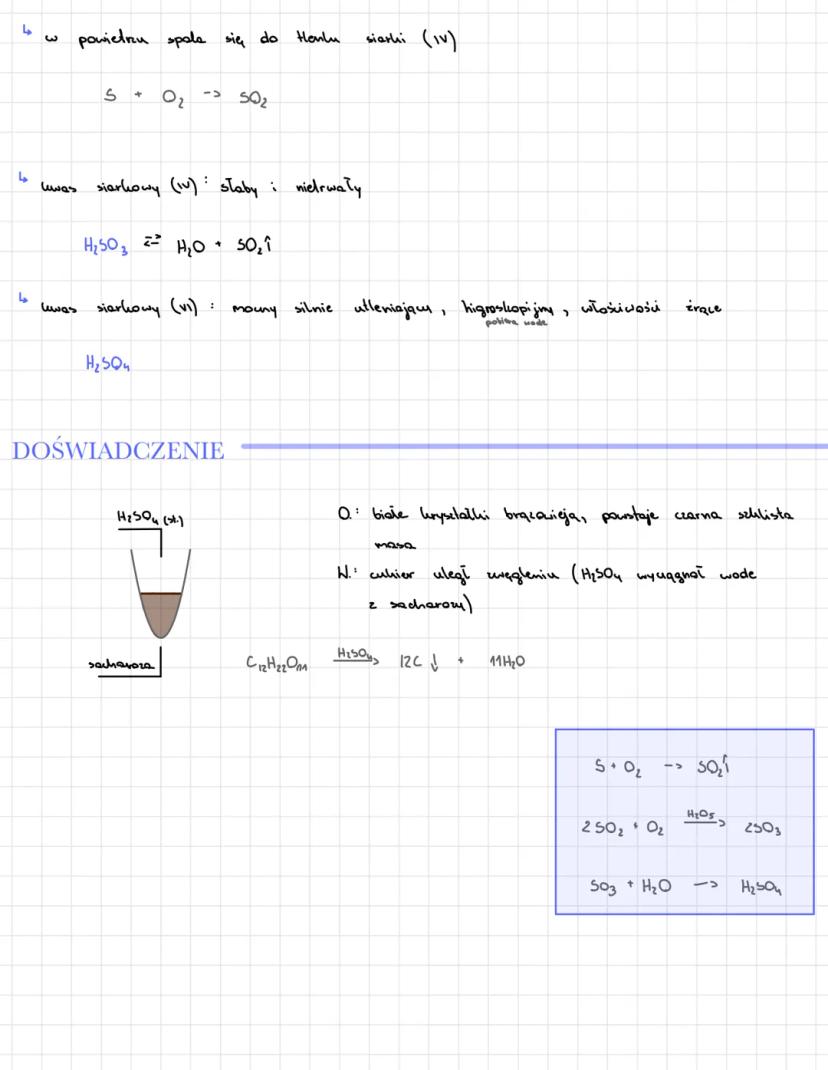
Tlenki i kwasy siarki
Gdy siarka spala się w powietrzu, powstaje tlenek siarki(IV): S + O₂ → SO₂. Ten gaz tworzy z wodą niestały kwas siarkowy(IV): H₂SO₃ ⇌ H₂O + SO₂.
Kwas siarkowy(VI) H₂SO₄ to mocny, silnie utleniający kwas o właściwościach higroskopijnych i żrących. W kontakcie z cukrem powoduje spektakularną reakcję - białe kryształki brązowieją i powstaje czarna masa węglowa.
Mechanizm działania: kwas siarkowy "usuwa" wodę z sacharozy , pozostawiając czysty węgiel. To proces odwodnienia, nie spalania!
Przemysłowo H₂SO₄ otrzymuje się w procesie kontaktowym: S + O₂ → SO₂, potem 2SO₂ + O₂ → 2SO₃, i na koniec SO₃ + H₂O → H₂SO₄.
💡 Eksperyment: Reakcja kwasu siarkowego z cukrem to klasyczna demonstracja odwodnania - nigdy nie próbuj tego w domu!
![NIEMETALE
PIERWIASTKI
BLOKU P # WĘGIEL I KRZEM
C
Si
K
L
L
M
1s² 2s² 2p²
1s² 2s² 2p⁶ 3s² 3p²
C [He] 2s² 2p²
Si' [Ne] 3s² 3p²
- odmia](/_next/image?url=https%3A%2F%2Fcontent-eu-central-1.knowunity.com%2FCONTENT%2F018ed75a-4f71-7cc4-b908-e8aab2f3eb14_image_page_10.webp&w=2048&q=75)
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Fluorowce - chemiczni agresorzy
Fluorowce to najbardziej reaktywna grupa niemetali, występująca w cząsteczkach dwuatomowych. Są słabo rozpuszczalne w wodzie, ale mają silne właściwości utleniające.
Aktywność chemiczna maleje w dół grupy: F₂ > Cl₂ > Br₂ > I₂, ale moc ich kwasów rośnie: HF < HCl < HBr < HI. To pozorny paradoks wynikający z różnych mechanizmów.
Fluor F₂ (żółty gaz) występuje tylko w stopniu -1 i reaguje z wodorem wybuchowo. Chlor Cl₂ ma stopnie od -1 do +7. Brom Br₂ to brunatno-czerwona ciecz, a jod I₂ - stalowo-czarne ciało stałe sublimujące do fioletowego gazu.
💡 Pamiętaj: Im większy atom fluorowca, tym słabiej utlenia, ale tym mocniejszy kwas tworzy z wodorem!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: Element
9Pierwiastki Bloku P
Odkryj właściwości i reakcje pierwiastków bloku P, w tym azot, fosfor, siarkę, węgiel oraz ich związki chemiczne. Zawiera informacje o kwasach, tlenkach, allotropach oraz eksperymentach chemicznych. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Chemia Bloku S
Zgłębiaj właściwości chemiczne pierwiastków bloku S, ich reakcje, otrzymywanie wodorotlenków oraz zastosowania w laboratoriach. Dowiedz się o charakterystyce metali alkalicznych i ziem alkalicznych, a także o ich wpływie na środowisko. Idealne dla uczniów i studentów chemii.
Układ Okresowy Pierwiastków
Zrozumienie układu okresowego pierwiastków chemicznych, ich symboli, liczby atomowej oraz mas atomowych. Materiał obejmuje kluczowe koncepcje chemii ogólnej, w tym strukturę materii i klasyfikację pierwiastków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Właściwości Wodoru i Helu
Odkryj kluczowe informacje o wodoru i helu, ich właściwościach fizycznych i chemicznych, a także metody ich otrzymywania. Notatka obejmuje przygotowanie wodorków, reakcje chemiczne oraz zastosowania tych pierwiastków w przemyśle. Idealna dla studentów chemii na poziomie nieorganicznym.
Właściwości Borowców
Zgłębiaj właściwości chemiczne i fizyczne borowców, ich zastosowanie w metalurgii oraz wytwarzaniu materiałów. Dowiedz się o najważniejszych minerałach, procesach pasywacji oraz roli boru, glinu i talu w przemyśle. Idealne dla studentów chemii i inżynierii materiałowej.
Wartościowość Pierwiastków
Odkryj zasady wartościowości pierwiastków chemicznych, w tym ich stany utlenienia i właściwości. Ta notatka zawiera kluczowe informacje o grupach pierwiastków oraz ich charakterystyce, co ułatwi naukę i zapamiętywanie. Idealna dla uczniów chemii, którzy chcą zrozumieć podstawowe koncepcje związane z wartościowością.
Właściwości metali alkalicznych
Zgłębiaj właściwości chemiczne metali alkalicznych, ich reakcje z wodą, kwasami oraz metody otrzymywania wodorotlenków. Notatka obejmuje kluczowe informacje o litowcach, ich konfiguracji elektronowej oraz zastosowaniach w przemyśle. Idealna dla studentów chemii.
Chemia: Budowa Atomów
Zrozumienie budowy atomów i ich właściwości chemicznych. Materiał obejmuje zagadnienia takie jak masa atomowa, konfiguracja elektronowa, izotopy oraz obliczanie mas cząsteczkowych. Idealne dla uczniów przygotowujących się do sprawdzianów z chemii.
Podstawowe pierwiastki chemiczne
Zrozumienie podstawowych pierwiastków chemicznych oraz ich symboli. Materiał obejmuje kluczowe informacje o pierwiastkach takich jak wodór, tlen, żelazo, srebro i wiele innych. Idealne dla uczniów klasy 7, którzy chcą zgłębić chemię. Typ: prezentacja.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.