Kwasy to ważne związki chemiczne, które spotykasz w życiu codziennym... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
205
•
Zaktualizowano May 7, 2026
•
Julianna Nowicka
@juliannanowicka
Kwasy to ważne związki chemiczne, które spotykasz w życiu codziennym... Pokaż więcej






Kwasy mają ogólny wzór H₍ᵐ₎R^m, gdzie H to atomy wodoru, a R to reszta kwasowa. Możemy je podzielić na dwie główne grupy:
Kwasy beztlenowe nie zawierają tlenu w swojej budowie. Przykładami są HCl (kwas chlorowodorowy) i H₂S (kwas siarkowodorowy). Możemy je otrzymać na różne sposoby, np. kwas chlorowodorowy powstaje w reakcji wodoru z chlorem: H₂+Cl₂→2HCl.
Kwasy tlenowe zawierają w swojej budowie tlen. Przykładami są H₂CO₃ (kwas węglowy) i H₂SO₃ (kwas siarkowy IV). Cząsteczki kwasów możemy zapisać używając wzoru sumarycznego (np. HCl) lub strukturalnego, który pokazuje, jak atomy są połączone .
Wskazówka: Zapamiętaj, że kwasy beztlenowe często mają końcówkę "-owodorowy" w nazwie (chlorowodorowy, siarkowodorowy), podczas gdy kwasy tlenowe zazwyczaj kończą się na "-owy" (węglowy, siarkowy).

Kwas siarkowodorowy (H₂S) można otrzymać w reakcji wodoru z siarką: H₂+S→H₂S. Jest to bezbarwna ciecz o charakterystycznym zapachu zgniłych jaj. Co ciekawe, mimo nieprzyjemnego zapachu, znajduje zastosowanie w przemyśle kosmetycznym do produkcji depilatorów chemicznych!
Kwas siarkowy(IV) (H₂SO₃) otrzymujemy w dwóch etapach: najpierw siarka reaguje z tlenem , a następnie dwutlenek siarki z wodą . Jest to bezbarwna ciecz o zapachu siarki, ale bardzo nietrwała - łatwo się rozkłada.
Wzór sumaryczny pokazuje nam skład kwasu (np. H₂SO₃), natomiast wzór strukturalny pokazuje nam, jak atomy są połączone w cząsteczce. Dzięki temu możemy lepiej zrozumieć właściwości kwasów.
Ciekawostka: Kwas siarkowodorowy jest tak wrażliwy na zapach, że ludzie wyczuwają go już w stężeniach kilku cząsteczek na milion! To naturalny mechanizm ostrzegawczy przed tą trującą substancją.

Kwas azotowy(V) (HNO₃) otrzymujemy w reakcji N₂O₅+H₂O→2HNO₃. Jest to bezbarwna ciecz, gęstsza od wody, o ostrym zapachu. Ten żrący kwas powoduje żółknięcie białek przy kontakcie. Mimo niebezpiecznych właściwości jest szeroko stosowany - od produkcji perfum po paliwa rakietowe!
Kwas fosforowy(V) (H₃PO₄) powstaje w dwuetapowej reakcji: 4P+5O₂→P₄O₁₀ a następnie P₄O₁₀+6H₂O→4H₃PO₄. W przeciwieństwie do większości kwasów występuje jako substancja stała - bezbarwne kryształy dobrze rozpuszczalne w wodzie.
Pamiętaj, że każdy z tych kwasów ma swoją charakterystyczną budowę pokazaną przez wzór strukturalny. Na przykład w H₃PO₄ mamy centralny atom fosforu połączony z czterema atomami tlenu, a trzy z nich są dodatkowo połączone z atomami wodoru.
Uważaj! Większość kwasów ma właściwości żrące i może spowodować poważne oparzenia. W laboratorium zawsze używaj okularów ochronnych i rękawic gdy pracujesz z kwasami!

Kwas siarkowy(VI) (H₂SO₄) to jeden z najważniejszych kwasów w przemyśle. Otrzymujemy go w trzech etapach: S+O₂→SO₂, SO₂+O₂→2SO₃, SO₃+H₂O→H₂SO₄. Jest bezbarwną, bezwonną cieczą gęstszą od wody, która ma zdolność zwęglania substancji organicznych.
Kwas siarkowy(VI) jest szeroko stosowany w produkcji nawozów sztucznych i w przemyśle chemicznym. Możesz go spotkać również w akumulatorach samochodowych! Jego wzór strukturalny H-O-S₂-O-H pokazuje, że siarka jest połączona z czterema atomami tlenu.
Kwas węglowy (H₂CO₃) powstaje w reakcji CO₂+H₂O→H₂CO₃. To bezbarwna ciecz bez zapachu, ale bardzo nietrwała - łatwo rozpada się na wodę i dwutlenek węgla. Właśnie dlatego napoje gazowane "uciekają" gdy stoją otwarte - kwas węglowy się rozkłada!
Czy wiesz? Kwas węglowy jest odpowiedzialny za musowanie napojów gazowanych! Gdy otwierasz butelkę z napojem gazowanym, zmniejsza się ciśnienie i kwas węglowy zaczyna się rozkładać, uwalniając bąbelki CO₂.

Dysocjacja elektrolityczna kwasów to proces rozpadu cząsteczek kwasu na kationy wodoru (H⁺) i aniony reszty kwasowej w środowisku wodnym. To właśnie dzięki temu kwasy przewodzą prąd elektryczny w roztworach!
Ogólne równanie dysocjacji kwasu można zapisać jako: H₍ₘ₎R ⟶(H₂O) mH⁺ + R^. Liczba m wskazuje, ile kationów wodoru może oddać jedna cząsteczka kwasu. Na przykład:
Dysocjacja jest procesem odwracalnym - kationy i aniony mogą ponownie łączyć się w cząsteczki kwasu. To zjawisko jest podstawą do zrozumienia odczynu roztworów i pH, o którym będziemy się uczyć w kolejnych lekcjach.
Praktyczna wskazówka: Jeśli chcesz szybko określić liczbę kationów wodoru powstających podczas dysocjacji kwasu, po prostu policz atomy wodoru w jego wzorze!
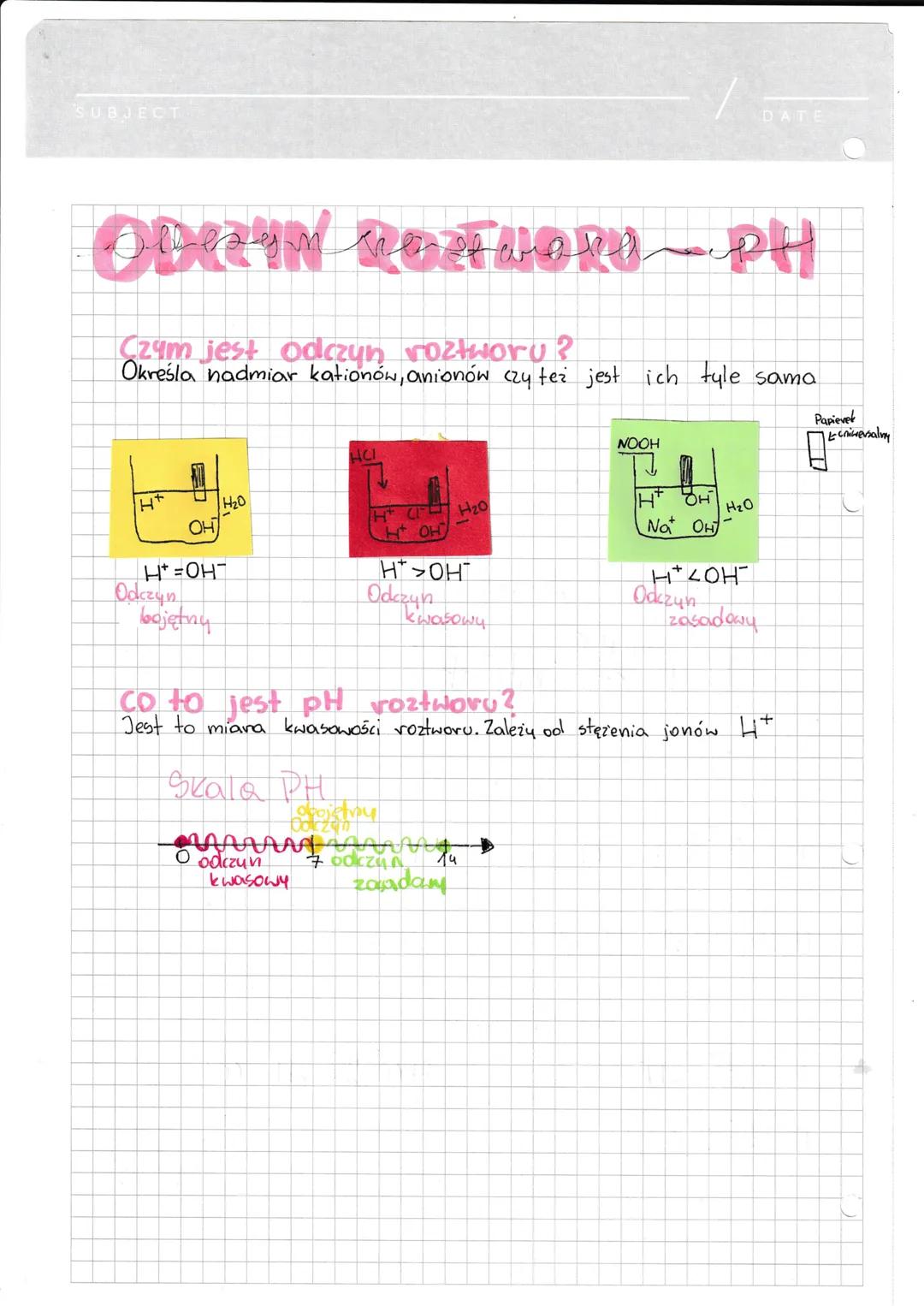
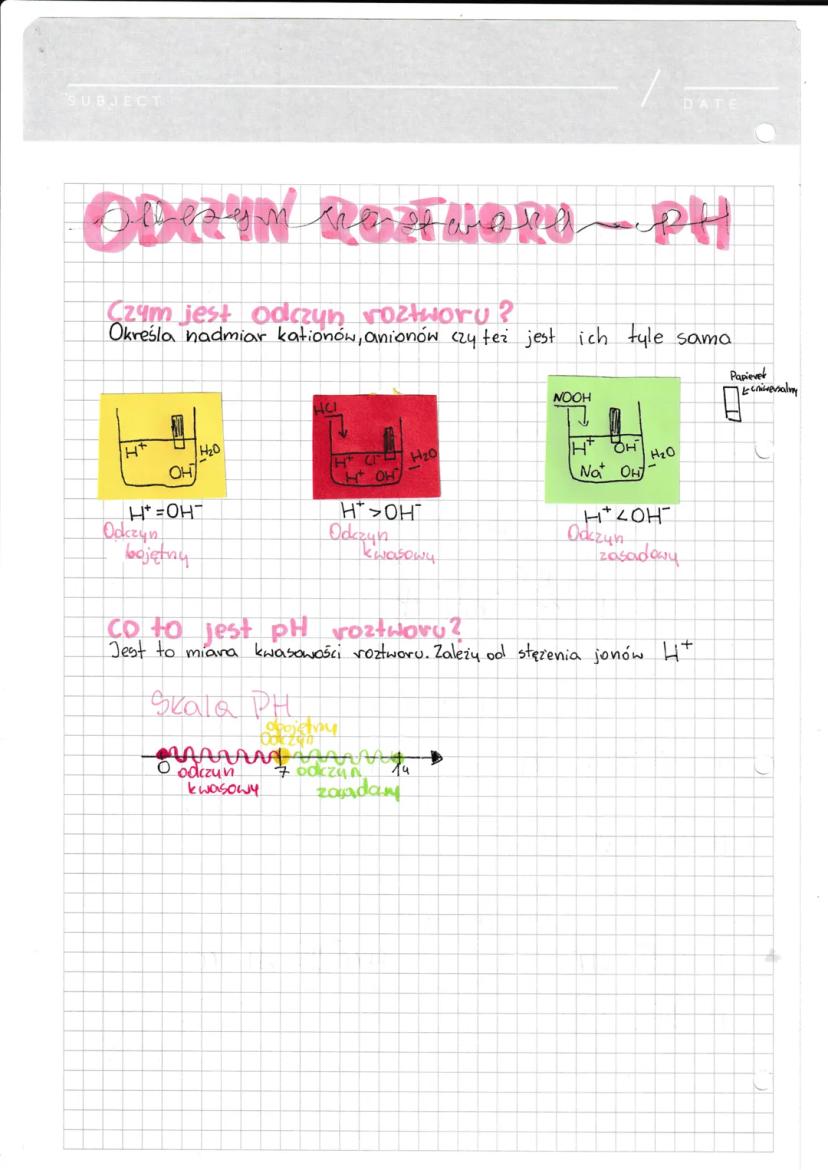
Odczyn roztworu określa, czy w roztworze występuje nadmiar kationów wodorowych (H⁺), anionów wodorotlenowych (OH⁻), czy też jest ich tyle samo. To właśnie stężenie jonów H⁺ decyduje o tym, czy roztwór ma odczyn kwasowy, zasadowy czy obojętny.
W roztworach kwasowych mamy nadmiar jonów H⁺ pochodzących z dysocjacji kwasów. Im więcej jonów wodorowych, tym silniejszy odczyn kwasowy. Kwasy, które łatwo oddają jony H⁺ (dysocjują w dużym stopniu), nazywamy kwasami mocnymi.
W roztworach zasadowych przeważają jony OH⁻. Natomiast w roztworach obojętnych stężenia jonów H⁺ i OH⁻ są równe. Odczyn roztworu możemy zmierzyć za pomocą skali pH lub używając wskaźników, takich jak papierek lakmusowy czy fenoloftaleina.
Eksperyment domowy: Możesz sprawdzić odczyn różnych płynów w domu używając soku z czerwonej kapusty jako wskaźnika! W środowisku kwasowym zmieni kolor na czerwony, a w zasadowym na niebieski lub zielony.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Julianna Nowicka
@juliannanowicka
Kwasy to ważne związki chemiczne, które spotykasz w życiu codziennym - od napojów gazowanych po środki czystości. Zrozumienie ich budowy, właściwości i zastosowań pomoże Ci nie tylko na lekcjach chemii, ale również w rozumieniu świata wokół nas.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwasy mają ogólny wzór H₍ᵐ₎R^m, gdzie H to atomy wodoru, a R to reszta kwasowa. Możemy je podzielić na dwie główne grupy:
Kwasy beztlenowe nie zawierają tlenu w swojej budowie. Przykładami są HCl (kwas chlorowodorowy) i H₂S (kwas siarkowodorowy). Możemy je otrzymać na różne sposoby, np. kwas chlorowodorowy powstaje w reakcji wodoru z chlorem: H₂+Cl₂→2HCl.
Kwasy tlenowe zawierają w swojej budowie tlen. Przykładami są H₂CO₃ (kwas węglowy) i H₂SO₃ (kwas siarkowy IV). Cząsteczki kwasów możemy zapisać używając wzoru sumarycznego (np. HCl) lub strukturalnego, który pokazuje, jak atomy są połączone .
Wskazówka: Zapamiętaj, że kwasy beztlenowe często mają końcówkę "-owodorowy" w nazwie (chlorowodorowy, siarkowodorowy), podczas gdy kwasy tlenowe zazwyczaj kończą się na "-owy" (węglowy, siarkowy).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas siarkowodorowy (H₂S) można otrzymać w reakcji wodoru z siarką: H₂+S→H₂S. Jest to bezbarwna ciecz o charakterystycznym zapachu zgniłych jaj. Co ciekawe, mimo nieprzyjemnego zapachu, znajduje zastosowanie w przemyśle kosmetycznym do produkcji depilatorów chemicznych!
Kwas siarkowy(IV) (H₂SO₃) otrzymujemy w dwóch etapach: najpierw siarka reaguje z tlenem , a następnie dwutlenek siarki z wodą . Jest to bezbarwna ciecz o zapachu siarki, ale bardzo nietrwała - łatwo się rozkłada.
Wzór sumaryczny pokazuje nam skład kwasu (np. H₂SO₃), natomiast wzór strukturalny pokazuje nam, jak atomy są połączone w cząsteczce. Dzięki temu możemy lepiej zrozumieć właściwości kwasów.
Ciekawostka: Kwas siarkowodorowy jest tak wrażliwy na zapach, że ludzie wyczuwają go już w stężeniach kilku cząsteczek na milion! To naturalny mechanizm ostrzegawczy przed tą trującą substancją.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas azotowy(V) (HNO₃) otrzymujemy w reakcji N₂O₅+H₂O→2HNO₃. Jest to bezbarwna ciecz, gęstsza od wody, o ostrym zapachu. Ten żrący kwas powoduje żółknięcie białek przy kontakcie. Mimo niebezpiecznych właściwości jest szeroko stosowany - od produkcji perfum po paliwa rakietowe!
Kwas fosforowy(V) (H₃PO₄) powstaje w dwuetapowej reakcji: 4P+5O₂→P₄O₁₀ a następnie P₄O₁₀+6H₂O→4H₃PO₄. W przeciwieństwie do większości kwasów występuje jako substancja stała - bezbarwne kryształy dobrze rozpuszczalne w wodzie.
Pamiętaj, że każdy z tych kwasów ma swoją charakterystyczną budowę pokazaną przez wzór strukturalny. Na przykład w H₃PO₄ mamy centralny atom fosforu połączony z czterema atomami tlenu, a trzy z nich są dodatkowo połączone z atomami wodoru.
Uważaj! Większość kwasów ma właściwości żrące i może spowodować poważne oparzenia. W laboratorium zawsze używaj okularów ochronnych i rękawic gdy pracujesz z kwasami!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas siarkowy(VI) (H₂SO₄) to jeden z najważniejszych kwasów w przemyśle. Otrzymujemy go w trzech etapach: S+O₂→SO₂, SO₂+O₂→2SO₃, SO₃+H₂O→H₂SO₄. Jest bezbarwną, bezwonną cieczą gęstszą od wody, która ma zdolność zwęglania substancji organicznych.
Kwas siarkowy(VI) jest szeroko stosowany w produkcji nawozów sztucznych i w przemyśle chemicznym. Możesz go spotkać również w akumulatorach samochodowych! Jego wzór strukturalny H-O-S₂-O-H pokazuje, że siarka jest połączona z czterema atomami tlenu.
Kwas węglowy (H₂CO₃) powstaje w reakcji CO₂+H₂O→H₂CO₃. To bezbarwna ciecz bez zapachu, ale bardzo nietrwała - łatwo rozpada się na wodę i dwutlenek węgla. Właśnie dlatego napoje gazowane "uciekają" gdy stoją otwarte - kwas węglowy się rozkłada!
Czy wiesz? Kwas węglowy jest odpowiedzialny za musowanie napojów gazowanych! Gdy otwierasz butelkę z napojem gazowanym, zmniejsza się ciśnienie i kwas węglowy zaczyna się rozkładać, uwalniając bąbelki CO₂.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dysocjacja elektrolityczna kwasów to proces rozpadu cząsteczek kwasu na kationy wodoru (H⁺) i aniony reszty kwasowej w środowisku wodnym. To właśnie dzięki temu kwasy przewodzą prąd elektryczny w roztworach!
Ogólne równanie dysocjacji kwasu można zapisać jako: H₍ₘ₎R ⟶(H₂O) mH⁺ + R^. Liczba m wskazuje, ile kationów wodoru może oddać jedna cząsteczka kwasu. Na przykład:
Dysocjacja jest procesem odwracalnym - kationy i aniony mogą ponownie łączyć się w cząsteczki kwasu. To zjawisko jest podstawą do zrozumienia odczynu roztworów i pH, o którym będziemy się uczyć w kolejnych lekcjach.
Praktyczna wskazówka: Jeśli chcesz szybko określić liczbę kationów wodoru powstających podczas dysocjacji kwasu, po prostu policz atomy wodoru w jego wzorze!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Odczyn roztworu określa, czy w roztworze występuje nadmiar kationów wodorowych (H⁺), anionów wodorotlenowych (OH⁻), czy też jest ich tyle samo. To właśnie stężenie jonów H⁺ decyduje o tym, czy roztwór ma odczyn kwasowy, zasadowy czy obojętny.
W roztworach kwasowych mamy nadmiar jonów H⁺ pochodzących z dysocjacji kwasów. Im więcej jonów wodorowych, tym silniejszy odczyn kwasowy. Kwasy, które łatwo oddają jony H⁺ (dysocjują w dużym stopniu), nazywamy kwasami mocnymi.
W roztworach zasadowych przeważają jony OH⁻. Natomiast w roztworach obojętnych stężenia jonów H⁺ i OH⁻ są równe. Odczyn roztworu możemy zmierzyć za pomocą skali pH lub używając wskaźników, takich jak papierek lakmusowy czy fenoloftaleina.
Eksperyment domowy: Możesz sprawdzić odczyn różnych płynów w domu używając soku z czerwonej kapusty jako wskaźnika! W środowisku kwasowym zmieni kolor na czerwony, a w zasadowym na niebieski lub zielony.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
3
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS