Dysocjacja elektrolityczna to jeden z najważniejszych procesów zachodzących w roztworach.... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
885
•
Zaktualizowano May 13, 2026
•
bita.śmietana
@karolina.l
Dysocjacja elektrolityczna to jeden z najważniejszych procesów zachodzących w roztworach.... Pokaż więcej







Stopień dysocjacji elektrolitycznej to parametr, który mówi nam, jaka część substancji rozpada się na jony. Określamy go jako stosunek liczby moli substancji, która uległa rozpadowi na jony, do całkowitej liczby moli substancji wprowadzonej do roztworu.
Stopień dysocjacji wyrażamy wzorem: α = nₛ/nₚ lub α = · 100%, gdzie:
⚡ Wskazówka: Stopień dysocjacji elektrolitycznej jest miarą mocy elektrolitu - im wyższa wartość α, tym mocniejszy elektrolit!

Mocne elektrolity, jak kwas chlorowodorowy (HCl), mają duże wartości stopnia dysocjacji - od kilkudziesięciu do nawet 100%. To oznacza, że prawie wszystkie ich cząsteczki w roztworze rozpadają się na jony.
Słabe elektrolity, jak kwas octowy (CH₃COOH), charakteryzują się małymi wartościami stopnia dysocjacji, zwykle poniżej 5%. Tylko niewielka część ich cząsteczek ulega dysocjacji. Pozostałe elektrolity, których α mieści się między tymi zakresami, nazywamy elektrolitami średniej mocy.
Dla słabych kwasów jednoprotonowych stopień dysocjacji można obliczyć ze wzoru: α = [H⁺]/Cₐ lub α = · 100%, gdzie [H⁺] to stężenie jonów wodorowych, a Cₐ to całkowite stężenie kwasu.
💡 Ciekawostka: W roztworze HCl o 25 cząsteczkach wszystkie 25 dysocjują (α = 100%), podczas gdy w roztworze CH₃COOH o tych samych wymiarach tylko 1 z 25 cząsteczek rozpada się na jony (α = 4%).

Dla słabych zasad stopień dysocjacji wyraża się wzorem: α = [OH⁻]/Cᵦ lub α = · 100%, gdzie [OH⁻] to stężenie jonów wodorotlenkowych, a Cᵦ to całkowite stężenie zasady.
Na wartość stopnia dysocjacji elektrolitycznej wpływa kilka kluczowych czynników:
🧪 Eksperyment: Sprawdź sam! Rozcieńczając roztwór słabego kwasu (np. octowego), możesz zaobserwować wzrost jego stopnia dysocjacji.

Stała dysocjacji elektrolitycznej (K) to stała równowagi chemicznej procesu dysocjacji. Jest równa stosunkowi iloczynu stężeń jonów powstałych podczas dysocjacji do stężenia cząsteczek niezdysocjowanych.
Dysocjacja elektrolityczna słabych elektrolitów jest przykładem reakcji odwracalnej, prowadzącej do ustalenia się równowagi dynamicznej. W tym stanie szybkości rozpadu cząsteczek na jony i łączenia się jonów w cząsteczki są równe.
Kwas octowy (etanowy) jest przykładem słabego kwasu jednoprotonowego, który ulega dysocjacji według równania: CH₃COOH + H₂O ⇄ CH₃COO⁻ + H₃O⁺
Stała dysocjacji tego kwasu wyrażona jest wzorem: Kₐ = ([H⁺]·[CH₃COO⁻])/[CH₃COOH] = [H⁺]/
🔑 Kluczowa różnica: W przeciwieństwie do stopnia dysocjacji, stała dysocjacji jest stałą równowagi i nie zależy od stężenia roztworu, tylko od temperatury!
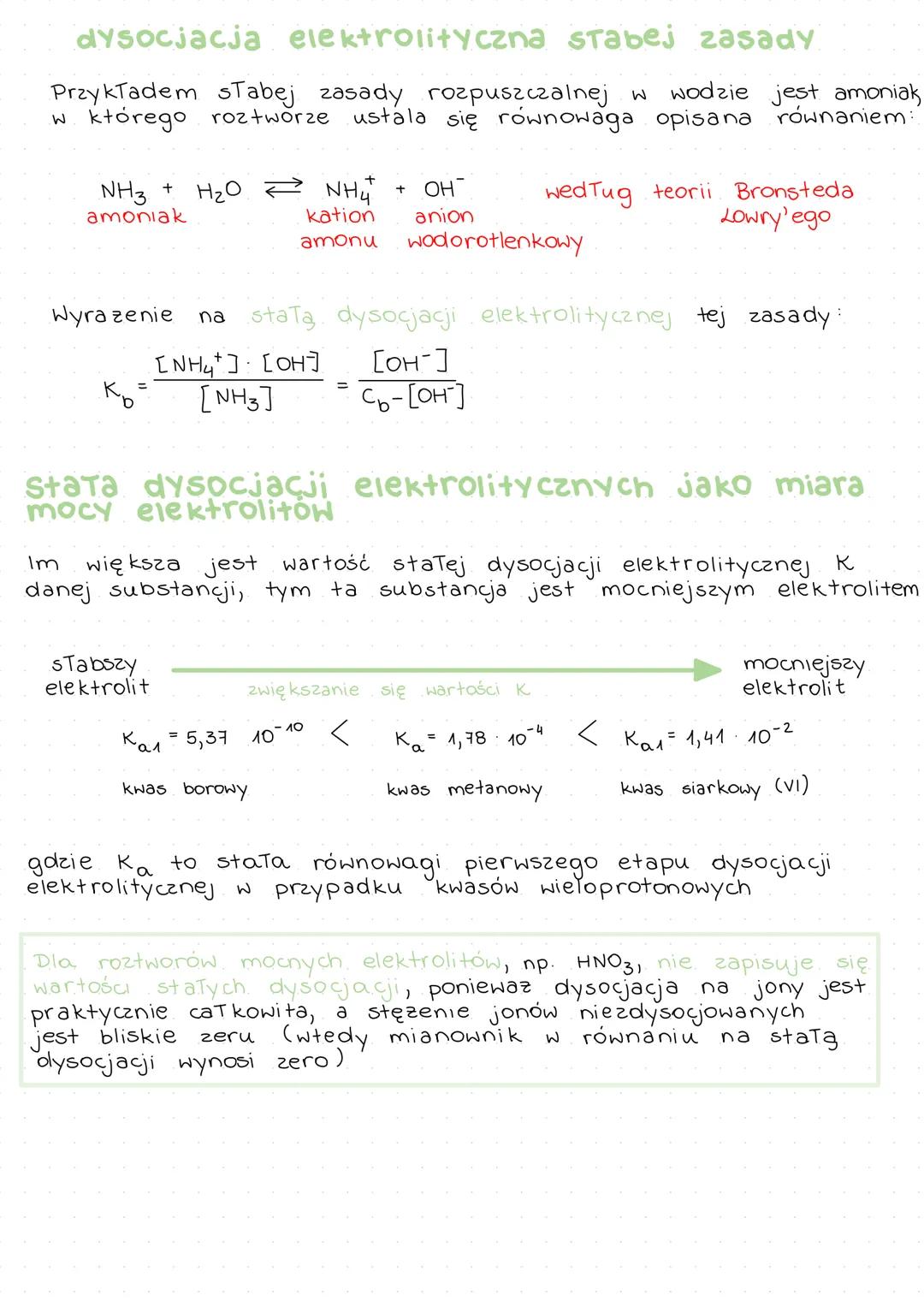
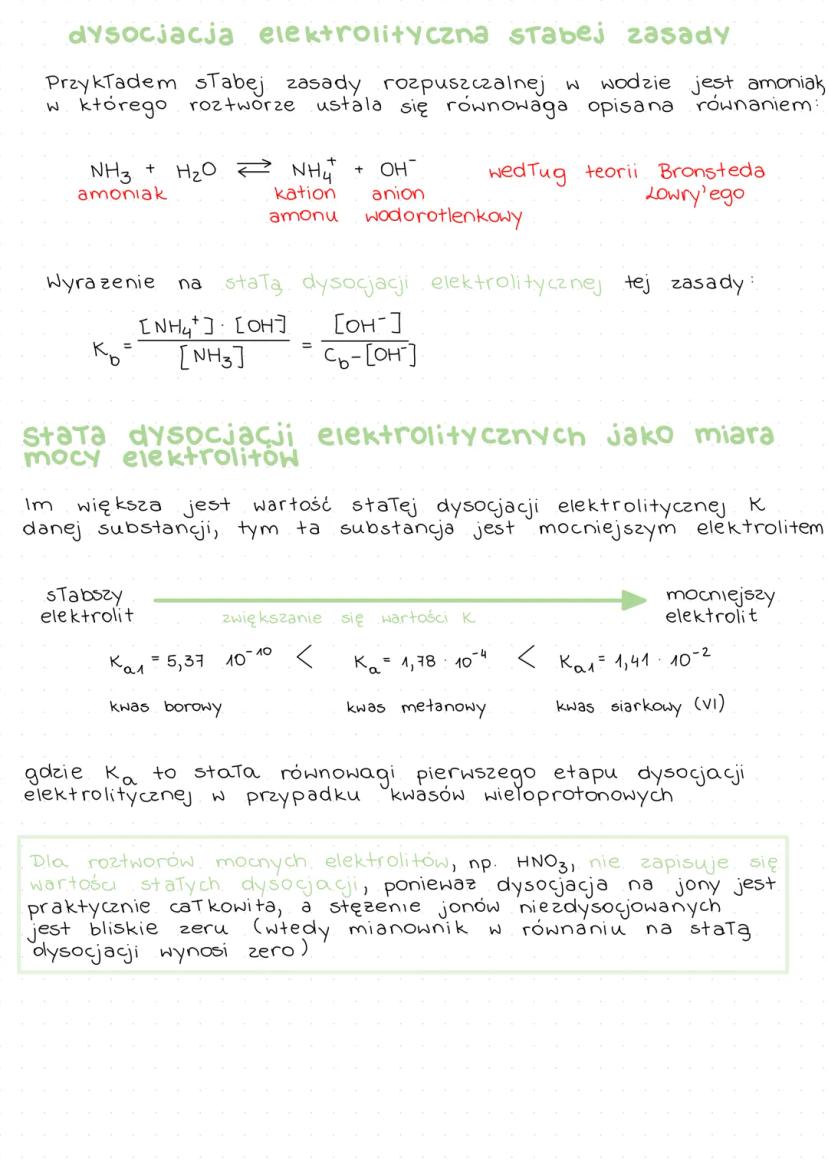
Amoniak (NH₃) jest przykładem słabej zasady rozpuszczalnej w wodzie. W jego roztworze ustala się równowaga: NH₃ + H₂O ⇄ NH₄⁺ + OH⁻
Stałą dysocjacji tej zasady wyrażamy wzorem: Kᵦ = ([NH₄⁺]·[OH⁻])/[NH₃] = [OH⁻]/
Wartość stałej dysocjacji elektrolitycznej K jest miarą mocy elektrolitu - im większa wartość K, tym substancja jest mocniejszym elektrolitem. Na przykład:
Kₐ₁ = 5,37·10⁻¹⁰ (kwas borowy) < Kₐ₁ = 1,78·10⁻⁴ (kwas metanowy) < Kₐ₁ = 1,41·10⁻² (kwas siarkowy(VI))
Dla mocnych elektrolitów, takich jak HNO₃, nie podaje się wartości stałych dysocjacji, ponieważ dysocjacja jest praktycznie całkowita, a stężenie cząsteczek niezdysocjowanych jest bliskie zeru.
⭐ Zapamiętaj: Im większa wartość K, tym mocniejszy elektrolit, niezależnie od jego stężenia!

Wartość stałej dysocjacji elektrolitycznej K zależy od:
W przeciwieństwie do stopnia dysocjacji α, wartość K nie zależy od początkowego stężenia substancji! Stała dysocjacji ma stałą wartość w określonej temperaturze.
Ze względu na małe wartości stałej dysocjacji dla słabych elektrolitów, często przedstawia się je jako ujemne logarytmy dziesiętne: pKₐ = -log Kₐ pKᵦ = -log Kᵦ
Prawo rozcieńczeń Ostwalda wiąże stałą dysocjacji elektrolitycznej K, stopień dysocjacji elektrolitycznej α i stężenie molowe elektrolitu C: K = (α²·C)/(1-α)
gdzie:
📝 Praktyczna rada: Kiedy stopień dysocjacji jest niewielki (α < 0,05), możesz uprościć obliczenia używając przybliżonego wzoru K = α²·C.

Gdy stopień dysocjacji α jest mniejszy od 0,05 , możemy stosować uproszczone zależności:
K = α²·C Kₐ = [H⁺]²/Cₐ Kᵦ = [OH⁻]²/Cᵦ
Te wzory znacznie ułatwiają obliczenia przy pracy ze słabymi elektrolitami.
Zależność stopnia dysocjacji α od stężenia powoduje, że nie jest on tak dobrą miarą mocy elektrolitu jak stałe dysocjacji Kₐ i Kᵦ. Stałe dysocjacji zależą tylko od temperatury, dlatego lepiej charakteryzują właściwości kwasowo-zasadowe substancji.
🧠 Ważna zasada: Stała dysocjacji elektrolitycznej K jest lepszym wskaźnikiem mocy elektrolitu niż stopień dysocjacji α, ponieważ nie zależy od stężenia roztworu!
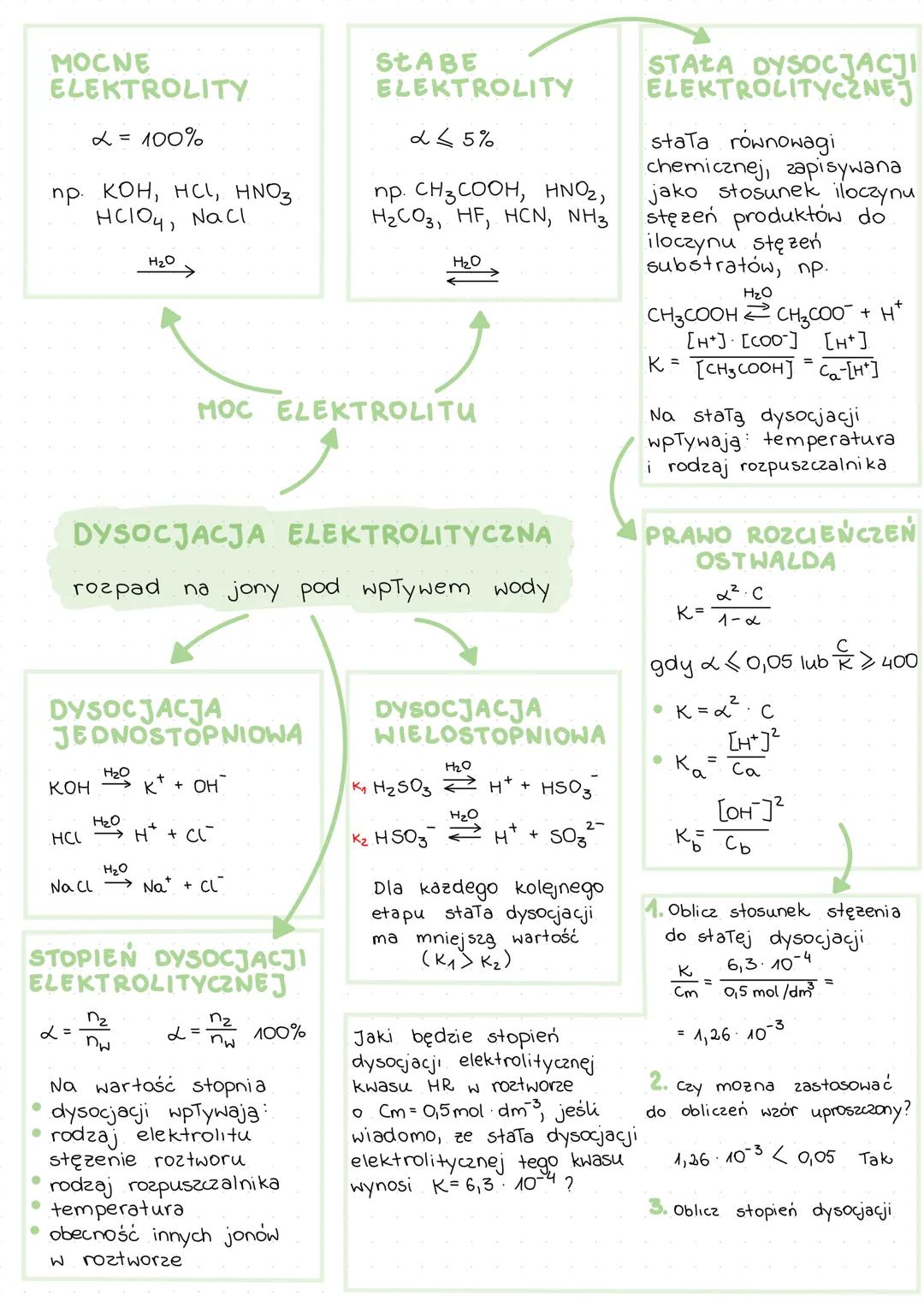
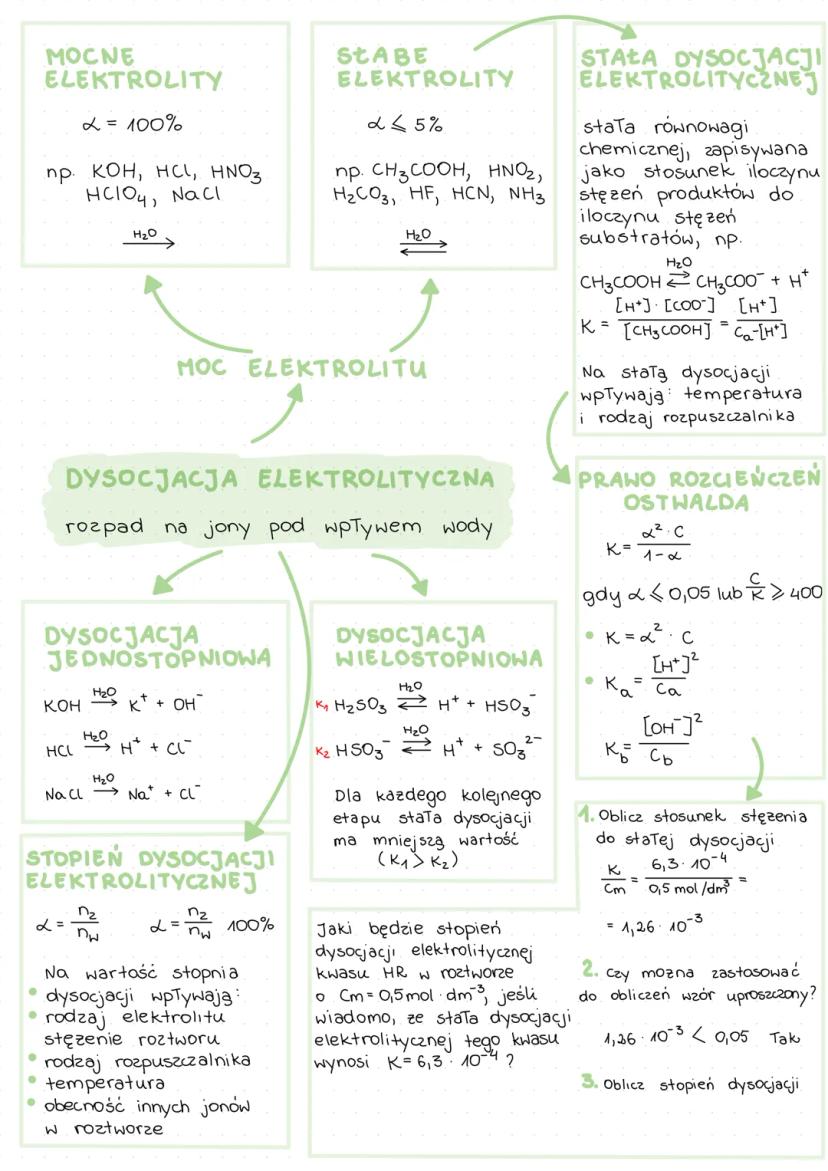
Dysocjacja elektrolityczna to rozpad substancji na jony pod wpływem wody. Elektrolity dzielimy na:
Dysocjacja może być:
Dla każdego kolejnego etapu dysocjacji wielostopniowej stała dysocjacji ma coraz mniejszą wartość (K₁ > K₂).
Prawo rozcieńczeń Ostwalda pozwala obliczyć stopień dysocjacji na podstawie stałej dysocjacji i stężenia roztworu. Gdy α << 0,05 lub C/K ≥ 400, możemy stosować uproszczone wzory:
💼 Zastosowanie praktyczne: Podczas rozwiązywania zadań sprawdź zawsze, czy możesz zastosować wzór uproszczony. Oblicz stosunek C/K - jeśli jest większy od 400 (lub α < 0,05), możesz użyć prostszego wzoru!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
bita.śmietana
@karolina.l
Dysocjacja elektrolityczna to jeden z najważniejszych procesów zachodzących w roztworach. To kluczowe zjawisko, w którym substancje rozpuszczone w wodzie rozpadają się na jony, umożliwiając przewodzenie prądu elektrycznego. Zrozumienie tego procesu jest niezbędne do pracy z kwasami, zasadami i solami.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Stopień dysocjacji elektrolitycznej to parametr, który mówi nam, jaka część substancji rozpada się na jony. Określamy go jako stosunek liczby moli substancji, która uległa rozpadowi na jony, do całkowitej liczby moli substancji wprowadzonej do roztworu.
Stopień dysocjacji wyrażamy wzorem: α = nₛ/nₚ lub α = · 100%, gdzie:
⚡ Wskazówka: Stopień dysocjacji elektrolitycznej jest miarą mocy elektrolitu - im wyższa wartość α, tym mocniejszy elektrolit!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Mocne elektrolity, jak kwas chlorowodorowy (HCl), mają duże wartości stopnia dysocjacji - od kilkudziesięciu do nawet 100%. To oznacza, że prawie wszystkie ich cząsteczki w roztworze rozpadają się na jony.
Słabe elektrolity, jak kwas octowy (CH₃COOH), charakteryzują się małymi wartościami stopnia dysocjacji, zwykle poniżej 5%. Tylko niewielka część ich cząsteczek ulega dysocjacji. Pozostałe elektrolity, których α mieści się między tymi zakresami, nazywamy elektrolitami średniej mocy.
Dla słabych kwasów jednoprotonowych stopień dysocjacji można obliczyć ze wzoru: α = [H⁺]/Cₐ lub α = · 100%, gdzie [H⁺] to stężenie jonów wodorowych, a Cₐ to całkowite stężenie kwasu.
💡 Ciekawostka: W roztworze HCl o 25 cząsteczkach wszystkie 25 dysocjują (α = 100%), podczas gdy w roztworze CH₃COOH o tych samych wymiarach tylko 1 z 25 cząsteczek rozpada się na jony (α = 4%).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dla słabych zasad stopień dysocjacji wyraża się wzorem: α = [OH⁻]/Cᵦ lub α = · 100%, gdzie [OH⁻] to stężenie jonów wodorotlenkowych, a Cᵦ to całkowite stężenie zasady.
Na wartość stopnia dysocjacji elektrolitycznej wpływa kilka kluczowych czynników:
🧪 Eksperyment: Sprawdź sam! Rozcieńczając roztwór słabego kwasu (np. octowego), możesz zaobserwować wzrost jego stopnia dysocjacji.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Stała dysocjacji elektrolitycznej (K) to stała równowagi chemicznej procesu dysocjacji. Jest równa stosunkowi iloczynu stężeń jonów powstałych podczas dysocjacji do stężenia cząsteczek niezdysocjowanych.
Dysocjacja elektrolityczna słabych elektrolitów jest przykładem reakcji odwracalnej, prowadzącej do ustalenia się równowagi dynamicznej. W tym stanie szybkości rozpadu cząsteczek na jony i łączenia się jonów w cząsteczki są równe.
Kwas octowy (etanowy) jest przykładem słabego kwasu jednoprotonowego, który ulega dysocjacji według równania: CH₃COOH + H₂O ⇄ CH₃COO⁻ + H₃O⁺
Stała dysocjacji tego kwasu wyrażona jest wzorem: Kₐ = ([H⁺]·[CH₃COO⁻])/[CH₃COOH] = [H⁺]/
🔑 Kluczowa różnica: W przeciwieństwie do stopnia dysocjacji, stała dysocjacji jest stałą równowagi i nie zależy od stężenia roztworu, tylko od temperatury!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Amoniak (NH₃) jest przykładem słabej zasady rozpuszczalnej w wodzie. W jego roztworze ustala się równowaga: NH₃ + H₂O ⇄ NH₄⁺ + OH⁻
Stałą dysocjacji tej zasady wyrażamy wzorem: Kᵦ = ([NH₄⁺]·[OH⁻])/[NH₃] = [OH⁻]/
Wartość stałej dysocjacji elektrolitycznej K jest miarą mocy elektrolitu - im większa wartość K, tym substancja jest mocniejszym elektrolitem. Na przykład:
Kₐ₁ = 5,37·10⁻¹⁰ (kwas borowy) < Kₐ₁ = 1,78·10⁻⁴ (kwas metanowy) < Kₐ₁ = 1,41·10⁻² (kwas siarkowy(VI))
Dla mocnych elektrolitów, takich jak HNO₃, nie podaje się wartości stałych dysocjacji, ponieważ dysocjacja jest praktycznie całkowita, a stężenie cząsteczek niezdysocjowanych jest bliskie zeru.
⭐ Zapamiętaj: Im większa wartość K, tym mocniejszy elektrolit, niezależnie od jego stężenia!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Wartość stałej dysocjacji elektrolitycznej K zależy od:
W przeciwieństwie do stopnia dysocjacji α, wartość K nie zależy od początkowego stężenia substancji! Stała dysocjacji ma stałą wartość w określonej temperaturze.
Ze względu na małe wartości stałej dysocjacji dla słabych elektrolitów, często przedstawia się je jako ujemne logarytmy dziesiętne: pKₐ = -log Kₐ pKᵦ = -log Kᵦ
Prawo rozcieńczeń Ostwalda wiąże stałą dysocjacji elektrolitycznej K, stopień dysocjacji elektrolitycznej α i stężenie molowe elektrolitu C: K = (α²·C)/(1-α)
gdzie:
📝 Praktyczna rada: Kiedy stopień dysocjacji jest niewielki (α < 0,05), możesz uprościć obliczenia używając przybliżonego wzoru K = α²·C.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Gdy stopień dysocjacji α jest mniejszy od 0,05 , możemy stosować uproszczone zależności:
K = α²·C Kₐ = [H⁺]²/Cₐ Kᵦ = [OH⁻]²/Cᵦ
Te wzory znacznie ułatwiają obliczenia przy pracy ze słabymi elektrolitami.
Zależność stopnia dysocjacji α od stężenia powoduje, że nie jest on tak dobrą miarą mocy elektrolitu jak stałe dysocjacji Kₐ i Kᵦ. Stałe dysocjacji zależą tylko od temperatury, dlatego lepiej charakteryzują właściwości kwasowo-zasadowe substancji.
🧠 Ważna zasada: Stała dysocjacji elektrolitycznej K jest lepszym wskaźnikiem mocy elektrolitu niż stopień dysocjacji α, ponieważ nie zależy od stężenia roztworu!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dysocjacja elektrolityczna to rozpad substancji na jony pod wpływem wody. Elektrolity dzielimy na:
Dysocjacja może być:
Dla każdego kolejnego etapu dysocjacji wielostopniowej stała dysocjacji ma coraz mniejszą wartość (K₁ > K₂).
Prawo rozcieńczeń Ostwalda pozwala obliczyć stopień dysocjacji na podstawie stałej dysocjacji i stężenia roztworu. Gdy α << 0,05 lub C/K ≥ 400, możemy stosować uproszczone wzory:
💼 Zastosowanie praktyczne: Podczas rozwiązywania zadań sprawdź zawsze, czy możesz zastosować wzór uproszczony. Oblicz stosunek C/K - jeśli jest większy od 400 (lub α < 0,05), możesz użyć prostszego wzoru!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
23
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS