Chemia otacza nas wszędzie, ale nie zawsze zdajemy sobie z... Pokaż więcej
Chemiczne substancje i ich przemiany: notatki







Substancje i ich właściwości
Czy zastanawiałeś się kiedyś, z czego tak naprawdę składają się przedmioty wokół ciebie? Ciało fizyczne to konkretny przedmiot, który widzisz (np. drut miedziany), natomiast substancja to materiał, z którego ten przedmiot jest wykonany (np. miedź).
Każda substancja ma charakterystyczne właściwości, które pozwalają ją odróżnić od innych. Właściwości dzielimy na:
- fizyczne - stan skupienia, barwa, połysk, gęstość, twardość, rozpuszczalność, temperatura wrzenia i topnienia
- chemiczne - zapach, smak, palność i aktywność chemiczna
Właściwości substancji badamy na różne sposoby. Możemy wykorzystać zmysły (wzrok, dotyk, węch, smak), przeprowadzić doświadczenia chemiczne lub odczytać informacje z tabel. Niektóre substancje mogą być niebezpieczne, dlatego oznacza się je specjalnymi piktogramami ostrzegawczymi.
💡 Ciekawostka: Nie wszystkie właściwości substancji możemy zbadać bezpośrednio zmysłami! Niektóre substancje chemiczne są bardzo niebezpieczne, dlatego nigdy nie próbuj ich smakować ani wąchać bez nadzoru nauczyciela.
Gęstość i rodzaje przemian
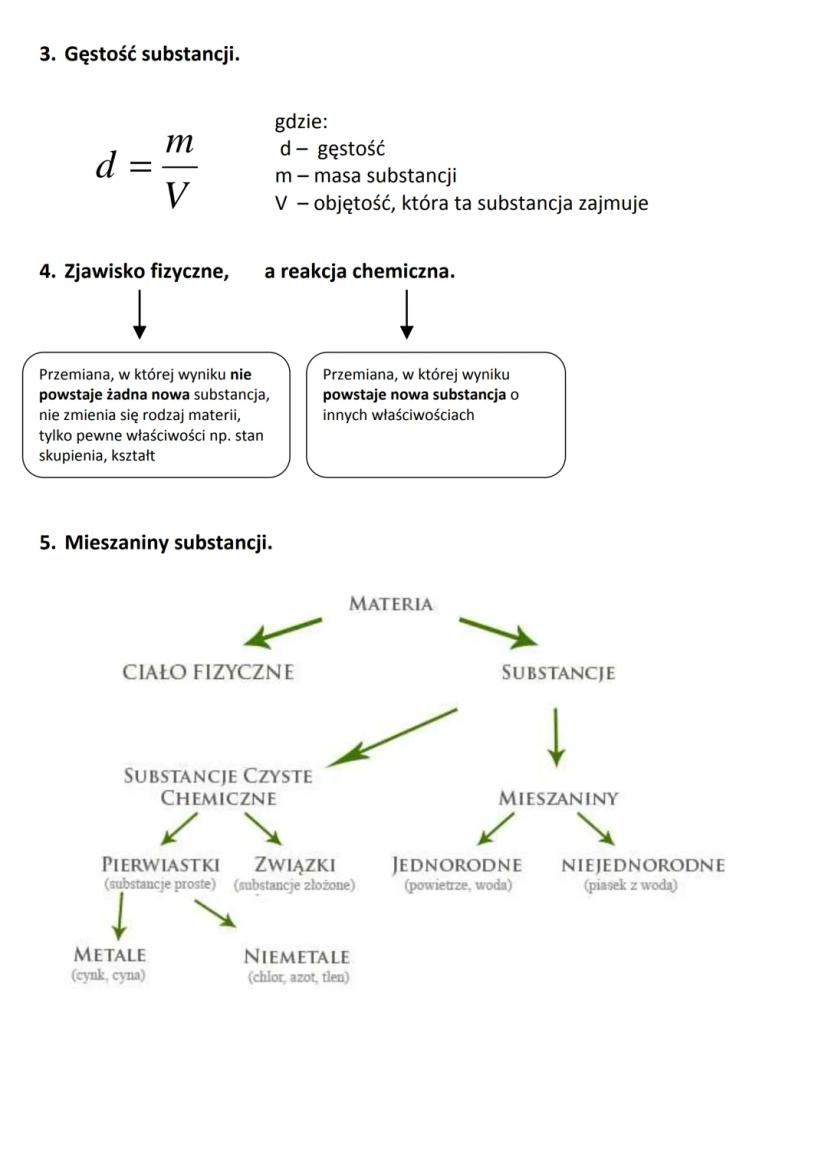
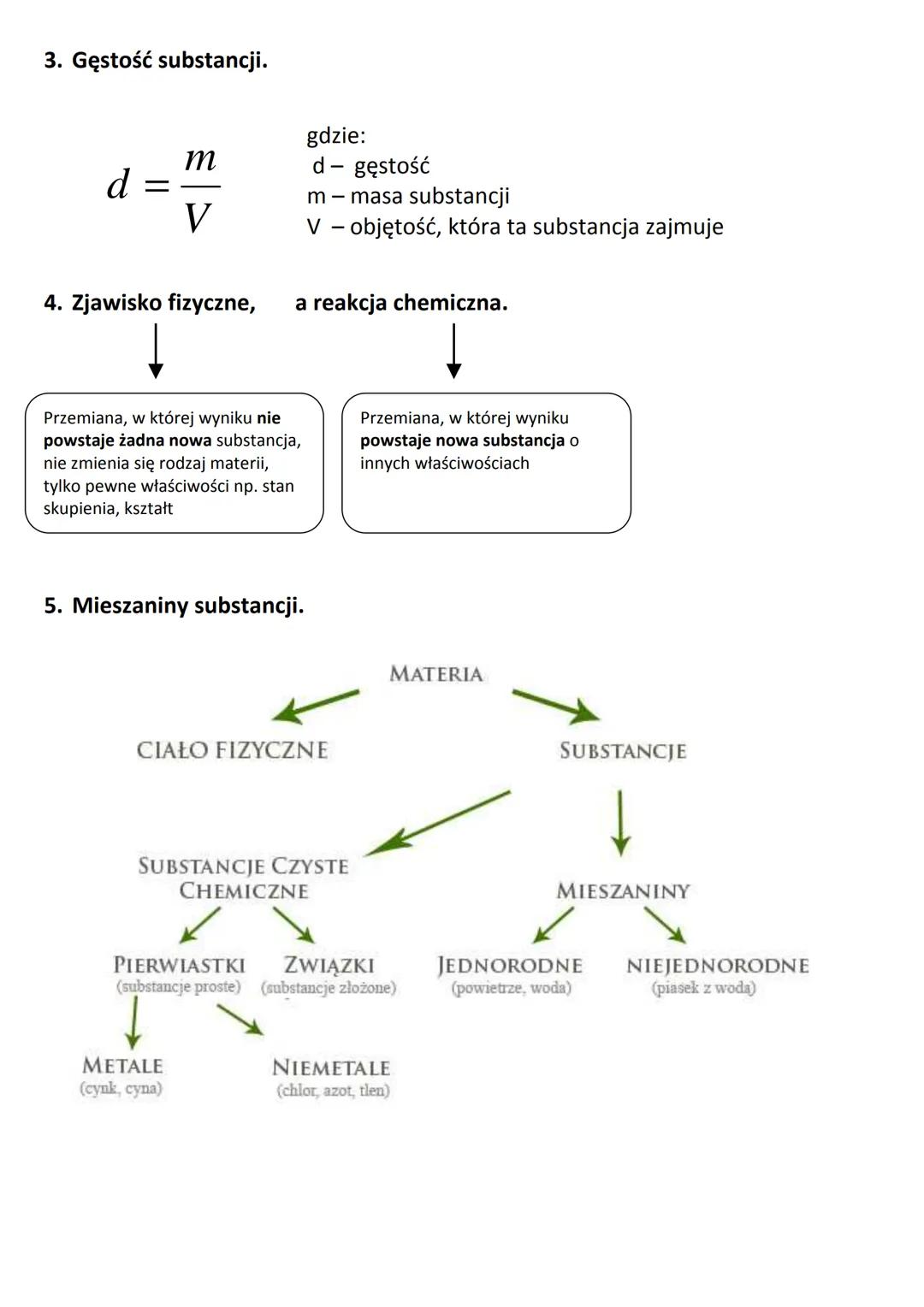
Gęstość to jedna z najważniejszych właściwości substancji. Obliczamy ją dzieląc masę substancji przez zajmowaną przez nią objętość: d = m/V. Ta właściwość pomaga nam zrozumieć, dlaczego niektóre przedmioty toną w wodzie, a inne unoszą się na jej powierzchni.
W przyrodzie zachodzą dwa rodzaje przemian:
- Zjawisko fizyczne - nie powstaje nowa substancja, zmienia się tylko kształt, stan skupienia lub inne właściwości fizyczne (np. topnienie lodu)
- Reakcja chemiczna - powstaje nowa substancja o innych właściwościach (np. spalanie drewna)
Substancje dzielimy na substancje czyste i mieszaniny. Substancje czyste to:
- Pierwiastki (substancje proste) - np. metale jak cynk i niemetale jak tlen
- Związki chemiczne (substancje złożone) - np. woda
Mieszaniny natomiast mogą być:
- Jednorodne - o jednakowym składzie w całej objętości (np. powietrze)
- Niejednorodne - o niejednakowym składzie (np. piasek z wodą)
🔍 Ważne: Mieszaniny można rozdzielić metodami fizycznymi, natomiast związki chemiczne można rozdzielić tylko za pomocą reakcji chemicznych!

Sposoby rozdzielania mieszanin
Czy wiesz, że istnieje wiele sposobów na rozdzielanie mieszanin? Poznanie ich przyda ci się nie tylko w laboratorium, ale też w codziennym życiu!
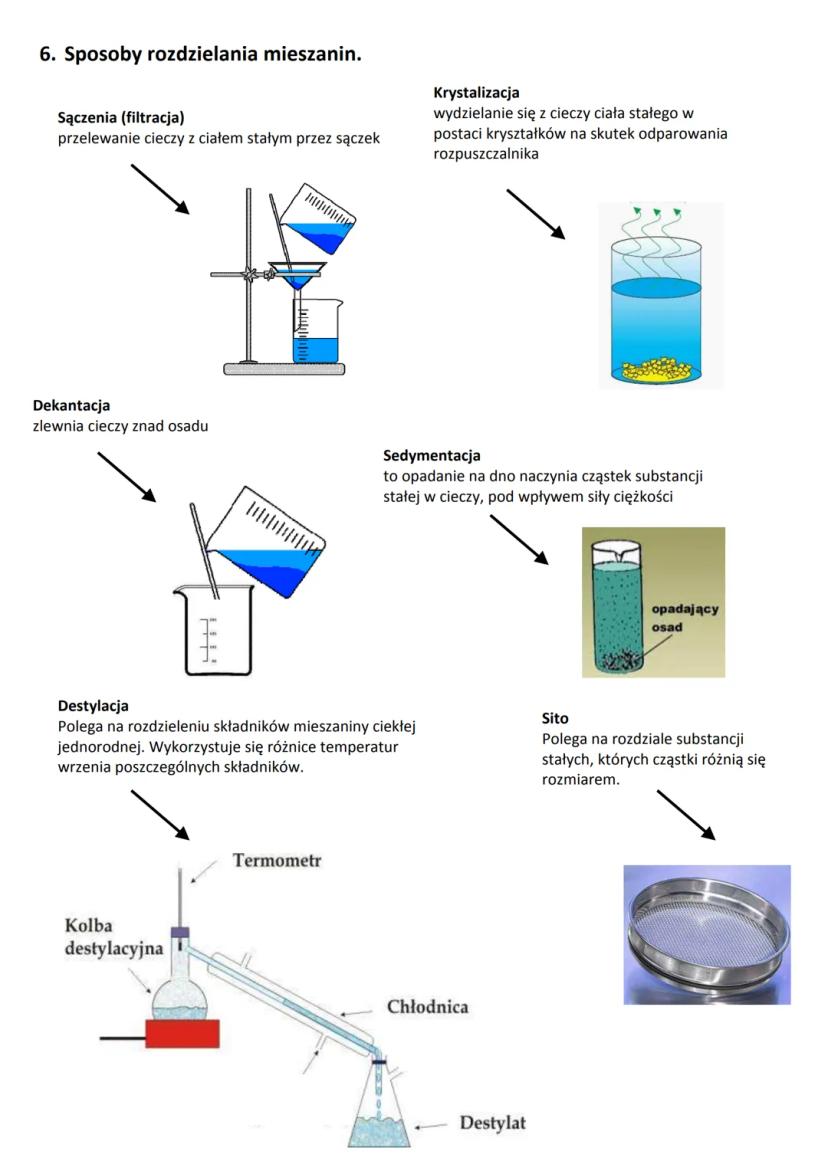
Sączenie (filtracja) - to przelewanie mieszaniny cieczy z ciałem stałym przez sączek, który zatrzymuje ciało stałe. Działa podobnie jak sito kuchenne, gdy odcedzasz makaron!
Sedymentacja i dekantacja - najpierw czekamy, aż cząstki ciała stałego opadną na dno (sedymentacja), a potem ostrożnie zlewamy ciecz znad osadu (dekantacja).
Krystalizacja - to proces, w którym substancja rozpuszczona wydziela się z roztworu w postaci kryształków, gdy rozpuszczalnik odparowuje.
Destylacja - służy do rozdzielania mieszanin cieczy o różnych temperaturach wrzenia. Wykorzystuje się specjalną aparaturę z kolbą destylacyjną i chłodnicą.
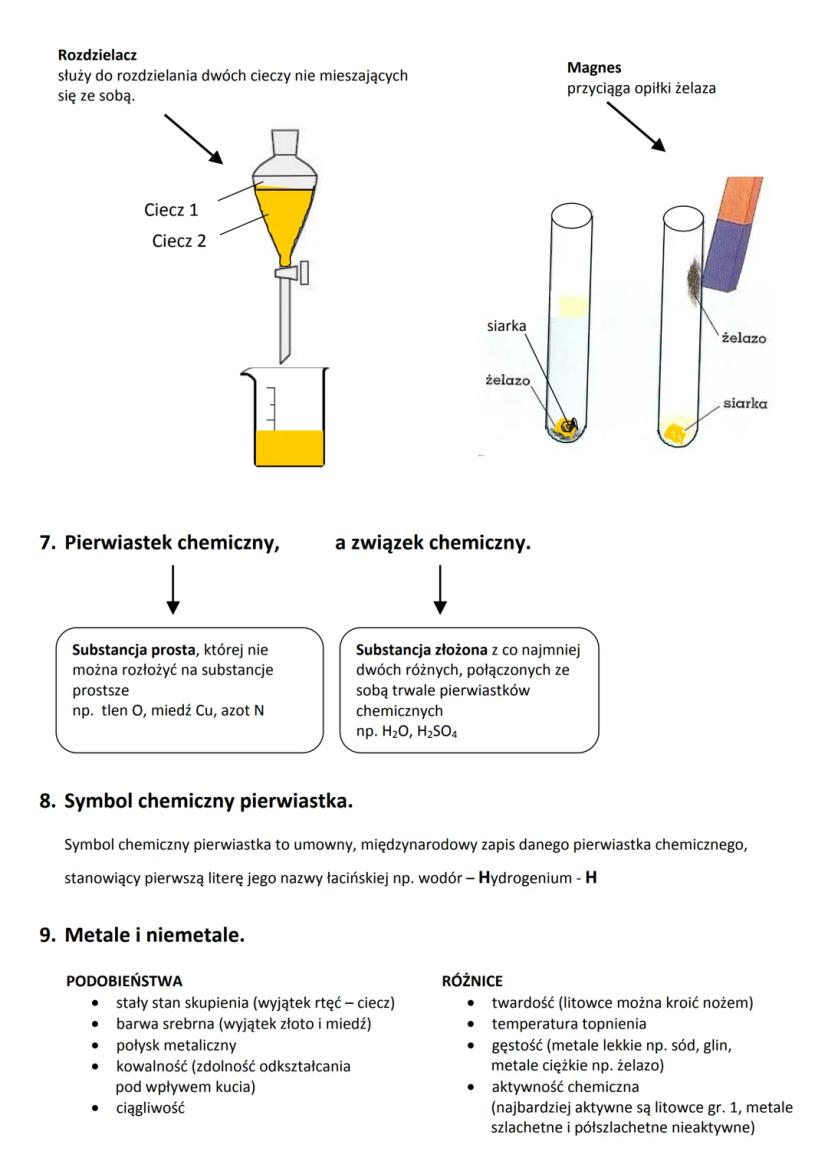
Inne metody to przesiewanie (rozdzielanie ciał stałych o różnej wielkości cząstek) oraz użycie magnesu (przyciąganie substancji magnetycznych, np. żelaza).
🧪 Eksperyment domowy: Spróbuj rozdzielić wodę i sól kuchenną przez odparowanie wody. Zobaczysz krystalizację soli na dnie naczynia!
Pierwiastki, związki chemiczne i symbole
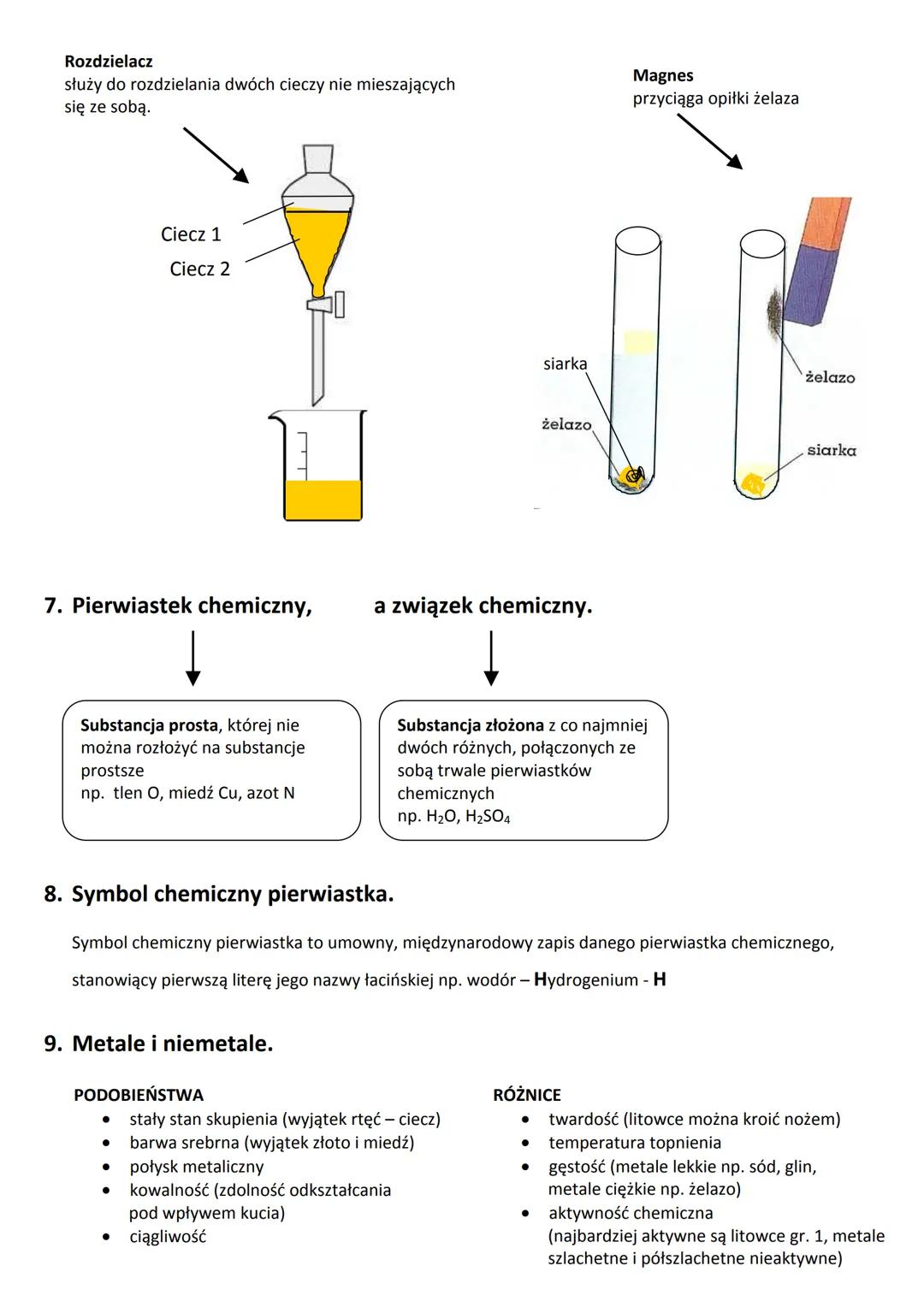
Pierwiastek chemiczny to substancja prosta, której nie można rozłożyć na prostsze substancje (np. tlen O, miedź Cu). Związek chemiczny natomiast składa się z co najmniej dwóch różnych pierwiastków połączonych ze sobą (np. woda H₂O).
Każdy pierwiastek ma swój symbol chemiczny - to skrót pochodzący od jego łacińskiej nazwy. Symbol składa się z jednej dużej litery lub z dużej i małej litery .
Metale i niemetale to dwie główne grupy pierwiastków. Metale najczęściej:
- występują w stałym stanie skupienia (wyjątek to rtęć)
- mają srebrzystą barwę i metaliczny połysk
- są kowalne i ciągliwe (można je kuć i rozciągać)
Metale różnią się między sobą twardością, temperaturą topnienia i aktywnością chemiczną. Najbardziej aktywne są litowce (grupa 1), najmniej aktywne są metale szlachetne (np. złoto, platyna).
🔎 Ciekawostka: Czy wiesz, że 80% pierwiastków to metale? Znajdują się po lewej stronie układu okresowego, a niemetale po prawej.

Stopy metali i korozja
Stopy metali to mieszaniny jednorodne różnych metali stopionych w odpowiednich proporcjach. Znasz je lepiej niż myślisz - używasz ich codziennie!
Popularne stopy to:
- mosiądz - klamki, okucia, ozdoby
- brąz - monety, rzeźby
- duraluminium - samoloty, części maszyn
- stal - wykorzystywana w prawie każdej gałęzi przemysłu
Metale ulegają korozji - procesowi niszczenia pod wpływem tlenu, wody, kwasów, zasad i soli. Najbardziej znanym przykładem korozji jest rdzewienie żelaza. Aby chronić metale przed korozją, stosujemy:
- pokrywanie powłokami ochronnymi (cynkowanie, chromowanie, malowanie)
- osłabianie agresywności środowiska
- stosowanie stopów odpornych na korozję
Powietrze to mieszanina gazów, w której przeważa azot (78%) i tlen (21%). Pozostały 1% to głównie gazy szlachetne (argon). Zawartość pary wodnej, dwutlenku węgla, ozonu i zanieczyszczeń może się zmieniać.
🛡️ Eksperyment: Porównaj dwa gwoździe - jeden pokryty warstwą farby, drugi niepokryty. Zanurz oba w wodzie na tydzień. Który z nich szybciej zardzewiejr i dlaczego?

Badanie składu powietrza i tlen
Możemy zbadać zawartość tlenu w powietrzu za pomocą prostego doświadczenia. Gdy zapalimy świeczkę pod odwróconym cylindrem w naczyniu z wodą, świeca po pewnym czasie gaśnie, a woda podnosi się w cylindrze. Dzieje się tak, ponieważ tlen zostaje zużyty podczas spalania. Poziom wody wskazuje, że tlen stanowi około 1/5 (21%) objętości powietrza.
Tlen (O₂) to niezwykle ważny pierwiastek dla życia na Ziemi. Jego właściwości fizyczne to:
- stan gazowy w temperaturze pokojowej
- bezbarwność
- słaba rozpuszczalność w wodzie
- brak zapachu
Z punktu widzenia chemii, tlen:
- jest niemetalem
- podtrzymuje spalanie (choć sam się nie pali)
- łączy się z wieloma pierwiastkami, tworząc tlenki
Tlen można otrzymać na kilka sposobów, np. przez rozkład związków bogatych w tlen lub przez elektrolizę wody.
🔥 Uwaga: Spalanie w czystym tlenie jest o wiele gwałtowniejsze niż w powietrzu! Dlatego w laboratoriach i przemyśle trzeba zachować szczególne środki ostrożności przy pracy z czystym tlenem.

Reakcje spalania i znaczenie tlenu
Spalanie to gwałtowne utlenianie (łączenie z tlenem), któremu towarzyszy wydzielanie energii w postaci światła i ciepła. Podczas spalania zachodzą reakcje syntezy:
siarka + tlen → tlenek siarki(IV)
S + O₂ → SO₂
węgiel + tlen → tlenek węgla(IV)
C + O₂ → CO₂
magnez + tlen → tlenek magnezu
2Mg + O₂ → 2MgO
Produkty spalania zależą od tego, co się spala:
- gdy spala się metal, powstaje tlenek metalu (np. MgO)
- gdy spala się niemetal, powstaje tlenek niemetalu (np. CO₂, SO₂)
Tlen ma ogromne znaczenie dla życia i procesów zachodzących na Ziemi:
- jest niezbędny do oddychania organizmów
- umożliwia spalanie (np. w silnikach samochodowych, piecach przemysłowych)
- powoduje wietrzenie skał, rdzewienie metali i butwienie szczątków organicznych
Tlen znajduje szerokie zastosowanie w:
- medycynie (maski tlenowe, butle z tlenem)
- przemyśle
- produkcji kwasów
- technice nurkowej i lotniczej
🌱 Pamiętaj: To rośliny dostarczają tlenu do atmosfery w procesie fotosyntezy. Bez nich nie byłoby możliwe życie w takiej formie, jaką znamy!

Azot i gazy szlachetne
Azot (N₂) to najważniejszy składnik powietrza (78%). Jest gazem bezbarwnym i bezwonnym, który słabo rozpuszcza się w wodzie. W przeciwieństwie do tlenu, azot nie podtrzymuje spalania i jest niepalny. To właśnie dzięki obecności azotu w powietrzu procesy spalania nie przebiegają zbyt gwałtownie.
Azot jest niezbędny dla prawidłowego rozwoju roślin. Wykorzystuje się go do produkcji:
- amoniaku
- nawozów sztucznych
- materiałów wybuchowych
Ciekły azot o temperaturze -196°C stosuje się do szybkiego zamrażania produktów spożywczych i w medycynie.
Gazy szlachetne (grupa 18 układu okresowego) to wyjątkowe pierwiastki, które występują w powietrzu w niewielkiej ilości (około 1%). Są to: hel, neon, argon, krypton, ksenon i radon. Ich nazwa pochodzi stąd, że są bardzo mało reaktywne - mają zapełnioną powłokę walencyjną (8 elektronów).
Gazy szlachetne są bezbarwne i bezwonne. Pobudzone polem elektrycznym pięknie świecą, dlatego stosuje się je w technice oświetleniowej (np. neony). Hel wykorzystuje się w medycynie, balonach i sondach meteorologicznych.
🎈 Eksperyment: Gdy wdychamy hel, nasz głos staje się bardzo wysoki. Dzieje się tak dlatego, że hel ma mniejszą gęstość niż powietrze i fale dźwiękowe rozchodzą się w nim szybciej.
Tlenek węgla(IV) - dwutlenek węgla
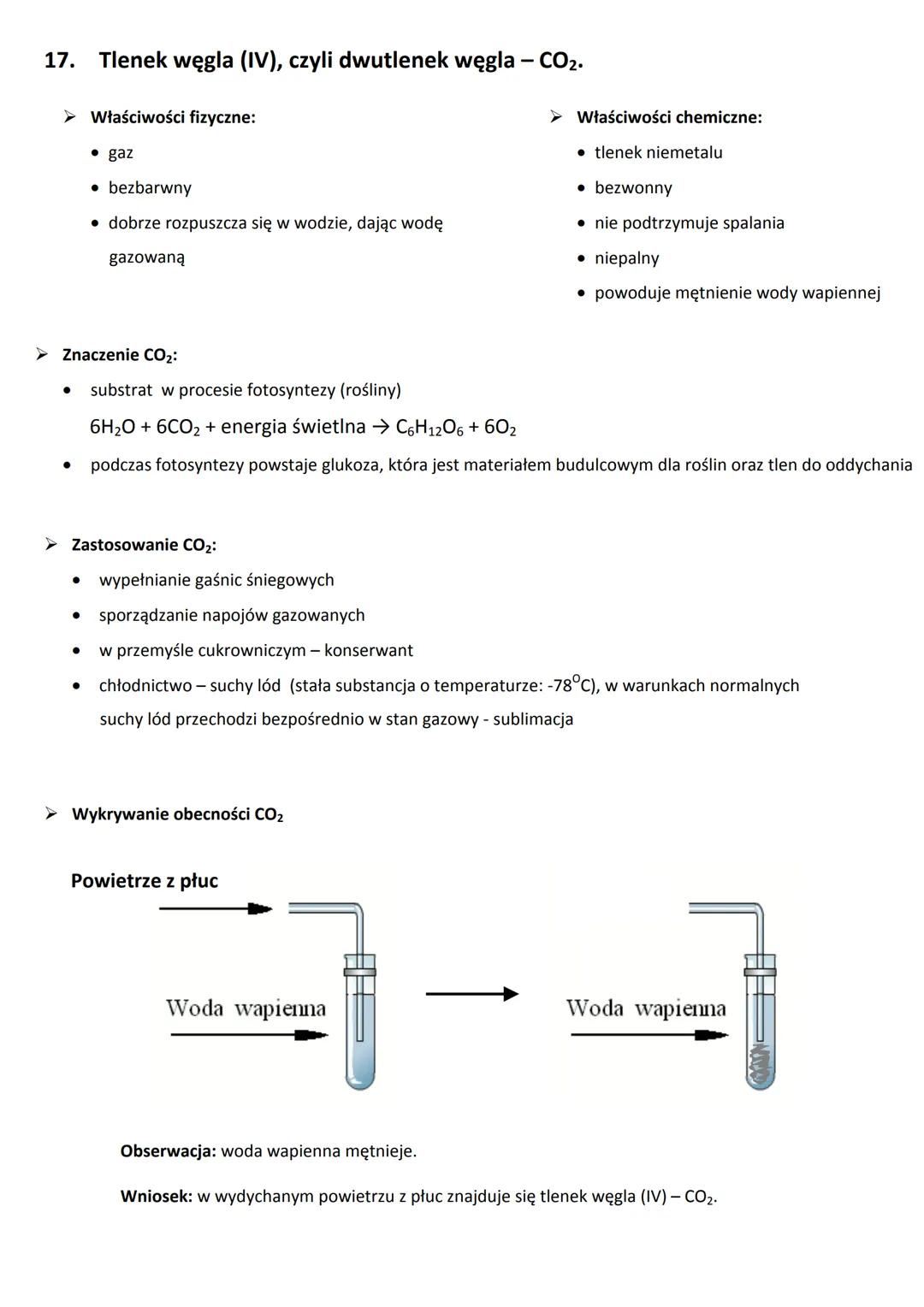
Tlenek węgla(IV) (CO₂), znany też jako dwutlenek węgla, to ważny składnik powietrza. Jest gazem bezbarwnym i bezwonnym, który dobrze rozpuszcza się w wodzie, tworząc wodę gazowaną.
Dwutlenek węgla:
- jest tlenkiem niemetalu
- nie podtrzymuje spalania
- sam się nie pali
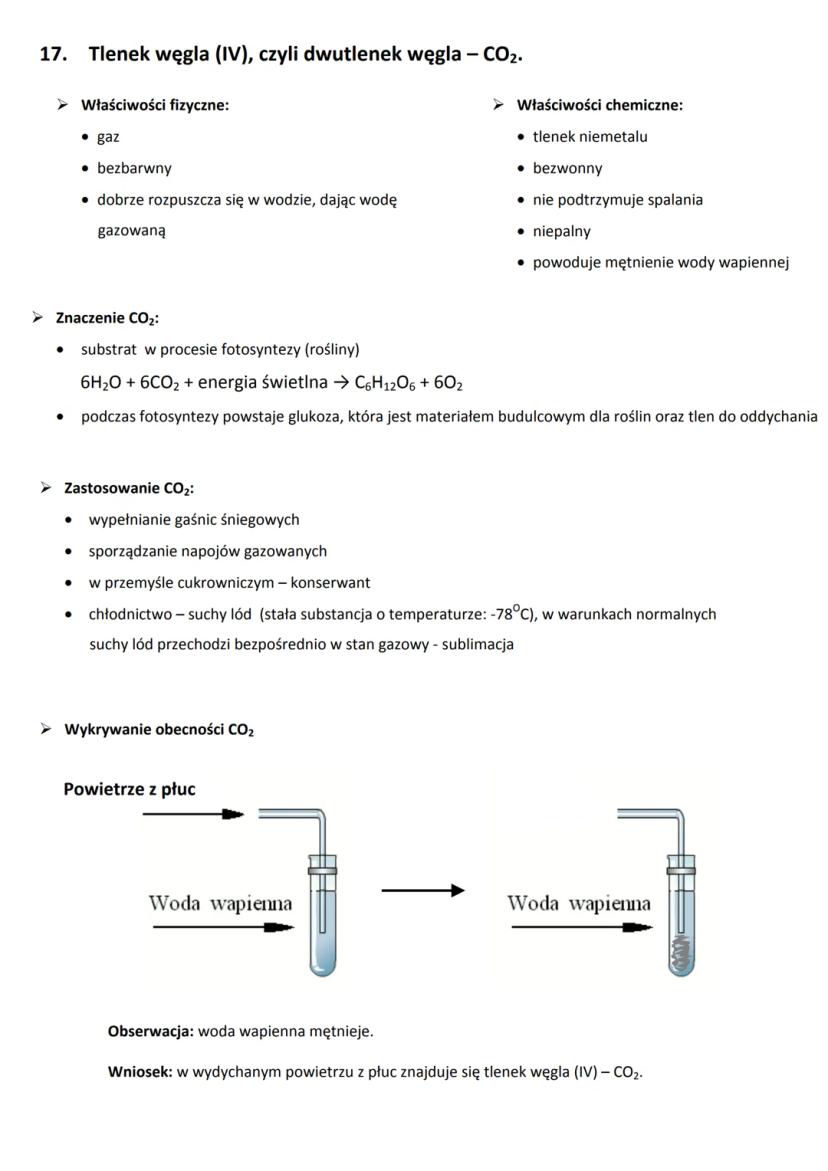
- powoduje mętnienie wody wapiennej (to jego charakterystyczna właściwość)
Możemy łatwo wykryć obecność CO₂ za pomocą wody wapiennej - jeśli przepuścimy przez nią wydychane powietrze, woda zmętnieje. Dzieje się tak, ponieważ w procesie oddychania wydzielamy dwutlenek węgla.
CO₂ odgrywa kluczową rolę w fotosyntezie - procesie, w którym rośliny wykorzystują dwutlenek węgla, wodę i energię słoneczną do produkcji glukozy i tlenu:
6H₂O + 6CO₂ + energia świetlna → C₆H₁₂O₆ + 6O₂
Dwutlenek węgla ma wiele zastosowań:
- w gaśnicach śniegowych
- jako składnik napojów gazowanych
- jako konserwant w przemyśle spożywczym
- w postaci suchego lodu w chłodnictwie
🧊 Ciekawostka: Suchy lód (stały CO₂) nie topi się, lecz od razu zamienia się w gaz - ten proces nazywamy sublimacją.

Właściwości CO₂ i para wodna
Tlenek węgla(IV) (CO₂) ma ciekawe właściwości chemiczne. Możemy je zbadać za pomocą prostych doświadczeń:
Gdy umieścimy płonące łuczywo (kawałek drewna) w naczyniu z CO₂, płomień zgaśnie - to dowód, że dwutlenek węgla nie podtrzymuje palenia. Jednak magnez płonie nawet w atmosferze CO₂! Podczas tej reakcji powstaje biały proszek (tlenek magnezu) oraz czarny nalot (węgiel):
2Mg + CO₂ → 2MgO + C
Jest to reakcja wymiany - magnez "odbiera" tlen z dwutlenku węgla.
Para wodna to woda w stanie gazowym. Wbrew powiedzeniom, pary wodnej nie widać - jest bezbarwnym, bezwonnym gazem. To, co często nazywamy "parą" (np. nad gotującą się wodą), to w rzeczywistości drobne kropelki wody zawieszone w powietrzu.
Obecność pary wodnej w powietrzu możemy wykazać za pomocą wodorotlenku sodu. Jest to substancja higroskopijną - ma zdolność pochłaniania wilgoci. Gdy wystawimy stały wodorotlenek sodu na działanie powietrza, stanie się błyszczący i śliski, a po dłuższym czasie rozpłynie się, ponieważ pochłonie wodę z powietrza.
💧 Ważne: Para wodna w atmosferze jest kluczowa dla klimatu Ziemi - zatrzymuje ciepło, tworzy chmury i jest źródłem opadów.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: zmiana chemiczna
2Estry
Chemia rozszerzona
Chemia: Podstawy Reakcji
Zgłębiaj podstawowe pojęcia chemiczne, w tym charakterystykę substancji, reakcje chemiczne oraz procesy laboratoryjne. Dowiedz się o dekantacji, filtracji, krystalizacji, oraz różnicach między reakcjami endo- i egzotermicznymi. Idealne dla uczniów klasy 8, którzy chcą powtórzyć materiał z klasy 7.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Chemiczne substancje i ich przemiany: notatki
Chemia otacza nas wszędzie, ale nie zawsze zdajemy sobie z tego sprawę! W tym podsumowaniu poznasz podstawowe pojęcia chemiczne, które pozwolą Ci lepiej rozumieć świat wokół Ciebie. Dowiesz się, czym są substancje, jak badać ich właściwości i jak odróżniać zjawiska... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Substancje i ich właściwości
Czy zastanawiałeś się kiedyś, z czego tak naprawdę składają się przedmioty wokół ciebie? Ciało fizyczne to konkretny przedmiot, który widzisz (np. drut miedziany), natomiast substancja to materiał, z którego ten przedmiot jest wykonany (np. miedź).
Każda substancja ma charakterystyczne właściwości, które pozwalają ją odróżnić od innych. Właściwości dzielimy na:
- fizyczne - stan skupienia, barwa, połysk, gęstość, twardość, rozpuszczalność, temperatura wrzenia i topnienia
- chemiczne - zapach, smak, palność i aktywność chemiczna
Właściwości substancji badamy na różne sposoby. Możemy wykorzystać zmysły (wzrok, dotyk, węch, smak), przeprowadzić doświadczenia chemiczne lub odczytać informacje z tabel. Niektóre substancje mogą być niebezpieczne, dlatego oznacza się je specjalnymi piktogramami ostrzegawczymi.
💡 Ciekawostka: Nie wszystkie właściwości substancji możemy zbadać bezpośrednio zmysłami! Niektóre substancje chemiczne są bardzo niebezpieczne, dlatego nigdy nie próbuj ich smakować ani wąchać bez nadzoru nauczyciela.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Gęstość i rodzaje przemian
Gęstość to jedna z najważniejszych właściwości substancji. Obliczamy ją dzieląc masę substancji przez zajmowaną przez nią objętość: d = m/V. Ta właściwość pomaga nam zrozumieć, dlaczego niektóre przedmioty toną w wodzie, a inne unoszą się na jej powierzchni.
W przyrodzie zachodzą dwa rodzaje przemian:
- Zjawisko fizyczne - nie powstaje nowa substancja, zmienia się tylko kształt, stan skupienia lub inne właściwości fizyczne (np. topnienie lodu)
- Reakcja chemiczna - powstaje nowa substancja o innych właściwościach (np. spalanie drewna)
Substancje dzielimy na substancje czyste i mieszaniny. Substancje czyste to:
- Pierwiastki (substancje proste) - np. metale jak cynk i niemetale jak tlen
- Związki chemiczne (substancje złożone) - np. woda
Mieszaniny natomiast mogą być:
- Jednorodne - o jednakowym składzie w całej objętości (np. powietrze)
- Niejednorodne - o niejednakowym składzie (np. piasek z wodą)
🔍 Ważne: Mieszaniny można rozdzielić metodami fizycznymi, natomiast związki chemiczne można rozdzielić tylko za pomocą reakcji chemicznych!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Sposoby rozdzielania mieszanin
Czy wiesz, że istnieje wiele sposobów na rozdzielanie mieszanin? Poznanie ich przyda ci się nie tylko w laboratorium, ale też w codziennym życiu!
Sączenie (filtracja) - to przelewanie mieszaniny cieczy z ciałem stałym przez sączek, który zatrzymuje ciało stałe. Działa podobnie jak sito kuchenne, gdy odcedzasz makaron!
Sedymentacja i dekantacja - najpierw czekamy, aż cząstki ciała stałego opadną na dno (sedymentacja), a potem ostrożnie zlewamy ciecz znad osadu (dekantacja).
Krystalizacja - to proces, w którym substancja rozpuszczona wydziela się z roztworu w postaci kryształków, gdy rozpuszczalnik odparowuje.
Destylacja - służy do rozdzielania mieszanin cieczy o różnych temperaturach wrzenia. Wykorzystuje się specjalną aparaturę z kolbą destylacyjną i chłodnicą.
Inne metody to przesiewanie (rozdzielanie ciał stałych o różnej wielkości cząstek) oraz użycie magnesu (przyciąganie substancji magnetycznych, np. żelaza).
🧪 Eksperyment domowy: Spróbuj rozdzielić wodę i sól kuchenną przez odparowanie wody. Zobaczysz krystalizację soli na dnie naczynia!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Pierwiastki, związki chemiczne i symbole
Pierwiastek chemiczny to substancja prosta, której nie można rozłożyć na prostsze substancje (np. tlen O, miedź Cu). Związek chemiczny natomiast składa się z co najmniej dwóch różnych pierwiastków połączonych ze sobą (np. woda H₂O).
Każdy pierwiastek ma swój symbol chemiczny - to skrót pochodzący od jego łacińskiej nazwy. Symbol składa się z jednej dużej litery lub z dużej i małej litery .
Metale i niemetale to dwie główne grupy pierwiastków. Metale najczęściej:
- występują w stałym stanie skupienia (wyjątek to rtęć)
- mają srebrzystą barwę i metaliczny połysk
- są kowalne i ciągliwe (można je kuć i rozciągać)
Metale różnią się między sobą twardością, temperaturą topnienia i aktywnością chemiczną. Najbardziej aktywne są litowce (grupa 1), najmniej aktywne są metale szlachetne (np. złoto, platyna).
🔎 Ciekawostka: Czy wiesz, że 80% pierwiastków to metale? Znajdują się po lewej stronie układu okresowego, a niemetale po prawej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Stopy metali i korozja
Stopy metali to mieszaniny jednorodne różnych metali stopionych w odpowiednich proporcjach. Znasz je lepiej niż myślisz - używasz ich codziennie!
Popularne stopy to:
- mosiądz - klamki, okucia, ozdoby
- brąz - monety, rzeźby
- duraluminium - samoloty, części maszyn
- stal - wykorzystywana w prawie każdej gałęzi przemysłu
Metale ulegają korozji - procesowi niszczenia pod wpływem tlenu, wody, kwasów, zasad i soli. Najbardziej znanym przykładem korozji jest rdzewienie żelaza. Aby chronić metale przed korozją, stosujemy:
- pokrywanie powłokami ochronnymi (cynkowanie, chromowanie, malowanie)
- osłabianie agresywności środowiska
- stosowanie stopów odpornych na korozję
Powietrze to mieszanina gazów, w której przeważa azot (78%) i tlen (21%). Pozostały 1% to głównie gazy szlachetne (argon). Zawartość pary wodnej, dwutlenku węgla, ozonu i zanieczyszczeń może się zmieniać.
🛡️ Eksperyment: Porównaj dwa gwoździe - jeden pokryty warstwą farby, drugi niepokryty. Zanurz oba w wodzie na tydzień. Który z nich szybciej zardzewiejr i dlaczego?

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Badanie składu powietrza i tlen
Możemy zbadać zawartość tlenu w powietrzu za pomocą prostego doświadczenia. Gdy zapalimy świeczkę pod odwróconym cylindrem w naczyniu z wodą, świeca po pewnym czasie gaśnie, a woda podnosi się w cylindrze. Dzieje się tak, ponieważ tlen zostaje zużyty podczas spalania. Poziom wody wskazuje, że tlen stanowi około 1/5 (21%) objętości powietrza.
Tlen (O₂) to niezwykle ważny pierwiastek dla życia na Ziemi. Jego właściwości fizyczne to:
- stan gazowy w temperaturze pokojowej
- bezbarwność
- słaba rozpuszczalność w wodzie
- brak zapachu
Z punktu widzenia chemii, tlen:
- jest niemetalem
- podtrzymuje spalanie (choć sam się nie pali)
- łączy się z wieloma pierwiastkami, tworząc tlenki
Tlen można otrzymać na kilka sposobów, np. przez rozkład związków bogatych w tlen lub przez elektrolizę wody.
🔥 Uwaga: Spalanie w czystym tlenie jest o wiele gwałtowniejsze niż w powietrzu! Dlatego w laboratoriach i przemyśle trzeba zachować szczególne środki ostrożności przy pracy z czystym tlenem.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje spalania i znaczenie tlenu
Spalanie to gwałtowne utlenianie (łączenie z tlenem), któremu towarzyszy wydzielanie energii w postaci światła i ciepła. Podczas spalania zachodzą reakcje syntezy:
siarka + tlen → tlenek siarki(IV)
S + O₂ → SO₂
węgiel + tlen → tlenek węgla(IV)
C + O₂ → CO₂
magnez + tlen → tlenek magnezu
2Mg + O₂ → 2MgO
Produkty spalania zależą od tego, co się spala:
- gdy spala się metal, powstaje tlenek metalu (np. MgO)
- gdy spala się niemetal, powstaje tlenek niemetalu (np. CO₂, SO₂)
Tlen ma ogromne znaczenie dla życia i procesów zachodzących na Ziemi:
- jest niezbędny do oddychania organizmów
- umożliwia spalanie (np. w silnikach samochodowych, piecach przemysłowych)
- powoduje wietrzenie skał, rdzewienie metali i butwienie szczątków organicznych
Tlen znajduje szerokie zastosowanie w:
- medycynie (maski tlenowe, butle z tlenem)
- przemyśle
- produkcji kwasów
- technice nurkowej i lotniczej
🌱 Pamiętaj: To rośliny dostarczają tlenu do atmosfery w procesie fotosyntezy. Bez nich nie byłoby możliwe życie w takiej formie, jaką znamy!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Azot i gazy szlachetne
Azot (N₂) to najważniejszy składnik powietrza (78%). Jest gazem bezbarwnym i bezwonnym, który słabo rozpuszcza się w wodzie. W przeciwieństwie do tlenu, azot nie podtrzymuje spalania i jest niepalny. To właśnie dzięki obecności azotu w powietrzu procesy spalania nie przebiegają zbyt gwałtownie.
Azot jest niezbędny dla prawidłowego rozwoju roślin. Wykorzystuje się go do produkcji:
- amoniaku
- nawozów sztucznych
- materiałów wybuchowych
Ciekły azot o temperaturze -196°C stosuje się do szybkiego zamrażania produktów spożywczych i w medycynie.
Gazy szlachetne (grupa 18 układu okresowego) to wyjątkowe pierwiastki, które występują w powietrzu w niewielkiej ilości (około 1%). Są to: hel, neon, argon, krypton, ksenon i radon. Ich nazwa pochodzi stąd, że są bardzo mało reaktywne - mają zapełnioną powłokę walencyjną (8 elektronów).
Gazy szlachetne są bezbarwne i bezwonne. Pobudzone polem elektrycznym pięknie świecą, dlatego stosuje się je w technice oświetleniowej (np. neony). Hel wykorzystuje się w medycynie, balonach i sondach meteorologicznych.
🎈 Eksperyment: Gdy wdychamy hel, nasz głos staje się bardzo wysoki. Dzieje się tak dlatego, że hel ma mniejszą gęstość niż powietrze i fale dźwiękowe rozchodzą się w nim szybciej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Tlenek węgla(IV) - dwutlenek węgla
Tlenek węgla(IV) (CO₂), znany też jako dwutlenek węgla, to ważny składnik powietrza. Jest gazem bezbarwnym i bezwonnym, który dobrze rozpuszcza się w wodzie, tworząc wodę gazowaną.
Dwutlenek węgla:
- jest tlenkiem niemetalu
- nie podtrzymuje spalania
- sam się nie pali
- powoduje mętnienie wody wapiennej (to jego charakterystyczna właściwość)
Możemy łatwo wykryć obecność CO₂ za pomocą wody wapiennej - jeśli przepuścimy przez nią wydychane powietrze, woda zmętnieje. Dzieje się tak, ponieważ w procesie oddychania wydzielamy dwutlenek węgla.
CO₂ odgrywa kluczową rolę w fotosyntezie - procesie, w którym rośliny wykorzystują dwutlenek węgla, wodę i energię słoneczną do produkcji glukozy i tlenu:
6H₂O + 6CO₂ + energia świetlna → C₆H₁₂O₆ + 6O₂
Dwutlenek węgla ma wiele zastosowań:
- w gaśnicach śniegowych
- jako składnik napojów gazowanych
- jako konserwant w przemyśle spożywczym
- w postaci suchego lodu w chłodnictwie
🧊 Ciekawostka: Suchy lód (stały CO₂) nie topi się, lecz od razu zamienia się w gaz - ten proces nazywamy sublimacją.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości CO₂ i para wodna
Tlenek węgla(IV) (CO₂) ma ciekawe właściwości chemiczne. Możemy je zbadać za pomocą prostych doświadczeń:
Gdy umieścimy płonące łuczywo (kawałek drewna) w naczyniu z CO₂, płomień zgaśnie - to dowód, że dwutlenek węgla nie podtrzymuje palenia. Jednak magnez płonie nawet w atmosferze CO₂! Podczas tej reakcji powstaje biały proszek (tlenek magnezu) oraz czarny nalot (węgiel):
2Mg + CO₂ → 2MgO + C
Jest to reakcja wymiany - magnez "odbiera" tlen z dwutlenku węgla.
Para wodna to woda w stanie gazowym. Wbrew powiedzeniom, pary wodnej nie widać - jest bezbarwnym, bezwonnym gazem. To, co często nazywamy "parą" (np. nad gotującą się wodą), to w rzeczywistości drobne kropelki wody zawieszone w powietrzu.
Obecność pary wodnej w powietrzu możemy wykazać za pomocą wodorotlenku sodu. Jest to substancja higroskopijną - ma zdolność pochłaniania wilgoci. Gdy wystawimy stały wodorotlenek sodu na działanie powietrza, stanie się błyszczący i śliski, a po dłuższym czasie rozpłynie się, ponieważ pochłonie wodę z powietrza.
💧 Ważne: Para wodna w atmosferze jest kluczowa dla klimatu Ziemi - zatrzymuje ciepło, tworzy chmury i jest źródłem opadów.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: zmiana chemiczna
2Estry
Chemia rozszerzona
Chemia: Podstawy Reakcji
Zgłębiaj podstawowe pojęcia chemiczne, w tym charakterystykę substancji, reakcje chemiczne oraz procesy laboratoryjne. Dowiedz się o dekantacji, filtracji, krystalizacji, oraz różnicach między reakcjami endo- i egzotermicznymi. Idealne dla uczniów klasy 8, którzy chcą powtórzyć materiał z klasy 7.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.