Tlenki, wodorki i wodorotlenki to podstawowe związki nieorganiczne, które musisz... Pokaż więcej
Kompletna wiedza o tlenkach, wodorotlenkach, wodorkach, kwasach i solach





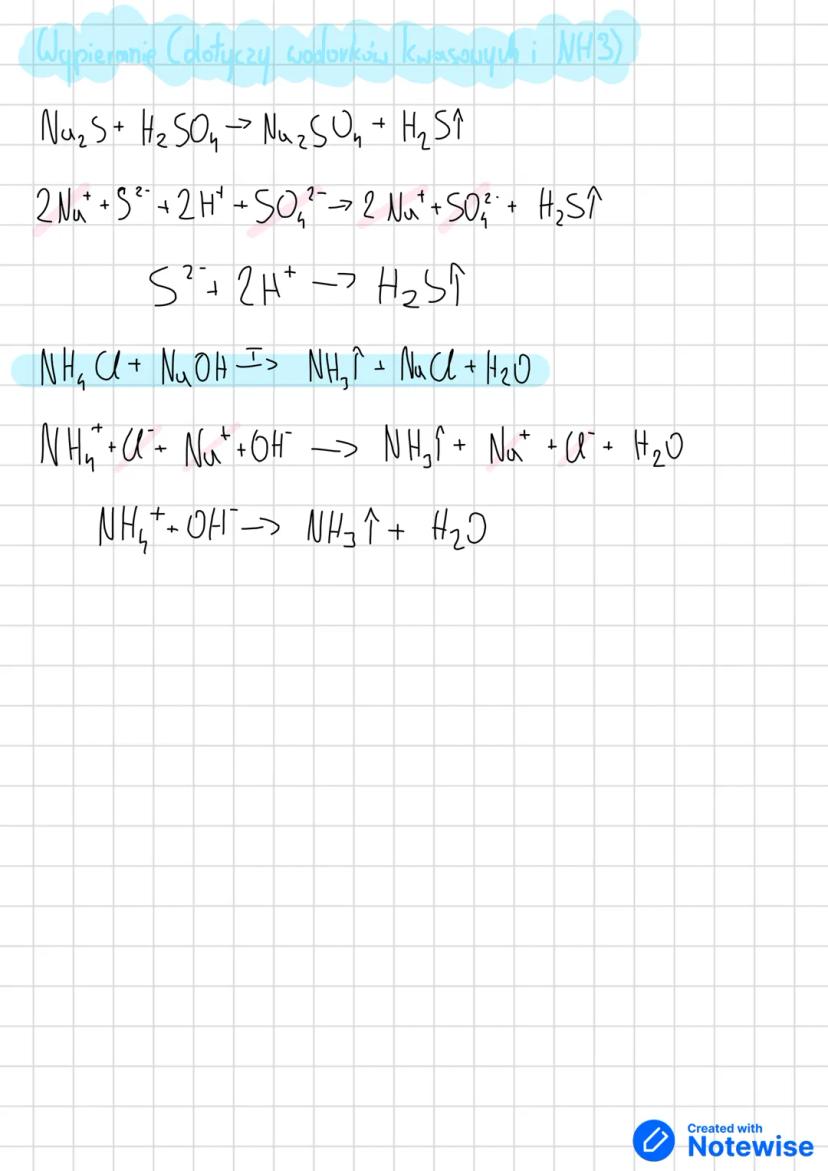



Tlenki - podstawy i wartościowości
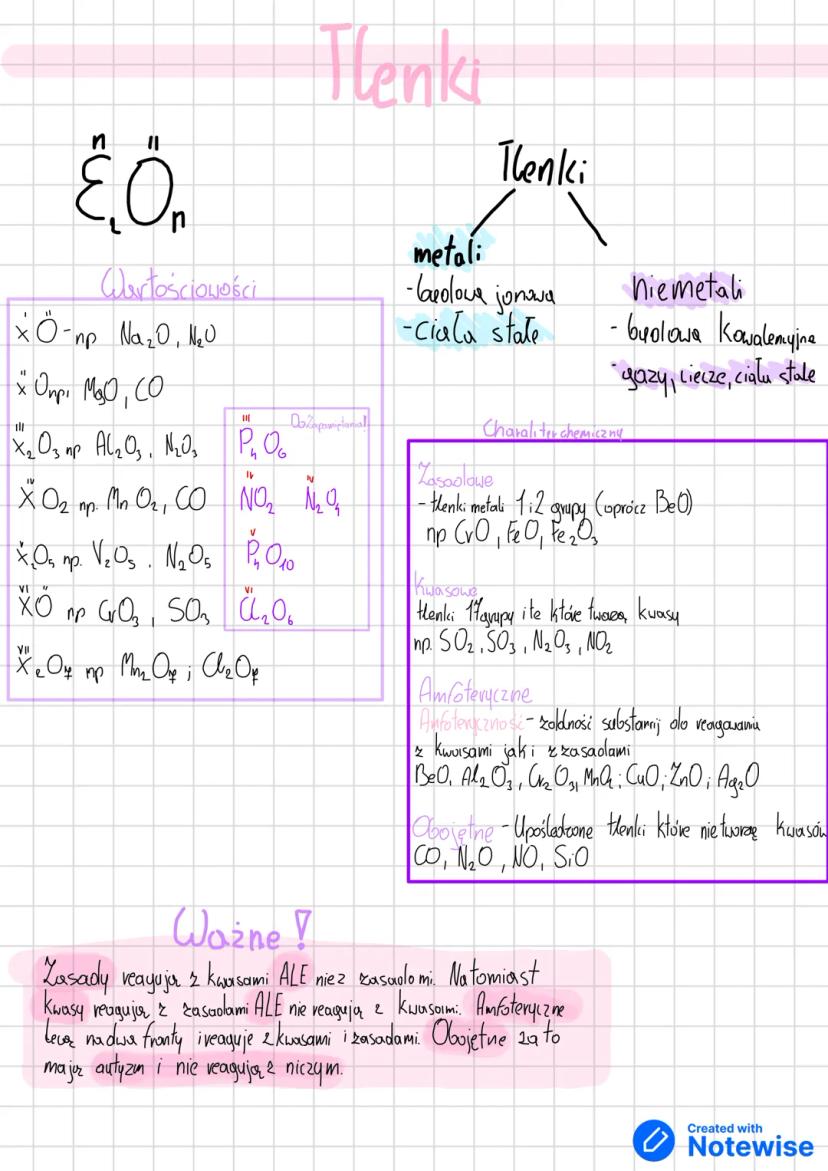
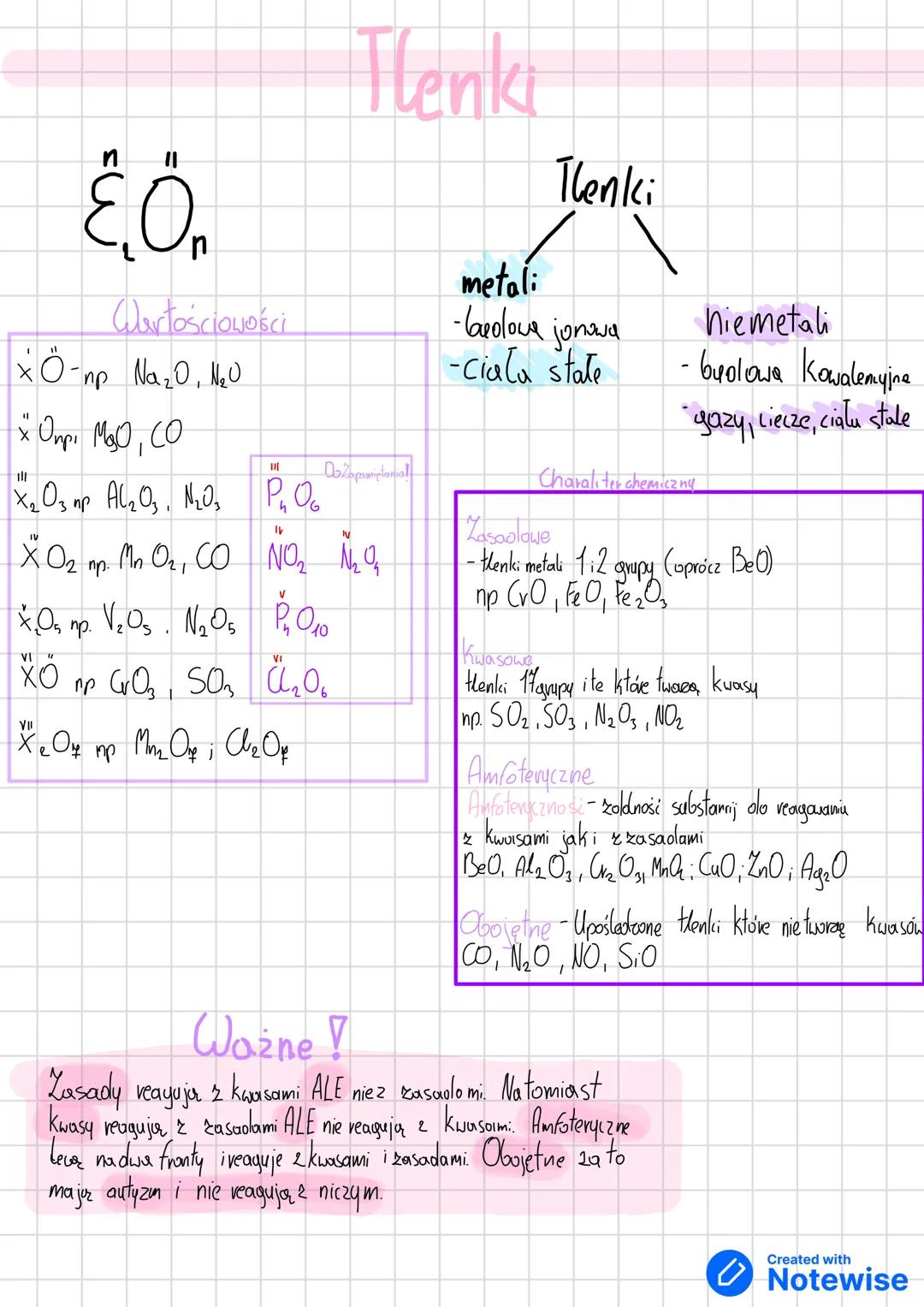
Tlenki to związki tlenu z innymi pierwiastkami, które poznasz po charakterystycznych wzorach. W zależności od wartościowości pierwiastka mogą mieć wzory X₂O, XO, X₂O₃, XO₂, X₂O₅ czy XO₃.
Najważniejszy podział to tlenki metali (budowa jonowa, ciała stałe) i tlenki niemetali (budowa kowalencyjna, różne stany skupienia). Ten podział determinuje ich właściwości chemiczne.
Ze względu na charakter chemiczny dzielisz tlenki na cztery typy. Tlenki zasadowe reagują z kwasami, tlenki kwasowe tworzą kwasy. Tlenki amfoteryczne jak BeO, Al₂O₃ reagują zarówno z kwasami jak i zasadami, a tlenki obojętne jak CO nie reagują z niczym.
💡 Zapamiętaj: Zasadowe + kwas = sól + woda, kwasowe + zasada = sól + woda, amfoteryczne reagują z obydwoma!

Reakcje tlenków z kwasami i zasadami
Tlenek zasadowy + kwas daje sól i wodę, np. CaO + 2HCl → CaCl₂ + H₂O. To klasyczna reakcja neutralizacji, którą napiszesz też w wersji jonowej.
Tlenek kwasowy + zasada też tworzy sól i wodę, jak SO₃ + 2NaOH → Na₂SO₄ + H₂O. Pamiętaj o zbilansowaniu równań - czasem potrzebujesz więcej cząsteczek zasady.
Większość tlenków reaguje z wodą tworząc odpowiednio zasady (tlenki zasadowe) lub kwasy (tlenki kwasowe). Na przykład Na₂O + H₂O → 2NaOH, a SO₃ + H₂O → H₂SO₄.
💡 Tip: Jeśli nie wiesz jakiego typu jest tlenek, sprawdź czy metal czy niemetal - to podpowie Ci typ reakcji!
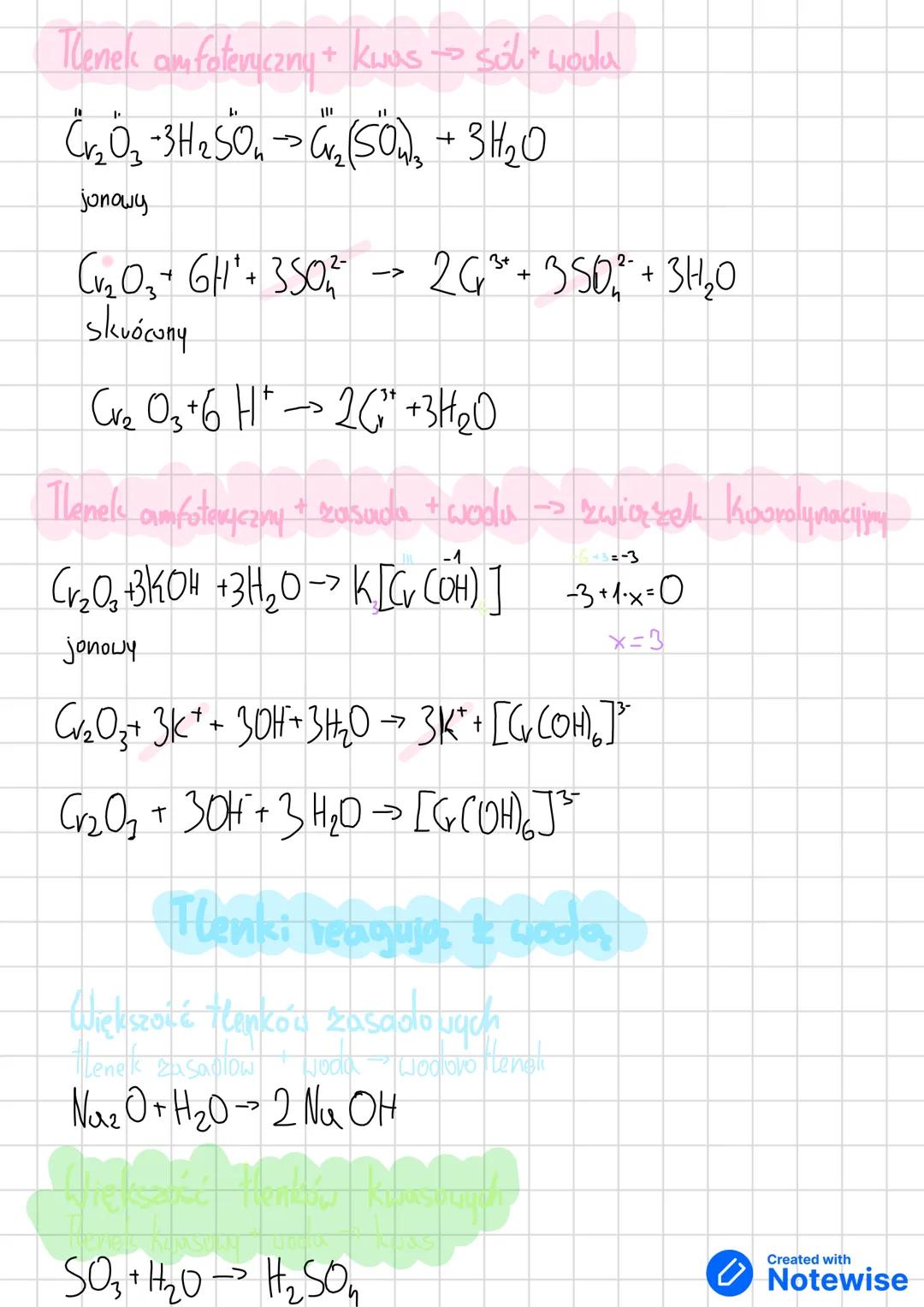
Tlenki amfoteryczne i ich specjalne reakcje
Tlenki amfoteryczne to "chemiczni dyplomaci" - reagują zarówno z kwasami jak i zasadami. Z kwasem zachowują się jak tlenki zasadowe: Cr₂O₃ + 3H₂SO₄ → Cr₂(SO₄)₃ + 3H₂O.
Z zasadą tworzą jednak związki koordinacyjne z wodą: Cr₂O₃ + 3KOH + 3H₂O → 3K[Cr(OH)₆]. To bardziej skomplikowane produkty niż zwykłe sole.
Kluczowe tlenki amfoteryczne to: BeO, Al₂O₃, Cr₂O₃, ZnO, CuO. Zapamiętaj je, bo często pojawiają się na sprawdzianach jako "pułapki" - wyglądają jak tlenki metali, ale reagują inaczej.
💡 Uwaga: Tlenki amfoteryczne to głównie metale przejściowe i te z granicy metali/niemetali!

Otrzymywanie tlenków
Najprostrza metoda to bezpośrednia synteza: metal + tlen = tlenek . To podstawowa reakcja spalania, którą znasz ze środowiska.
Rozkład termiczny to podgrzewanie węglanów czy wodorotlenków: CaCO₃ → CaO + CO₂. Często wykorzystywane w przemyśle, np. przy produkcji wapna.
Inne metody to utlenianie tlenków czy redukcja . Możesz też rozkładać kwasy: H₂SO₄ → SO₂ + H₂O.
💡 Praktycznie: Większość tlenków w przyrodzie powstaje przez spalanie lub rozkład termiczny!

Wodorki - związki wodoru
Wodorki to połączenia wodoru z innymi pierwiastkami. Wzór zależy od grupy: dla grup 1-15 piszesz XHₙ, dla grup 16-17 HₙX.
Dzielą się podobnie jak tlenki. Wodorki zasadowe reagują z kwasami: NaH + HCl → NaCl + H₂. Wodorki kwasowe reagują z zasadami.
Reakcja wodorku z kwasem często daje gaz wodór - to charakterystyczne "bulgotanie". Wyjątek to amoniak NH₃, który reaguje inaczej: NH₃ + HCl → NH₄Cl.
💡 Ciekawostka: Wodorki metali to doskonałe źródła wodoru - wystarczy dodać kwas!

Reakcje wodorków z wodą i kwasami
Wodorki metali z wodą dają zasadę i wodór: NaH + H₂O → NaOH + H₂↑. To reakcja gwałtowna - wodór może się zapalić!
Amoniak z wodą tworzy słabą zasadę: NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. Symbol równowagi pokazuje, że reakcja jest odwracalna.
Wodorki kwasowe w wodzie rozpadają się na jony: HCl → H⁺ + Cl⁻. To typowe kwasy, które znasz z codzienności.
💡 Bezpieczeństwo: Reakcje wodorków z wodą mogą być bardzo gwałtowne - zawsze ostrożnie!
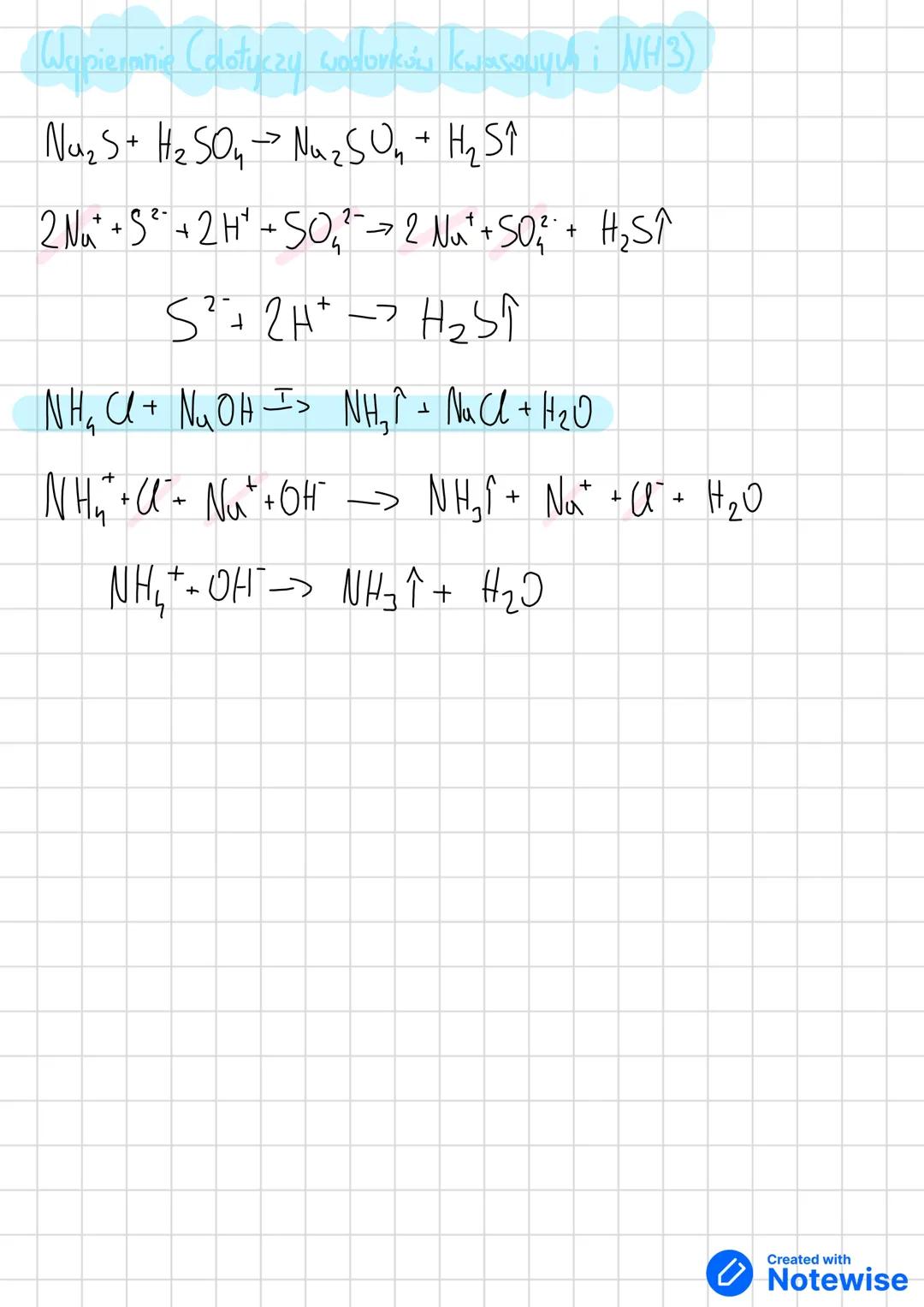
Otrzymywanie wodorków
Bezpośrednia synteza to reakcja pierwiastka z wodorem: 2Na + H₂ → 2NaH lub N₂ + 3H₂ → 2NH₃. Druga reakcja wymaga katalizatora i ciśnienia.
Wypieranie z soli to klasyczna metoda dla wodorków kwasowych: Na₂S + H₂SO₄ → Na₂SO₄ + H₂S↑. Mocniejszy kwas wypiera słabszy.
Dla amoniaku używasz reakcji: NH₄Cl + NaOH → NH₃↑ + NaCl + H₂O. Podgrzewanie zwiększa wydajność - amoniak ma charakterystyczny ostry zapach.
💡 W laboratorium: Wodorki kwasowe najłatwiej otrzymać przez wypieranie z soli!

Wodorotlenki - budowa i nazewnictwo
Wodorotlenki to związki jonowe składające się z kationu metalu i anionu OH⁻. Wszystkie to ciała stałe o charakterystycznej budowie krystalicznej.
W nazewnictwie dodajesz "wodorotlenek" przed nazwą metalu: Ca(OH)₂ to wodorotlenek wapnia, Al(OH)₃ to wodorotlenek glinu. Dla metali o zmiennej wartościowości dodajesz rzymską cyfrę.
Charakter chemiczny dzieli je na zasadowe , amfoteryczne (Be(OH)₂, Al(OH)₃, Zn(OH)₂) i praktycznie nierozpuszczalne. Tylko wodorotlenki grup 1 i Ba(OH)₂ są dobrze rozpuszczalne.
💡 Pamiętaj: Im bardziej w lewo w układzie okresowym, tym bardziej zasadowy wodorotlenek!

Reakcje wodorotlenków
Wodorotlenek zasadowy + kwas to klasyczna neutralizacja: 2Fe(OH)₃ + 3H₂SO₄ → Fe₂(SO₄)₃ + 6H₂O. Pamiętaj o bilansowaniu - często potrzebujesz więcej cząsteczek.
Wodorotlenki amfoteryczne reagują też z zasadami tworząc związki koordynacyjne: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄]. To bardziej złożone struktury niż zwykłe sole.
Reakcje w wersji jonowej pokazują istotę procesu - przejście protonów H⁺ lub jonów OH⁻. To pomaga zrozumieć mechanizm reakcji.
💡 Na sprawdzianie: Zawsze sprawdzaj czy wodorotlenek jest zasadowy czy amfoteryczny!

Otrzymywanie wodorotlenków
Metal aktywny + woda daje wodorotlenek i wodór: 2Na + 2H₂O → 2NaOH + H₂↑. Tylko metale grup 1-2 (bez berylu) reagują tak bezpośrednio.
Tlenek zasadowy + woda to najprostsza metoda: Na₂O + H₂O → 2NaOH. Nie wszystkie tlenki tak reagują - sprawdź w tabeli rozpuszczalności.
Strącanie z soli wykorzystujesz gdy inne metody nie działają: BeSO₄ + 2NaOH → Na₂SO₄ + Be(OH)₂↓. Strzałka w dół pokazuje wytrącający się osad.
💡 W przemyśle: Wodorotlenek sodu (soda kaustyczna) otrzymuje się głównie z elektrolizy solanki!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: zasada
9Otrzymywanie Wodorotlenków
Zrozumienie procesu otrzymywania wodorotlenków, ich właściwości oraz reakcji chemicznych. Dowiedz się o wodorotlenkach sodu, wapnia i żelaza (III), ich amfoteryczności oraz zastosowaniach w chemii. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Wodorotlenki: Właściwości i Reakcje
Zgłębiaj właściwości wodorotlenków, ich przygotowanie oraz reakcje z kwasami i solami. Dowiedz się o amfoteryczności, dysocjacji jonowej oraz przykładach wodorotlenków rozpuszczalnych w wodzie. Idealne dla uczniów chemii i studentów. Typ: Podsumowanie.
Wodorotlenki cały dział
Notatka z wodorotlenków - cały dział. Wzory, nazwy, dysocjacja i otrzymywanie wodorotlenków.
Wodorotlenki: Systematyka i Właściwości
Odkryj kluczowe informacje o wodorotlenkach, ich systematyce, właściwościach amfoterycznych oraz sposobach przygotowania. Materiał zawiera szczegółowe opisy wodorotlenków sodu, potasu, wapnia i innych, zgodne z wymaganiami maturalnymi 2023/24. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Właściwości Wodorotlenków
Zgłębiaj właściwości chemiczne wodorotlenków, ich reakcje z kwasami, tlenkami oraz metalami. Dowiedz się o amfoteryczności, przygotowaniu oraz zastosowaniach wodorotlenków, takich jak NaOH, Ca(OH)₂ i Al(OH)₃. Idealne dla uczniów i studentów chemii.
Teorie Kwasów i Zasad
Zgłębiaj teorie kwasów i zasad, w tym teorię Arrheniusa, Brønsteda-Lowry'ego oraz Lewisa. Dowiedz się o roli kwasów i zasad, ich autodysocjacji oraz amfoteryczności. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe koncepcje chemiczne i ich zastosowania w roztworach wodnych.
Wodorotlenki
Notatka z wodorotlenków chemia rozszerzona
Charakterystyka Bloku S
Zgłębiaj właściwości litowców i berylowców, ich reakcje oraz przygotowanie wodorotlenków. Materiał zawiera kluczowe informacje na temat reakcji chemicznych, takich jak tworzenie Ca(OH)2 i NaOH, oraz ich zastosowania w kontekście zadań maturalnych. Idealne dla uczniów przygotowujących się do egzaminów.
Teorie Kwasów i Zasad
Zgłębiaj teorie kwasów i zasad, w tym Arrheniusa, Bronsteda-Lowry'ego oraz Lewisa. Dowiedz się, jak kwasy i zasady dysocjują, jakie mają właściwości oraz jak woda działa jako amfoteryczna substancja. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe koncepcje chemiczne.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Kompletna wiedza o tlenkach, wodorotlenkach, wodorkach, kwasach i solach
Tlenki, wodorki i wodorotlenki to podstawowe związki nieorganiczne, które musisz znać na chemii. Te trzy grupy związków różnią się właściwościami i sposobami reakcji, ale łączą je wspólne zasady tworzenia i nazewnictwa.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Tlenki - podstawy i wartościowości
Tlenki to związki tlenu z innymi pierwiastkami, które poznasz po charakterystycznych wzorach. W zależności od wartościowości pierwiastka mogą mieć wzory X₂O, XO, X₂O₃, XO₂, X₂O₅ czy XO₃.
Najważniejszy podział to tlenki metali (budowa jonowa, ciała stałe) i tlenki niemetali (budowa kowalencyjna, różne stany skupienia). Ten podział determinuje ich właściwości chemiczne.
Ze względu na charakter chemiczny dzielisz tlenki na cztery typy. Tlenki zasadowe reagują z kwasami, tlenki kwasowe tworzą kwasy. Tlenki amfoteryczne jak BeO, Al₂O₃ reagują zarówno z kwasami jak i zasadami, a tlenki obojętne jak CO nie reagują z niczym.
💡 Zapamiętaj: Zasadowe + kwas = sól + woda, kwasowe + zasada = sól + woda, amfoteryczne reagują z obydwoma!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje tlenków z kwasami i zasadami
Tlenek zasadowy + kwas daje sól i wodę, np. CaO + 2HCl → CaCl₂ + H₂O. To klasyczna reakcja neutralizacji, którą napiszesz też w wersji jonowej.
Tlenek kwasowy + zasada też tworzy sól i wodę, jak SO₃ + 2NaOH → Na₂SO₄ + H₂O. Pamiętaj o zbilansowaniu równań - czasem potrzebujesz więcej cząsteczek zasady.
Większość tlenków reaguje z wodą tworząc odpowiednio zasady (tlenki zasadowe) lub kwasy (tlenki kwasowe). Na przykład Na₂O + H₂O → 2NaOH, a SO₃ + H₂O → H₂SO₄.
💡 Tip: Jeśli nie wiesz jakiego typu jest tlenek, sprawdź czy metal czy niemetal - to podpowie Ci typ reakcji!
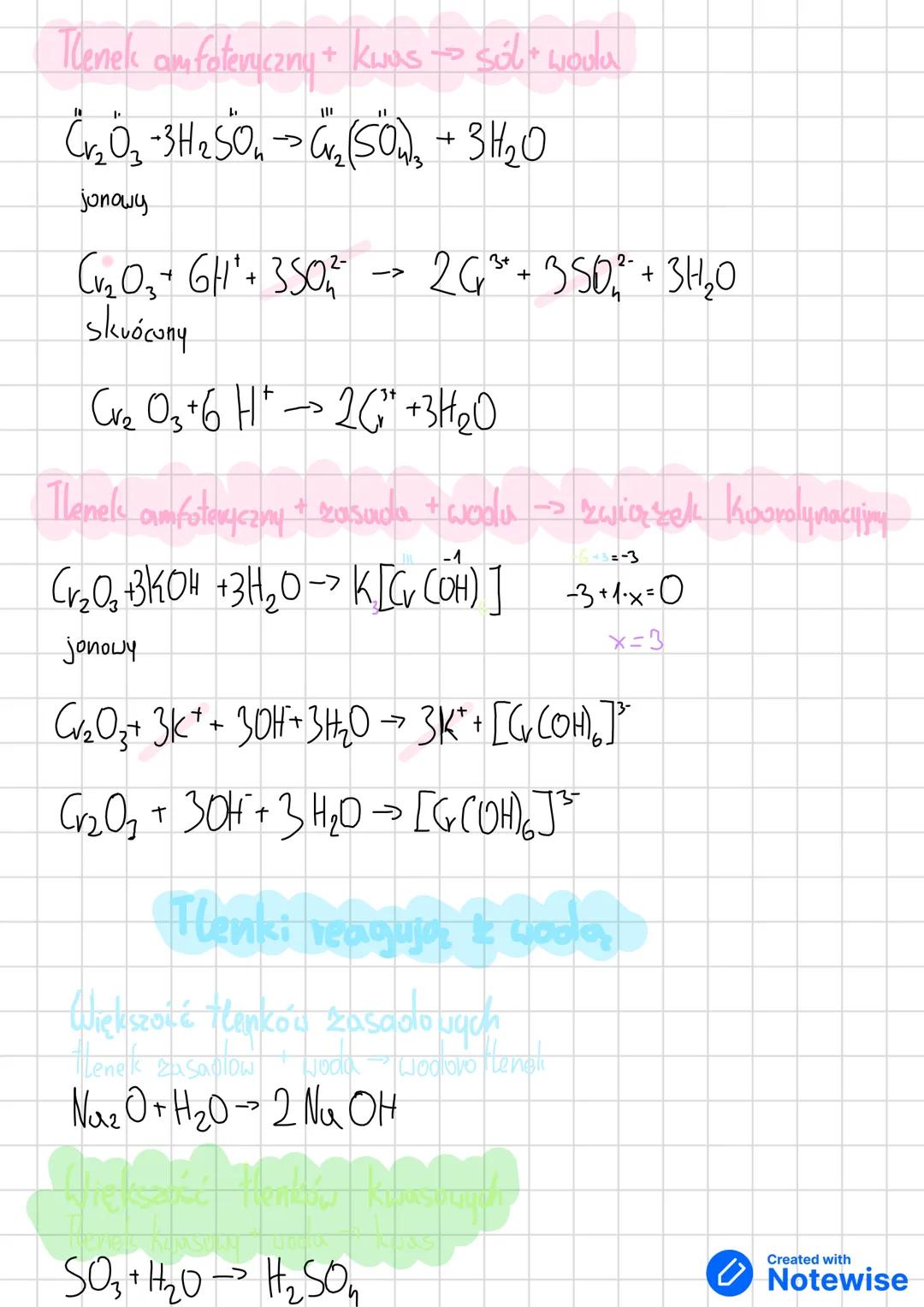
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Tlenki amfoteryczne i ich specjalne reakcje
Tlenki amfoteryczne to "chemiczni dyplomaci" - reagują zarówno z kwasami jak i zasadami. Z kwasem zachowują się jak tlenki zasadowe: Cr₂O₃ + 3H₂SO₄ → Cr₂(SO₄)₃ + 3H₂O.
Z zasadą tworzą jednak związki koordinacyjne z wodą: Cr₂O₃ + 3KOH + 3H₂O → 3K[Cr(OH)₆]. To bardziej skomplikowane produkty niż zwykłe sole.
Kluczowe tlenki amfoteryczne to: BeO, Al₂O₃, Cr₂O₃, ZnO, CuO. Zapamiętaj je, bo często pojawiają się na sprawdzianach jako "pułapki" - wyglądają jak tlenki metali, ale reagują inaczej.
💡 Uwaga: Tlenki amfoteryczne to głównie metale przejściowe i te z granicy metali/niemetali!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie tlenków
Najprostrza metoda to bezpośrednia synteza: metal + tlen = tlenek . To podstawowa reakcja spalania, którą znasz ze środowiska.
Rozkład termiczny to podgrzewanie węglanów czy wodorotlenków: CaCO₃ → CaO + CO₂. Często wykorzystywane w przemyśle, np. przy produkcji wapna.
Inne metody to utlenianie tlenków czy redukcja . Możesz też rozkładać kwasy: H₂SO₄ → SO₂ + H₂O.
💡 Praktycznie: Większość tlenków w przyrodzie powstaje przez spalanie lub rozkład termiczny!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wodorki - związki wodoru
Wodorki to połączenia wodoru z innymi pierwiastkami. Wzór zależy od grupy: dla grup 1-15 piszesz XHₙ, dla grup 16-17 HₙX.
Dzielą się podobnie jak tlenki. Wodorki zasadowe reagują z kwasami: NaH + HCl → NaCl + H₂. Wodorki kwasowe reagują z zasadami.
Reakcja wodorku z kwasem często daje gaz wodór - to charakterystyczne "bulgotanie". Wyjątek to amoniak NH₃, który reaguje inaczej: NH₃ + HCl → NH₄Cl.
💡 Ciekawostka: Wodorki metali to doskonałe źródła wodoru - wystarczy dodać kwas!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje wodorków z wodą i kwasami
Wodorki metali z wodą dają zasadę i wodór: NaH + H₂O → NaOH + H₂↑. To reakcja gwałtowna - wodór może się zapalić!
Amoniak z wodą tworzy słabą zasadę: NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. Symbol równowagi pokazuje, że reakcja jest odwracalna.
Wodorki kwasowe w wodzie rozpadają się na jony: HCl → H⁺ + Cl⁻. To typowe kwasy, które znasz z codzienności.
💡 Bezpieczeństwo: Reakcje wodorków z wodą mogą być bardzo gwałtowne - zawsze ostrożnie!
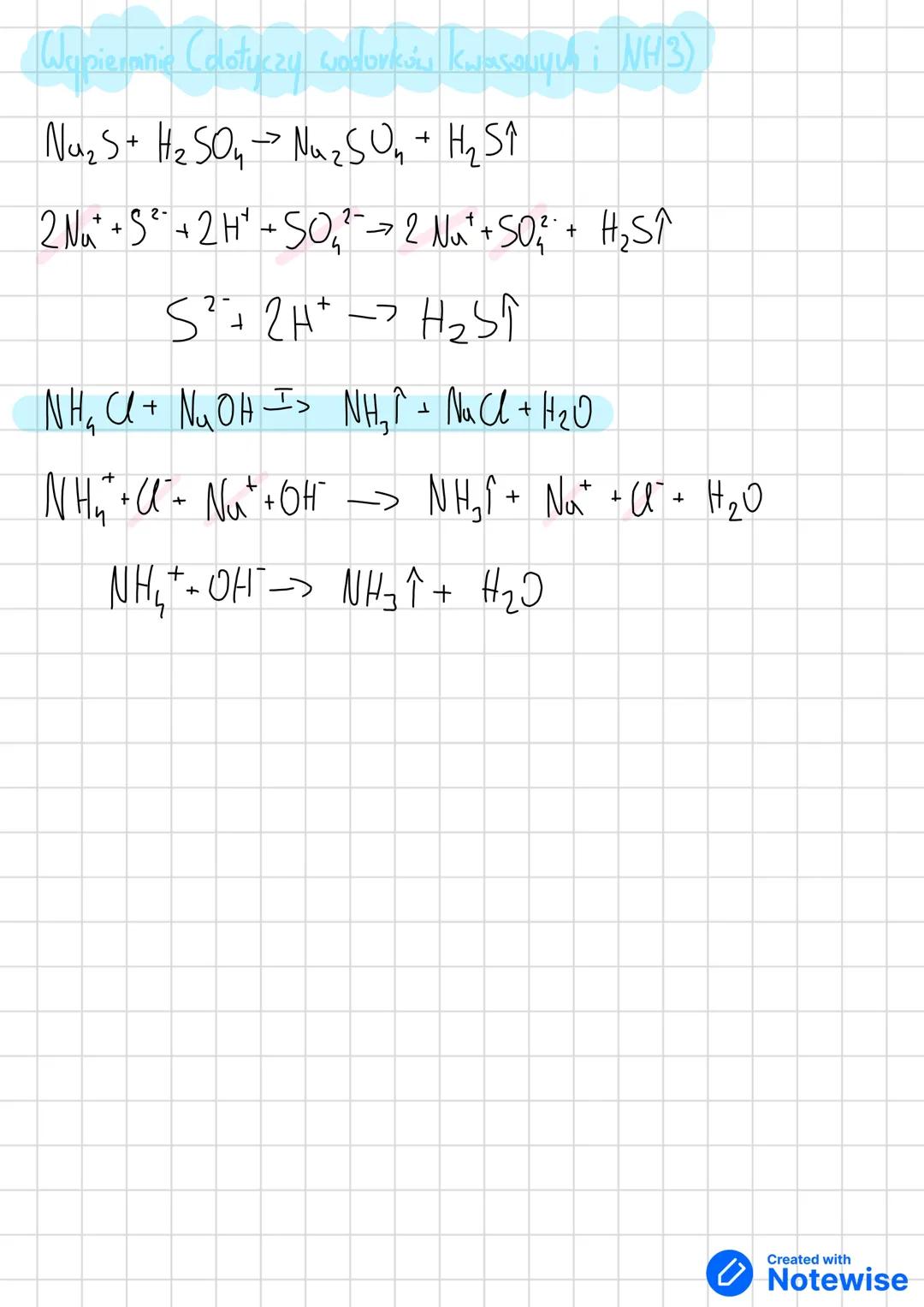
Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie wodorków
Bezpośrednia synteza to reakcja pierwiastka z wodorem: 2Na + H₂ → 2NaH lub N₂ + 3H₂ → 2NH₃. Druga reakcja wymaga katalizatora i ciśnienia.
Wypieranie z soli to klasyczna metoda dla wodorków kwasowych: Na₂S + H₂SO₄ → Na₂SO₄ + H₂S↑. Mocniejszy kwas wypiera słabszy.
Dla amoniaku używasz reakcji: NH₄Cl + NaOH → NH₃↑ + NaCl + H₂O. Podgrzewanie zwiększa wydajność - amoniak ma charakterystyczny ostry zapach.
💡 W laboratorium: Wodorki kwasowe najłatwiej otrzymać przez wypieranie z soli!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Wodorotlenki - budowa i nazewnictwo
Wodorotlenki to związki jonowe składające się z kationu metalu i anionu OH⁻. Wszystkie to ciała stałe o charakterystycznej budowie krystalicznej.
W nazewnictwie dodajesz "wodorotlenek" przed nazwą metalu: Ca(OH)₂ to wodorotlenek wapnia, Al(OH)₃ to wodorotlenek glinu. Dla metali o zmiennej wartościowości dodajesz rzymską cyfrę.
Charakter chemiczny dzieli je na zasadowe , amfoteryczne (Be(OH)₂, Al(OH)₃, Zn(OH)₂) i praktycznie nierozpuszczalne. Tylko wodorotlenki grup 1 i Ba(OH)₂ są dobrze rozpuszczalne.
💡 Pamiętaj: Im bardziej w lewo w układzie okresowym, tym bardziej zasadowy wodorotlenek!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje wodorotlenków
Wodorotlenek zasadowy + kwas to klasyczna neutralizacja: 2Fe(OH)₃ + 3H₂SO₄ → Fe₂(SO₄)₃ + 6H₂O. Pamiętaj o bilansowaniu - często potrzebujesz więcej cząsteczek.
Wodorotlenki amfoteryczne reagują też z zasadami tworząc związki koordynacyjne: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄]. To bardziej złożone struktury niż zwykłe sole.
Reakcje w wersji jonowej pokazują istotę procesu - przejście protonów H⁺ lub jonów OH⁻. To pomaga zrozumieć mechanizm reakcji.
💡 Na sprawdzianie: Zawsze sprawdzaj czy wodorotlenek jest zasadowy czy amfoteryczny!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie wodorotlenków
Metal aktywny + woda daje wodorotlenek i wodór: 2Na + 2H₂O → 2NaOH + H₂↑. Tylko metale grup 1-2 (bez berylu) reagują tak bezpośrednio.
Tlenek zasadowy + woda to najprostsza metoda: Na₂O + H₂O → 2NaOH. Nie wszystkie tlenki tak reagują - sprawdź w tabeli rozpuszczalności.
Strącanie z soli wykorzystujesz gdy inne metody nie działają: BeSO₄ + 2NaOH → Na₂SO₄ + Be(OH)₂↓. Strzałka w dół pokazuje wytrącający się osad.
💡 W przemyśle: Wodorotlenek sodu (soda kaustyczna) otrzymuje się głównie z elektrolizy solanki!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: zasada
9Otrzymywanie Wodorotlenków
Zrozumienie procesu otrzymywania wodorotlenków, ich właściwości oraz reakcji chemicznych. Dowiedz się o wodorotlenkach sodu, wapnia i żelaza (III), ich amfoteryczności oraz zastosowaniach w chemii. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Wodorotlenki: Właściwości i Reakcje
Zgłębiaj właściwości wodorotlenków, ich przygotowanie oraz reakcje z kwasami i solami. Dowiedz się o amfoteryczności, dysocjacji jonowej oraz przykładach wodorotlenków rozpuszczalnych w wodzie. Idealne dla uczniów chemii i studentów. Typ: Podsumowanie.
Wodorotlenki cały dział
Notatka z wodorotlenków - cały dział. Wzory, nazwy, dysocjacja i otrzymywanie wodorotlenków.
Wodorotlenki: Systematyka i Właściwości
Odkryj kluczowe informacje o wodorotlenkach, ich systematyce, właściwościach amfoterycznych oraz sposobach przygotowania. Materiał zawiera szczegółowe opisy wodorotlenków sodu, potasu, wapnia i innych, zgodne z wymaganiami maturalnymi 2023/24. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Właściwości Wodorotlenków
Zgłębiaj właściwości chemiczne wodorotlenków, ich reakcje z kwasami, tlenkami oraz metalami. Dowiedz się o amfoteryczności, przygotowaniu oraz zastosowaniach wodorotlenków, takich jak NaOH, Ca(OH)₂ i Al(OH)₃. Idealne dla uczniów i studentów chemii.
Teorie Kwasów i Zasad
Zgłębiaj teorie kwasów i zasad, w tym teorię Arrheniusa, Brønsteda-Lowry'ego oraz Lewisa. Dowiedz się o roli kwasów i zasad, ich autodysocjacji oraz amfoteryczności. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe koncepcje chemiczne i ich zastosowania w roztworach wodnych.
Wodorotlenki
Notatka z wodorotlenków chemia rozszerzona
Charakterystyka Bloku S
Zgłębiaj właściwości litowców i berylowców, ich reakcje oraz przygotowanie wodorotlenków. Materiał zawiera kluczowe informacje na temat reakcji chemicznych, takich jak tworzenie Ca(OH)2 i NaOH, oraz ich zastosowania w kontekście zadań maturalnych. Idealne dla uczniów przygotowujących się do egzaminów.
Teorie Kwasów i Zasad
Zgłębiaj teorie kwasów i zasad, w tym Arrheniusa, Bronsteda-Lowry'ego oraz Lewisa. Dowiedz się, jak kwasy i zasady dysocjują, jakie mają właściwości oraz jak woda działa jako amfoteryczna substancja. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe koncepcje chemiczne.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.