Witaj! Zapraszam do poznania świata związków węgla, które są podstawą... Pokaż więcej
Węgiel i Węglowodory: Alkan, Alken, Alkin oraz Areny







Odmiany alotropowe węgla
Węgiel występuje w każdym organizmie żywym, a także w minerałach i węglanach jak kalcyt czy dolomit. Ten wszechobecny pierwiastek tworzy cztery różne odmiany alotropowe, każda o unikatowych właściwościach:
Diament to najtwardsza naturalna substancja na Ziemi. Zawdzięcza to bardzo silnym wiązaniom kowalencyjnym tworzącym sztywną strukturę. Jest bezbarwny, nierozpuszczalny w wodzie i nie przewodzi prądu, choć dobrze przewodzi ciepło.
Grafit ma strukturę warstwową, gdzie poszczególne płaszczyzny atomów węgla połączone są słabymi oddziaływaniami van der Waalsa. To sprawia, że jest łupliwy i ścierny. W przeciwieństwie do diamentu, grafit dobrze przewodzi prąd elektryczny dzięki zdelokalizowanym elektronom π, które mogą swobodnie przemieszczać się między warstwami.
Grafen składa się z pojedynczej warstwy atomów węgla. Jest niezwykle wytrzymały, przezroczysty i świetnie przewodzi prąd i ciepło, co czyni go materiałem przyszłości w elektronice.
💡 Pamiętaj, że grafit i grafen przewodzą prąd elektryczny, a diament nie - to kluczowa różnica wynikająca z ich struktury atomowej!
Fulereny to kuliste struktury węglowe, które pod wpływem światła ulegają rozkładowi i reagują z litowcami. Mają metaliczny połysk i barwę od żółtej do czerwonobrązowej.

Reakcje w chemii organicznej
Zrozumienie mechanizmów reakcji to klucz do opanowania chemii organicznej. Istnieją dwa główne typy mechanizmów:
Mechanizmy jonowe tworzą jako produkty pośrednie karbokationy lub karboaniony, gdzie ładunki elektryczne są zlokalizowane na atomach węgla. Przykładem jest addycja elektrofilowa, gdzie elektrofile (cząsteczki poszukujące elektronów) przyłączają się do wiązania podwójnego:
- Rozpad wiązania kowalencyjnego w cząsteczce bromu: Br-Br → Br⁺ + Br⁻
- Addycja jonu Br⁺ do elektronów π w etenie i powstanie karbokationu
- Addycja jonu Br⁻ do karbokationu i utworzenie końcowego produktu
Mechanizmy rodnikowe tworzą produkty pośrednie zawierające niesparowane elektrony. Przykładem jest substytucja rodnikowa:
- Inicjacja: utworzenie rodników
- Propagacja: atak rodnika na cząsteczkę metanu i tworzenie nowych rodników
- Terminacja: przerwanie reakcji łańcuchowej
💡 Na egzaminie zawsze zwracaj uwagę na typ mechanizmu reakcji - jonowy czy rodnikowy - to pomaga przewidzieć produkty!
W chemii organicznej występują trzy główne typy reakcji:
- Substytucja: zastąpienie atomu lub grupy atomów innym atomem lub grupą
- Addycja: przyłączenie substancji do wiązania wielokrotnego
- Eliminacja: odłączenie atomów od cząsteczki i utworzenie wiązania wielokrotnego
Rzędowość atomów węgla określa liczbę innych atomów węgla bezpośrednio z nim połączonych .

Alkany
Alkany to najprostsze węglowodory, które zawierają tylko pojedyncze wiązania między atomami węgla. Można je podzielić na łańcuchowe i pierścieniowe (cykloalkany).
Atomy węgla w alkanach mają hybrydyzację sp³, co daje tetraedryczną strukturę o kącie między wiązaniami 109°28'. Każdy atom węgla tworzy cztery wiązania pojedyncze (sigma). Ta struktura sprawia, że alkany są bardzo mało reaktywne.
Metan (CH₄) - najprostszy alkan - jest bezbarwnym, bezwonnym gazem o gęstości mniejszej od powietrza. Można go otrzymać przez:
- Reakcję octanu sodu z wodorotlenkiem sodu
- Hydrolizę węgliku glinu
Najważniejsze reakcje alkanów to:
- Spalanie
- Substytucja z chlorem, bromem i fluorem (reakcja rodnikowa)
💡 Zapamiętaj wzór ogólny alkanów: C₍ₙ₎H₍₂ₙ₊₂₎ - to podstawa do obliczania wszystkich wzorów!
Alkany tworzą szereg homologiczny, gdzie każdy kolejny związek różni się od poprzedniego o grupę -CH₂-. Wraz ze wzrostem liczby atomów węgla rośnie temperatura wrzenia i topnienia .
Alkany występują w postaci izomerów konstytucyjnych - związków o tym samym wzorze sumarycznym, ale różnej budowie i właściwościach. Najważniejsze typy izomerii to łańcuchy proste i rozgałęzione .

Nazewnictwo alkanów
Znajomość zasad nazewnictwa jest niezbędna do opisywania i rozpoznawania związków organicznych. Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) ustaliła jednolity system, który stosuje się na całym świecie.
Nazwy alkanów o prostym łańcuchu to: metan, etan, propan, butan, pentan, heksan, heptan, oktan, nonan i dekan. Te nazwy stanowią podstawę do nazywania bardziej złożonych związków.
Przy tworzeniu nazw systematycznych alkanów należy przestrzegać pięciu głównych zasad:
- Ustal najdłuższy łańcuch węglowy - jego nazwa będzie podstawą nazwy związku.
- Ponumeruj atomy węgla w łańcuchu tak, by lokalizacja podstawników miała jak najmniejsze numery.
- Wymień nazwy podstawników (grup alkilowych) w kolejności alfabetycznej.
- Oznacz liczbę identycznych podstawników przedrostkami: di-, tri-, tetra-, penta- itd.
- Zapisz pełną nazwę, podając na początku numery, liczbę i rodzaj podstawników, a na końcu nazwę alkanu odpowiadającego najdłuższemu łańcuchowi.
💡 Grupę alkilową tworzy się przez oderwanie atomu wodoru od alkanu i zmianę końcówki nazwy z -an na -yl (np. metan → metyl, etan → etyl).
Podstawniki to atomy lub grupy atomów związane z łańcuchem głównym. Ich położenie określają lokanty - liczby wskazujące numery atomów węgla, do których są przyłączone.
Przykład poprawnie utworzonej nazwy: 2,2-dichloropropan , gdzie dwa atomy chloru są przyłączone do drugiego atomu węgla w łańcuchu propanu.
Cykloalkany
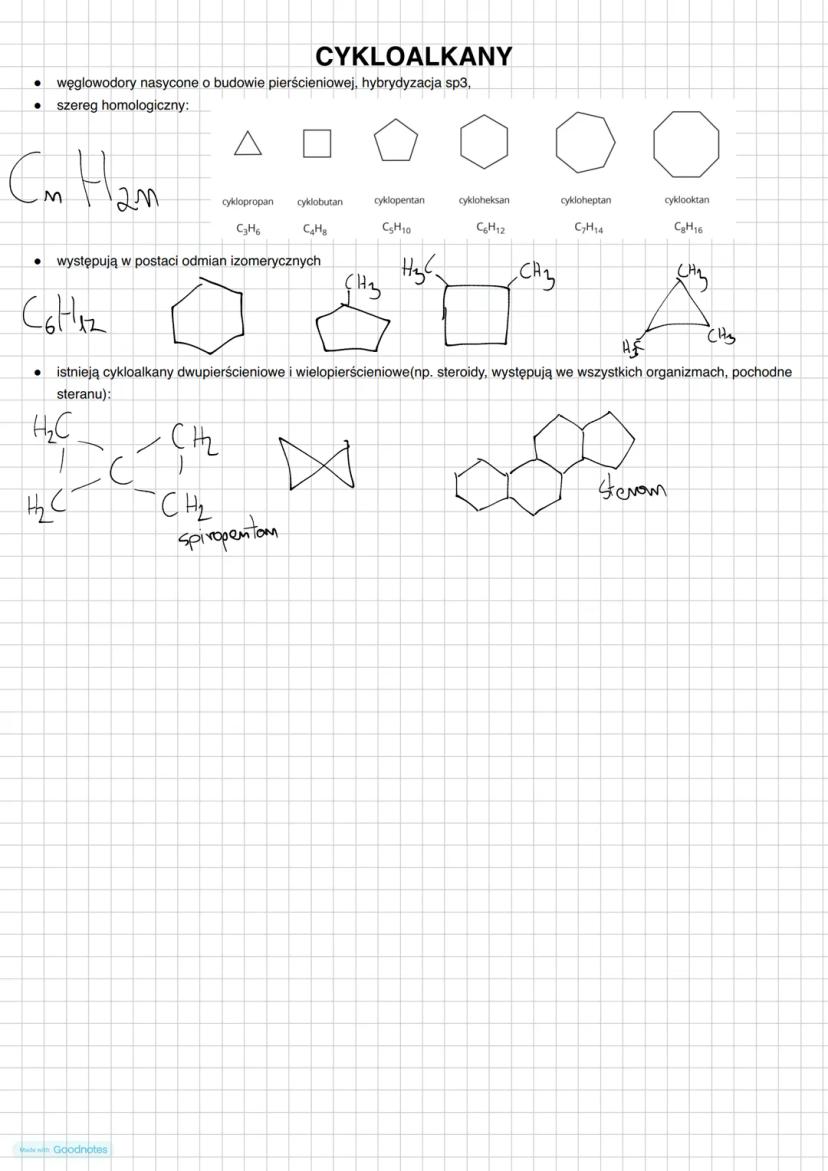
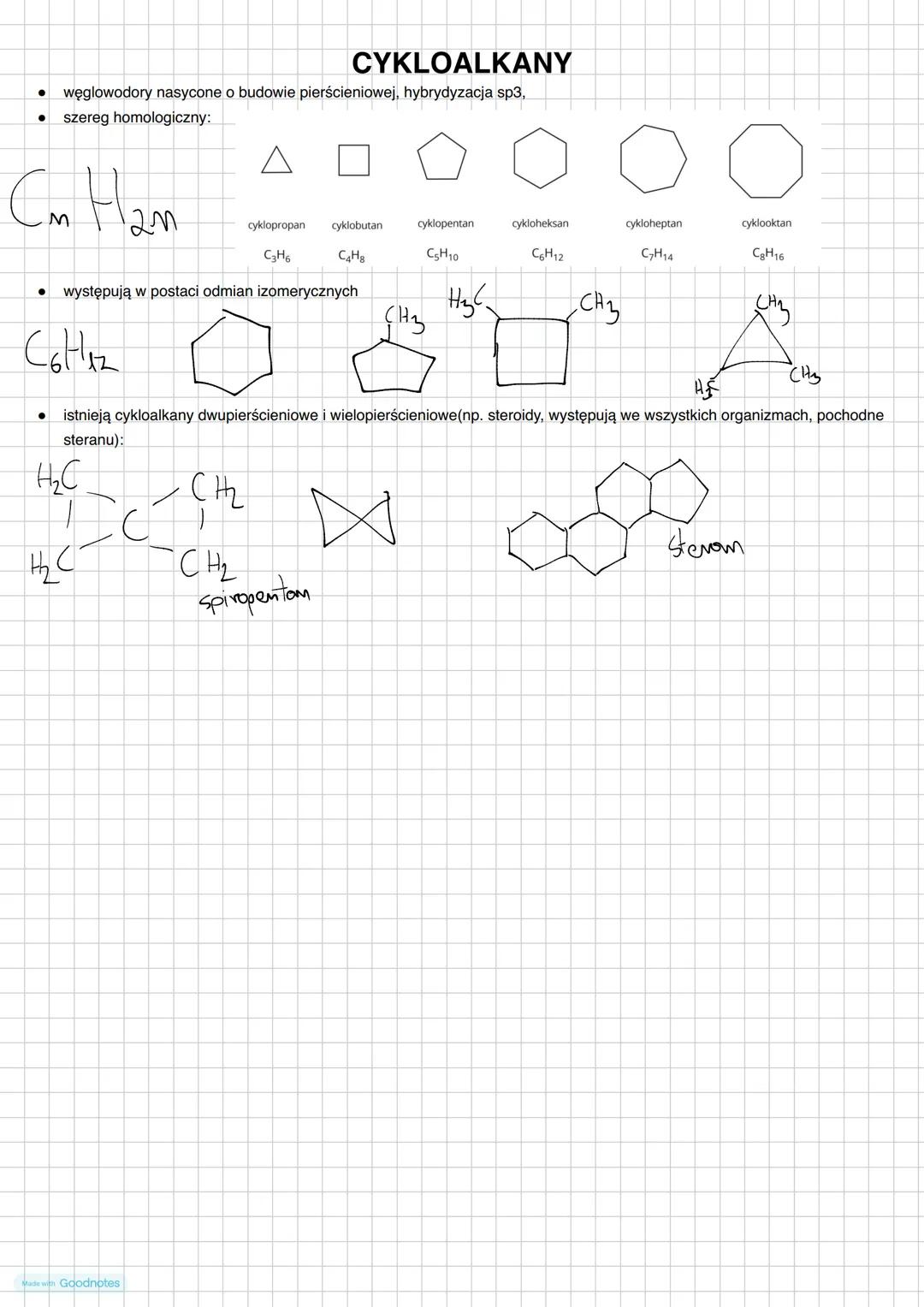
Cykloalkany to węglowodory nasycone o budowie pierścieniowej, w których atomy węgla tworzą zamknięty pierścień. Podobnie jak alkany, mają hybrydyzację sp³, ale różnią się wzorem ogólnym.
Szereg homologiczny cykloalkanów opisuje wzór C₍ₙ₎H₍₂ₙ₎, co oznacza, że mają o dwa atomy wodoru mniej niż odpowiadające im alkany. Najprostsze cykloalkany to:
- Cyklopropan (C₃H₆) - trójkątny pierścień
- Cyklobutan (C₄H₈) - czworokątny pierścień
- Cyklopentan (C₅H₁₀) - pięciokątny pierścień
- Cykloheksan (C₆H₁₂) - sześciokątny pierścień
Cykloalkany mogą występować w postaci różnych odmian izomerycznych. Na przykład, związek o wzorze C₆H₁₂ może być zarówno cykloheksanem jak i innymi izomerami.
💡 Pierścienie cykloalkanów mogą być napięte (jak w cyklopropanie) lub stabilne (jak w cykloheksanie), co wpływa na ich reaktywność!
W przyrodzie występują również bardziej złożone struktury - cykloalkany dwupierścieniowe i wielopierścieniowe. Szczególnie ważne są steroidy (pochodne steranu), które występują we wszystkich organizmach i pełnią kluczowe funkcje biologiczne.
Spiropentan jest przykładem cykloalkanu, w którym dwa pierścienie łączą się przez pojedynczy atom węgla, tworząc charakterystyczną strukturę.

Alkeny
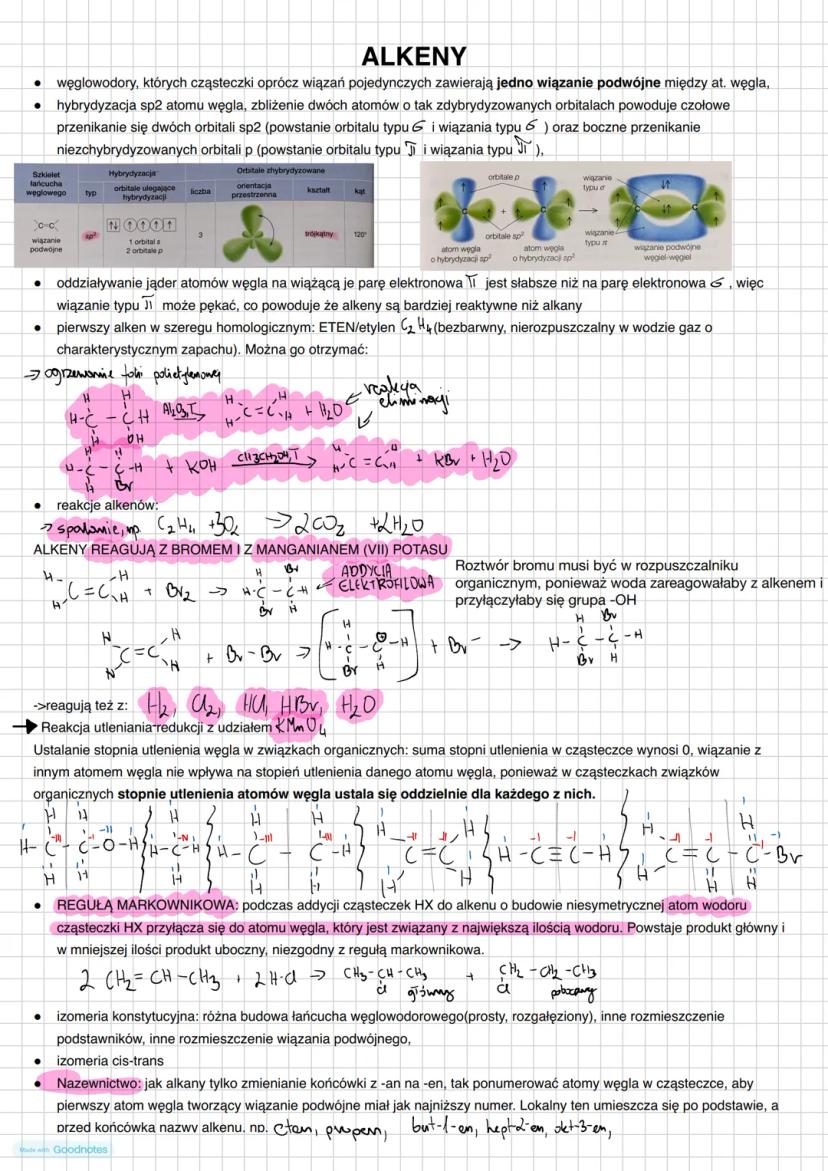
Alkeny to węglowodory zawierające przynajmniej jedno wiązanie podwójne między atomami węgla. Ta cecha strukturalna nadaje im specyficzne właściwości i reaktywność.
Atomy węgla tworzące wiązanie podwójne mają hybrydyzację sp². Wiązanie podwójne składa się z:
- Wiązania sigma (σ) - powstaje przez czołowe nakładanie orbitali sp²
- Wiązania pi (π) - powstaje przez boczne nakładanie niezhydrydyzowanych orbitali p
Wiązanie π jest słabsze niż wiązanie σ i może łatwiej pękać, co sprawia, że alkeny są bardziej reaktywne niż alkany.
Najprostszym alkenem jest eten - bezbarwny gaz o charakterystycznym zapachu. Można go otrzymać przez ogrzewanie folii polietylenowej lub przez odwodnienie etanolu.
Najważniejsze reakcje alkenów:
- Spalanie
- Addycja elektrofilowa (reagują z Br₂, H₂, Cl₂, HCl, HBr, H₂O)
- Reakcje z manganianem(VII) potasu (KMnO₄)
💡 WAŻNE! Alkeny odbarwiają zarówno roztwór bromu, jak i roztwór manganianu(VII) potasu - to kluczowy test na ich obecność!
Przy addycji niesymetrycznych reagentów do niesymetrycznych alkenów obowiązuje reguła Markownikowa: atom wodoru przyłącza się do tego atomu węgla, który jest związany z większą liczbą atomów wodoru.
Alkeny wykazują izomerię konstytucyjną (różna budowa łańcucha, różne rozmieszczenie wiązania podwójnego) oraz izomerię cis-trans.
Nazwa alkenów tworzy się podobnie jak alkanów, zmieniając końcówkę z -an na -en i dodając lokant wskazujący położenie wiązania podwójnego .

Szereg homologiczny alkenów i polimeryzacja
Alkeny tworzą szereg homologiczny o wzorze ogólnym C₍ₙ₎H₍₂ₙ₎. Pierwszy członek szeregu to eten (C₂H₄), a kolejne to: propen (C₃H₆), but-1-en (C₄H₈), pent-1-en (C₅H₁₀) itd.
Wzory alkenów można zapisywać na różne sposoby:
- Strukturalny (pokazuje wszystkie atomy i wiązania)
- Półstrukturalny
- Grupowy (np. CH₂CH(CH₂)₂CH₃)
- Szkieletowy/kreskowy (najprostszy, pokazuje tylko szkielet węglowy)
Podobnie jak w przypadku alkanów, wraz ze wzrostem liczby atomów węgla w cząsteczce rosną temperatury wrzenia i topnienia oraz gęstość. Alkeny o 2-4 atomach węgla są gazami, o 5-10 atomach - cieczami, a o większej liczbie - substancjami stałymi.
💡 Różnice w zapisie wzorów nie są tylko kosmetyczne - różne sposoby zapisu pomagają podkreślić inne aspekty budowy cząsteczki!
Alkeny mogą tworzyć związki z wieloma wiązaniami podwójnymi - alkadieny (dwa wiązania podwójne) i alkatrieny (trzy wiązania podwójne).
Niezwykle ważną reakcją alkenów jest polimeryzacja - łączenie się pojedynczych cząsteczek (monomerów) w wielkocząsteczkowy związek (polimer). Mer to powtarzający się fragment w polimerze. Przykłady:
- Z etenu powstaje polietylen
- Z propenu powstaje polipropylen
Polimery są odporne na działanie kwasów, zasad i większości rozpuszczalników organicznych, co czyni je niezwykle użytecznymi materiałami w życiu codziennym.

Alkiny
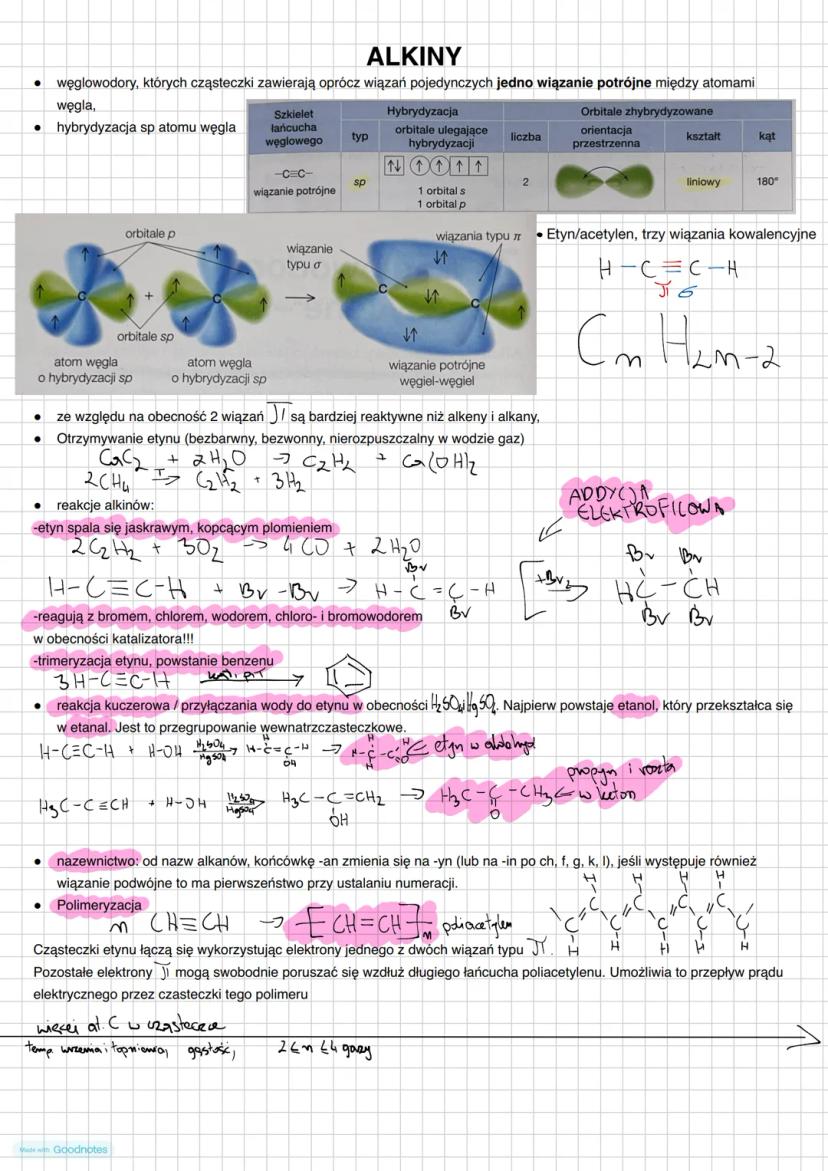
Alkiny to węglowodory zawierające wiązanie potrójne między atomami węgla. Ta specyficzna cecha strukturalna nadaje im unikalne właściwości chemiczne.
Atomy węgla tworzące wiązanie potrójne mają hybrydyzację sp. W wiązaniu potrójnym występuje:
- Jedno wiązanie sigma (σ) - powstaje przez czołowe nakładanie orbitali sp
- Dwa wiązania pi (π) - powstają przez boczne nakładanie niezhydrydyzowanych orbitali p
Ze względu na obecność dwóch wiązań π, alkiny są jeszcze bardziej reaktywne niż alkeny.
Najprostszym alkinem jest etyn (acetyen, C₂H₂) - bezbarwny, bezwonny gaz nierozpuszczalny w wodzie. Można go otrzymać w reakcji: 2CaC₂ + 2H₂O → C₂H₂ + Ca(OH)₂
Najważniejsze reakcje alkinów:
- Spalanie (etyn spala się jaskrawym, kopcącym płomieniem)
- Addycja (reagują z Br₂, Cl₂, H₂, HCl, HBr)
- Trimeryzacja etynu z powstaniem benzenu
- Reakcja Kuczerowa - przyłączanie wody do etynu
💡 Etyn może tworzyć poliacetylen, który - w przeciwieństwie do większości polimerów - przewodzi prąd elektryczny!
Nazewnictwo alkinów jest podobne do alkenów - końcówkę -an zmienia się na -yn . Jeśli w cząsteczce występuje również wiązanie podwójne, to ma ono pierwszeństwo przy ustalaniu numeracji.
Szereg homologiczny alkinów opisuje wzór ogólny C₍ₙ₎H₍₂ₙ₋₂₎. Pierwsze alkiny są gazami, a wraz ze wzrostem łańcucha węglowego rosną temperatury wrzenia i topnienia.
Szereg homologiczny alkinów
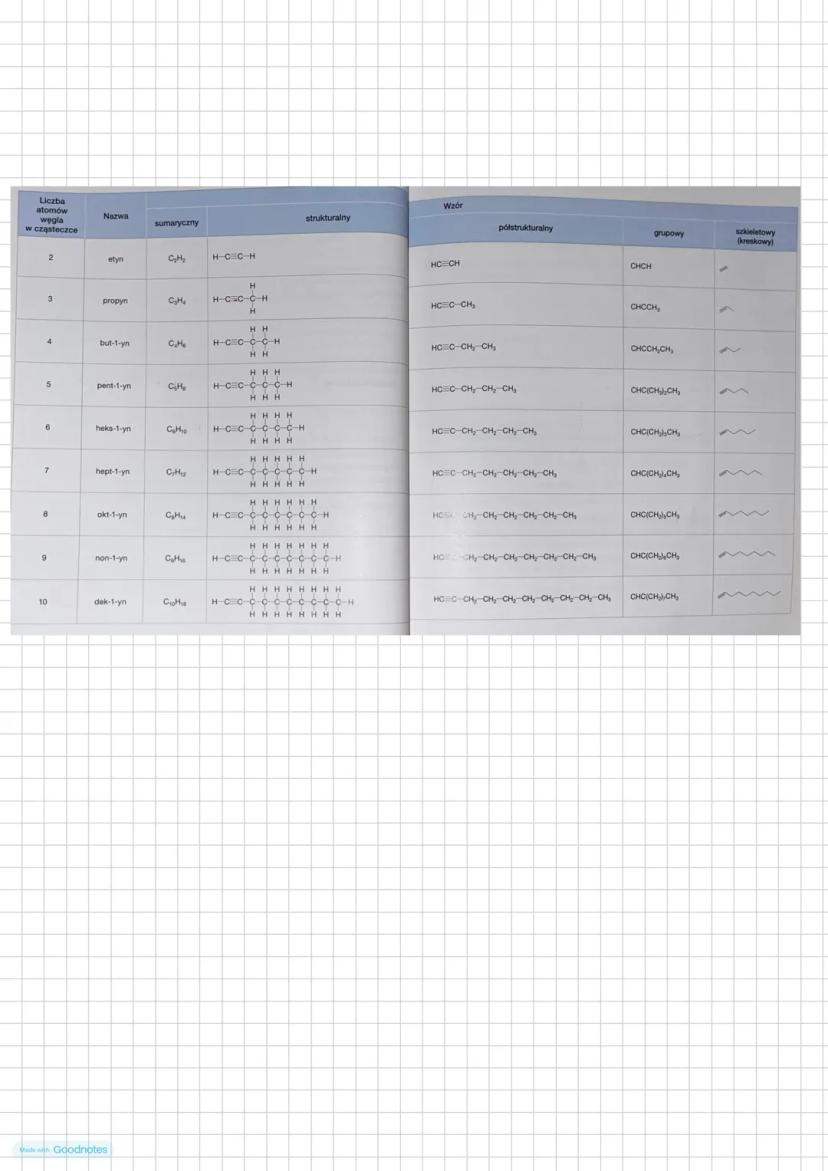
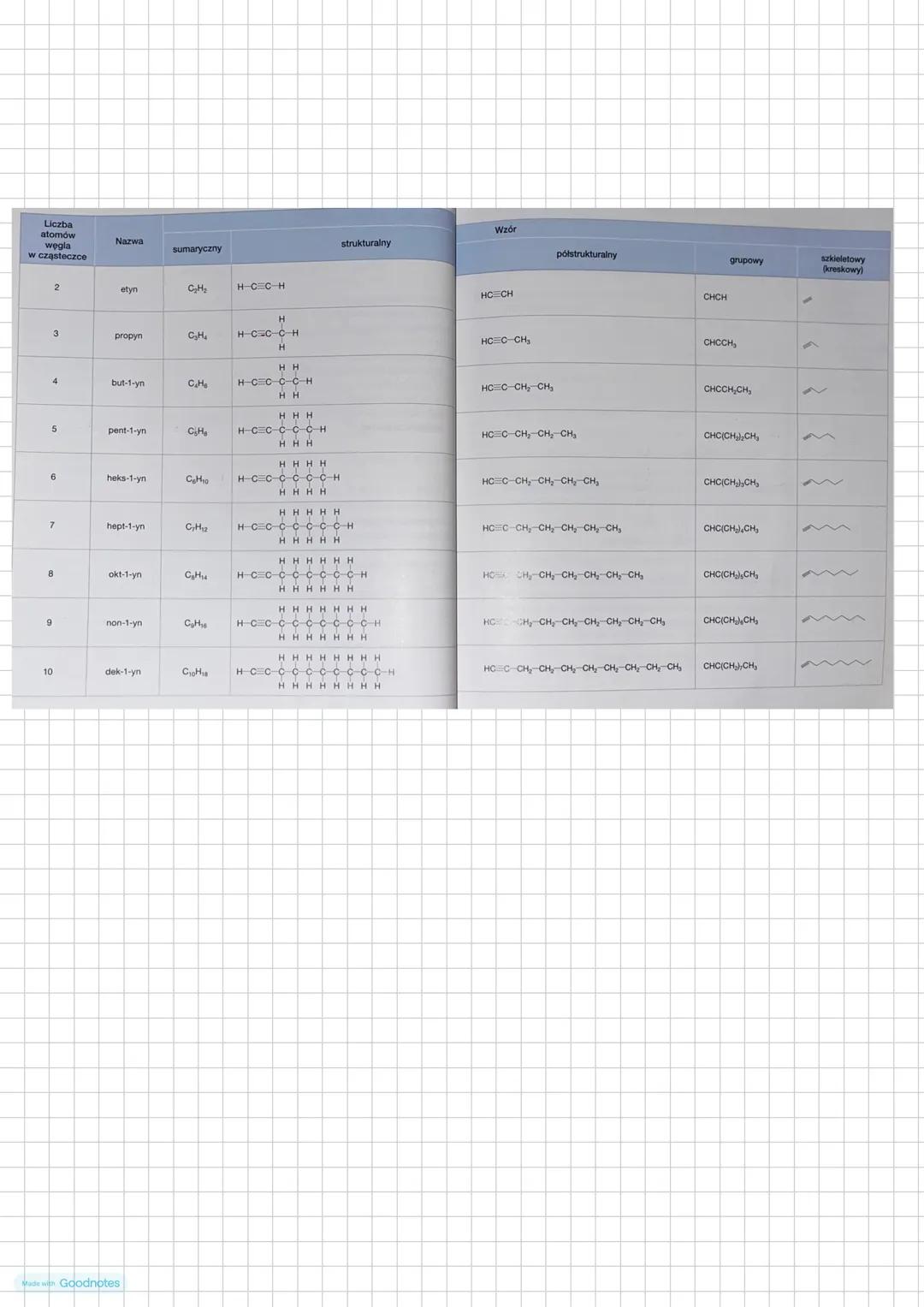
Alkiny tworzą szereg homologiczny, w którym każdy kolejny członek różni się od poprzedniego o grupę -CH₂-. Wzór ogólny alkinów to C₍ₙ₎H₍₂ₙ₋₂₎.
Pierwszy członek szeregu to etyn (C₂H₂), a kolejne to: propyn (C₃H₄), but-1-yn (C₄H₆), pent-1-yn (C₅H₈) itd.
Podobnie jak w przypadku alkenów, wzory alkinów można zapisywać na różne sposoby:
- Strukturalny (pokazuje wszystkie atomy i wiązania)
- Półstrukturalny
- Grupowy
- Szkieletowy/kreskowy (najprostszy, pokazuje tylko szkielet węglowy)
💡 Przy zapisywaniu wzorów alkinów zawsze pamiętaj o wiązaniu potrójnym (≡) - to kluczowy element budowy tych związków!
W miarę wzrostu długości łańcucha węglowego zmieniają się właściwości fizyczne alkinów:
- Etyn to gaz
- But-1-yn i propyn to również gazy w warunkach normalnych
- Dłuższe alkiny to ciecze
- Alkiny o bardzo długich łańcuchach są substancjami stałymi
Warto pamiętać, że alkiny można zapisać za pomocą tzw. izomerii położeniowej - wiązanie potrójne może znajdować się przy różnych atomach węgla, np. but-1-yn i but-2-yn to dwa różne związki o tym samym wzorze sumarycznym, ale innych właściwościach.
Każdy z tych wzorów służy nieco innemu celowi - strukturalny pokazuje dokładną budowę, a szkieletowy pozwala szybko zauważyć istotne elementy struktury, co jest przydatne przy analizowaniu złożonych związków.

Areny (węglowodory aromatyczne)
Areny to wyjątkowa grupa węglowodorów posiadających pierścieniowy układ sprzężonych wiązań podwójnych. Nazwa pochodzi od aromatycznych zapachów wielu z tych związków.
Najpopularniejsze areny to: benzen, metylobenzen (toluen), etylobenzen i propylobenzen. Charakteryzują się niezwykłą trwałością dzięki zdelokalizowanym elektronom w pierścieniu.
Budowa benzenu:
- Płaska, pierścieniowa struktura
- Atomy węgla w hybrydyzacji sp²
- Każdy atom węgla tworzy dwa wiązania z sąsiednimi atomami węgla i jedno z wodorem
- Sześć elektronów tworzy zdelokalizowane wiązania π nad i pod płaszczyzną pierścienia
Zgodnie z regułą Hückla, związki aromatyczne mają 4n+2 elektronów zdelokalizowanych (gdzie n to liczba naturalna). Benzen ma 6 elektronów zdelokalizowanych .
💡 Najważniejszy test na aromatyczność: benzen NIE odbarwia wody bromowej ani roztworu KMnO₄, co odróżnia go od alkenów i alkinów!
Benzen to bezbarwna ciecz o charakterystycznym zapachu, o gęstości mniejszej od wody. Nie rozpuszcza się w wodzie i spala się kopcącym płomieniem, co świadczy o dużej zawartości węgla.
Najważniejsze reakcje benzenu:
- Spalanie: 2C₆H₆ + 15O₂ → 12CO₂ + 6H₂O
- Substytucja elektrofilowa (a nie addycja jak w alkenach!):
- Bromowanie (z FeBr₃ jako katalizatorem)
- Nitrowanie (z mieszaniną HNO₃ i H₂SO₄)
Benzen można otrzymać przez destylację smoły węglowej, trimeryzację etynu lub w procesie reformingu.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Węglowodory: Alkany, Alkeny, Alkiny
Zgłębiaj właściwości, reakcje i zastosowania węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o ich strukturze, procesach spalania, polimeryzacji oraz naturalnych źródłach. Idealne dla uczniów 8 klasy.
Węglowodory: Alkany, Alkeny, Alkiny
Zrozumienie węglowodorów nasyconych i nienasyconych: alkany, alkeny i alkiny. Dowiedz się o ich strukturze, właściwościach, zastosowaniach oraz reakcjach chemicznych. Idealne dla uczniów szkół podstawowych i średnich. Typ: Podsumowanie.
Alkiny
Chemia organiczna Notatka na podstawie portalu dlaucznia.pl i podręcznika Chemia Nowej Ery 8
Węglowodory sprawdzian Nowa Era
Test z nowej ery z chemii
Alkany: Właściwości i Reakcje
Odkryj kluczowe informacje o alkanach, ich właściwościach, nomenklaturze oraz reakcjach spalania. Dowiedz się, jak nazywać alkany i jakie mają zastosowania. Idealne dla studentów chemii. Typ: Podsumowanie.
Alkeny: Struktura i Właściwości
Zgłębiaj alkeny, nienasycone węglowodory z podwójnymi wiązaniami. Dowiedz się o ich budowie, właściwościach fizycznych i chemicznych, regule Markownikowa oraz procesie polimeryzacji. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje związane z alkenami.
Właściwości i Budowa Alkinów
Zgłębiaj właściwości, budowę i reakcje alkinów, w tym ich izomery i reakcje spalania. Dowiedz się, jak tworzyć nazwy alkinów oraz poznaj ich wzory strukturalne i ogólne. Idealne dla studentów chemii poszukujących zrozumienia węglowodorów nienasyconych.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Węgiel i Węglowodory: Alkan, Alken, Alkin oraz Areny
Witaj! Zapraszam do poznania świata związków węgla, które są podstawą chemii organicznej. Odkryjemy różne formy i właściwości węgla oraz poznamy najważniejsze klasy związków organicznych: alkany, cykloalkany, alkeny, alkiny i areny. Każda z tych grup ma charakterystyczne cechy i reaktywność, które... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Odmiany alotropowe węgla
Węgiel występuje w każdym organizmie żywym, a także w minerałach i węglanach jak kalcyt czy dolomit. Ten wszechobecny pierwiastek tworzy cztery różne odmiany alotropowe, każda o unikatowych właściwościach:
Diament to najtwardsza naturalna substancja na Ziemi. Zawdzięcza to bardzo silnym wiązaniom kowalencyjnym tworzącym sztywną strukturę. Jest bezbarwny, nierozpuszczalny w wodzie i nie przewodzi prądu, choć dobrze przewodzi ciepło.
Grafit ma strukturę warstwową, gdzie poszczególne płaszczyzny atomów węgla połączone są słabymi oddziaływaniami van der Waalsa. To sprawia, że jest łupliwy i ścierny. W przeciwieństwie do diamentu, grafit dobrze przewodzi prąd elektryczny dzięki zdelokalizowanym elektronom π, które mogą swobodnie przemieszczać się między warstwami.
Grafen składa się z pojedynczej warstwy atomów węgla. Jest niezwykle wytrzymały, przezroczysty i świetnie przewodzi prąd i ciepło, co czyni go materiałem przyszłości w elektronice.
💡 Pamiętaj, że grafit i grafen przewodzą prąd elektryczny, a diament nie - to kluczowa różnica wynikająca z ich struktury atomowej!
Fulereny to kuliste struktury węglowe, które pod wpływem światła ulegają rozkładowi i reagują z litowcami. Mają metaliczny połysk i barwę od żółtej do czerwonobrązowej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje w chemii organicznej
Zrozumienie mechanizmów reakcji to klucz do opanowania chemii organicznej. Istnieją dwa główne typy mechanizmów:
Mechanizmy jonowe tworzą jako produkty pośrednie karbokationy lub karboaniony, gdzie ładunki elektryczne są zlokalizowane na atomach węgla. Przykładem jest addycja elektrofilowa, gdzie elektrofile (cząsteczki poszukujące elektronów) przyłączają się do wiązania podwójnego:
- Rozpad wiązania kowalencyjnego w cząsteczce bromu: Br-Br → Br⁺ + Br⁻
- Addycja jonu Br⁺ do elektronów π w etenie i powstanie karbokationu
- Addycja jonu Br⁻ do karbokationu i utworzenie końcowego produktu
Mechanizmy rodnikowe tworzą produkty pośrednie zawierające niesparowane elektrony. Przykładem jest substytucja rodnikowa:
- Inicjacja: utworzenie rodników
- Propagacja: atak rodnika na cząsteczkę metanu i tworzenie nowych rodników
- Terminacja: przerwanie reakcji łańcuchowej
💡 Na egzaminie zawsze zwracaj uwagę na typ mechanizmu reakcji - jonowy czy rodnikowy - to pomaga przewidzieć produkty!
W chemii organicznej występują trzy główne typy reakcji:
- Substytucja: zastąpienie atomu lub grupy atomów innym atomem lub grupą
- Addycja: przyłączenie substancji do wiązania wielokrotnego
- Eliminacja: odłączenie atomów od cząsteczki i utworzenie wiązania wielokrotnego
Rzędowość atomów węgla określa liczbę innych atomów węgla bezpośrednio z nim połączonych .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkany
Alkany to najprostsze węglowodory, które zawierają tylko pojedyncze wiązania między atomami węgla. Można je podzielić na łańcuchowe i pierścieniowe (cykloalkany).
Atomy węgla w alkanach mają hybrydyzację sp³, co daje tetraedryczną strukturę o kącie między wiązaniami 109°28'. Każdy atom węgla tworzy cztery wiązania pojedyncze (sigma). Ta struktura sprawia, że alkany są bardzo mało reaktywne.
Metan (CH₄) - najprostszy alkan - jest bezbarwnym, bezwonnym gazem o gęstości mniejszej od powietrza. Można go otrzymać przez:
- Reakcję octanu sodu z wodorotlenkiem sodu
- Hydrolizę węgliku glinu
Najważniejsze reakcje alkanów to:
- Spalanie
- Substytucja z chlorem, bromem i fluorem (reakcja rodnikowa)
💡 Zapamiętaj wzór ogólny alkanów: C₍ₙ₎H₍₂ₙ₊₂₎ - to podstawa do obliczania wszystkich wzorów!
Alkany tworzą szereg homologiczny, gdzie każdy kolejny związek różni się od poprzedniego o grupę -CH₂-. Wraz ze wzrostem liczby atomów węgla rośnie temperatura wrzenia i topnienia .
Alkany występują w postaci izomerów konstytucyjnych - związków o tym samym wzorze sumarycznym, ale różnej budowie i właściwościach. Najważniejsze typy izomerii to łańcuchy proste i rozgałęzione .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo alkanów
Znajomość zasad nazewnictwa jest niezbędna do opisywania i rozpoznawania związków organicznych. Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) ustaliła jednolity system, który stosuje się na całym świecie.
Nazwy alkanów o prostym łańcuchu to: metan, etan, propan, butan, pentan, heksan, heptan, oktan, nonan i dekan. Te nazwy stanowią podstawę do nazywania bardziej złożonych związków.
Przy tworzeniu nazw systematycznych alkanów należy przestrzegać pięciu głównych zasad:
- Ustal najdłuższy łańcuch węglowy - jego nazwa będzie podstawą nazwy związku.
- Ponumeruj atomy węgla w łańcuchu tak, by lokalizacja podstawników miała jak najmniejsze numery.
- Wymień nazwy podstawników (grup alkilowych) w kolejności alfabetycznej.
- Oznacz liczbę identycznych podstawników przedrostkami: di-, tri-, tetra-, penta- itd.
- Zapisz pełną nazwę, podając na początku numery, liczbę i rodzaj podstawników, a na końcu nazwę alkanu odpowiadającego najdłuższemu łańcuchowi.
💡 Grupę alkilową tworzy się przez oderwanie atomu wodoru od alkanu i zmianę końcówki nazwy z -an na -yl (np. metan → metyl, etan → etyl).
Podstawniki to atomy lub grupy atomów związane z łańcuchem głównym. Ich położenie określają lokanty - liczby wskazujące numery atomów węgla, do których są przyłączone.
Przykład poprawnie utworzonej nazwy: 2,2-dichloropropan , gdzie dwa atomy chloru są przyłączone do drugiego atomu węgla w łańcuchu propanu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Cykloalkany
Cykloalkany to węglowodory nasycone o budowie pierścieniowej, w których atomy węgla tworzą zamknięty pierścień. Podobnie jak alkany, mają hybrydyzację sp³, ale różnią się wzorem ogólnym.
Szereg homologiczny cykloalkanów opisuje wzór C₍ₙ₎H₍₂ₙ₎, co oznacza, że mają o dwa atomy wodoru mniej niż odpowiadające im alkany. Najprostsze cykloalkany to:
- Cyklopropan (C₃H₆) - trójkątny pierścień
- Cyklobutan (C₄H₈) - czworokątny pierścień
- Cyklopentan (C₅H₁₀) - pięciokątny pierścień
- Cykloheksan (C₆H₁₂) - sześciokątny pierścień
Cykloalkany mogą występować w postaci różnych odmian izomerycznych. Na przykład, związek o wzorze C₆H₁₂ może być zarówno cykloheksanem jak i innymi izomerami.
💡 Pierścienie cykloalkanów mogą być napięte (jak w cyklopropanie) lub stabilne (jak w cykloheksanie), co wpływa na ich reaktywność!
W przyrodzie występują również bardziej złożone struktury - cykloalkany dwupierścieniowe i wielopierścieniowe. Szczególnie ważne są steroidy (pochodne steranu), które występują we wszystkich organizmach i pełnią kluczowe funkcje biologiczne.
Spiropentan jest przykładem cykloalkanu, w którym dwa pierścienie łączą się przez pojedynczy atom węgla, tworząc charakterystyczną strukturę.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkeny
Alkeny to węglowodory zawierające przynajmniej jedno wiązanie podwójne między atomami węgla. Ta cecha strukturalna nadaje im specyficzne właściwości i reaktywność.
Atomy węgla tworzące wiązanie podwójne mają hybrydyzację sp². Wiązanie podwójne składa się z:
- Wiązania sigma (σ) - powstaje przez czołowe nakładanie orbitali sp²
- Wiązania pi (π) - powstaje przez boczne nakładanie niezhydrydyzowanych orbitali p
Wiązanie π jest słabsze niż wiązanie σ i może łatwiej pękać, co sprawia, że alkeny są bardziej reaktywne niż alkany.
Najprostszym alkenem jest eten - bezbarwny gaz o charakterystycznym zapachu. Można go otrzymać przez ogrzewanie folii polietylenowej lub przez odwodnienie etanolu.
Najważniejsze reakcje alkenów:
- Spalanie
- Addycja elektrofilowa (reagują z Br₂, H₂, Cl₂, HCl, HBr, H₂O)
- Reakcje z manganianem(VII) potasu (KMnO₄)
💡 WAŻNE! Alkeny odbarwiają zarówno roztwór bromu, jak i roztwór manganianu(VII) potasu - to kluczowy test na ich obecność!
Przy addycji niesymetrycznych reagentów do niesymetrycznych alkenów obowiązuje reguła Markownikowa: atom wodoru przyłącza się do tego atomu węgla, który jest związany z większą liczbą atomów wodoru.
Alkeny wykazują izomerię konstytucyjną (różna budowa łańcucha, różne rozmieszczenie wiązania podwójnego) oraz izomerię cis-trans.
Nazwa alkenów tworzy się podobnie jak alkanów, zmieniając końcówkę z -an na -en i dodając lokant wskazujący położenie wiązania podwójnego .

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Szereg homologiczny alkenów i polimeryzacja
Alkeny tworzą szereg homologiczny o wzorze ogólnym C₍ₙ₎H₍₂ₙ₎. Pierwszy członek szeregu to eten (C₂H₄), a kolejne to: propen (C₃H₆), but-1-en (C₄H₈), pent-1-en (C₅H₁₀) itd.
Wzory alkenów można zapisywać na różne sposoby:
- Strukturalny (pokazuje wszystkie atomy i wiązania)
- Półstrukturalny
- Grupowy (np. CH₂CH(CH₂)₂CH₃)
- Szkieletowy/kreskowy (najprostszy, pokazuje tylko szkielet węglowy)
Podobnie jak w przypadku alkanów, wraz ze wzrostem liczby atomów węgla w cząsteczce rosną temperatury wrzenia i topnienia oraz gęstość. Alkeny o 2-4 atomach węgla są gazami, o 5-10 atomach - cieczami, a o większej liczbie - substancjami stałymi.
💡 Różnice w zapisie wzorów nie są tylko kosmetyczne - różne sposoby zapisu pomagają podkreślić inne aspekty budowy cząsteczki!
Alkeny mogą tworzyć związki z wieloma wiązaniami podwójnymi - alkadieny (dwa wiązania podwójne) i alkatrieny (trzy wiązania podwójne).
Niezwykle ważną reakcją alkenów jest polimeryzacja - łączenie się pojedynczych cząsteczek (monomerów) w wielkocząsteczkowy związek (polimer). Mer to powtarzający się fragment w polimerze. Przykłady:
- Z etenu powstaje polietylen
- Z propenu powstaje polipropylen
Polimery są odporne na działanie kwasów, zasad i większości rozpuszczalników organicznych, co czyni je niezwykle użytecznymi materiałami w życiu codziennym.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkiny
Alkiny to węglowodory zawierające wiązanie potrójne między atomami węgla. Ta specyficzna cecha strukturalna nadaje im unikalne właściwości chemiczne.
Atomy węgla tworzące wiązanie potrójne mają hybrydyzację sp. W wiązaniu potrójnym występuje:
- Jedno wiązanie sigma (σ) - powstaje przez czołowe nakładanie orbitali sp
- Dwa wiązania pi (π) - powstają przez boczne nakładanie niezhydrydyzowanych orbitali p
Ze względu na obecność dwóch wiązań π, alkiny są jeszcze bardziej reaktywne niż alkeny.
Najprostszym alkinem jest etyn (acetyen, C₂H₂) - bezbarwny, bezwonny gaz nierozpuszczalny w wodzie. Można go otrzymać w reakcji: 2CaC₂ + 2H₂O → C₂H₂ + Ca(OH)₂
Najważniejsze reakcje alkinów:
- Spalanie (etyn spala się jaskrawym, kopcącym płomieniem)
- Addycja (reagują z Br₂, Cl₂, H₂, HCl, HBr)
- Trimeryzacja etynu z powstaniem benzenu
- Reakcja Kuczerowa - przyłączanie wody do etynu
💡 Etyn może tworzyć poliacetylen, który - w przeciwieństwie do większości polimerów - przewodzi prąd elektryczny!
Nazewnictwo alkinów jest podobne do alkenów - końcówkę -an zmienia się na -yn . Jeśli w cząsteczce występuje również wiązanie podwójne, to ma ono pierwszeństwo przy ustalaniu numeracji.
Szereg homologiczny alkinów opisuje wzór ogólny C₍ₙ₎H₍₂ₙ₋₂₎. Pierwsze alkiny są gazami, a wraz ze wzrostem łańcucha węglowego rosną temperatury wrzenia i topnienia.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Szereg homologiczny alkinów
Alkiny tworzą szereg homologiczny, w którym każdy kolejny członek różni się od poprzedniego o grupę -CH₂-. Wzór ogólny alkinów to C₍ₙ₎H₍₂ₙ₋₂₎.
Pierwszy członek szeregu to etyn (C₂H₂), a kolejne to: propyn (C₃H₄), but-1-yn (C₄H₆), pent-1-yn (C₅H₈) itd.
Podobnie jak w przypadku alkenów, wzory alkinów można zapisywać na różne sposoby:
- Strukturalny (pokazuje wszystkie atomy i wiązania)
- Półstrukturalny
- Grupowy
- Szkieletowy/kreskowy (najprostszy, pokazuje tylko szkielet węglowy)
💡 Przy zapisywaniu wzorów alkinów zawsze pamiętaj o wiązaniu potrójnym (≡) - to kluczowy element budowy tych związków!
W miarę wzrostu długości łańcucha węglowego zmieniają się właściwości fizyczne alkinów:
- Etyn to gaz
- But-1-yn i propyn to również gazy w warunkach normalnych
- Dłuższe alkiny to ciecze
- Alkiny o bardzo długich łańcuchach są substancjami stałymi
Warto pamiętać, że alkiny można zapisać za pomocą tzw. izomerii położeniowej - wiązanie potrójne może znajdować się przy różnych atomach węgla, np. but-1-yn i but-2-yn to dwa różne związki o tym samym wzorze sumarycznym, ale innych właściwościach.
Każdy z tych wzorów służy nieco innemu celowi - strukturalny pokazuje dokładną budowę, a szkieletowy pozwala szybko zauważyć istotne elementy struktury, co jest przydatne przy analizowaniu złożonych związków.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Areny (węglowodory aromatyczne)
Areny to wyjątkowa grupa węglowodorów posiadających pierścieniowy układ sprzężonych wiązań podwójnych. Nazwa pochodzi od aromatycznych zapachów wielu z tych związków.
Najpopularniejsze areny to: benzen, metylobenzen (toluen), etylobenzen i propylobenzen. Charakteryzują się niezwykłą trwałością dzięki zdelokalizowanym elektronom w pierścieniu.
Budowa benzenu:
- Płaska, pierścieniowa struktura
- Atomy węgla w hybrydyzacji sp²
- Każdy atom węgla tworzy dwa wiązania z sąsiednimi atomami węgla i jedno z wodorem
- Sześć elektronów tworzy zdelokalizowane wiązania π nad i pod płaszczyzną pierścienia
Zgodnie z regułą Hückla, związki aromatyczne mają 4n+2 elektronów zdelokalizowanych (gdzie n to liczba naturalna). Benzen ma 6 elektronów zdelokalizowanych .
💡 Najważniejszy test na aromatyczność: benzen NIE odbarwia wody bromowej ani roztworu KMnO₄, co odróżnia go od alkenów i alkinów!
Benzen to bezbarwna ciecz o charakterystycznym zapachu, o gęstości mniejszej od wody. Nie rozpuszcza się w wodzie i spala się kopcącym płomieniem, co świadczy o dużej zawartości węgla.
Najważniejsze reakcje benzenu:
- Spalanie: 2C₆H₆ + 15O₂ → 12CO₂ + 6H₂O
- Substytucja elektrofilowa (a nie addycja jak w alkenach!):
- Bromowanie (z FeBr₃ jako katalizatorem)
- Nitrowanie (z mieszaniną HNO₃ i H₂SO₄)
Benzen można otrzymać przez destylację smoły węglowej, trimeryzację etynu lub w procesie reformingu.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: węglowodory
9Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Węglowodory: Alkany, Alkeny, Alkiny
Zgłębiaj właściwości, reakcje i zastosowania węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o ich strukturze, procesach spalania, polimeryzacji oraz naturalnych źródłach. Idealne dla uczniów 8 klasy.
Węglowodory: Alkany, Alkeny, Alkiny
Zrozumienie węglowodorów nasyconych i nienasyconych: alkany, alkeny i alkiny. Dowiedz się o ich strukturze, właściwościach, zastosowaniach oraz reakcjach chemicznych. Idealne dla uczniów szkół podstawowych i średnich. Typ: Podsumowanie.
Alkiny
Chemia organiczna Notatka na podstawie portalu dlaucznia.pl i podręcznika Chemia Nowej Ery 8
Węglowodory sprawdzian Nowa Era
Test z nowej ery z chemii
Alkany: Właściwości i Reakcje
Odkryj kluczowe informacje o alkanach, ich właściwościach, nomenklaturze oraz reakcjach spalania. Dowiedz się, jak nazywać alkany i jakie mają zastosowania. Idealne dla studentów chemii. Typ: Podsumowanie.
Alkeny: Struktura i Właściwości
Zgłębiaj alkeny, nienasycone węglowodory z podwójnymi wiązaniami. Dowiedz się o ich budowie, właściwościach fizycznych i chemicznych, regule Markownikowa oraz procesie polimeryzacji. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje związane z alkenami.
Właściwości i Budowa Alkinów
Zgłębiaj właściwości, budowę i reakcje alkinów, w tym ich izomery i reakcje spalania. Dowiedz się, jak tworzyć nazwy alkinów oraz poznaj ich wzory strukturalne i ogólne. Idealne dla studentów chemii poszukujących zrozumienia węglowodorów nienasyconych.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.