Poznasz tu trzy główne grupy węglowodorów - alkany, alkeny i... Pokaż więcej
Węglowodory: Alkany, Alkeny, Alkiny i Związki Aromatyczne









Alkany - podstawowe węglowodory
Alkany to najprostrze węglowodory o wzorze ogólnym CnH2n+2. Kluczowe jest rozróżnienie atomów równocennych (jak te w metanie CH4) i nierównocennych - to wpływa na to, ile produktów powstaje w reakcjach.
Spalanie może przebiegać na trzy sposoby. Spalanie całkowite daje CO2 i H2O, niecałkowite (przy ograniczonym dostępie tlenu) tworzy tlenek węgla CO, a przy bardzo małej ilości tlenu powstaje sadza (węgiel).
Najważniejsza reakcja to bromowanie - typ substytucji z mechanizmem rodnikowym. Światło inicjuje reakcję, tworząc rodniki Br•. Przy monochlorowaniu propanu głównym produktem jest 2-chloropropan, bo rodnik częściej przyłącza się do węgla o wyższej gęstości elektronowej.
Zapamiętaj: Liczba produktów = liczba różnych (nierównocennych) atomów węgla w cząsteczce!
Synteza Wurtza łączy dwie cząsteczki organiczne przez sód metaliczny: 2 CH3Cl + 2 Na → CH3-CH3 + 2 NaCl. W krzyżowej syntezie Wurtza mogą powstawać produkty uboczne.

Właściwości fizyczne i chemiczne alkanów
Alkany mają gęstość zawsze mniejszą od wody i nie rozpuszczają się w wodzie ani polarnych rozpuszczalnikach. To dlatego, że są niepolarne.
Temperatura wrzenia rośnie wraz z masą cząsteczkową, ale maleje przy rozgałęzieniu łańcucha. Alkany liniowe mają większe oddziaływania międzycząsteczkowe niż rozgałęzione, stąd wyższe temperatury wrzenia.
Chemicznie alkany są mało reaktywne - dlatego nazywa się je parafinami (od łac. "małe powinowactwo"). Reagują głównie w reakcjach spalania i halogenowania w obecności światła.
Ważne: Rozgałęzienie obniża temperaturę wrzenia, bo cząsteczki słabiej się przyciągają!

Cykloalkany - alkany w pierścieniu
Cykloalkany mają wzór CnH2n i powstają gdy odległość między atomami bromu wynosi dokładnie 3 węgle. To umożliwia zamknięcie pierścienia po eliminacji HBr.
Występuje izomeria pierścieniowa - dla C5H10 możesz mieć cyklopentan, metylocyklobutan i inne struktury pierścieniowe. Każda ma inną budowę, ale ten sam wzór sumaryczny.
Cykloalkany mają wyższe temperatury wrzenia i topnienia niż odpowiednie alkany liniowe. Dzieje się tak, bo cząsteczki w pierścieniu mają więcej kontaktów między sobą = silniejsze oddziaływania międzycząsteczkowe.
Spalanie przebiega podobnie jak u alkanów: całkowite daje CO2 + H2O, niecałkowite CO + H2O, a przy deficycie tlenu powstaje sadza.
Wskazówka: Cykloalkany = "alkany w kółku" z wszystkimi konsekwencjami dla właściwości!
Stereoizomeria - przestrzenny świat cząsteczek
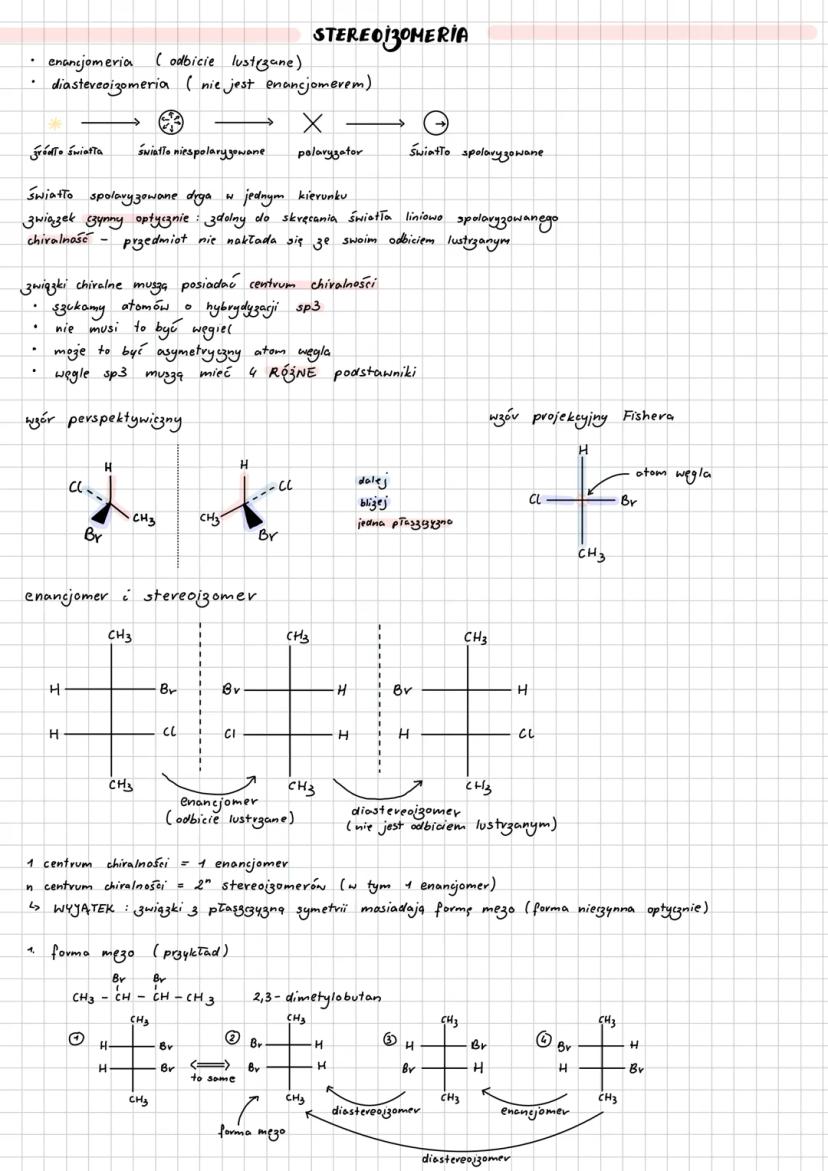
Stereoizomeria to zjawisko, gdy cząsteczki mają ten sam wzór, ale różną orientację w przestrzeni. Dzieli się na enancjomerię (odbicia lustrzane) i diastereoizomerię.
Chiralność występuje gdy cząsteczka nie nakłada się na swoje odbicie lustrzane. Potrzebny jest atom węgla sp³ z czterema różnymi podstawnikami - to centrum chiralności.
Liczba stereoizomerów = 2ⁿ . Wyjątek: związki z płaszczyzną symetrii mają formę mezo - są nieczynne optycznie mimo centrów chiralności.
Enancjomery różnią się tylko kierunkiem skręcania światła spolaryzowanego. Mieszanina racemiczna (racemat) to równomolowa mieszanka dwóch enancjomerów - jest optycznie nieaktywna.
Kluczowe: 1 centrum chiralności = 1 para enancjomerów. Więcej centrów = więcej możliwości!

Izomeria geometryczna E/Z
Izomeria cis-trans to szczególny przypadek izomerii E/Z przy wiązaniach podwójnych. Warunek: różne podstawniki przy każdym węglu podwójnego wiązania.
Izomer cis ma podobne grupy po tej samej stronie wiązania. Ma moment dipolowy ≠ 0, wyższą temperaturę wrzenia, większą energię i reaktywność.
Izomer trans ma podobne grupy po przeciwnych stronach. Moment dipolowy = 0, niższa energia, wyższa temperatura topnienia, większa stabilność.
Przy oznaczaniu E/Z liczy się pierwszeństwo podstawników według liczby atomowej: I > Br > Cl > O > N > C > H. E = podstawniki o wyższym pierwszeństwie po przeciwnych stronach, Z = po tej samej.
Zapamiętaj: Cis = "po tej samej stronie", Trans = "na przeciwko"

Alkeny - węglowodory z wiązaniem podwójnym
Alkeny mają wzór CnH2n i zawierają wiązanie podwójne C=C. Atomy przy wiązaniu podwójnym mają hybrydyzację sp² i leżą w jednej płaszczyźnie.
Występują różne typy izomerii: położenia , konstytucyjna i geometryczna. Alkadieny mają dwa wiązania podwójne - mogą być skumulowane, sprzężone lub izolowane.
Główne reakcje to addycja elektrofilowa. Przy HCl do propenu powstaje 2-chloropropan zgodnie z regułą Markownikowa - wodór przyłącza się do węgla z większą liczbą wodorów.
Polimeryzacja łączy małe cząsteczki (monomery) w długie łańcuchy. Eten → polietylen (PE), propen → polipropylen (PP), chlorek winylu → PVC.
Ważne: Reguła Markownikowa - "bogaty się bogaci" (wodór do węgla z więcej wodorów)!

Reakcje alkenów - addycja i eliminacja
Addycja wody w środowisku kwasowym daje alkohole. H+ przyłącza się według reguły Markownikowa, potem H₂O jako nukleofil, na koniec odłącza się H+ tworząc alkohol.
Addycja wodoru (z katalizatorem) przekształca alken w alkan. Eliminacja to reakcja odwrotna - z alkanu powstaje alken. Te reakcje są odwracalne.
Przy addycji HBr do but-2-enu powstają dwa produkty w podobnych ilościach - reguła Markownikowa nie działa, bo oba węgle mają podobną gęstość elektronową.
Polimeryzacja tworzy ważne tworzywa: PE (polieten) odporny chemicznie, PP (polipropylen), PVC (z chlorku winylu), PTFE (teflon) odporny na wysokie temperatury.
Praktycznie: Znając te reakcje, możesz przewidzieć produkty większości przemian alkenów!

Utlenianie alkenów
Utlenianie w środowisku obojętnym manganianem(VII) daje diole. Eten + MnO₄⁻ → etano-1,2-diol + MnO₂. Obserwujesz odbarwienie fioletowego roztworu i brunatny osad MnO₂.
W środowisku kwasowym manganian(VII) redukuje się do Mn²⁺ - również obserwujesz odbarwienie fioletowego roztworu, ale bez osadu.
To są reakcje charakterystyczne do wykrywania alkenów - zmiana barwy z fioletowej na bezbarwną to pewny znak obecności wiązania podwójnego.
Test na alkeny: Fioletowy KMnO₄ + alken = odbarwienie roztworu!

Alkiny - potrójne wiązania
Alkiny mają wzór CnH₂ⁿ⁻² i wiązanie potrójne C≡C. Etyn (acetylen) ma kształt liniowy z kątem 180° i hybrydyzację sp.
Reguła nazewnictwa: wiązanie podwójne ma mniejszy numer niż potrójne w nazwie związku.
Reakcja Kuczerowa to addycja wody do etynu przez niestabilny enol, dając aldehyd octowy (CH₃CHO). Inne alkiny + woda = ketony.
Alkiny przechodzą stopniową addycję: alkin + H₂ → alken + H₂ → alkan. Przy addycji HBr do alkinów powstają geminalne dibromki (dwa bromy przy tym samym węglu).
Ważne: Alkiny są bardziej reaktywne niż alkeny przez większe napięcie wiązania potrójnego!
Benzen - król związków aromatycznych
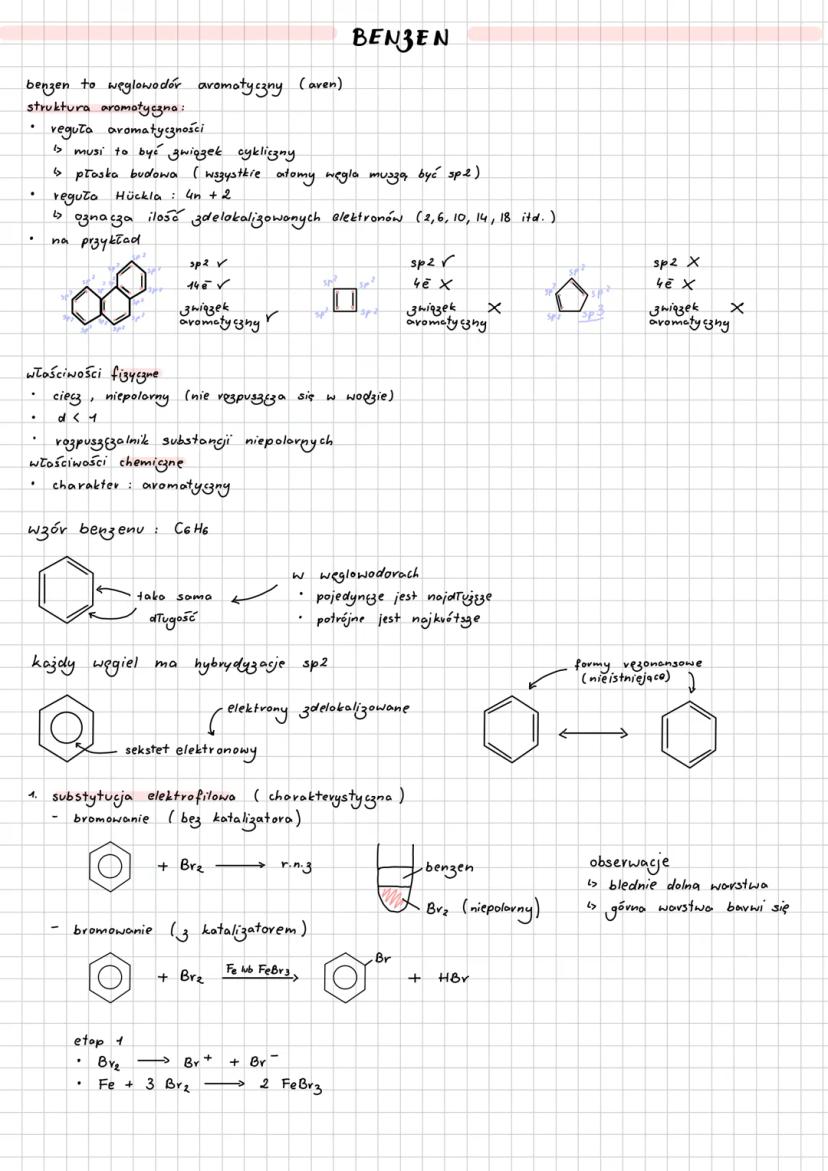
Benzen (C₆H₆) to podstawowy węglowodór aromatyczny o płaskiej, cyklicznej budowie. Wszystkie węgle mają hybrydyzację sp² z elektronami zdelokalizowanymi.
Reguła aromatyczności: związek musi być cykliczny, płaski i mieć 4n+2 zdelokalizowanych elektronów (reguła Hückla). Dla benzenu: 6 elektronów = 4×1+2 ✓
Właściwości fizyczne: ciecz niepolarna, gęstość < 1, nie rozpuszcza się w wodzie, dobry rozpuszczalnik substancji niepolarnych.
Substytucja elektrofilowa to charakterystyczna reakcja. Bromowanie bez katalizatora nie zachodzi, z katalizatorem (Fe lub FeBr₃) powstaje bromobenzen + HBr. Obserwujesz blaknięcie dolnej warstwy i barwienie górnej.
Kluczowe: Benzen = stabilny pierścień aromatyczny, trudny do "złamania"!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: prawa chemii
2Prawo Stałości Składu
Zrozumienie Prawa Stałości Składu Związków Chemicznych: Obliczanie stosunków masowych i procentowych pierwiastków w związkach chemicznych, takich jak CO₂. Dowiedz się, jak stosować masy atomowe do obliczeń oraz jak interpretować wyniki. Idealne dla uczniów chemii na poziomie średnim.
Prawa Chemiczne: Skład i Masa
Zgłębiaj kluczowe prawa chemiczne, w tym prawo stałości składu związków chemicznych oraz prawo zachowania masy. Dowiedz się o odkryciach Joseph'a Louisa Prousta i Michaiła Wasiliewicza Łomonosowa, które ukształtowały współczesną chemię. Idealne dla studentów chemii i biologii. Typ: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Węglowodory: Alkany, Alkeny, Alkiny i Związki Aromatyczne
Poznasz tu trzy główne grupy węglowodorów - alkany, alkeny i alkiny - oraz dowiesz się o ich strukturze, reakcjach i właściwościach. To fundamentalna wiedza z chemii organicznej, która przyda Ci się na każdej klasówce!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkany - podstawowe węglowodory
Alkany to najprostrze węglowodory o wzorze ogólnym CnH2n+2. Kluczowe jest rozróżnienie atomów równocennych (jak te w metanie CH4) i nierównocennych - to wpływa na to, ile produktów powstaje w reakcjach.
Spalanie może przebiegać na trzy sposoby. Spalanie całkowite daje CO2 i H2O, niecałkowite (przy ograniczonym dostępie tlenu) tworzy tlenek węgla CO, a przy bardzo małej ilości tlenu powstaje sadza (węgiel).
Najważniejsza reakcja to bromowanie - typ substytucji z mechanizmem rodnikowym. Światło inicjuje reakcję, tworząc rodniki Br•. Przy monochlorowaniu propanu głównym produktem jest 2-chloropropan, bo rodnik częściej przyłącza się do węgla o wyższej gęstości elektronowej.
Zapamiętaj: Liczba produktów = liczba różnych (nierównocennych) atomów węgla w cząsteczce!
Synteza Wurtza łączy dwie cząsteczki organiczne przez sód metaliczny: 2 CH3Cl + 2 Na → CH3-CH3 + 2 NaCl. W krzyżowej syntezie Wurtza mogą powstawać produkty uboczne.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości fizyczne i chemiczne alkanów
Alkany mają gęstość zawsze mniejszą od wody i nie rozpuszczają się w wodzie ani polarnych rozpuszczalnikach. To dlatego, że są niepolarne.
Temperatura wrzenia rośnie wraz z masą cząsteczkową, ale maleje przy rozgałęzieniu łańcucha. Alkany liniowe mają większe oddziaływania międzycząsteczkowe niż rozgałęzione, stąd wyższe temperatury wrzenia.
Chemicznie alkany są mało reaktywne - dlatego nazywa się je parafinami (od łac. "małe powinowactwo"). Reagują głównie w reakcjach spalania i halogenowania w obecności światła.
Ważne: Rozgałęzienie obniża temperaturę wrzenia, bo cząsteczki słabiej się przyciągają!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Cykloalkany - alkany w pierścieniu
Cykloalkany mają wzór CnH2n i powstają gdy odległość między atomami bromu wynosi dokładnie 3 węgle. To umożliwia zamknięcie pierścienia po eliminacji HBr.
Występuje izomeria pierścieniowa - dla C5H10 możesz mieć cyklopentan, metylocyklobutan i inne struktury pierścieniowe. Każda ma inną budowę, ale ten sam wzór sumaryczny.
Cykloalkany mają wyższe temperatury wrzenia i topnienia niż odpowiednie alkany liniowe. Dzieje się tak, bo cząsteczki w pierścieniu mają więcej kontaktów między sobą = silniejsze oddziaływania międzycząsteczkowe.
Spalanie przebiega podobnie jak u alkanów: całkowite daje CO2 + H2O, niecałkowite CO + H2O, a przy deficycie tlenu powstaje sadza.
Wskazówka: Cykloalkany = "alkany w kółku" z wszystkimi konsekwencjami dla właściwości!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
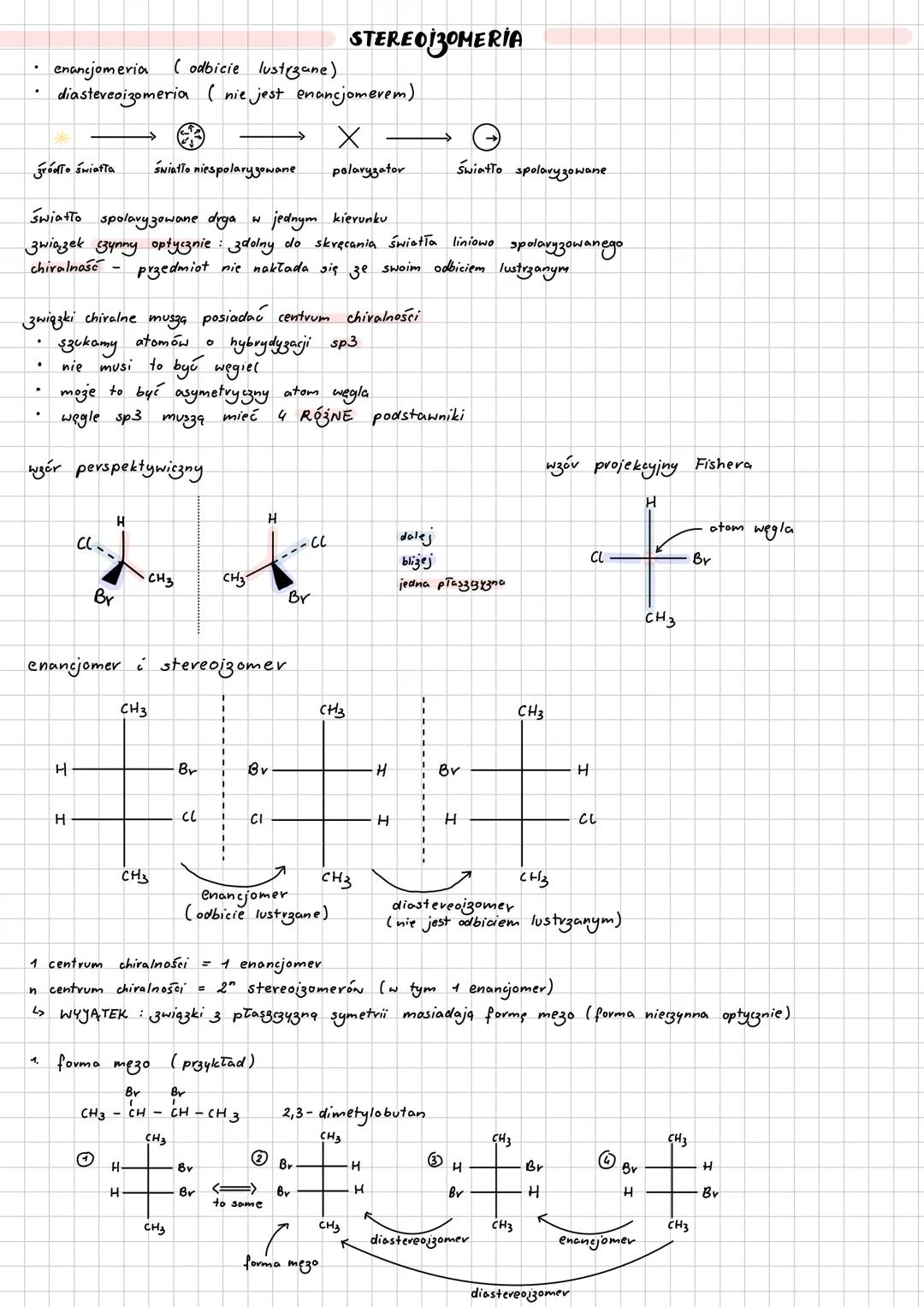
Stereoizomeria - przestrzenny świat cząsteczek
Stereoizomeria to zjawisko, gdy cząsteczki mają ten sam wzór, ale różną orientację w przestrzeni. Dzieli się na enancjomerię (odbicia lustrzane) i diastereoizomerię.
Chiralność występuje gdy cząsteczka nie nakłada się na swoje odbicie lustrzane. Potrzebny jest atom węgla sp³ z czterema różnymi podstawnikami - to centrum chiralności.
Liczba stereoizomerów = 2ⁿ . Wyjątek: związki z płaszczyzną symetrii mają formę mezo - są nieczynne optycznie mimo centrów chiralności.
Enancjomery różnią się tylko kierunkiem skręcania światła spolaryzowanego. Mieszanina racemiczna (racemat) to równomolowa mieszanka dwóch enancjomerów - jest optycznie nieaktywna.
Kluczowe: 1 centrum chiralności = 1 para enancjomerów. Więcej centrów = więcej możliwości!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Izomeria geometryczna E/Z
Izomeria cis-trans to szczególny przypadek izomerii E/Z przy wiązaniach podwójnych. Warunek: różne podstawniki przy każdym węglu podwójnego wiązania.
Izomer cis ma podobne grupy po tej samej stronie wiązania. Ma moment dipolowy ≠ 0, wyższą temperaturę wrzenia, większą energię i reaktywność.
Izomer trans ma podobne grupy po przeciwnych stronach. Moment dipolowy = 0, niższa energia, wyższa temperatura topnienia, większa stabilność.
Przy oznaczaniu E/Z liczy się pierwszeństwo podstawników według liczby atomowej: I > Br > Cl > O > N > C > H. E = podstawniki o wyższym pierwszeństwie po przeciwnych stronach, Z = po tej samej.
Zapamiętaj: Cis = "po tej samej stronie", Trans = "na przeciwko"

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkeny - węglowodory z wiązaniem podwójnym
Alkeny mają wzór CnH2n i zawierają wiązanie podwójne C=C. Atomy przy wiązaniu podwójnym mają hybrydyzację sp² i leżą w jednej płaszczyźnie.
Występują różne typy izomerii: położenia , konstytucyjna i geometryczna. Alkadieny mają dwa wiązania podwójne - mogą być skumulowane, sprzężone lub izolowane.
Główne reakcje to addycja elektrofilowa. Przy HCl do propenu powstaje 2-chloropropan zgodnie z regułą Markownikowa - wodór przyłącza się do węgla z większą liczbą wodorów.
Polimeryzacja łączy małe cząsteczki (monomery) w długie łańcuchy. Eten → polietylen (PE), propen → polipropylen (PP), chlorek winylu → PVC.
Ważne: Reguła Markownikowa - "bogaty się bogaci" (wodór do węgla z więcej wodorów)!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje alkenów - addycja i eliminacja
Addycja wody w środowisku kwasowym daje alkohole. H+ przyłącza się według reguły Markownikowa, potem H₂O jako nukleofil, na koniec odłącza się H+ tworząc alkohol.
Addycja wodoru (z katalizatorem) przekształca alken w alkan. Eliminacja to reakcja odwrotna - z alkanu powstaje alken. Te reakcje są odwracalne.
Przy addycji HBr do but-2-enu powstają dwa produkty w podobnych ilościach - reguła Markownikowa nie działa, bo oba węgle mają podobną gęstość elektronową.
Polimeryzacja tworzy ważne tworzywa: PE (polieten) odporny chemicznie, PP (polipropylen), PVC (z chlorku winylu), PTFE (teflon) odporny na wysokie temperatury.
Praktycznie: Znając te reakcje, możesz przewidzieć produkty większości przemian alkenów!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Utlenianie alkenów
Utlenianie w środowisku obojętnym manganianem(VII) daje diole. Eten + MnO₄⁻ → etano-1,2-diol + MnO₂. Obserwujesz odbarwienie fioletowego roztworu i brunatny osad MnO₂.
W środowisku kwasowym manganian(VII) redukuje się do Mn²⁺ - również obserwujesz odbarwienie fioletowego roztworu, ale bez osadu.
To są reakcje charakterystyczne do wykrywania alkenów - zmiana barwy z fioletowej na bezbarwną to pewny znak obecności wiązania podwójnego.
Test na alkeny: Fioletowy KMnO₄ + alken = odbarwienie roztworu!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Alkiny - potrójne wiązania
Alkiny mają wzór CnH₂ⁿ⁻² i wiązanie potrójne C≡C. Etyn (acetylen) ma kształt liniowy z kątem 180° i hybrydyzację sp.
Reguła nazewnictwa: wiązanie podwójne ma mniejszy numer niż potrójne w nazwie związku.
Reakcja Kuczerowa to addycja wody do etynu przez niestabilny enol, dając aldehyd octowy (CH₃CHO). Inne alkiny + woda = ketony.
Alkiny przechodzą stopniową addycję: alkin + H₂ → alken + H₂ → alkan. Przy addycji HBr do alkinów powstają geminalne dibromki (dwa bromy przy tym samym węglu).
Ważne: Alkiny są bardziej reaktywne niż alkeny przez większe napięcie wiązania potrójnego!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
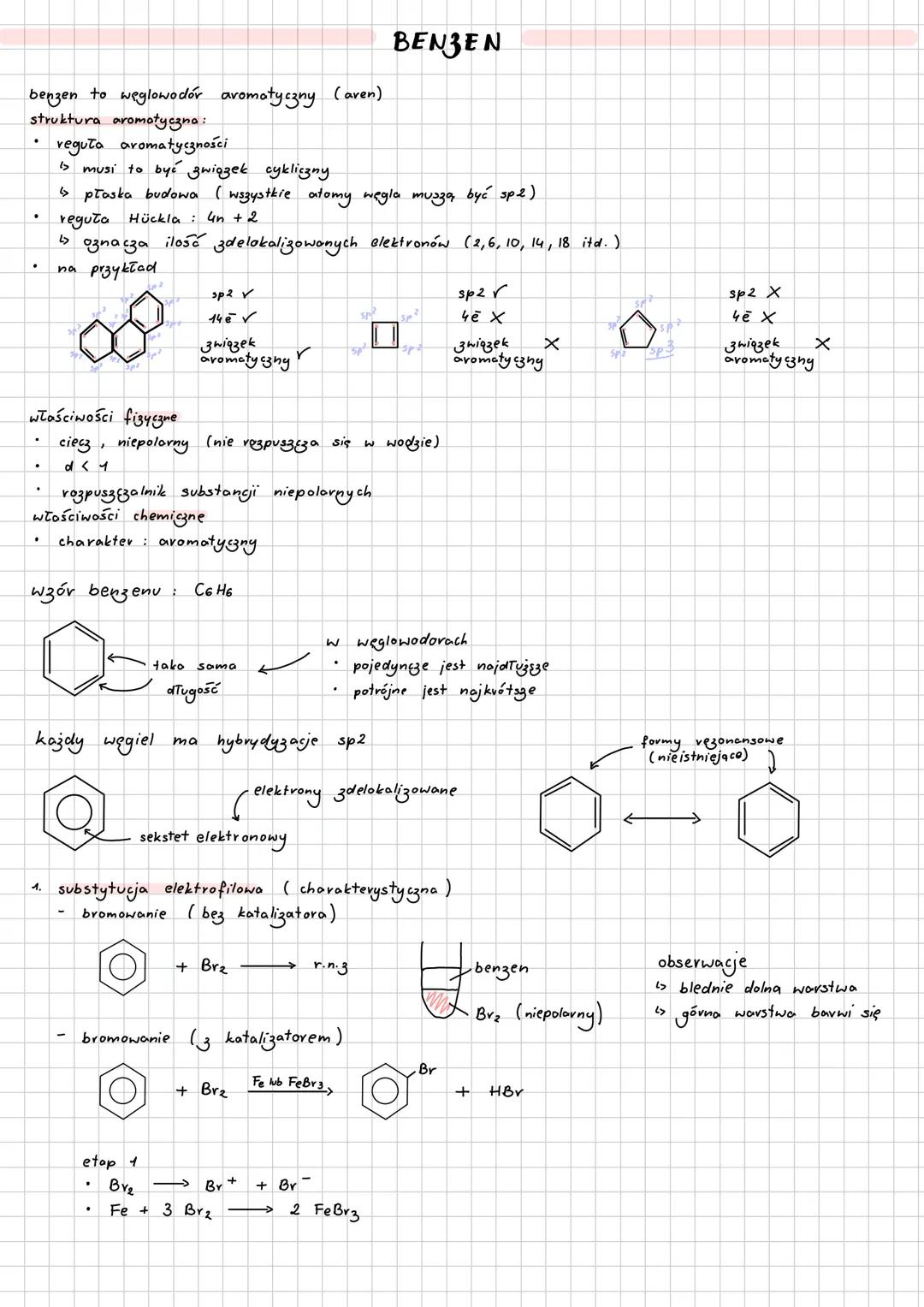
Benzen - król związków aromatycznych
Benzen (C₆H₆) to podstawowy węglowodór aromatyczny o płaskiej, cyklicznej budowie. Wszystkie węgle mają hybrydyzację sp² z elektronami zdelokalizowanymi.
Reguła aromatyczności: związek musi być cykliczny, płaski i mieć 4n+2 zdelokalizowanych elektronów (reguła Hückla). Dla benzenu: 6 elektronów = 4×1+2 ✓
Właściwości fizyczne: ciecz niepolarna, gęstość < 1, nie rozpuszcza się w wodzie, dobry rozpuszczalnik substancji niepolarnych.
Substytucja elektrofilowa to charakterystyczna reakcja. Bromowanie bez katalizatora nie zachodzi, z katalizatorem (Fe lub FeBr₃) powstaje bromobenzen + HBr. Obserwujesz blaknięcie dolnej warstwy i barwienie górnej.
Kluczowe: Benzen = stabilny pierścień aromatyczny, trudny do "złamania"!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Najpopularniejsze notatki: prawa chemii
2Prawo Stałości Składu
Zrozumienie Prawa Stałości Składu Związków Chemicznych: Obliczanie stosunków masowych i procentowych pierwiastków w związkach chemicznych, takich jak CO₂. Dowiedz się, jak stosować masy atomowe do obliczeń oraz jak interpretować wyniki. Idealne dla uczniów chemii na poziomie średnim.
Prawa Chemiczne: Skład i Masa
Zgłębiaj kluczowe prawa chemiczne, w tym prawo stałości składu związków chemicznych oraz prawo zachowania masy. Dowiedz się o odkryciach Joseph'a Louisa Prousta i Michaiła Wasiliewicza Łomonosowa, które ukształtowały współczesną chemię. Idealne dla studentów chemii i biologii. Typ: podsumowanie.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.