Izomeria to fascynujące zjawisko w chemii, które pokazuje, jak te... Pokaż więcej
Co to jest zjawisko izomerii? Przykłady izomerów alkanów
Izomeria - podstawy i przykłady
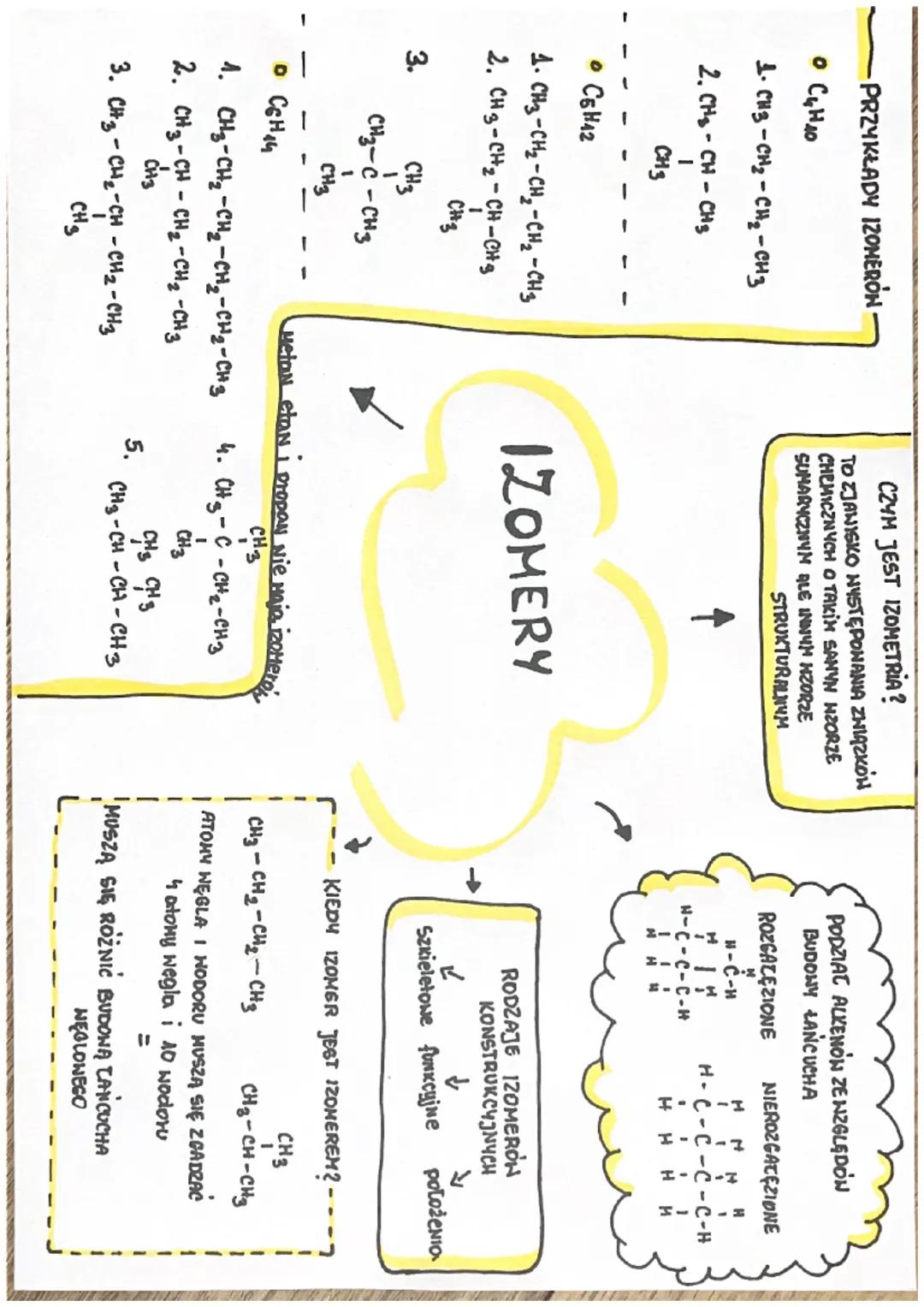
Izomeria to zjawisko występowania związków chemicznych o takim samym wzorze sumarycznym, ale różnej budowie strukturalnej. Brzmi skomplikowanie? W praktyce oznacza to, że masz te same atomy, ale ułożone w różny sposób!
Żeby związki były izomerami, muszą spełniać dwa warunki: po pierwsze - liczba atomów węgla i wodoru musi się zgadzać (np. C₄H₁₀), po drugie - muszą różnić się budową łańcucha węglowego.
Spójrz na przykład C₄H₁₀. Możesz ułożyć te atomy na dwa sposoby: jako prosty łańcuch CH₃-CH₂-CH₂-CH₃ lub z rozgałęzieniem CH₃-CH(CH₃)-CH₃. Oba mają 4 węgle i 10 wodorów, ale różną strukturę!
Alkany dzielą się na nierozgałęzione (prosty łańcuch) i rozgałęzione (z bocznymi grupami CH₃). Metan, etan i propan nie mają izomerów - są za małe, żeby można było je ułożyć na różne sposoby.
💡 Zapamiętaj: Im więcej atomów węgla, tym więcej możliwych izomerów! C₆H₁₄ ma już 5 różnych izomerów.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: izomeria
8Izomeria Cis-Trans Węglowodorów
Zgłębiaj izomerię cis-trans w węglowodorach, odkrywając różnice między izomerami oraz ich strukturalne właściwości. Dowiedz się, jak różne podstawników wpływają na geometrię cząsteczek. Materiał obejmuje kluczowe pojęcia, takie jak izomeria geometryczna, struktura alkanów oraz przykłady izomerów. Idealne dla studentów chemii.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym ich klasyfikację, nazewnictwo oraz właściwości chemiczne i fizyczne. Dowiedz się, jak ustalać nazwy izomerów oraz jakie są różnice między izomerami konstytucyjnymi a przestrzennymi. Idealne dla studentów chemii poszukujących zrozumienia struktury i właściwości węglowodorów nasyconych.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym butan i jego izomery. Dowiedz się o różnych rodzajach izomerów, ich strukturze oraz właściwościach chemicznych i fizycznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje związane z węglowodorami nasyconymi.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym różnice między izomerami strukturalnymi i szkieletowymi. Dowiedz się o właściwościach alkanów, grupach funkcyjnych oraz ich zastosowaniach. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe pojęcia dotyczące węglowodorów nasyconych.
Izomeria Alkanów
Zgłębiaj pojęcie izomerii, odkrywając różnice między izomerami oraz podział alkanów na rozgałęzione i nierozgałęzione. Dowiedz się, jak struktura cząsteczek wpływa na ich właściwości chemiczne. Idealne dla studentów chemii.
Izomeria w Alkanach
Zrozumienie izomerii w alkanach: definicje, rodzaje izomerów oraz przykłady strukturalne. Dowiedz się, jak różne połączenia atomów wpływają na właściwości chemiczne związków. Idealne dla studentów chemii, którzy chcą zgłębić temat izomerii konstytucyjnej i jej zastosowań.
Izomeria Alkanów
Zgłębiaj zasady nazewnictwa i izomerii konstytucyjnej alkanów. Dowiedz się o strukturach, właściwościach oraz homologach alkanów. Idealne dla uczniów na poziomie rozszerzonym, którzy chcą zrozumieć kluczowe koncepcje chemii organicznej.
Izomery Konstytucyjne Alkanów
Zgłębiaj izomery konstytucyjne alkanów, ich struktury oraz właściwości. Dowiedz się, jak różne układy atomów wpływają na charakterystykę związków organicznych. Materiał obejmuje alkanowe szkieletowe struktury, takie jak propan-1-ol i propan-2-ol, oraz ich izomery. Idealne dla studentów chemii i osób przygotowujących się do egzaminów.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Co to jest zjawisko izomerii? Przykłady izomerów alkanów
Izomeria to fascynujące zjawisko w chemii, które pokazuje, jak te same atomy mogą tworzyć zupełnie różne związki. Poznasz tutaj podstawy izomerii i nauczysz się rozpoznawać różne typy izomerów na konkretnych przykładach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Izomeria - podstawy i przykłady
Izomeria to zjawisko występowania związków chemicznych o takim samym wzorze sumarycznym, ale różnej budowie strukturalnej. Brzmi skomplikowanie? W praktyce oznacza to, że masz te same atomy, ale ułożone w różny sposób!
Żeby związki były izomerami, muszą spełniać dwa warunki: po pierwsze - liczba atomów węgla i wodoru musi się zgadzać (np. C₄H₁₀), po drugie - muszą różnić się budową łańcucha węglowego.
Spójrz na przykład C₄H₁₀. Możesz ułożyć te atomy na dwa sposoby: jako prosty łańcuch CH₃-CH₂-CH₂-CH₃ lub z rozgałęzieniem CH₃-CH(CH₃)-CH₃. Oba mają 4 węgle i 10 wodorów, ale różną strukturę!
Alkany dzielą się na nierozgałęzione (prosty łańcuch) i rozgałęzione (z bocznymi grupami CH₃). Metan, etan i propan nie mają izomerów - są za małe, żeby można było je ułożyć na różne sposoby.
💡 Zapamiętaj: Im więcej atomów węgla, tym więcej możliwych izomerów! C₆H₁₄ ma już 5 różnych izomerów.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: izomeria
8Izomeria Cis-Trans Węglowodorów
Zgłębiaj izomerię cis-trans w węglowodorach, odkrywając różnice między izomerami oraz ich strukturalne właściwości. Dowiedz się, jak różne podstawników wpływają na geometrię cząsteczek. Materiał obejmuje kluczowe pojęcia, takie jak izomeria geometryczna, struktura alkanów oraz przykłady izomerów. Idealne dla studentów chemii.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym ich klasyfikację, nazewnictwo oraz właściwości chemiczne i fizyczne. Dowiedz się, jak ustalać nazwy izomerów oraz jakie są różnice między izomerami konstytucyjnymi a przestrzennymi. Idealne dla studentów chemii poszukujących zrozumienia struktury i właściwości węglowodorów nasyconych.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym butan i jego izomery. Dowiedz się o różnych rodzajach izomerów, ich strukturze oraz właściwościach chemicznych i fizycznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje związane z węglowodorami nasyconymi.
Izomeria Alkanów
Zgłębiaj zjawisko izomerii alkanów, w tym różnice między izomerami strukturalnymi i szkieletowymi. Dowiedz się o właściwościach alkanów, grupach funkcyjnych oraz ich zastosowaniach. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe pojęcia dotyczące węglowodorów nasyconych.
Izomeria Alkanów
Zgłębiaj pojęcie izomerii, odkrywając różnice między izomerami oraz podział alkanów na rozgałęzione i nierozgałęzione. Dowiedz się, jak struktura cząsteczek wpływa na ich właściwości chemiczne. Idealne dla studentów chemii.
Izomeria w Alkanach
Zrozumienie izomerii w alkanach: definicje, rodzaje izomerów oraz przykłady strukturalne. Dowiedz się, jak różne połączenia atomów wpływają na właściwości chemiczne związków. Idealne dla studentów chemii, którzy chcą zgłębić temat izomerii konstytucyjnej i jej zastosowań.
Izomeria Alkanów
Zgłębiaj zasady nazewnictwa i izomerii konstytucyjnej alkanów. Dowiedz się o strukturach, właściwościach oraz homologach alkanów. Idealne dla uczniów na poziomie rozszerzonym, którzy chcą zrozumieć kluczowe koncepcje chemii organicznej.
Izomery Konstytucyjne Alkanów
Zgłębiaj izomery konstytucyjne alkanów, ich struktury oraz właściwości. Dowiedz się, jak różne układy atomów wpływają na charakterystykę związków organicznych. Materiał obejmuje alkanowe szkieletowe struktury, takie jak propan-1-ol i propan-2-ol, oraz ich izomery. Idealne dla studentów chemii i osób przygotowujących się do egzaminów.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.