Aminy i amidy to związki organiczne zawierające azot, które odgrywają... Pokaż więcej
Czego jeszcze nie wiesz o aminach i amidach? Poznaj wszystko jasno i prosto!

Aminy - budowa i klasyfikacja
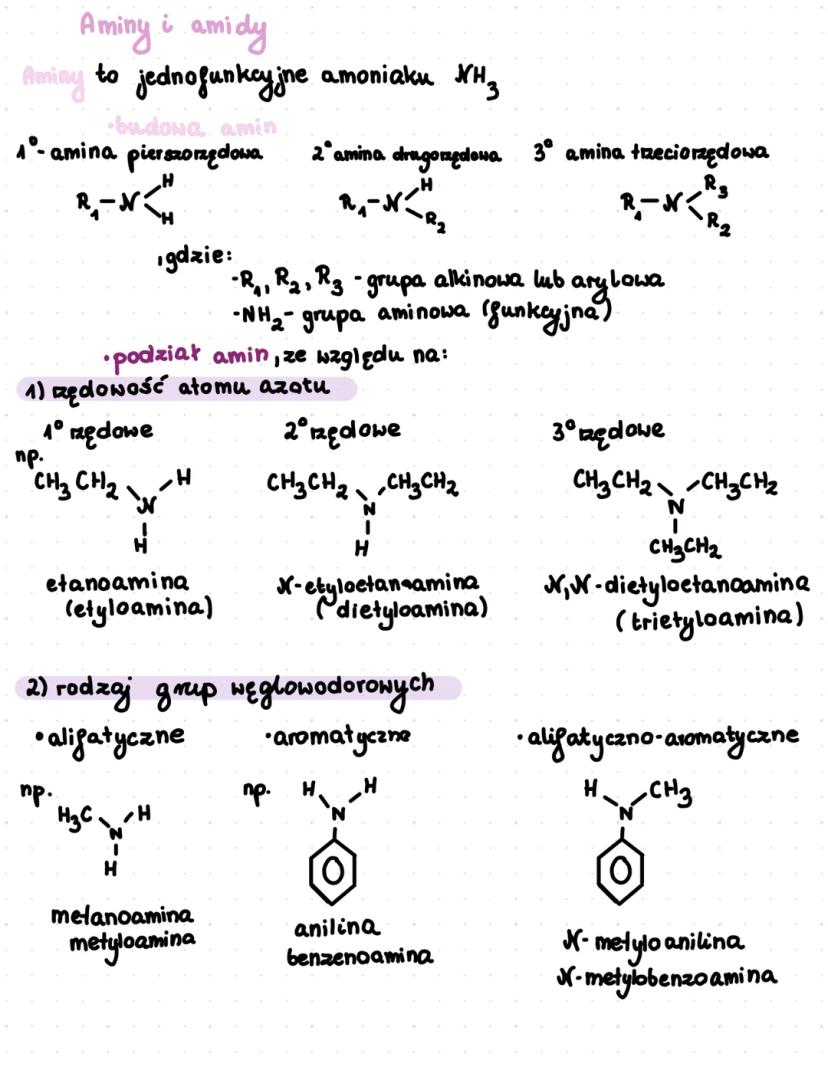
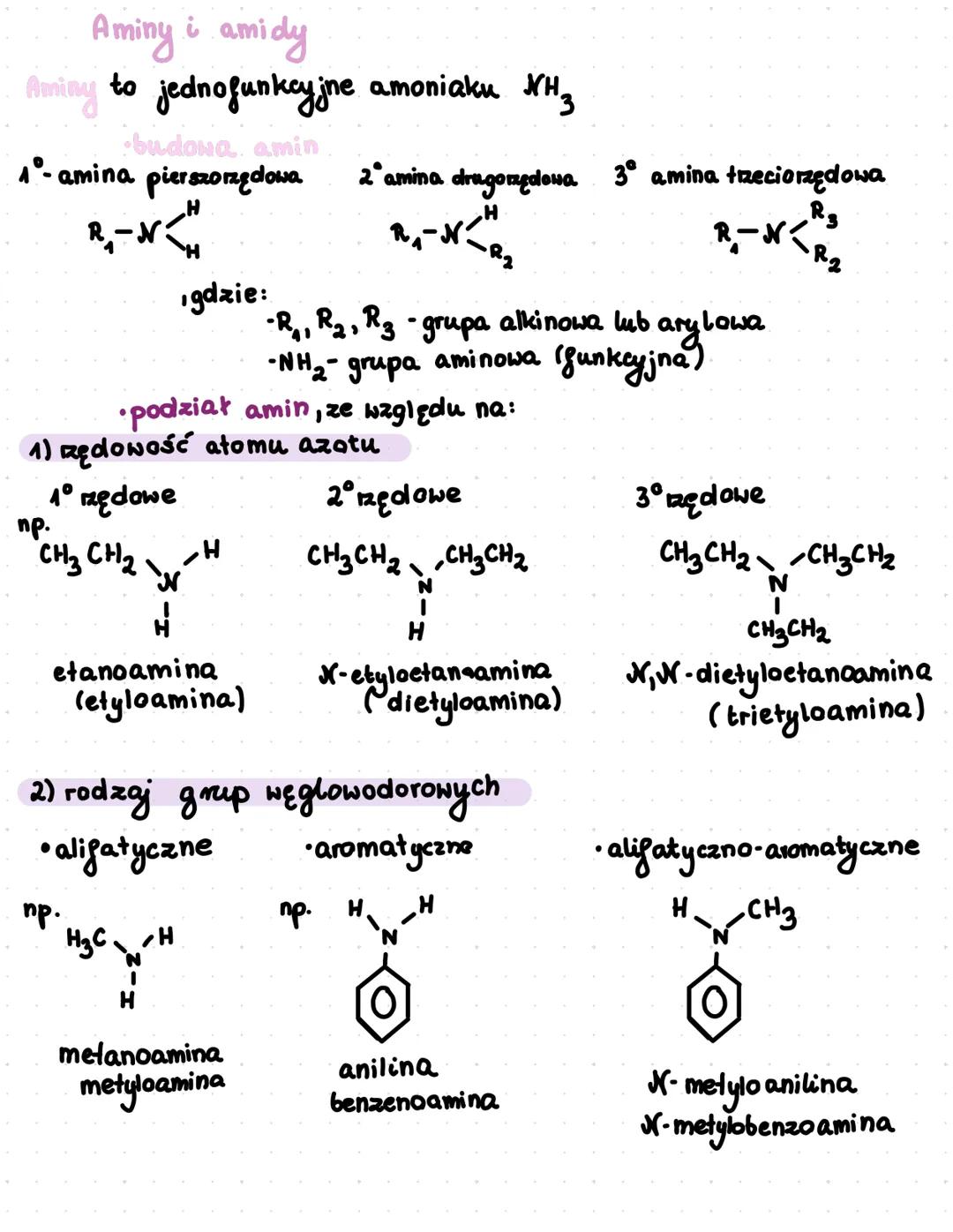
Aminy to związki chemiczne będące pochodnymi amoniaku (NH₃). Ich cechą charakterystyczną jest grupa aminowa . Możemy je podzielić ze względu na rzędowość atomu azotu na: pierwszorzędowe , drugorzędowe i trzeciorzędowe .
Inny podział amin dotyczy rodzaju grup węglowodorowych. Wyróżniamy aminy alifatyczne (np. metyloamina), aromatyczne (np. anilina) oraz alifatyczno-aromatyczne .
Nazewnictwo amin jest proste - dla amin pierwszorzędowych używamy nazwy węglowodoru z przyrostkiem "-amina", np. etanoamina (etyloamina), propano-1-amina czy benzenoamina (anilina).
💡 Warto zapamiętać: Rzędowość aminy określa się na podstawie liczby podstawników przyłączonych do atomu azotu, nie mylić z ilością atomów węgla!
Nazewnictwo amin
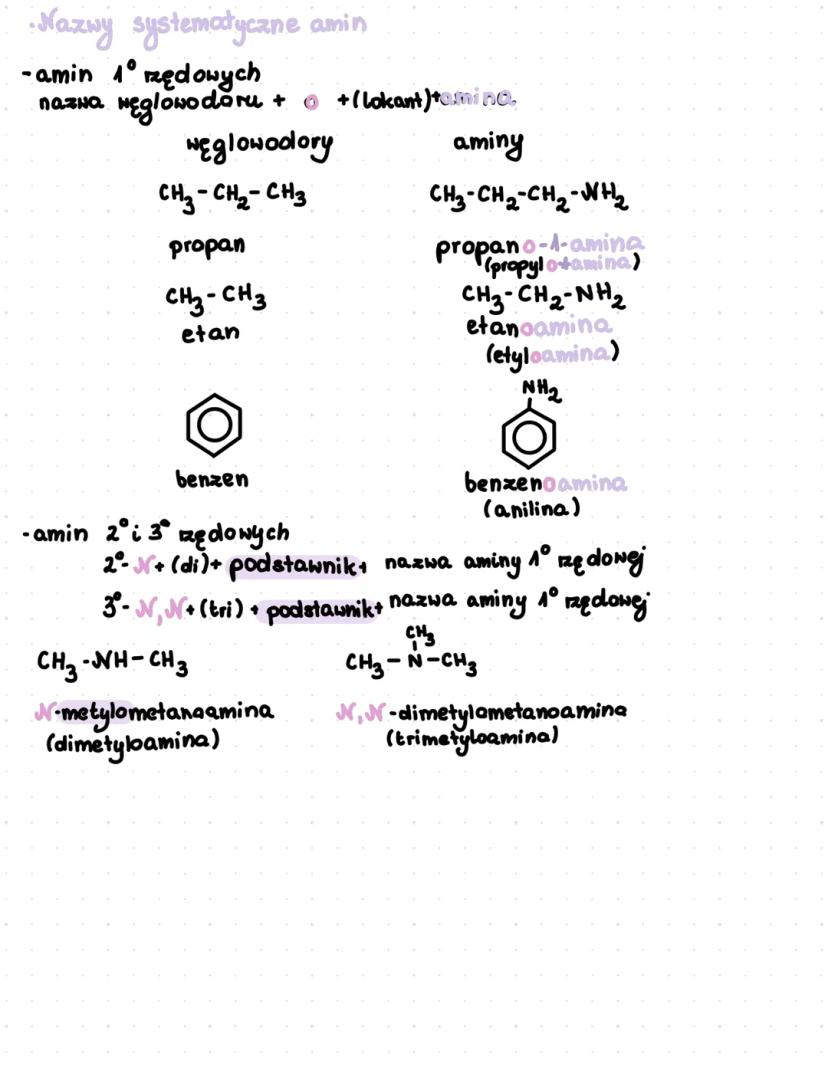
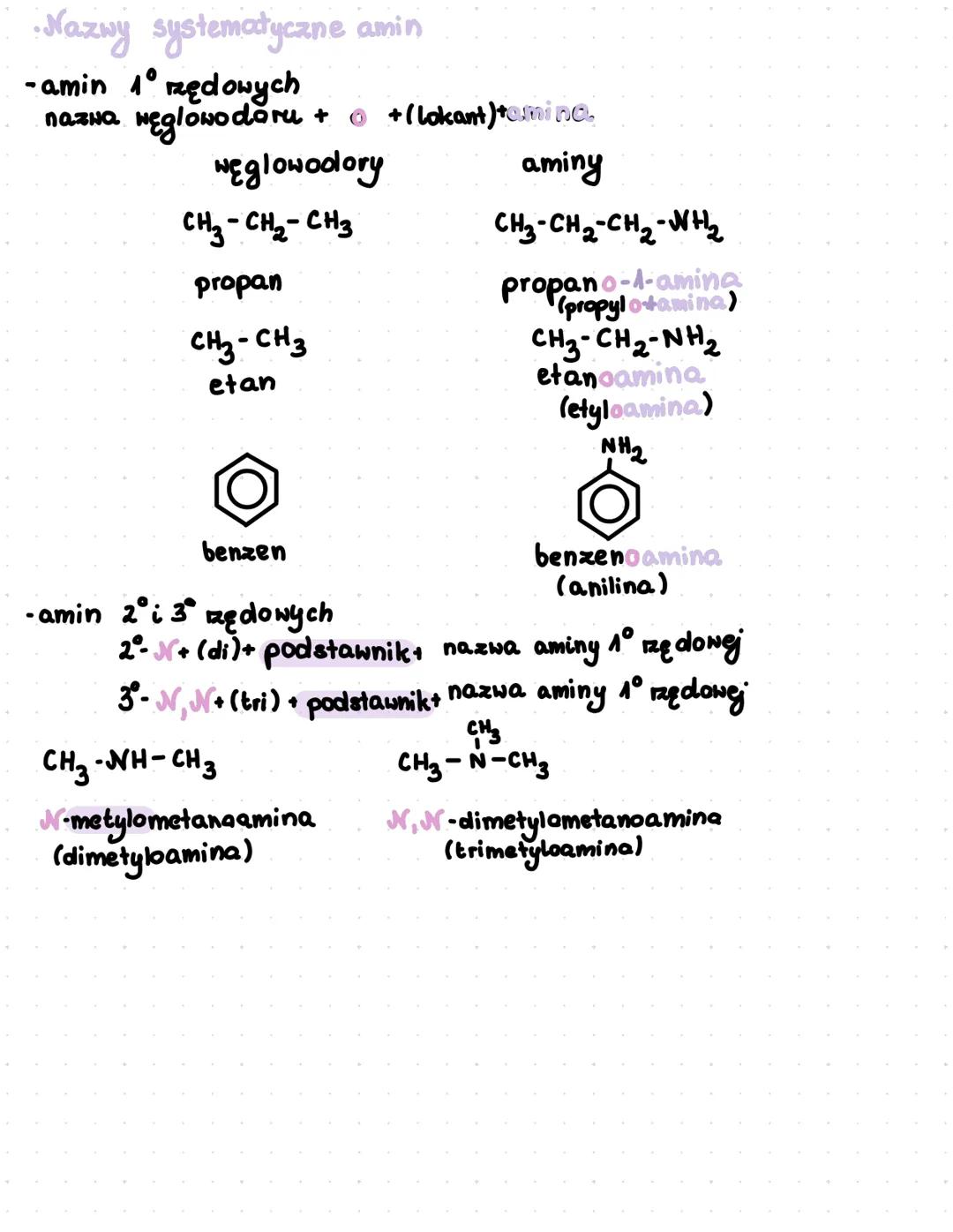
Nazwy systematyczne amin pierwszorzędowych tworzymy przez dodanie przyrostka "-amina" do nazwy węglowodoru, np. propan → propano-1-amina, etan → etanoamina (etyloamina), benzen → benzenoamina (anilina).
Dla amin drugorzędowych używamy przedrostka "N-" i wymieniamy nazwę podstawnika, np. N-metylometanoamina (dimetyloamina). W przypadku amin trzeciorzędowych stosujemy przedrostek "N,N-" i wymieniamy nazwy obu podstawników, np. N,N-dimetylometanoamina (trimetyloamina).
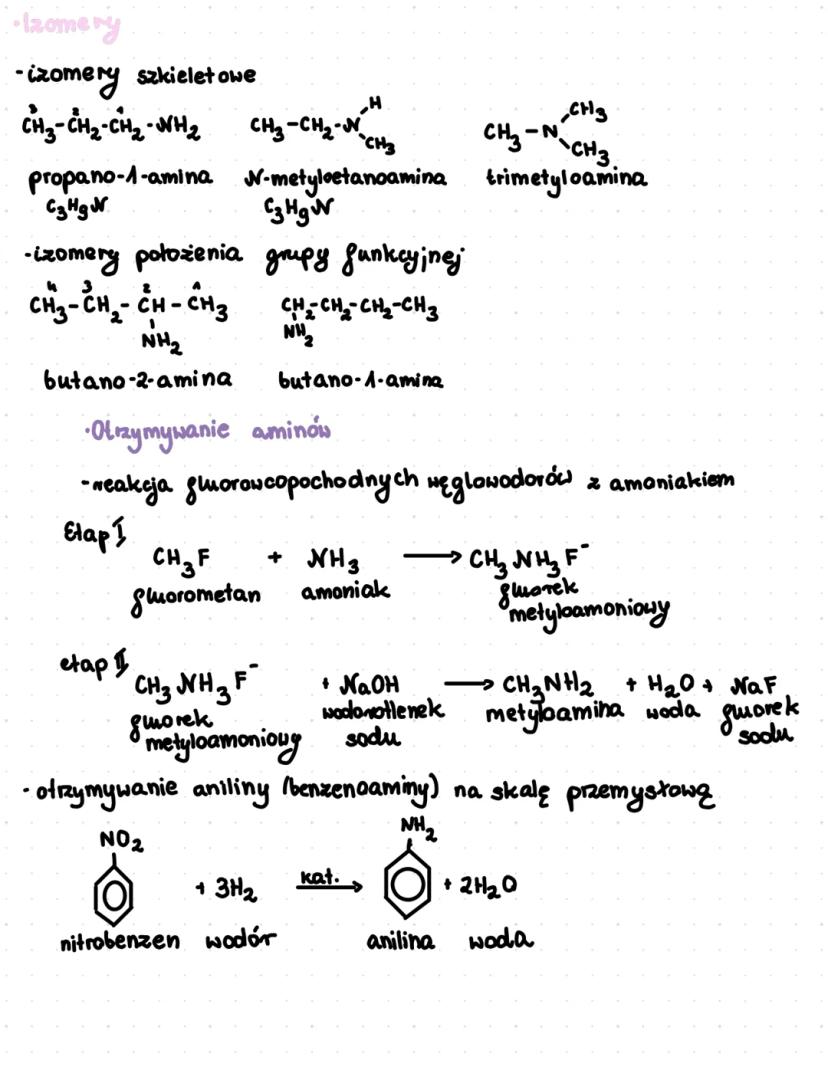
Aminy mogą tworzyć różne typy izomerów. Izomery szkieletowe mają różne ułożenie atomów węgla, np. propano-1-amina i N-metyloetanoamina (oba o wzorze C₃H₉N). Występują też izomery położenia grupy funkcyjnej, np. butano-1-amina i butano-2-amina.
⚠️ Uwaga: Przy nazywaniu amin drugorzędowych i trzeciorzędowych pamiętaj o dodaniu przedrostków N- i N,N- przed nazwą podstawników, to częsty błąd na sprawdzianach!

Otrzymywanie amin
Aminy można otrzymać na kilka sposobów. Jednym z podstawowych jest reakcja fluorowcopochodnych węglowodorów z amoniakiem. Ten proces zachodzi dwuetapowo - najpierw powstaje sól amoniowa, a następnie w reakcji z wodorotlenkiem sodu tworzy się amina.
Na przykład otrzymywanie metyloaminy: najpierw fluorometan reaguje z amoniakiem dając fluorek metyloamoniowy, który następnie w reakcji z NaOH daje metyloaminę, wodę i fluorek sodu.
W przemyśle anilinę (benzenoaminę) otrzymuje się w procesie redukcji nitrobenzenu wodorem. W wyniku tej reakcji powstaje anilina i woda: nitrobenzen + 3H₂ → anilina + 2H₂O.
💡 Ciekawostka: Anilina jest ważnym surowcem w przemyśle barwników - większość kolorowych ubrań, które nosisz, zawdzięcza swoje barwy związkom pochodnym od aniliny!

Właściwości amin
Proste aminy jak metyloamina i etyloamina występują jako gazy, natomiast pozostałe aminy alifatyczne i aromatyczne są zazwyczaj cieczami. Aminy alifatyczne świetnie rozpuszczają się w wodzie dzięki wiązaniom wodorowym, podczas gdy aminy aromatyczne rozpuszczają się słabiej.
Temperatury wrzenia i topnienia amin są wyższe niż analogicznych węglowodorów, ale niższe niż alkoholi o podobnej masie cząsteczkowej. Można to zapisać jako: węglowodory < aminy < alkohole.
Ważną cechą amin jest ich zasadowy charakter - reagują z kwasami i wodą. W reakcji z wodą tworzą jony amoniowe i wodorotlenkowe, np. etyloamina + woda ⇌ kation etyloamoniowy + anion wodorotlenkowy. Z kwasami tworzą sole, np. etyloamina + HCl ⇌ chlorek etyloamoniowy.
⚠️ Zapamiętaj: Aminy są bazami organicznymi i mogą neutralizować kwasy. To odróżnia je od innych związków organicznych, które często mają charakter obojętny lub kwasowy!
Amidy - budowa i nazewnictwo
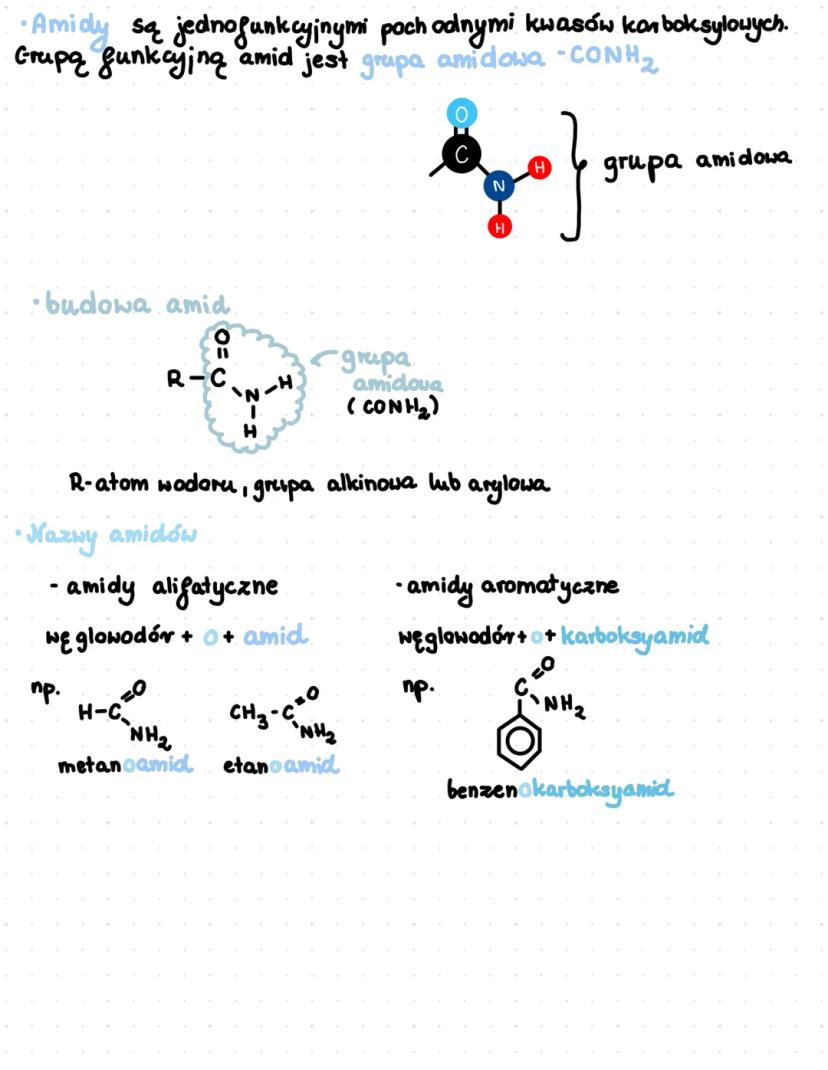
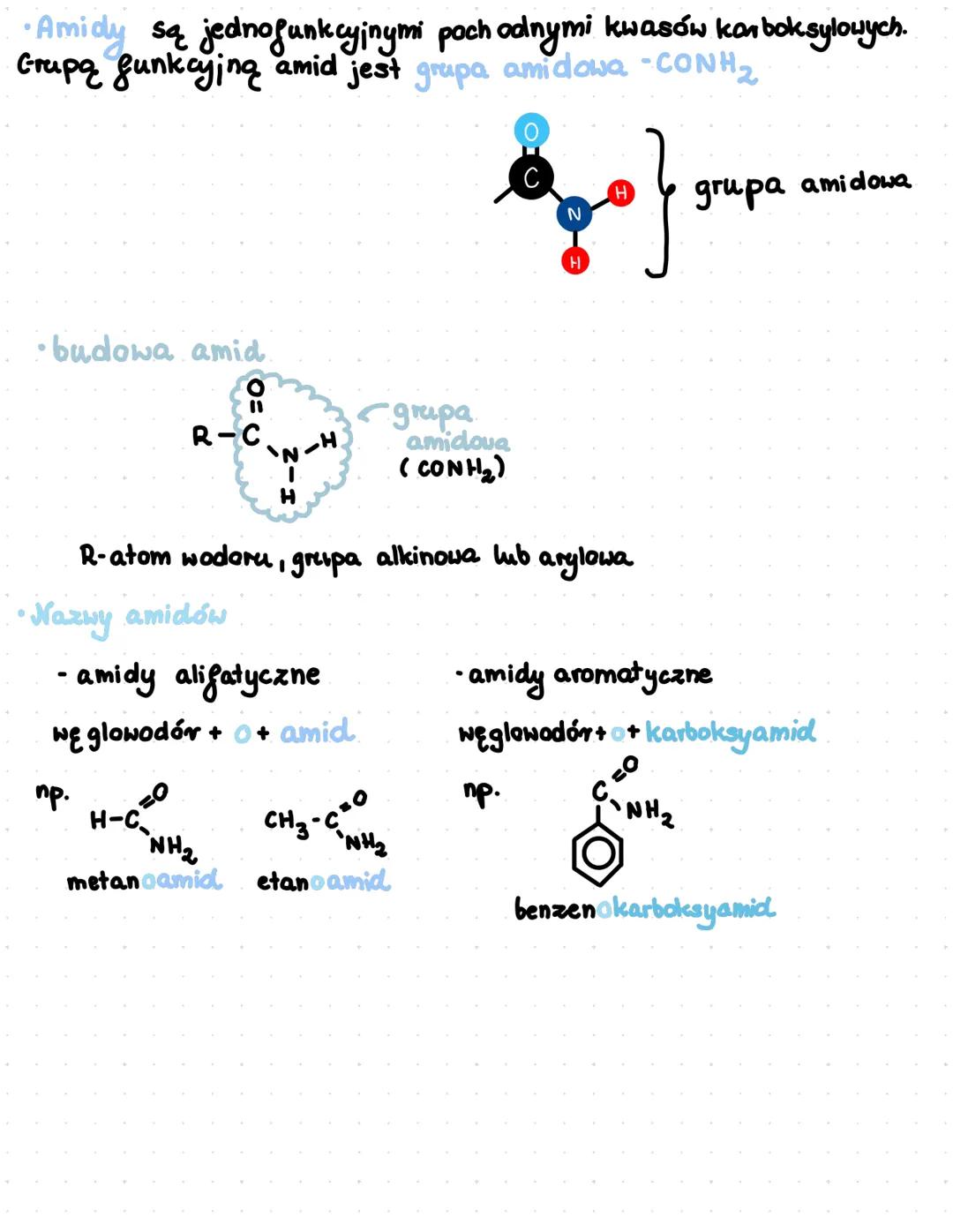
Amidy to jednofunkcyjne pochodne kwasów karboksylowych, które zawierają charakterystyczną grupę amidową -CONH₂. Ich ogólna struktura to R-CONH₂, gdzie R może być atomem wodoru, grupą alkilową lub arylową.
Nazwy amidów tworzymy według prostych zasad. Dla amidów alifatycznych stosujemy nazwę węglowodoru z przyrostkiem "-oamid", np. metanoamid, etanoamid. W przypadku amidów aromatycznych używamy nazwy węglowodoru z przyrostkiem "-okarboksyamid", np. benzenokarboksyamid.
Grupa amidowa jest kluczowa w biochemii, ponieważ tworzy wiązanie peptydowe w białkach i peptydach. To właśnie dzięki tej grupie funkcyjnej aminokwasy mogą łączyć się ze sobą, tworząc długie łańcuchy białkowe.
💡 Ciekawostka: Właściwości amidów bardzo się różnią od amin, mimo podobieństwa w nazwie. Amidy nie mają zasadowego charakteru i nie reagują z kwasami jak aminy!
Otrzymywanie i właściwości amidów
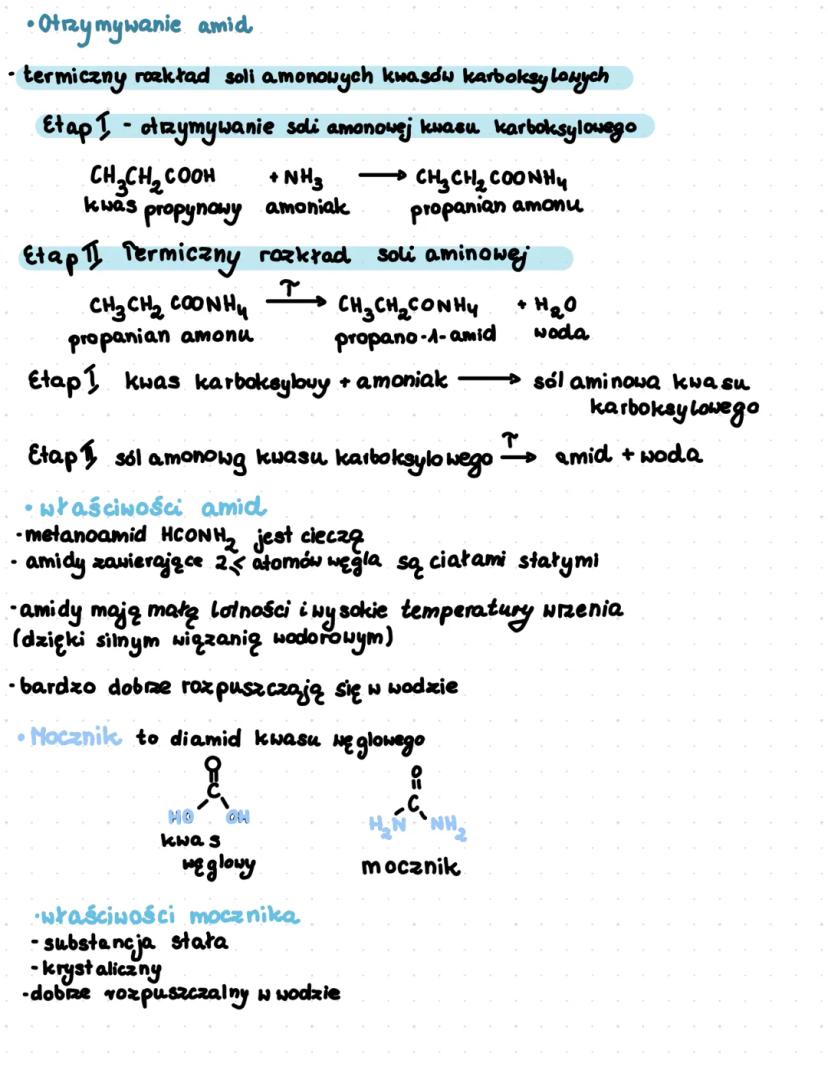
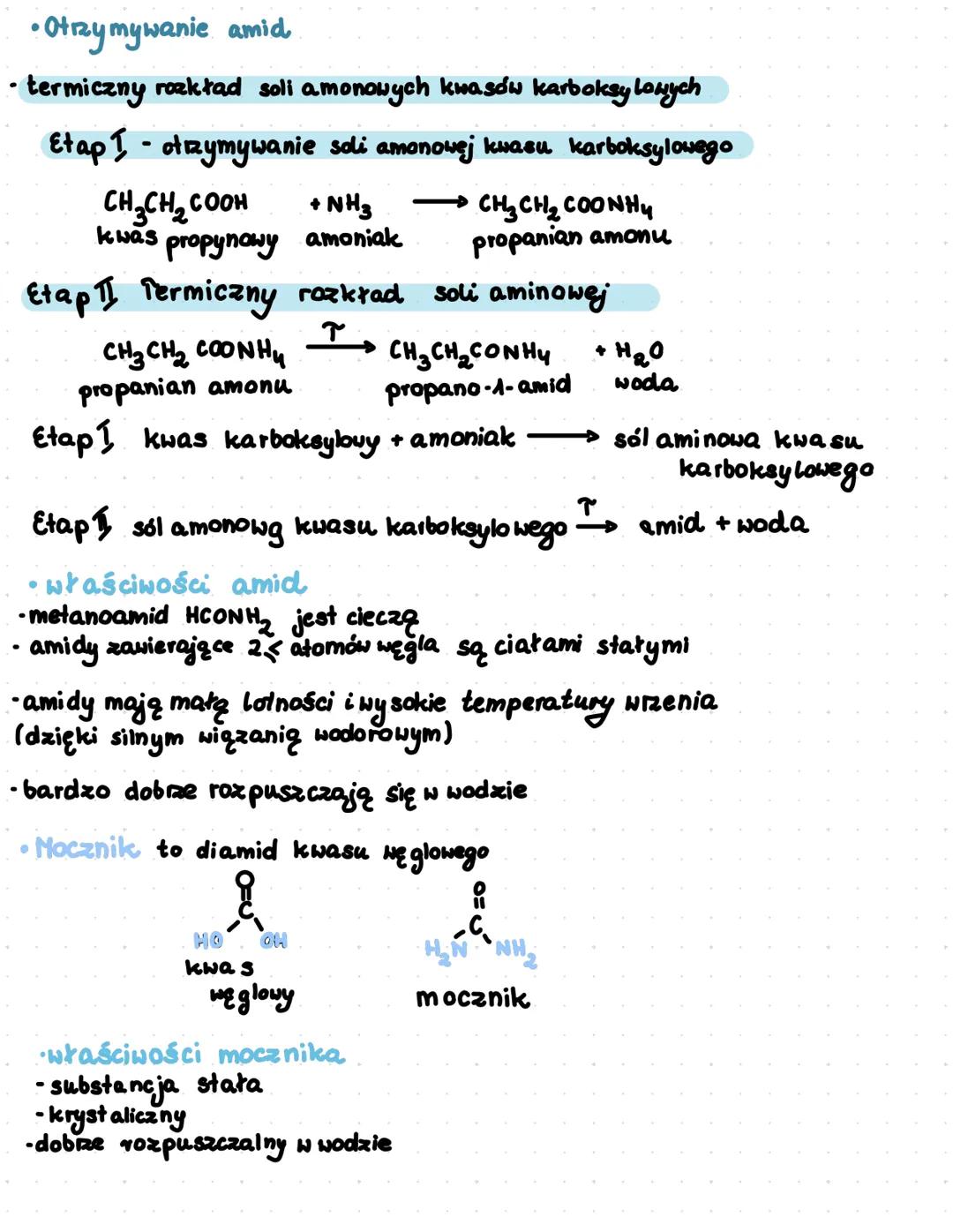
Amidy można otrzymać przez termiczny rozkład soli amonowych kwasów karboksylowych. Proces ten składa się z kilku etapów: najpierw kwas karboksylowy reaguje z amoniakiem, tworząc sól amonową, która następnie pod wpływem temperatury rozkłada się do amidu i wody.
Na przykład, kwas propanowy reaguje z amoniakiem, tworząc propanian amonu, który następnie rozkłada się termicznie do propano-1-amidu i wody.
Metanoamid (HCONH₂) jest cieczą, natomiast amidy zawierające 2 lub więcej atomów węgla występują jako ciała stałe. Amidy charakteryzują się małą lotnością i wysokimi temperaturami wrzenia dzięki silnym wiązaniom wodorowym. Bardzo dobrze rozpuszczają się w wodzie.
Mocznik to ważny związek chemiczny będący diamidem kwasu węglowego. Jest substancją krystaliczną, dobrze rozpuszczalną w wodzie. Znajduje szerokie zastosowanie w rolnictwie jako nawóz azotowy oraz w przemyśle chemicznym.
⚠️ Uwaga: Nie mylcie mocznika z kwasem moczowym - to dwa zupełnie różne związki o odmiennych właściwościach i funkcjach biologicznych!
Reakcje mocznika i wiązanie amidowe
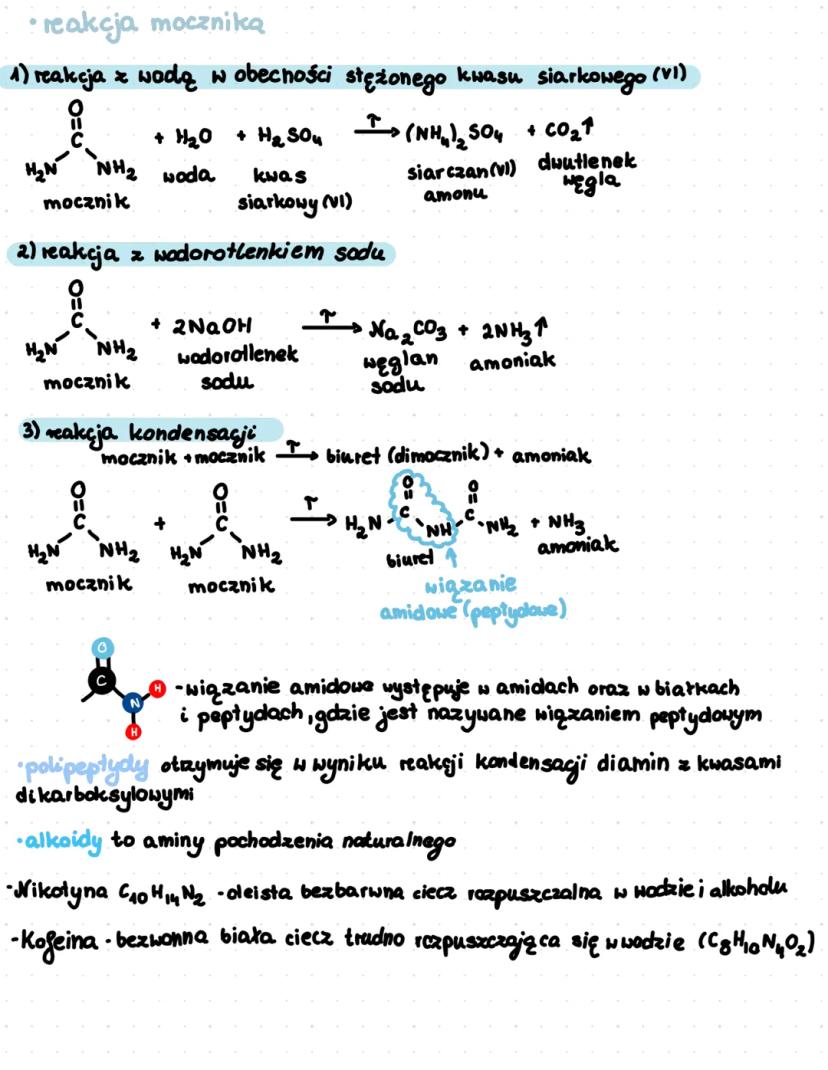
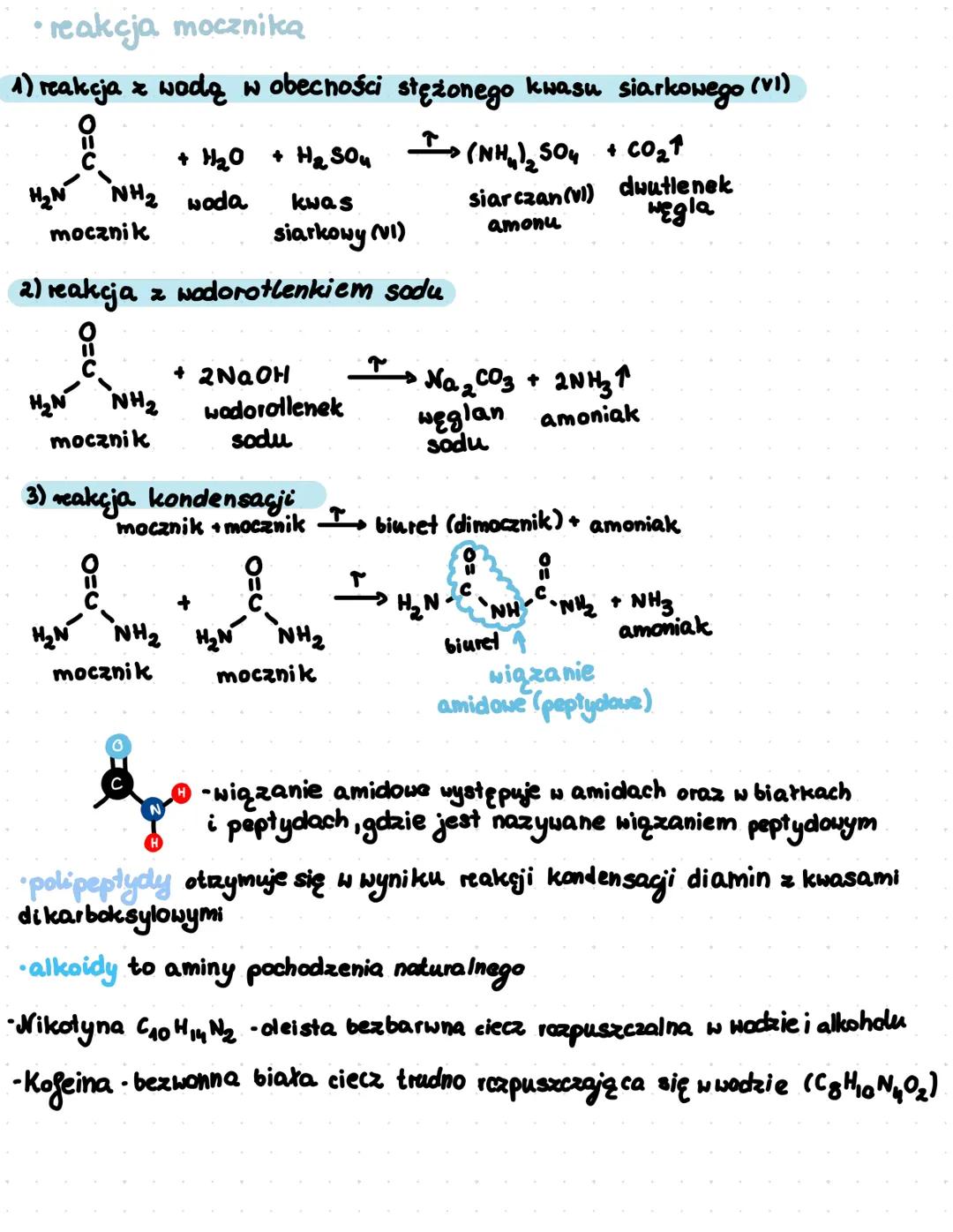
Mocznik wchodzi w szereg reakcji chemicznych. Z wodą w obecności stężonego kwasu siarkowego(VI) tworzy siarczan(VI) amonu i dwutlenek węgla. Z wodorotlenkiem sodu reaguje, dając węglan sodu i amoniak. W reakcji kondensacji dwie cząsteczki mocznika mogą utworzyć biuret (dimocznik) i amoniak.
Wiązanie amidowe (peptydowe) występuje w amidach, peptydach i białkach. Polipeptydy otrzymuje się poprzez reakcje kondensacji diamin z kwasami dikarboksylowymi. To właśnie dzięki wiązaniom peptydowym aminokwasy mogą tworzyć długie łańcuchy białkowe.
W przyrodzie występują alkaloidy - naturalne związki zawierające azot, które często są aminami. Ważne przykłady to nikotyna (C₁₀H₁₄N₂) - oleista, bezbarwna ciecz rozpuszczalna w wodzie i alkoholu, oraz kofeina (C₈H₁₀N₄O₂) - bezwonna, biała substancja trudno rozpuszczalna w wodzie.
💡 Warto wiedzieć: Wiązanie peptydowe w białkach to tak naprawdę wiązanie amidowe! Ta sama grupa funkcyjna występuje zarówno w prostych amidach, jak i w skomplikowanych strukturach białkowych w Twoim organizmie.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Związki azotu
9Aminy i Amidy
Chemia nowej ery - klasa 3 - zakres podstawowy.
Aminy i Amidy: Reakcje i Właściwości
Zgłębiaj właściwości i reakcje amin oraz amidów, w tym reakcje kondensacji, zasadowe właściwości amin, oraz ich zastosowania. Dowiedz się o strukturze chemicznej, nazewnictwie oraz reakcjach z kwasami i zasadami. Idealne dla studentów chemii poszukujących szczegółowych informacji na temat związków azotowych.
Rodzaje i Synteza Amin
Odkryj różnorodność amin, ich klasyfikację (pierwszorzędowe, drugorzędowe, trzeciorzędowe) oraz metody syntezy. Zrozumienie hybrydyzacji i nazewnictwa amin. Idealne dla studentów chemii. Typ: Podsumowanie.
Aminy: Właściwości i Reakcje
Zgłębiaj temat amin, ich nazewnictwa, podziału, sposobów otrzymywania oraz właściwości zasadowych. Dowiedz się, jak aminy reagują z innymi związkami chemicznymi. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe aspekty związków azotowych.
Aminy i Amidy
Zrozumienie różnic między aminami a amidami. Ta charakterystyka omawia ich właściwości chemiczne, zastosowania oraz porównania strukturalne. Idealne dla studentów chemii szukających jasnych i zwięzłych informacji na temat tych dwóch grup związków organicznych.
Aminy
aminy, chemia organiczna
Otrzymywanie i Właściwości Amin
Zgłębiaj temat amin w chemii organicznej, w tym ich otrzymywanie, właściwości oraz rzędowość. Dowiedz się, jak aminy alifatyczne i aromatyczne reagują z kwasami oraz jak powstają sole. Idealne dla studentów chemii poszukujących zrozumienia związków azotowych.
Składniki Powietrza i Ich Właściwości
Odkryj składniki powietrza, ich właściwości oraz zastosowania. Dowiedz się o roli tlenu i azotu w procesach spalania oraz ich znaczeniu w przemyśle. Zawiera obserwacje eksperymentalne dotyczące tlenku węgla (IV) i jego interakcji z wodą wapienną. Typ: Podsumowanie.
Charakterystyka Azotowców
Zgłębiaj właściwości pierwiastków grupy 15, w tym azotu i fosforu. Dowiedz się o ich stanach skupienia, reaktywności oraz zastosowaniach w chemii. Materiał przeznaczony dla uczniów klas 2/3 LO na poziomie rozszerzonym.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Czego jeszcze nie wiesz o aminach i amidach? Poznaj wszystko jasno i prosto!
Aminy i amidy to związki organiczne zawierające azot, które odgrywają istotną rolę w chemii i biologii. Aminy można rozumieć jako pochodne amoniaku, gdzie atomy wodoru zostały zastąpione grupami alkilowymi lub arylowymi. Z kolei amidy są pochodnymi kwasów karboksylowych i zawierają... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Aminy - budowa i klasyfikacja
Aminy to związki chemiczne będące pochodnymi amoniaku (NH₃). Ich cechą charakterystyczną jest grupa aminowa . Możemy je podzielić ze względu na rzędowość atomu azotu na: pierwszorzędowe , drugorzędowe i trzeciorzędowe .
Inny podział amin dotyczy rodzaju grup węglowodorowych. Wyróżniamy aminy alifatyczne (np. metyloamina), aromatyczne (np. anilina) oraz alifatyczno-aromatyczne .
Nazewnictwo amin jest proste - dla amin pierwszorzędowych używamy nazwy węglowodoru z przyrostkiem "-amina", np. etanoamina (etyloamina), propano-1-amina czy benzenoamina (anilina).
💡 Warto zapamiętać: Rzędowość aminy określa się na podstawie liczby podstawników przyłączonych do atomu azotu, nie mylić z ilością atomów węgla!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo amin
Nazwy systematyczne amin pierwszorzędowych tworzymy przez dodanie przyrostka "-amina" do nazwy węglowodoru, np. propan → propano-1-amina, etan → etanoamina (etyloamina), benzen → benzenoamina (anilina).
Dla amin drugorzędowych używamy przedrostka "N-" i wymieniamy nazwę podstawnika, np. N-metylometanoamina (dimetyloamina). W przypadku amin trzeciorzędowych stosujemy przedrostek "N,N-" i wymieniamy nazwy obu podstawników, np. N,N-dimetylometanoamina (trimetyloamina).
Aminy mogą tworzyć różne typy izomerów. Izomery szkieletowe mają różne ułożenie atomów węgla, np. propano-1-amina i N-metyloetanoamina (oba o wzorze C₃H₉N). Występują też izomery położenia grupy funkcyjnej, np. butano-1-amina i butano-2-amina.
⚠️ Uwaga: Przy nazywaniu amin drugorzędowych i trzeciorzędowych pamiętaj o dodaniu przedrostków N- i N,N- przed nazwą podstawników, to częsty błąd na sprawdzianach!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie amin
Aminy można otrzymać na kilka sposobów. Jednym z podstawowych jest reakcja fluorowcopochodnych węglowodorów z amoniakiem. Ten proces zachodzi dwuetapowo - najpierw powstaje sól amoniowa, a następnie w reakcji z wodorotlenkiem sodu tworzy się amina.
Na przykład otrzymywanie metyloaminy: najpierw fluorometan reaguje z amoniakiem dając fluorek metyloamoniowy, który następnie w reakcji z NaOH daje metyloaminę, wodę i fluorek sodu.
W przemyśle anilinę (benzenoaminę) otrzymuje się w procesie redukcji nitrobenzenu wodorem. W wyniku tej reakcji powstaje anilina i woda: nitrobenzen + 3H₂ → anilina + 2H₂O.
💡 Ciekawostka: Anilina jest ważnym surowcem w przemyśle barwników - większość kolorowych ubrań, które nosisz, zawdzięcza swoje barwy związkom pochodnym od aniliny!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Właściwości amin
Proste aminy jak metyloamina i etyloamina występują jako gazy, natomiast pozostałe aminy alifatyczne i aromatyczne są zazwyczaj cieczami. Aminy alifatyczne świetnie rozpuszczają się w wodzie dzięki wiązaniom wodorowym, podczas gdy aminy aromatyczne rozpuszczają się słabiej.
Temperatury wrzenia i topnienia amin są wyższe niż analogicznych węglowodorów, ale niższe niż alkoholi o podobnej masie cząsteczkowej. Można to zapisać jako: węglowodory < aminy < alkohole.
Ważną cechą amin jest ich zasadowy charakter - reagują z kwasami i wodą. W reakcji z wodą tworzą jony amoniowe i wodorotlenkowe, np. etyloamina + woda ⇌ kation etyloamoniowy + anion wodorotlenkowy. Z kwasami tworzą sole, np. etyloamina + HCl ⇌ chlorek etyloamoniowy.
⚠️ Zapamiętaj: Aminy są bazami organicznymi i mogą neutralizować kwasy. To odróżnia je od innych związków organicznych, które często mają charakter obojętny lub kwasowy!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Amidy - budowa i nazewnictwo
Amidy to jednofunkcyjne pochodne kwasów karboksylowych, które zawierają charakterystyczną grupę amidową -CONH₂. Ich ogólna struktura to R-CONH₂, gdzie R może być atomem wodoru, grupą alkilową lub arylową.
Nazwy amidów tworzymy według prostych zasad. Dla amidów alifatycznych stosujemy nazwę węglowodoru z przyrostkiem "-oamid", np. metanoamid, etanoamid. W przypadku amidów aromatycznych używamy nazwy węglowodoru z przyrostkiem "-okarboksyamid", np. benzenokarboksyamid.
Grupa amidowa jest kluczowa w biochemii, ponieważ tworzy wiązanie peptydowe w białkach i peptydach. To właśnie dzięki tej grupie funkcyjnej aminokwasy mogą łączyć się ze sobą, tworząc długie łańcuchy białkowe.
💡 Ciekawostka: Właściwości amidów bardzo się różnią od amin, mimo podobieństwa w nazwie. Amidy nie mają zasadowego charakteru i nie reagują z kwasami jak aminy!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie i właściwości amidów
Amidy można otrzymać przez termiczny rozkład soli amonowych kwasów karboksylowych. Proces ten składa się z kilku etapów: najpierw kwas karboksylowy reaguje z amoniakiem, tworząc sól amonową, która następnie pod wpływem temperatury rozkłada się do amidu i wody.
Na przykład, kwas propanowy reaguje z amoniakiem, tworząc propanian amonu, który następnie rozkłada się termicznie do propano-1-amidu i wody.
Metanoamid (HCONH₂) jest cieczą, natomiast amidy zawierające 2 lub więcej atomów węgla występują jako ciała stałe. Amidy charakteryzują się małą lotnością i wysokimi temperaturami wrzenia dzięki silnym wiązaniom wodorowym. Bardzo dobrze rozpuszczają się w wodzie.
Mocznik to ważny związek chemiczny będący diamidem kwasu węglowego. Jest substancją krystaliczną, dobrze rozpuszczalną w wodzie. Znajduje szerokie zastosowanie w rolnictwie jako nawóz azotowy oraz w przemyśle chemicznym.
⚠️ Uwaga: Nie mylcie mocznika z kwasem moczowym - to dwa zupełnie różne związki o odmiennych właściwościach i funkcjach biologicznych!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje mocznika i wiązanie amidowe
Mocznik wchodzi w szereg reakcji chemicznych. Z wodą w obecności stężonego kwasu siarkowego(VI) tworzy siarczan(VI) amonu i dwutlenek węgla. Z wodorotlenkiem sodu reaguje, dając węglan sodu i amoniak. W reakcji kondensacji dwie cząsteczki mocznika mogą utworzyć biuret (dimocznik) i amoniak.
Wiązanie amidowe (peptydowe) występuje w amidach, peptydach i białkach. Polipeptydy otrzymuje się poprzez reakcje kondensacji diamin z kwasami dikarboksylowymi. To właśnie dzięki wiązaniom peptydowym aminokwasy mogą tworzyć długie łańcuchy białkowe.
W przyrodzie występują alkaloidy - naturalne związki zawierające azot, które często są aminami. Ważne przykłady to nikotyna (C₁₀H₁₄N₂) - oleista, bezbarwna ciecz rozpuszczalna w wodzie i alkoholu, oraz kofeina (C₈H₁₀N₄O₂) - bezwonna, biała substancja trudno rozpuszczalna w wodzie.
💡 Warto wiedzieć: Wiązanie peptydowe w białkach to tak naprawdę wiązanie amidowe! Ta sama grupa funkcyjna występuje zarówno w prostych amidach, jak i w skomplikowanych strukturach białkowych w Twoim organizmie.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Związki azotu
9Aminy i Amidy
Chemia nowej ery - klasa 3 - zakres podstawowy.
Aminy i Amidy: Reakcje i Właściwości
Zgłębiaj właściwości i reakcje amin oraz amidów, w tym reakcje kondensacji, zasadowe właściwości amin, oraz ich zastosowania. Dowiedz się o strukturze chemicznej, nazewnictwie oraz reakcjach z kwasami i zasadami. Idealne dla studentów chemii poszukujących szczegółowych informacji na temat związków azotowych.
Rodzaje i Synteza Amin
Odkryj różnorodność amin, ich klasyfikację (pierwszorzędowe, drugorzędowe, trzeciorzędowe) oraz metody syntezy. Zrozumienie hybrydyzacji i nazewnictwa amin. Idealne dla studentów chemii. Typ: Podsumowanie.
Aminy: Właściwości i Reakcje
Zgłębiaj temat amin, ich nazewnictwa, podziału, sposobów otrzymywania oraz właściwości zasadowych. Dowiedz się, jak aminy reagują z innymi związkami chemicznymi. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe aspekty związków azotowych.
Aminy i Amidy
Zrozumienie różnic między aminami a amidami. Ta charakterystyka omawia ich właściwości chemiczne, zastosowania oraz porównania strukturalne. Idealne dla studentów chemii szukających jasnych i zwięzłych informacji na temat tych dwóch grup związków organicznych.
Aminy
aminy, chemia organiczna
Otrzymywanie i Właściwości Amin
Zgłębiaj temat amin w chemii organicznej, w tym ich otrzymywanie, właściwości oraz rzędowość. Dowiedz się, jak aminy alifatyczne i aromatyczne reagują z kwasami oraz jak powstają sole. Idealne dla studentów chemii poszukujących zrozumienia związków azotowych.
Składniki Powietrza i Ich Właściwości
Odkryj składniki powietrza, ich właściwości oraz zastosowania. Dowiedz się o roli tlenu i azotu w procesach spalania oraz ich znaczeniu w przemyśle. Zawiera obserwacje eksperymentalne dotyczące tlenku węgla (IV) i jego interakcji z wodą wapienną. Typ: Podsumowanie.
Charakterystyka Azotowców
Zgłębiaj właściwości pierwiastków grupy 15, w tym azotu i fosforu. Dowiedz się o ich stanach skupienia, reaktywności oraz zastosowaniach w chemii. Materiał przeznaczony dla uczniów klas 2/3 LO na poziomie rozszerzonym.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.