Atom to podstawowa jednostka materii, która składa się z jądra... Pokaż więcej
Atom - Podstawowe informacje o budowie atomu







Budowa atomu i mechanika kwantowa
Atom składa się z jądra zawierającego protony (ładunek dodatni, masa 1u) i neutrony (elektrycznie obojętne, masa 1u) oraz elektronów krążących wokół jądra.
W mechanice kwantowej stan elektronów opisują cztery liczby kwantowe:
- Główna liczba kwantowa (n) - określa powłokę elektronową i rozmiar orbitali (przyjmuje wartości od 1 do ∞)
- Poboczna liczba kwantowa (l) - określa kształt orbitali i podpowłoki
- Magnetyczna liczba kwantowa (m) - określa orientację przestrzenną orbitali
- Spinowa liczba kwantowa (ms) - określa kierunek spinu elektronu (±1/2)
💡 Pamiętaj! Każdy orbital może pomieścić maksymalnie 2 elektrony, które muszą różnić się kierunkiem spinu.
Orbitale i podpowłoki elektronowe
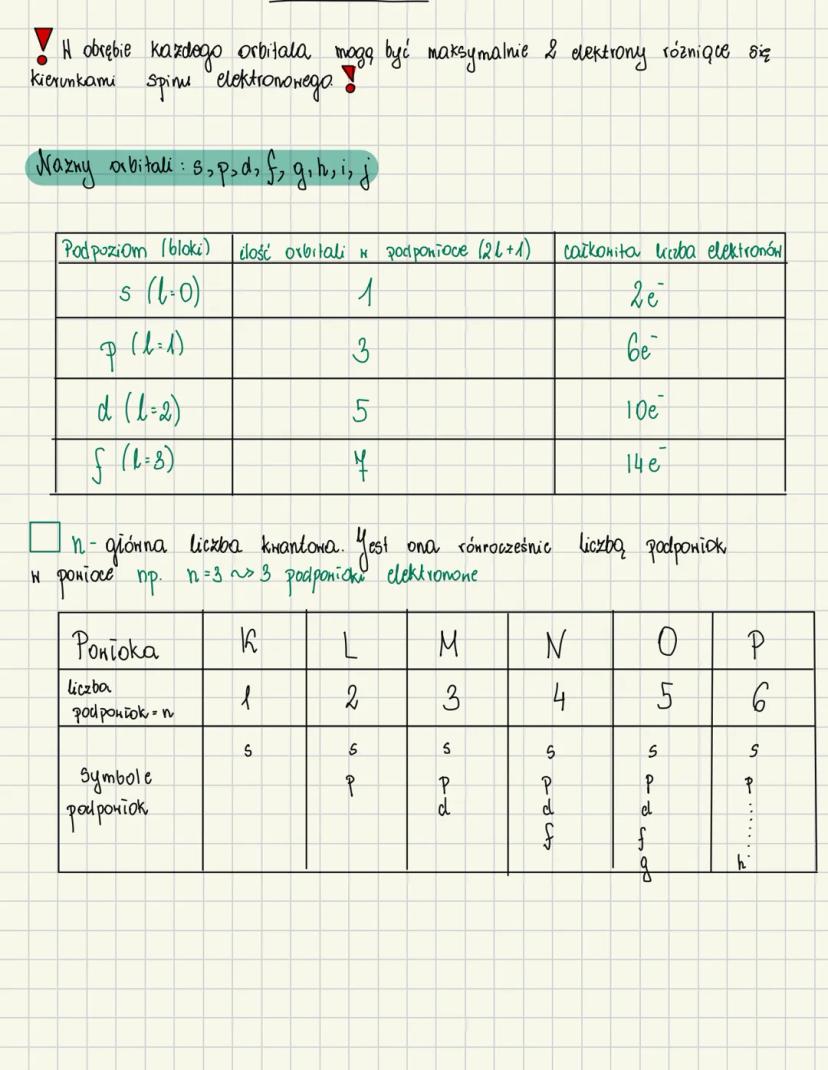
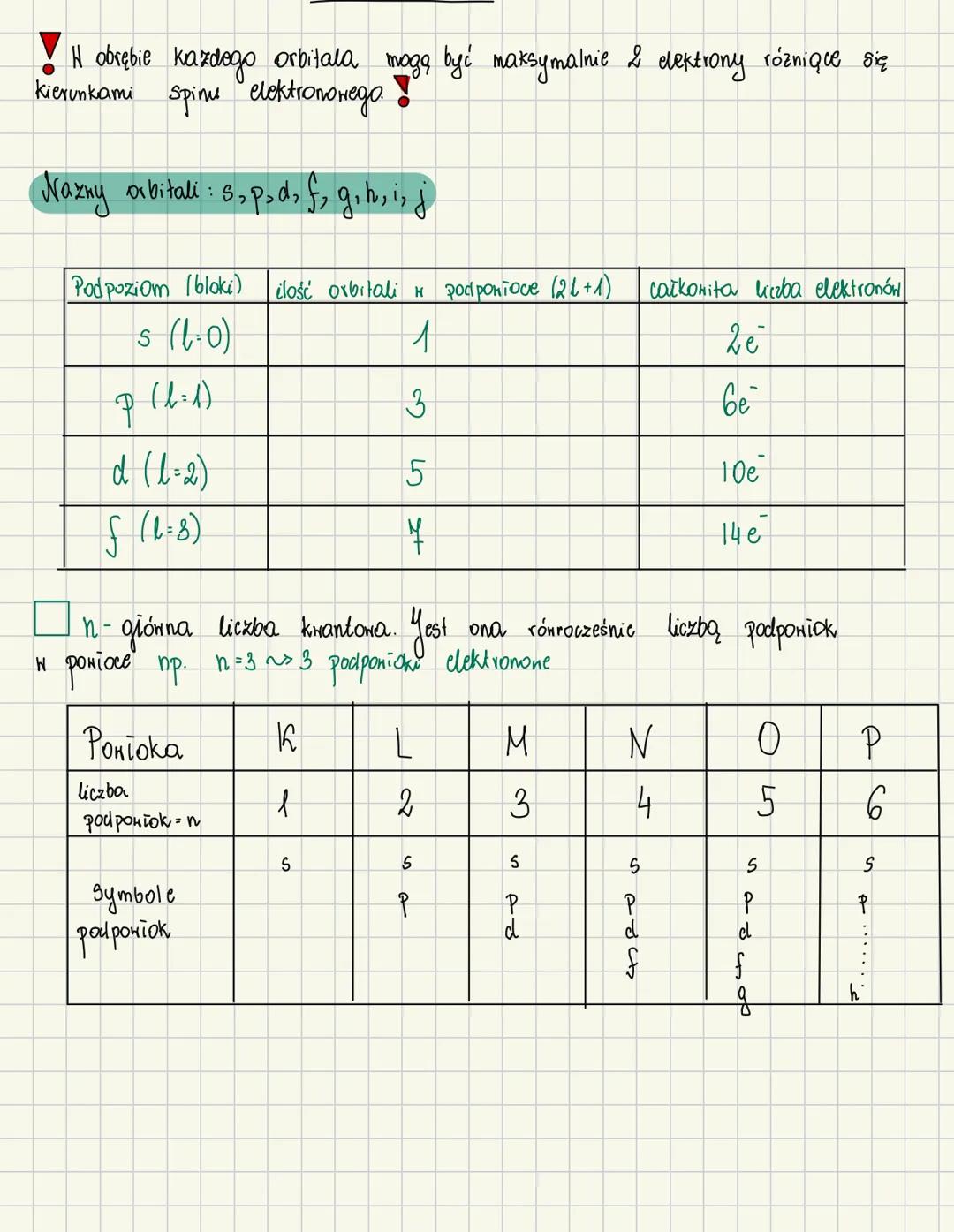
Orbitale atomowe oznaczamy symbolami: s, p, d, f, g, h, i, j. Każdy typ orbitalu może pomieścić określoną liczbę elektronów:
- Orbital s - 1 orbital, mieści 2 elektrony
- Orbital p - 3 orbitale, mieszczą łącznie 6 elektronów
- Orbital d - 5 orbitali, mieszczą łącznie 10 elektronów
- Orbital f - 7 orbitali, mieszczą łącznie 14 elektronów
Główna liczba kwantowa (n) określa liczbę podpowłok w danej powłoce. Na przykład, dla n=3 mamy 3 podpowłoki elektronowe. Powłoki oznaczamy literami K, L, M, N, O, P, które odpowiadają wartościom n od 1 do 6.
Powłoka K zawiera tylko podpowłokę s, powłoka L zawiera podpowłoki s i p, a powłoka M zawiera podpowłoki s, p i d. Z każdą kolejną powłoką rośnie liczba możliwych podpowłok.
🧪 Ciekawostka: Liczba elektronów na danej podpowłoce zawsze wynosi 2, gdzie l to poboczna liczba kwantowa.

Stany kwantowe i konfiguracja elektronowa
Dla n=1 (powłoka K) mamy tylko jedną możliwą kombinację liczb kwantowych:
- Poboczna liczba kwantowa l=0 (podpowłoka s)
- Magnetyczna liczba kwantowa m=0
- Spinowa liczba kwantowa ms = ±1/2
Daje to łącznie 2 stany kwantowe, co oznacza, że na pierwszej powłoce może znajdować się maksymalnie 2 elektrony.
Konfiguracja elektronowa atomów opisuje rozmieszczenie elektronów na powłokach i podpowłokach. Elektrony wypełniają orbitale zgodnie z zasadą minimalnej energii, zaczynając od 1s, następnie 2s, 2p itd.
Kolejność zapełniania podpowłok: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
⚡ Zapamiętaj tę kolejność! Zauważ, że niekiedy elektrony najpierw zapełniają podpowłoki o wyższej głównej liczbie kwantowej (np. 4s przed 3d).

Zapis konfiguracji elektronowej
Konfigurację elektronową zapisujemy w formie:
- Pełny zapis: pokazuje wszystkie podpowłoki, np. 1s² 2s² 2p²
- Skrócony zapis: używa symbolu gazu szlachetnego w nawiasie kwadratowym, np. węgiel 6C: [He] 2s² 2p²
W zapisie konfiguracji elektronowej:
- Liczba w indeksie dolnym oznacza liczbę elektronów na danej podpowłoce
- Cyfra przed symbolem podpowłoki to numer powłoki (główna liczba kwantowa)
- Symbol podpowłoki (s, p, d, f) odpowiada pobocznej liczbie kwantowej
Schemat klatkowy pokazuje graficznie rozmieszczenie elektronów na orbitalach, używając strzałek do reprezentowania elektronów o różnych spinach.
🔍 Skrócony zapis konfiguracji jest szczególnie przydatny dla pierwiastków o dużej liczbie elektronów - oszczędza czas i jest bardziej przejrzysty!

Liczba atomowa i liczba masowa
Liczba atomowa (Z) to liczba protonów w jądrze atomowym. Jest ona unikalna dla każdego pierwiastka i określa jego miejsce w układzie okresowym. Dla atomu obojętnego liczba protonów równa się liczbie elektronów.
Liczba masowa (A) to suma liczby protonów i neutronów w jądrze atomowym. Obliczamy ją ze wzoru: A = Z + liczba neutronów
Przykład: tlen ma liczbę atomową Z=8 i liczbę masową A=16, co oznacza, że ma 8 protonów i 8 neutronów (16-8).
Liczbę masową i atomową zapisujemy przy symbolu pierwiastka w formie: X, np. O
Masy atomowe podaje się w jednostkach masy atomowej (u), która została zdefiniowana jako 1/12 masy atomu węgla C.
💡 Zapamiętaj: liczba atomowa Z = liczba protonów = ładunek jądra, a liczba masowa A = liczba protonów + liczba neutronów.

Izotopy i masa atomowa
Izotopy to atomy tego samego pierwiastka (mają taką samą liczbę Z), ale różnią się liczbą neutronów (mają różne liczby A). Przykładowo, wodór ma trzy izotopy: prot $^1_1$H, deuter $^2_1$H i tryt $^3_1$H.
Obok izotopów wyróżniamy:
- Izobary - atomy różnych pierwiastków o tej samej liczbie masowej A
- Izotony - atomy różnych pierwiastków mające tę samą liczbę neutronów
Masa atomowa pierwiastka podawana w układzie okresowym jest średnią ważoną mas jego izotopów, z uwzględnieniem ich procentowego udziału w przyrodzie:
M_{at} = \frac{%m_1 \cdot A_1 + %m_2 \cdot A_2 + ...}{100%}
gdzie to procentowe zawartości poszczególnych izotopów, a to ich liczby masowe.
🧪 Dlaczego masa atomowa tlenu to około 15,999, a nie dokładnie 16? Ponieważ w przyrodzie występuje mieszanina izotopów tlenu o różnych masach!

Promieniotwórczość
Promieniotwórczość to zdolność jąder atomowych do samorzutnego rozpadu, któremu towarzyszy emisja promieniowania. Wyróżniamy:
-
Przemiana α (alfa): jądro emituje cząstkę α (jądro helu), tracąc 2 protony i 2 neutrony.
-
Przemiana β- (beta minus): neutron zamienia się w proton, emitując elektron.
-
Przemiana β+ (beta plus): proton zamienia się w neutron, emitując pozyton.
Okres półrozpadu to czas, po którym połowa jąder promieniotwórczych ulega rozpadowi. Jest charakterystyczny dla danego izotopu, nie zależy od czynników zewnętrznych i nie zmienia się w czasie.
⚠️ Im krótszy okres półrozpadu, tym większa aktywność promieniotwórcza izotopu - taki izotop szybciej się rozpada!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Atom
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Atom - Podstawowe informacje o budowie atomu
Atom to podstawowa jednostka materii, która składa się z jądra i otaczających je elektronów. Zrozumienie budowy atomu i mechaniki kwantowej jest kluczowe dla chemii, fizyki i wielu innych dziedzin nauki.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa atomu i mechanika kwantowa
Atom składa się z jądra zawierającego protony (ładunek dodatni, masa 1u) i neutrony (elektrycznie obojętne, masa 1u) oraz elektronów krążących wokół jądra.
W mechanice kwantowej stan elektronów opisują cztery liczby kwantowe:
- Główna liczba kwantowa (n) - określa powłokę elektronową i rozmiar orbitali (przyjmuje wartości od 1 do ∞)
- Poboczna liczba kwantowa (l) - określa kształt orbitali i podpowłoki
- Magnetyczna liczba kwantowa (m) - określa orientację przestrzenną orbitali
- Spinowa liczba kwantowa (ms) - określa kierunek spinu elektronu (±1/2)
💡 Pamiętaj! Każdy orbital może pomieścić maksymalnie 2 elektrony, które muszą różnić się kierunkiem spinu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Orbitale i podpowłoki elektronowe
Orbitale atomowe oznaczamy symbolami: s, p, d, f, g, h, i, j. Każdy typ orbitalu może pomieścić określoną liczbę elektronów:
- Orbital s - 1 orbital, mieści 2 elektrony
- Orbital p - 3 orbitale, mieszczą łącznie 6 elektronów
- Orbital d - 5 orbitali, mieszczą łącznie 10 elektronów
- Orbital f - 7 orbitali, mieszczą łącznie 14 elektronów
Główna liczba kwantowa (n) określa liczbę podpowłok w danej powłoce. Na przykład, dla n=3 mamy 3 podpowłoki elektronowe. Powłoki oznaczamy literami K, L, M, N, O, P, które odpowiadają wartościom n od 1 do 6.
Powłoka K zawiera tylko podpowłokę s, powłoka L zawiera podpowłoki s i p, a powłoka M zawiera podpowłoki s, p i d. Z każdą kolejną powłoką rośnie liczba możliwych podpowłok.
🧪 Ciekawostka: Liczba elektronów na danej podpowłoce zawsze wynosi 2, gdzie l to poboczna liczba kwantowa.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Stany kwantowe i konfiguracja elektronowa
Dla n=1 (powłoka K) mamy tylko jedną możliwą kombinację liczb kwantowych:
- Poboczna liczba kwantowa l=0 (podpowłoka s)
- Magnetyczna liczba kwantowa m=0
- Spinowa liczba kwantowa ms = ±1/2
Daje to łącznie 2 stany kwantowe, co oznacza, że na pierwszej powłoce może znajdować się maksymalnie 2 elektrony.
Konfiguracja elektronowa atomów opisuje rozmieszczenie elektronów na powłokach i podpowłokach. Elektrony wypełniają orbitale zgodnie z zasadą minimalnej energii, zaczynając od 1s, następnie 2s, 2p itd.
Kolejność zapełniania podpowłok: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
⚡ Zapamiętaj tę kolejność! Zauważ, że niekiedy elektrony najpierw zapełniają podpowłoki o wyższej głównej liczbie kwantowej (np. 4s przed 3d).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zapis konfiguracji elektronowej
Konfigurację elektronową zapisujemy w formie:
- Pełny zapis: pokazuje wszystkie podpowłoki, np. 1s² 2s² 2p²
- Skrócony zapis: używa symbolu gazu szlachetnego w nawiasie kwadratowym, np. węgiel 6C: [He] 2s² 2p²
W zapisie konfiguracji elektronowej:
- Liczba w indeksie dolnym oznacza liczbę elektronów na danej podpowłoce
- Cyfra przed symbolem podpowłoki to numer powłoki (główna liczba kwantowa)
- Symbol podpowłoki (s, p, d, f) odpowiada pobocznej liczbie kwantowej
Schemat klatkowy pokazuje graficznie rozmieszczenie elektronów na orbitalach, używając strzałek do reprezentowania elektronów o różnych spinach.
🔍 Skrócony zapis konfiguracji jest szczególnie przydatny dla pierwiastków o dużej liczbie elektronów - oszczędza czas i jest bardziej przejrzysty!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Liczba atomowa i liczba masowa
Liczba atomowa (Z) to liczba protonów w jądrze atomowym. Jest ona unikalna dla każdego pierwiastka i określa jego miejsce w układzie okresowym. Dla atomu obojętnego liczba protonów równa się liczbie elektronów.
Liczba masowa (A) to suma liczby protonów i neutronów w jądrze atomowym. Obliczamy ją ze wzoru: A = Z + liczba neutronów
Przykład: tlen ma liczbę atomową Z=8 i liczbę masową A=16, co oznacza, że ma 8 protonów i 8 neutronów (16-8).
Liczbę masową i atomową zapisujemy przy symbolu pierwiastka w formie: X, np. O
Masy atomowe podaje się w jednostkach masy atomowej (u), która została zdefiniowana jako 1/12 masy atomu węgla C.
💡 Zapamiętaj: liczba atomowa Z = liczba protonów = ładunek jądra, a liczba masowa A = liczba protonów + liczba neutronów.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Izotopy i masa atomowa
Izotopy to atomy tego samego pierwiastka (mają taką samą liczbę Z), ale różnią się liczbą neutronów (mają różne liczby A). Przykładowo, wodór ma trzy izotopy: prot $^1_1$H, deuter $^2_1$H i tryt $^3_1$H.
Obok izotopów wyróżniamy:
- Izobary - atomy różnych pierwiastków o tej samej liczbie masowej A
- Izotony - atomy różnych pierwiastków mające tę samą liczbę neutronów
Masa atomowa pierwiastka podawana w układzie okresowym jest średnią ważoną mas jego izotopów, z uwzględnieniem ich procentowego udziału w przyrodzie:
M_{at} = \frac{%m_1 \cdot A_1 + %m_2 \cdot A_2 + ...}{100%}
gdzie to procentowe zawartości poszczególnych izotopów, a to ich liczby masowe.
🧪 Dlaczego masa atomowa tlenu to około 15,999, a nie dokładnie 16? Ponieważ w przyrodzie występuje mieszanina izotopów tlenu o różnych masach!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Promieniotwórczość
Promieniotwórczość to zdolność jąder atomowych do samorzutnego rozpadu, któremu towarzyszy emisja promieniowania. Wyróżniamy:
-
Przemiana α (alfa): jądro emituje cząstkę α (jądro helu), tracąc 2 protony i 2 neutrony.
-
Przemiana β- (beta minus): neutron zamienia się w proton, emitując elektron.
-
Przemiana β+ (beta plus): proton zamienia się w neutron, emitując pozyton.
Okres półrozpadu to czas, po którym połowa jąder promieniotwórczych ulega rozpadowi. Jest charakterystyczny dla danego izotopu, nie zależy od czynników zewnętrznych i nie zmienia się w czasie.
⚠️ Im krótszy okres półrozpadu, tym większa aktywność promieniotwórcza izotopu - taki izotop szybciej się rozpada!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Atom
9Najpopularniejsze notatki z Chemia
9Najpopularniejsze notatki
9Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.