Witaj! W dzisiejszej notce poznasz budowę atomu oraz układ okresowy... Pokaż więcej
Struktura i Budowa Atomów






Budowa atomu
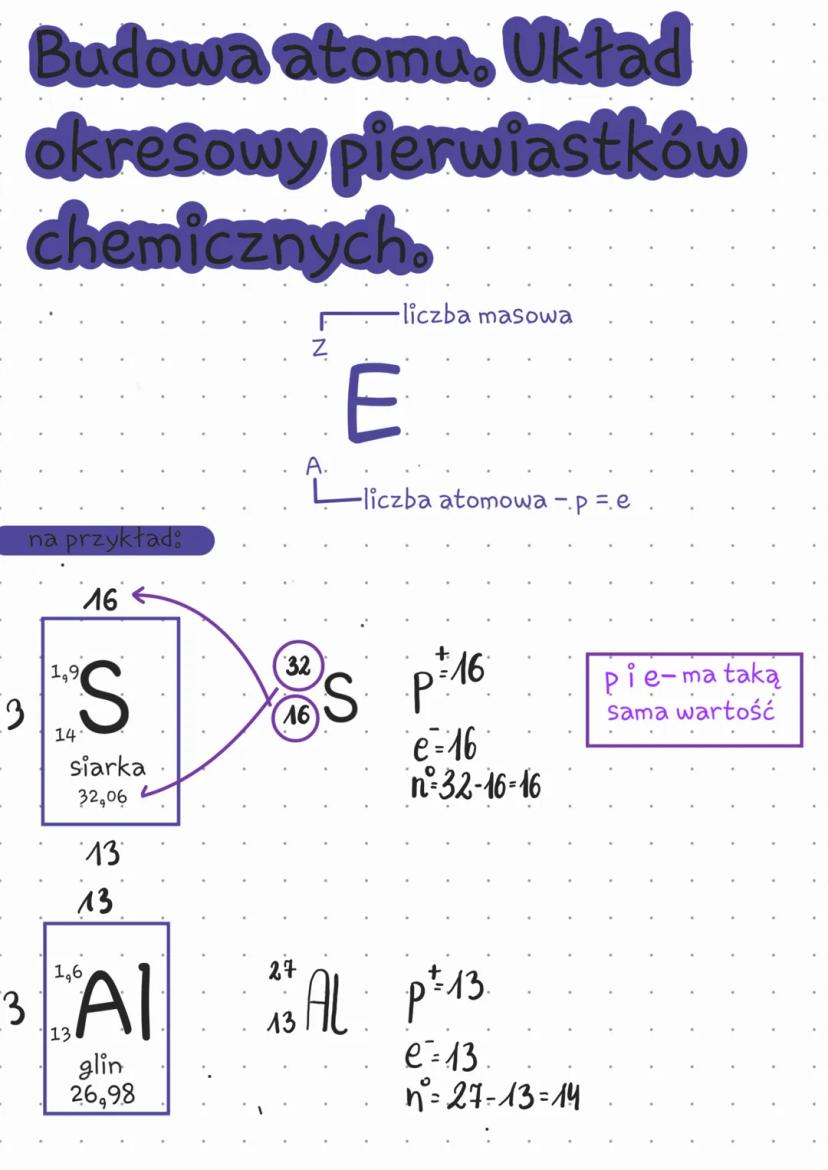
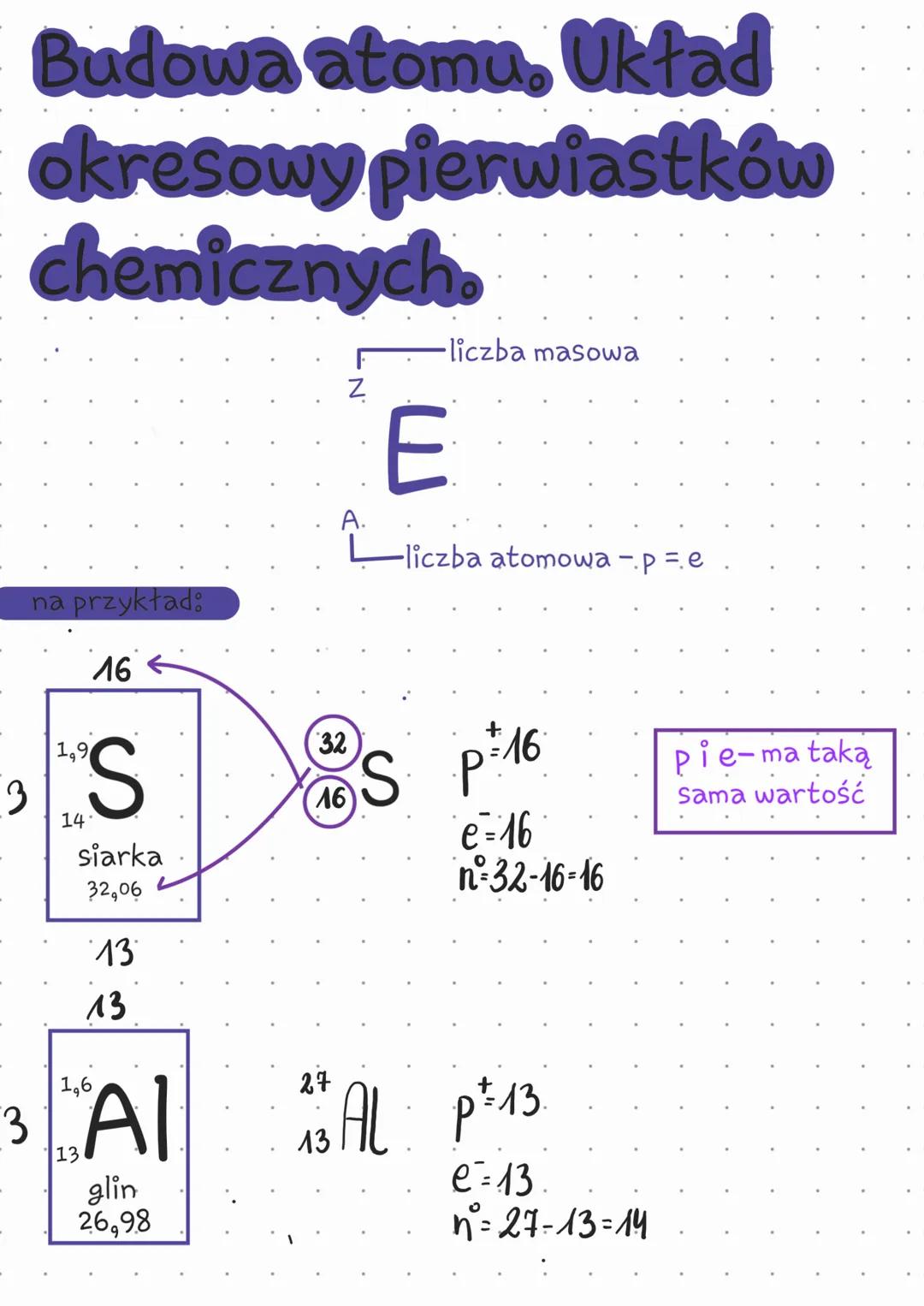
Atom składa się z protonów, neutronów i elektronów. Liczba atomowa (Z) określa liczbę protonów w jądrze, a jednocześnie liczbę elektronów w atomie. Liczba masowa (A) to suma protonów i neutronów.
Analizując przykłady, możemy łatwo obliczyć liczbę neutronów. Dla siarki (S): liczba atomowa to 16 (czyli 16 protonów i 16 elektronów), liczba masowa to 32, więc neutronów jest 32-16=16. Dla glinu (Al): liczba atomowa to 13, liczba masowa to 27, więc neutronów jest 27-13=14.
Wskazówka! Zawsze możesz obliczyć liczbę neutronów odejmując liczbę protonów od liczby masowej: n = A - Z.

Układ okresowy pierwiastków
Układ okresowy to mapa wszystkich pierwiastków chemicznych. Każdy pierwiastek ma swój symbol chemiczny , liczbę atomową i względną masę atomową (np. złoto: 196,97).
Położenie pierwiastka w układzie okresowym daje nam informacje o jego właściwościach. Pierwiastki są ułożone w grupy (kolumny) i okresy (rzędy). Grupa określa liczbę elektronów walencyjnych, np. pierwiastek z 16 grupy ma 6 elektronów walencyjnych.
Konfiguracja elektronowa opisuje rozmieszczenie elektronów na powłokach i podpowłokach. Na przykład, dla siarki (S) z liczbą atomową 16, elektrony rozmieszczone są według wzoru: K²L⁸M⁶, gdzie podpowłoki to: 1s²2s²2p⁶3s²3p⁴.
Zapamiętaj! Numer grupy często określa liczbę elektronów walencyjnych pierwiastka, które decydują o jego właściwościach chemicznych.

Określanie składu atomu
Dzięki znajomości liczby atomowej i masowej możemy określić pełny skład atomu. Dla wapnia (Ca): liczba atomowa to 20, liczba masowa to 40, więc mamy 20 protonów, 20 elektronów i 40-20=20 neutronów.
Dla berylu (Be): liczba atomowa to 4, liczba masowa to 9, więc mamy 4 protony, 4 elektrony i 9-4=5 neutronów. Jego konfiguracja elektronowa to K²L².
Ćwiczenie: Dla uranu (U) liczba atomowa wynosi 92. Jeśli liczba nukleonów to 238, to liczba neutronów to 238-92=146. Uran ma więc 92 protony, 92 elektrony i 146 neutronów.
Spróbuj! Samodzielnie określ liczbę protonów, neutronów i elektronów dla dowolnego pierwiastka z układu okresowego. To świetne ćwiczenie na zrozumienie podstaw budowy atomu.

Konfiguracja elektronowa
Konfiguracja elektronowa pokazuje, jak elektrony są rozmieszczone na powłokach i podpowłokach atomu. Dla pierwiastka z 3 okresu i 16 grupy (siarki) konfiguracja to: K²L⁸M⁶ lub szczegółowo: 1s²2s²2p⁶3s²3p⁴.
W konfiguracji elektronowej rozróżniamy elektrony walencyjne (zewnętrzne) oraz elektrony rdzeniowe (wewnętrzne). Dla siarki 6 elektronów to elektrony walencyjne, a 10 to elektrony rdzeniowe.
Pierwiastki z tego samego okresu mają podobny schemat wypełniania powłok. Przykładowo, pierwiastki z 3 okresu (Mg, Si, S, Ar) mają zapełnione powłoki K i L oraz częściowo zapełnioną powłokę M, różniąc się liczbą elektronów na podpowłokach 3s i 3p.
Ciekawostka: Skrócony zapis konfiguracji elektronowej można przedstawić używając symbolu gazu szlachetnego w nawiasie kwadratowym, np. dla siarki: [Ne]3s²3p⁴.

Konfiguracje jonów
Jony powstają przez dodanie lub utratę elektronów przez atom. Kation powstaje, gdy atom traci elektron (np. K⁺), a anion, gdy atom przyjmuje elektron (np. Cl⁻).
Kation potasu (K⁺) powstaje, gdy potas (19 elektronów) traci jeden elektron, mając wtedy 18 elektronów. Anion chlorkowy (Cl⁻) powstaje, gdy chlor (17 elektronów) przyjmuje elektron, mając 18 elektronów. Oba jony mają konfigurację elektronową argonu (Ar).
Wiedząc, że helowiec (pierwiastek 18 grupy) ma taką samą konfigurację jak kation potasu i anion chlorkowy, możemy ustalić, że jest to argon (Ar) o konfiguracji 1s²2s²2p⁶3s²3p⁶.
Uproszczenie! Jony dążą do uzyskania stabilnej konfiguracji elektronowej najbliższego gazu szlachetnego, co często oznacza 8 elektronów na zewnętrznej powłoce (reguła oktetu).

Obliczenia dla jonów i wiązania chemiczne
W jonie tlenkowym O²⁻ liczba protonów wynosi 8 (liczba atomowa tlenu), liczba elektronów to 8+2=10 (atom przyjął 2 elektrony), a liczba neutronów to 16-8=8, zakładając liczbę masową 16.
Rodzaj wiązania chemicznego zależy od różnicy elektroujemności (ΔE) między pierwiastkami. Dla przykładu, w związku LiF różnica wynosi ΔE=3,4-1,0=2,4, co wskazuje na wiązanie jonowe (ΔE>1,7).
W przypadku związków jak CH₄, NH₃, czy MgH₂, różnica elektroujemności jest mniejsza, wskazując na wiązanie kowalencyjne spolaryzowane (0,4<ΔE<1,7) lub niespolaryzowane (ΔE<0,4).
Zapamiętaj wzór! Im większa różnica elektroujemności między pierwiastkami, tym wiązanie ma bardziej jonowy charakter. Przyjmujemy, że przy ΔE>1,7 wiązanie jest jonowe.
Elektroujemność i typy wiązań
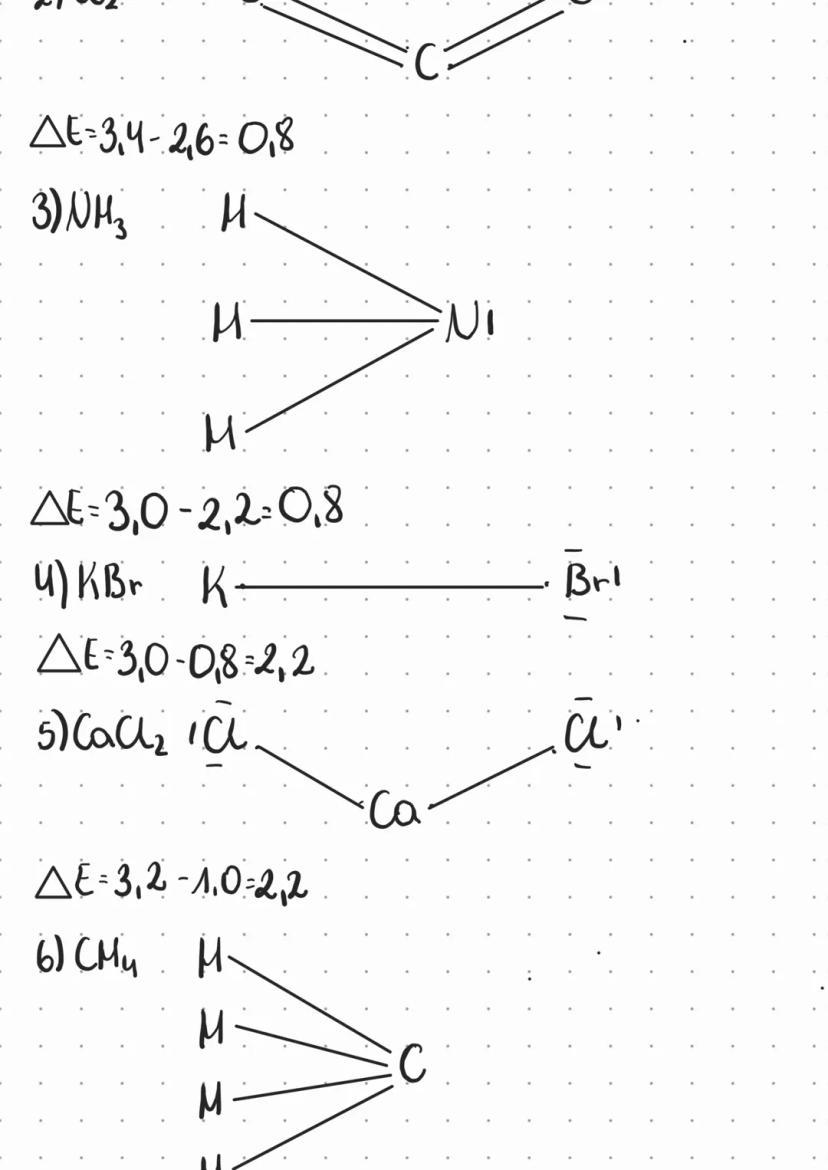
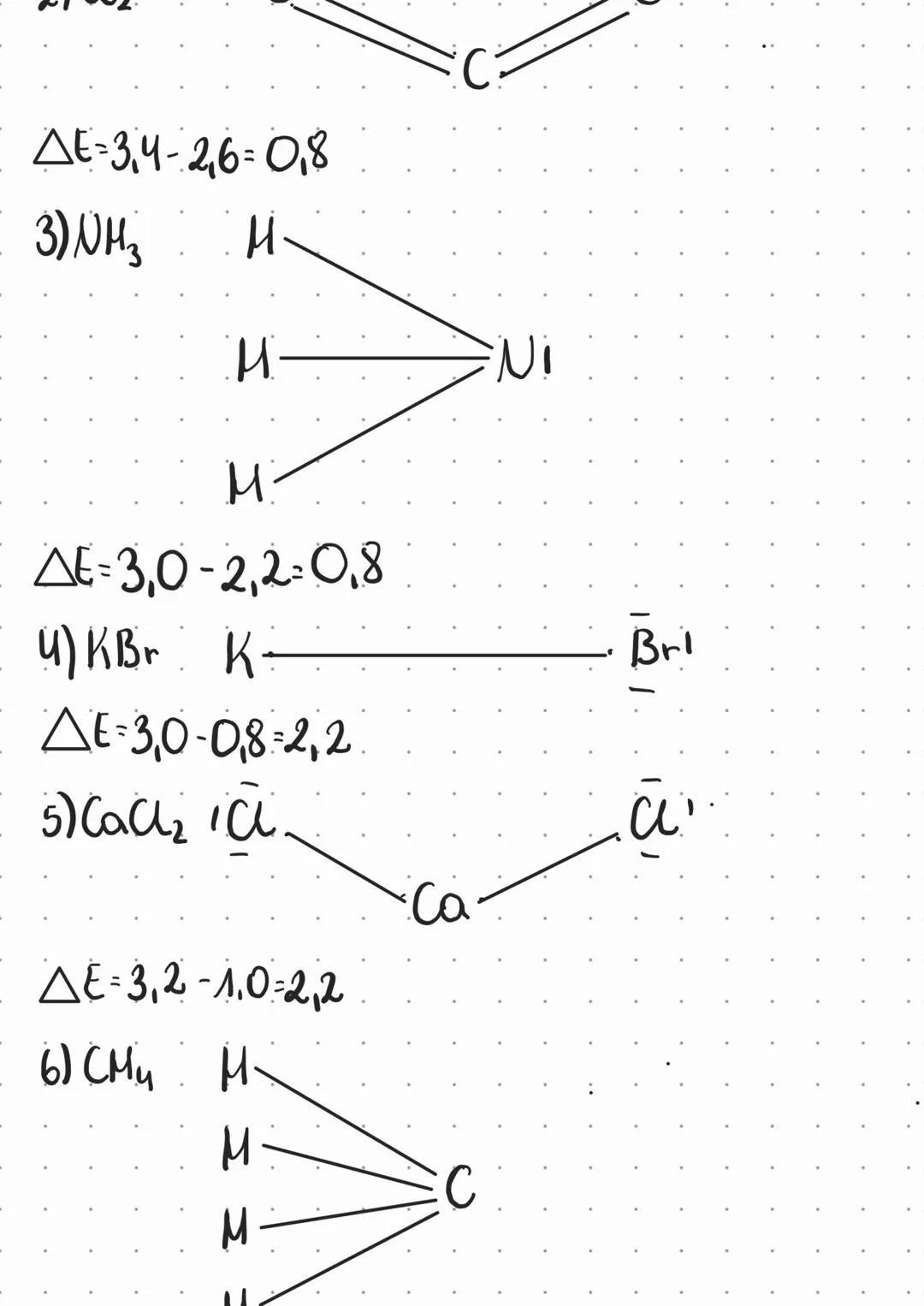
Różnica elektroujemności determinuje typ wiązania chemicznego między pierwiastkami. Dla związku NH₃, różnica elektroujemności wynosi ΔE=3,0-2,2=0,8, co wskazuje na wiązanie kowalencyjne spolaryzowane.
Podobnie w KBr różnica wynosi ΔE=3,0-0,8=2,2, co świadczy o wiązaniu jonowym. W przypadku CaH₂ różnica wynosi ΔE=3,2-1,0=2,2, również wskazując na wiązanie jonowe.
Wiedza o elektroujemności pozwala przewidzieć, jak pierwiastki będą się ze sobą łączyć i jaki charakter będzie miało powstałe wiązanie. Im większa różnica, tym bardziej wiązanie ma charakter jonowy.
Praktyczna rada: Zapamiętaj wartości elektroujemności najważniejszych pierwiastków - to ułatwi Ci szybkie określanie typów wiązań chemicznych.

Obliczanie elektroujemności w związkach chemicznych
Dla związków zawierających magnez (Mg), różnica elektroujemności wynosi ΔE=2,6-2,2=0,4. Ta wartość znajduje się na granicy między wiązaniem kowalencyjnym niespolaryzowanym a spolaryzowanym.
Przy małej różnicy elektroujemności (ΔE<0,4) mówimy o wiązaniu kowalencyjnym niespolaryzowanym, gdzie elektrony są równomiernie rozłożone między atomami. Takie wiązania występują głównie między atomami tego samego pierwiastka lub pierwiastkami o bardzo zbliżonej elektroujemności.
Uproszczenie! Szybka zasada: ΔE<0,4 → wiązanie kowalencyjne niespolaryzowane, 0,4≤ΔE≤1,7 → wiązanie kowalencyjne spolaryzowane, ΔE>1,7 → wiązanie jonowe.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: liczba atomowa
7Struktura Atomu
Zrozumienie struktury atomu: liczba masowa, liczba atomowa, protony, neutrony i elektrony. Dowiedz się, jak te elementy wpływają na właściwości chemiczne pierwiastków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Budowa atomu. Układ okresowy pierwiastków. Chemia.
Chemia klasa 1 LO. Dział pierwszy. Poziom podstawowy
Konfigurację elektronowe
Mam nadzieję że po mojej notatce zrozumieliście ten temat
Elektrony Walencyjne i Powłoki
Zrozumienie, jak odczytać liczbę elektronów walencyjnych i powłok elektronowych pierwiastków z układu okresowego. Notatka zawiera przykłady dla sodu i fosforu oraz zasady dotyczące grup 1-2 i 13-18. Idealna dla uczniów chemii.
Budowa i Przemiany Atomów
Zrozumienie budowy atomu, w tym protonów, neutronów i elektronów, oraz kluczowych pojęć takich jak liczba atomowa, liczba masowa, izotopy, izobary i promieniotwórczość. Obejmuje również zasady mechaniki kwantowej, takie jak zasada nieoznaczoności Heisenberga oraz różne rodzaje promieniowania (α, β, γ). Idealne dla uczniów przygotowujących się do egzaminów z fizyki i chemii.
Budowa Atomu: Kluczowe Modele
Zrozumienie budowy atomu w kontekście modeli Thomsona, Rutherforda i Bohra. Dowiedz się o liczbach atomowych i masowych oraz ich znaczeniu w chemii. Idealne dla uczniów 8 klasy i 1 liceum. Typ: Podsumowanie.
Budowa Atomów i Cząsteczek
Zrozumienie budowy atomu: liczba protonów, neutronów i elektronów. Obliczanie liczby cząstek elementarnych dla różnych pierwiastków. Idealne dla uczniów liceum na poziomie podstawowym. Tematyka obejmuje liczby atomowe i masowe oraz ich znaczenie w chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Struktura i Budowa Atomów
Witaj! W dzisiejszej notce poznasz budowę atomu oraz układ okresowy pierwiastków chemicznych. Zrozumiesz, jak odczytywać informacje o pierwiastkach oraz jak określać ich strukturę elektronową.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa atomu
Atom składa się z protonów, neutronów i elektronów. Liczba atomowa (Z) określa liczbę protonów w jądrze, a jednocześnie liczbę elektronów w atomie. Liczba masowa (A) to suma protonów i neutronów.
Analizując przykłady, możemy łatwo obliczyć liczbę neutronów. Dla siarki (S): liczba atomowa to 16 (czyli 16 protonów i 16 elektronów), liczba masowa to 32, więc neutronów jest 32-16=16. Dla glinu (Al): liczba atomowa to 13, liczba masowa to 27, więc neutronów jest 27-13=14.
Wskazówka! Zawsze możesz obliczyć liczbę neutronów odejmując liczbę protonów od liczby masowej: n = A - Z.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Układ okresowy pierwiastków
Układ okresowy to mapa wszystkich pierwiastków chemicznych. Każdy pierwiastek ma swój symbol chemiczny , liczbę atomową i względną masę atomową (np. złoto: 196,97).
Położenie pierwiastka w układzie okresowym daje nam informacje o jego właściwościach. Pierwiastki są ułożone w grupy (kolumny) i okresy (rzędy). Grupa określa liczbę elektronów walencyjnych, np. pierwiastek z 16 grupy ma 6 elektronów walencyjnych.
Konfiguracja elektronowa opisuje rozmieszczenie elektronów na powłokach i podpowłokach. Na przykład, dla siarki (S) z liczbą atomową 16, elektrony rozmieszczone są według wzoru: K²L⁸M⁶, gdzie podpowłoki to: 1s²2s²2p⁶3s²3p⁴.
Zapamiętaj! Numer grupy często określa liczbę elektronów walencyjnych pierwiastka, które decydują o jego właściwościach chemicznych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Określanie składu atomu
Dzięki znajomości liczby atomowej i masowej możemy określić pełny skład atomu. Dla wapnia (Ca): liczba atomowa to 20, liczba masowa to 40, więc mamy 20 protonów, 20 elektronów i 40-20=20 neutronów.
Dla berylu (Be): liczba atomowa to 4, liczba masowa to 9, więc mamy 4 protony, 4 elektrony i 9-4=5 neutronów. Jego konfiguracja elektronowa to K²L².
Ćwiczenie: Dla uranu (U) liczba atomowa wynosi 92. Jeśli liczba nukleonów to 238, to liczba neutronów to 238-92=146. Uran ma więc 92 protony, 92 elektrony i 146 neutronów.
Spróbuj! Samodzielnie określ liczbę protonów, neutronów i elektronów dla dowolnego pierwiastka z układu okresowego. To świetne ćwiczenie na zrozumienie podstaw budowy atomu.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Konfiguracja elektronowa
Konfiguracja elektronowa pokazuje, jak elektrony są rozmieszczone na powłokach i podpowłokach atomu. Dla pierwiastka z 3 okresu i 16 grupy (siarki) konfiguracja to: K²L⁸M⁶ lub szczegółowo: 1s²2s²2p⁶3s²3p⁴.
W konfiguracji elektronowej rozróżniamy elektrony walencyjne (zewnętrzne) oraz elektrony rdzeniowe (wewnętrzne). Dla siarki 6 elektronów to elektrony walencyjne, a 10 to elektrony rdzeniowe.
Pierwiastki z tego samego okresu mają podobny schemat wypełniania powłok. Przykładowo, pierwiastki z 3 okresu (Mg, Si, S, Ar) mają zapełnione powłoki K i L oraz częściowo zapełnioną powłokę M, różniąc się liczbą elektronów na podpowłokach 3s i 3p.
Ciekawostka: Skrócony zapis konfiguracji elektronowej można przedstawić używając symbolu gazu szlachetnego w nawiasie kwadratowym, np. dla siarki: [Ne]3s²3p⁴.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Konfiguracje jonów
Jony powstają przez dodanie lub utratę elektronów przez atom. Kation powstaje, gdy atom traci elektron (np. K⁺), a anion, gdy atom przyjmuje elektron (np. Cl⁻).
Kation potasu (K⁺) powstaje, gdy potas (19 elektronów) traci jeden elektron, mając wtedy 18 elektronów. Anion chlorkowy (Cl⁻) powstaje, gdy chlor (17 elektronów) przyjmuje elektron, mając 18 elektronów. Oba jony mają konfigurację elektronową argonu (Ar).
Wiedząc, że helowiec (pierwiastek 18 grupy) ma taką samą konfigurację jak kation potasu i anion chlorkowy, możemy ustalić, że jest to argon (Ar) o konfiguracji 1s²2s²2p⁶3s²3p⁶.
Uproszczenie! Jony dążą do uzyskania stabilnej konfiguracji elektronowej najbliższego gazu szlachetnego, co często oznacza 8 elektronów na zewnętrznej powłoce (reguła oktetu).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczenia dla jonów i wiązania chemiczne
W jonie tlenkowym O²⁻ liczba protonów wynosi 8 (liczba atomowa tlenu), liczba elektronów to 8+2=10 (atom przyjął 2 elektrony), a liczba neutronów to 16-8=8, zakładając liczbę masową 16.
Rodzaj wiązania chemicznego zależy od różnicy elektroujemności (ΔE) między pierwiastkami. Dla przykładu, w związku LiF różnica wynosi ΔE=3,4-1,0=2,4, co wskazuje na wiązanie jonowe (ΔE>1,7).
W przypadku związków jak CH₄, NH₃, czy MgH₂, różnica elektroujemności jest mniejsza, wskazując na wiązanie kowalencyjne spolaryzowane (0,4<ΔE<1,7) lub niespolaryzowane (ΔE<0,4).
Zapamiętaj wzór! Im większa różnica elektroujemności między pierwiastkami, tym wiązanie ma bardziej jonowy charakter. Przyjmujemy, że przy ΔE>1,7 wiązanie jest jonowe.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Elektroujemność i typy wiązań
Różnica elektroujemności determinuje typ wiązania chemicznego między pierwiastkami. Dla związku NH₃, różnica elektroujemności wynosi ΔE=3,0-2,2=0,8, co wskazuje na wiązanie kowalencyjne spolaryzowane.
Podobnie w KBr różnica wynosi ΔE=3,0-0,8=2,2, co świadczy o wiązaniu jonowym. W przypadku CaH₂ różnica wynosi ΔE=3,2-1,0=2,2, również wskazując na wiązanie jonowe.
Wiedza o elektroujemności pozwala przewidzieć, jak pierwiastki będą się ze sobą łączyć i jaki charakter będzie miało powstałe wiązanie. Im większa różnica, tym bardziej wiązanie ma charakter jonowy.
Praktyczna rada: Zapamiętaj wartości elektroujemności najważniejszych pierwiastków - to ułatwi Ci szybkie określanie typów wiązań chemicznych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczanie elektroujemności w związkach chemicznych
Dla związków zawierających magnez (Mg), różnica elektroujemności wynosi ΔE=2,6-2,2=0,4. Ta wartość znajduje się na granicy między wiązaniem kowalencyjnym niespolaryzowanym a spolaryzowanym.
Przy małej różnicy elektroujemności (ΔE<0,4) mówimy o wiązaniu kowalencyjnym niespolaryzowanym, gdzie elektrony są równomiernie rozłożone między atomami. Takie wiązania występują głównie między atomami tego samego pierwiastka lub pierwiastkami o bardzo zbliżonej elektroujemności.
Uproszczenie! Szybka zasada: ΔE<0,4 → wiązanie kowalencyjne niespolaryzowane, 0,4≤ΔE≤1,7 → wiązanie kowalencyjne spolaryzowane, ΔE>1,7 → wiązanie jonowe.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: liczba atomowa
7Struktura Atomu
Zrozumienie struktury atomu: liczba masowa, liczba atomowa, protony, neutrony i elektrony. Dowiedz się, jak te elementy wpływają na właściwości chemiczne pierwiastków. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Budowa atomu. Układ okresowy pierwiastków. Chemia.
Chemia klasa 1 LO. Dział pierwszy. Poziom podstawowy
Konfigurację elektronowe
Mam nadzieję że po mojej notatce zrozumieliście ten temat
Elektrony Walencyjne i Powłoki
Zrozumienie, jak odczytać liczbę elektronów walencyjnych i powłok elektronowych pierwiastków z układu okresowego. Notatka zawiera przykłady dla sodu i fosforu oraz zasady dotyczące grup 1-2 i 13-18. Idealna dla uczniów chemii.
Budowa i Przemiany Atomów
Zrozumienie budowy atomu, w tym protonów, neutronów i elektronów, oraz kluczowych pojęć takich jak liczba atomowa, liczba masowa, izotopy, izobary i promieniotwórczość. Obejmuje również zasady mechaniki kwantowej, takie jak zasada nieoznaczoności Heisenberga oraz różne rodzaje promieniowania (α, β, γ). Idealne dla uczniów przygotowujących się do egzaminów z fizyki i chemii.
Budowa Atomu: Kluczowe Modele
Zrozumienie budowy atomu w kontekście modeli Thomsona, Rutherforda i Bohra. Dowiedz się o liczbach atomowych i masowych oraz ich znaczeniu w chemii. Idealne dla uczniów 8 klasy i 1 liceum. Typ: Podsumowanie.
Budowa Atomów i Cząsteczek
Zrozumienie budowy atomu: liczba protonów, neutronów i elektronów. Obliczanie liczby cząstek elementarnych dla różnych pierwiastków. Idealne dla uczniów liceum na poziomie podstawowym. Tematyka obejmuje liczby atomowe i masowe oraz ich znaczenie w chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.