Kwasy to ważne związki chemiczne, które dyspocjują w wodzie na... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
607
•
Zaktualizowano Apr 18, 2026
•
Nadia Jaouhari
@nadiajaouhari_bwpl
Kwasy to ważne związki chemiczne, które dyspocjują w wodzie na... Pokaż więcej
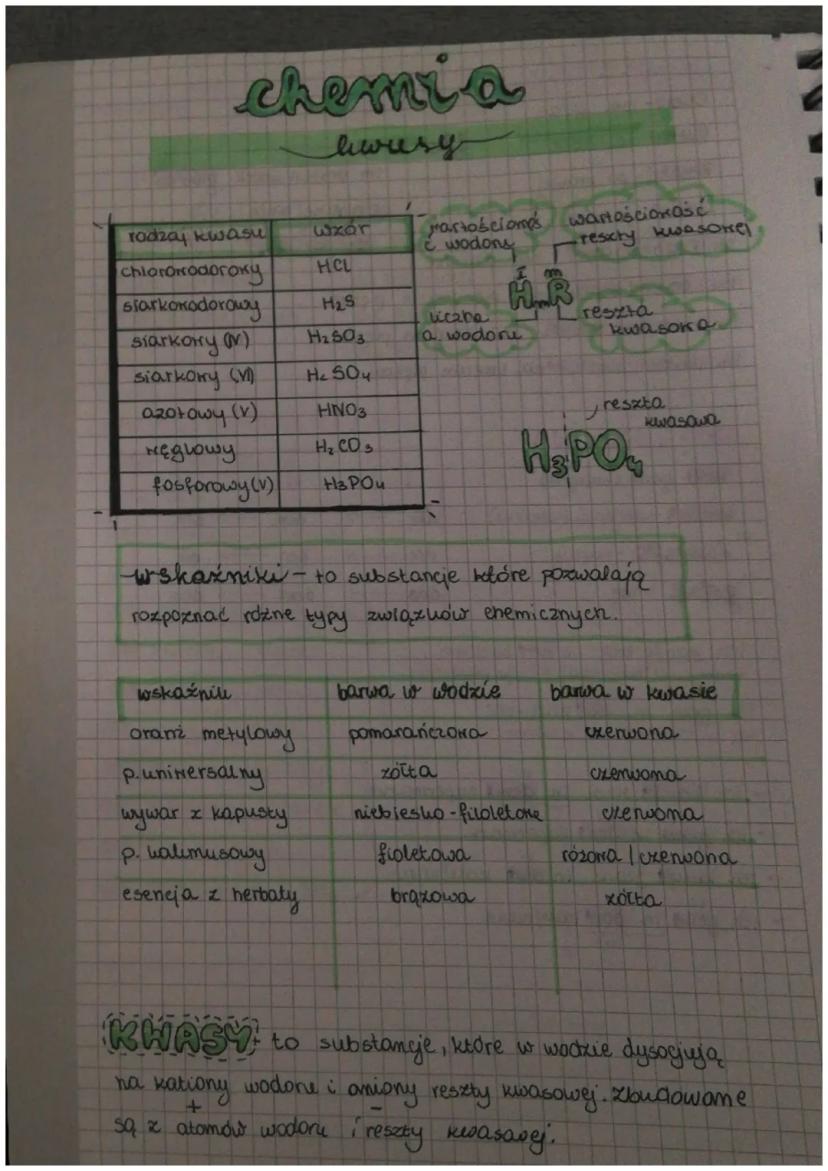






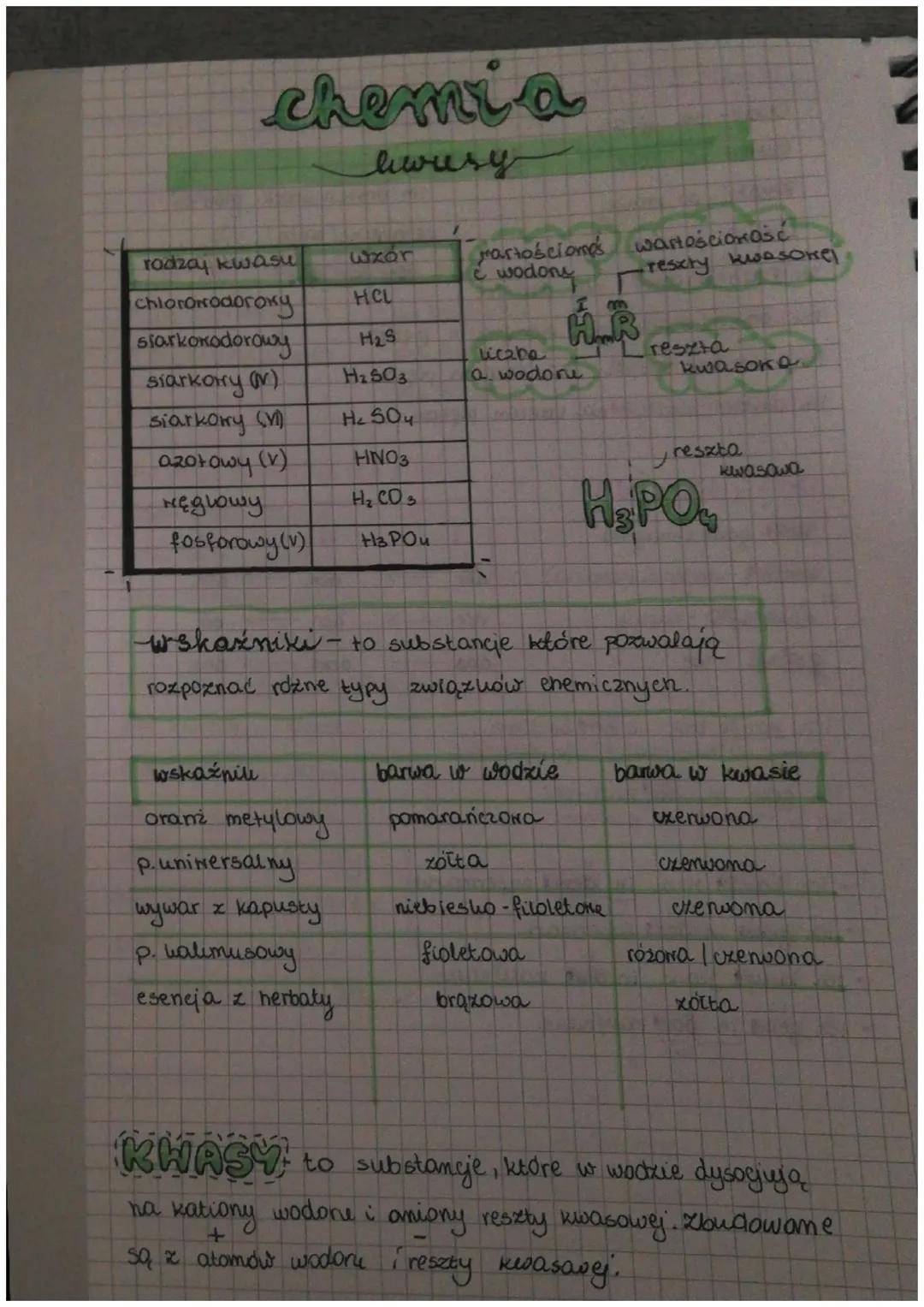
Kwasy to substancje, które w wodzie dyspocjują na kationy wodorowe i aniony reszty kwasowej. Są zbudowane z atomów wodoru i reszty kwasowej, która nadaje im charakterystyczne właściwości.
Istnieje wiele różnych kwasów, które możemy podzielić na beztlenowe (np. HCl, H₂S) oraz tlenowe (np. H₂SO₄, HNO₃, H₂CO₃, H₃PO₄). W nazwie kwasu tlenowego wartościowość pierwiastka zaznaczamy cyfrą rzymską w nawiasie, np. siarkowy (VI).
Do rozpoznawania kwasów używamy wskaźników - substancji zmieniających barwę w zależności od środowiska. Najpopularniejsze wskaźniki to oranż metylowy (zmienia kolor z pomarańczowego na czerwony), papierek uniwersalny (z żółtego na czerwony), wywar z czerwonej kapusty czy nawet zwykła esencja herbaciana (z brązowej na żółtą).
💡 Ciekawostka: Wiele produktów spożywczych może służyć jako naturalne wskaźniki kwasowości - sok z czerwonej kapusty jest jednym z najlepszych domowych wskaźników!

Kwas chlorowodorowy (HCl) to jeden z najpopularniejszych kwasów. Otrzymuje się go przez reakcję wodoru z chlorem, a następnie rozpuszczenie powstałego gazu w wodzie. Jest to bezbarwna ciecz o drażniącym zapachu, która doskonale przewodzi prąd elektryczny.
HCl ma wiele zastosowań - używamy go w przemyśle chemicznym jako odczynnik, w motoryzacji, przy produkcji tworzyw sztucznych i leków. W żołądku występuje jako składnik soku żołądkowego i pomaga w trawieniu pokarmów.
Kwas siarkowodorowy (H₂S) powstaje w reakcji wodoru z siarką, a następnie przez rozpuszczenie powstałego gazu w wodzie. Jego najbardziej charakterystyczną cechą jest zapach zgniłych jaj. Jest trujący, ale w małych stężeniach znajduje zastosowanie w produkcji siarki, kremach do depilacji oraz wodach leczniczych.
🧪 Uwaga! Nigdy nie wąchaj bezpośrednio kwasów! H₂S jest szczególnie niebezpieczny, bo w większych stężeniach uszkadza zmysł węchu, przez co przestajemy go wyczuwać i możemy się zatruć.

Kwas siarkowy (IV) (H₂SO₃) powstaje przez reakcję dwutlenku siarki z wodą. Jest to bezbarwna ciecz o drażniącym zapachu, która łatwo ulega rozkładowi na SO₂ i wodę. Ma właściwości wybielające i słabo dysocjuje w roztworze.
Kwas siarkowy (IV) jest wykorzystywany głównie jako konserwant żywności (oznaczany jako E220) oraz w preparatach dezynfekcyjnych. Może jednak wywoływać reakcje alergiczne u osób wrażliwych na siarczyny.
Kwas siarkowy (VI) (H₂SO₄) to jeden z najważniejszych kwasów w przemyśle. Otrzymuje się go przez rozpuszczenie tritlenku siarki w wodzie. Jest to bezbarwna, oleista ciecz bez zapachu, która ma silne właściwości higroskopijne (pochłania wodę z otoczenia).
Ten kwas znajduje zastosowanie w produkcji nawozów sztucznych, akumulatorach samochodowych, przemyśle papierniczym i włókienniczym oraz w środkach czystości. Jest żrący i wymaga ostrożnego obchodzenia się z nim.
💡 Ciekawostka: Kwas siarkowy (VI) tak silnie pochłania wodę, że może nawet odciągać wodę z cukru, zwęglając go - dlatego nigdy nie należy go rozlewać!

Kwas azotowy (V) (HNO₃) otrzymujemy przez reakcję tlenku azotu (V) z wodą. Jest bezbarwną cieczą o charakterystycznym zapachu, która ma silne właściwości utleniające. To właśnie dzięki nim barwi białka na żółto (plama na skórze).
Zastosowanie kwasu azotowego jest bardzo szerokie - produkuje się z niego nawozy azotowe, materiały wybuchowe, rozpuszczalniki i barwniki. Wykorzystywany jest również w farmacji do produkcji leków na serce (nitrogliceryna).
Kwas fosforowy (V) (H₃PO₄) powstaje w reakcji tlenku fosforu (V) z wodą. W stanie stężonym ma postać stałą i wykazuje właściwości żrące. Dobrze rozpuszcza się w wodzie i ma zdolność do usuwania rdzy.
Ten kwas znajdziesz w napojach gazowanych typu cola, proszkach do prania, w stomatologii oraz jako składnik nawozów sztucznych. Dzięki właściwościom odrdzewiającym jest też składnikiem preparatów do usuwania rdzy.
⚡ Zapamiętaj: Kwas azotowy (V) jest jednym z najsilniejszych utleniaczy wśród kwasów, dlatego może reagować nawet z metalami szlachetnymi jak srebro!

Kwas węglowy (H₂CO₃) powstaje, gdy dwutlenek węgla rozpuszcza się w wodzie. Jest to bezbarwna ciecz o kwaśnym smaku, którą znasz z napojów gazowanych. Właśnie ten kwas nadaje im charakterystyczny musujący smak.
Kwas węglowy jest bardzo nietrwały i łatwo rozpada się z powrotem na dwutlenek węgla i wodę. Występuje naturalnie w wodach mineralnych i leczniczych. Gdy otwierasz butelkę napoju gazowanego, obserwujesz jak kwas węglowy rozpada się, uwalniając dwutlenek węgla w postaci bąbelków.
Dysocjacja jonowa to proces rozpadu cząsteczek na jony pod wpływem wody. Dla kwasów można ją zapisać ogólnym równaniem: H₃R ⇌ mH⁺ + R^m-, gdzie H to atom wodoru, R to reszta kwasowa, a m to liczba atomów wodoru równa wartościowości reszty kwasowej.
Ten proces decyduje o tym, czy roztwór ma odczyn kwaśny. Im więcej jonów H⁺ w roztworze, tym kwas jest mocniejszy i ma niższe pH.
🧪 Eksperyment domowy: Możesz zaobserwować działanie kwasu węglowego, wrzucając tabletkę musującą do wody - bąbelki to uwalniający się CO₂!

Dysocjacja jonowa to kluczowy proces zachodzący, gdy kwas rozpuszcza się w wodzie. Dzięki temu kwas może pełnić swoją funkcję chemiczną i wykazywać charakterystyczne właściwości.
Kwasy jednoprotonowe, jak kwas chlorowodorowy (HCl) czy kwas azotowy (HNO₃), dysocjują w jednym etapie, uwalniając jeden jon wodorowy: HCl ⇌ H⁺ + Cl⁻ HNO₃ ⇌ H⁺ + NO₃⁻
Kwasy wieloprotonowe dysocjują w kilku etapach. Na przykład kwas siarkowy (VI) (H₂SO₄) uwalnia dwa jony wodorowe: H₂SO₄ ⇌ 2H⁺ + SO₄²⁻, a kwas fosforowy (H₃PO₄) uwalnia aż trzy jony wodorowe: H₃PO₄ ⇌ 3H⁺ + PO₄³⁻.
Stopień dysocjacji kwasu określa jego moc - kwasy mocne (jak HCl, H₂SO₄) dysocjują prawie całkowicie, natomiast słabe (jak H₂S, H₂CO₃) dysocjują tylko częściowo.
💡 Wskazówka: Zapamiętaj, że liczba jonów H⁺ uwolnionych w dysocjacji odpowiada liczbie atomów wodoru w cząsteczce kwasu zdolnych do odłączenia się w postaci jonów.

Kwaśne opady to jedno z poważniejszych zagrożeń dla środowiska. Powstają, gdy zanieczyszczenia powietrza w postaci tlenków niemetali (głównie SO₂ i NOₓ) reagują z wodą w atmosferze, tworząc roztwory kwasów.
Kwaśne deszcze, śniegi i mgły mają niszczący wpływ na przyrodę i infrastrukturę. Powodują korozję budynków i zabytków, zakwaszają gleby i zbiorniki wodne, prowadząc do wymierania roślin i zwierząt. W zakwaszonej glebie rośliny mają problemy z fotosyntezą i pobieraniem składników odżywczych.
Do określania kwasowości roztworów używamy skali pH, która przyjmuje wartości od 1 do 14. Roztwory o pH poniżej 7 mają odczyn kwaśny (więcej jonów H⁺ niż OH⁻), pH równe 7 oznacza odczyn obojętny (równowaga jonów H⁺ i OH⁻), a pH powyżej 7 wskazuje na odczyn zasadowy (więcej jonów OH⁻ niż H⁺).
Do otrzymywania kwasów stosujemy dwie metody: dla kwasów beztlenowych - reakcja wodoru z niemetalem, a dla kwasów tlenowych - reakcja tlenku niemetalu z wodą.
🌧️ Pamiętaj: Naturalne opady deszczu mają pH około 5,6 (lekko kwaśne) ze względu na rozpuszczony CO₂, ale kwaśne deszcze mogą mieć pH nawet poniżej 4, co jest szkodliwe dla środowiska!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Nadia Jaouhari
@nadiajaouhari_bwpl
Kwasy to ważne związki chemiczne, które dyspocjują w wodzie na kationy wodorowe i aniony reszty kwasowej. Poznamy różne rodzaje kwasów, ich właściwości, otrzymywanie oraz zastosowanie w życiu codziennym i przemyśle.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwasy to substancje, które w wodzie dyspocjują na kationy wodorowe i aniony reszty kwasowej. Są zbudowane z atomów wodoru i reszty kwasowej, która nadaje im charakterystyczne właściwości.
Istnieje wiele różnych kwasów, które możemy podzielić na beztlenowe (np. HCl, H₂S) oraz tlenowe (np. H₂SO₄, HNO₃, H₂CO₃, H₃PO₄). W nazwie kwasu tlenowego wartościowość pierwiastka zaznaczamy cyfrą rzymską w nawiasie, np. siarkowy (VI).
Do rozpoznawania kwasów używamy wskaźników - substancji zmieniających barwę w zależności od środowiska. Najpopularniejsze wskaźniki to oranż metylowy (zmienia kolor z pomarańczowego na czerwony), papierek uniwersalny (z żółtego na czerwony), wywar z czerwonej kapusty czy nawet zwykła esencja herbaciana (z brązowej na żółtą).
💡 Ciekawostka: Wiele produktów spożywczych może służyć jako naturalne wskaźniki kwasowości - sok z czerwonej kapusty jest jednym z najlepszych domowych wskaźników!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas chlorowodorowy (HCl) to jeden z najpopularniejszych kwasów. Otrzymuje się go przez reakcję wodoru z chlorem, a następnie rozpuszczenie powstałego gazu w wodzie. Jest to bezbarwna ciecz o drażniącym zapachu, która doskonale przewodzi prąd elektryczny.
HCl ma wiele zastosowań - używamy go w przemyśle chemicznym jako odczynnik, w motoryzacji, przy produkcji tworzyw sztucznych i leków. W żołądku występuje jako składnik soku żołądkowego i pomaga w trawieniu pokarmów.
Kwas siarkowodorowy (H₂S) powstaje w reakcji wodoru z siarką, a następnie przez rozpuszczenie powstałego gazu w wodzie. Jego najbardziej charakterystyczną cechą jest zapach zgniłych jaj. Jest trujący, ale w małych stężeniach znajduje zastosowanie w produkcji siarki, kremach do depilacji oraz wodach leczniczych.
🧪 Uwaga! Nigdy nie wąchaj bezpośrednio kwasów! H₂S jest szczególnie niebezpieczny, bo w większych stężeniach uszkadza zmysł węchu, przez co przestajemy go wyczuwać i możemy się zatruć.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas siarkowy (IV) (H₂SO₃) powstaje przez reakcję dwutlenku siarki z wodą. Jest to bezbarwna ciecz o drażniącym zapachu, która łatwo ulega rozkładowi na SO₂ i wodę. Ma właściwości wybielające i słabo dysocjuje w roztworze.
Kwas siarkowy (IV) jest wykorzystywany głównie jako konserwant żywności (oznaczany jako E220) oraz w preparatach dezynfekcyjnych. Może jednak wywoływać reakcje alergiczne u osób wrażliwych na siarczyny.
Kwas siarkowy (VI) (H₂SO₄) to jeden z najważniejszych kwasów w przemyśle. Otrzymuje się go przez rozpuszczenie tritlenku siarki w wodzie. Jest to bezbarwna, oleista ciecz bez zapachu, która ma silne właściwości higroskopijne (pochłania wodę z otoczenia).
Ten kwas znajduje zastosowanie w produkcji nawozów sztucznych, akumulatorach samochodowych, przemyśle papierniczym i włókienniczym oraz w środkach czystości. Jest żrący i wymaga ostrożnego obchodzenia się z nim.
💡 Ciekawostka: Kwas siarkowy (VI) tak silnie pochłania wodę, że może nawet odciągać wodę z cukru, zwęglając go - dlatego nigdy nie należy go rozlewać!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas azotowy (V) (HNO₃) otrzymujemy przez reakcję tlenku azotu (V) z wodą. Jest bezbarwną cieczą o charakterystycznym zapachu, która ma silne właściwości utleniające. To właśnie dzięki nim barwi białka na żółto (plama na skórze).
Zastosowanie kwasu azotowego jest bardzo szerokie - produkuje się z niego nawozy azotowe, materiały wybuchowe, rozpuszczalniki i barwniki. Wykorzystywany jest również w farmacji do produkcji leków na serce (nitrogliceryna).
Kwas fosforowy (V) (H₃PO₄) powstaje w reakcji tlenku fosforu (V) z wodą. W stanie stężonym ma postać stałą i wykazuje właściwości żrące. Dobrze rozpuszcza się w wodzie i ma zdolność do usuwania rdzy.
Ten kwas znajdziesz w napojach gazowanych typu cola, proszkach do prania, w stomatologii oraz jako składnik nawozów sztucznych. Dzięki właściwościom odrdzewiającym jest też składnikiem preparatów do usuwania rdzy.
⚡ Zapamiętaj: Kwas azotowy (V) jest jednym z najsilniejszych utleniaczy wśród kwasów, dlatego może reagować nawet z metalami szlachetnymi jak srebro!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwas węglowy (H₂CO₃) powstaje, gdy dwutlenek węgla rozpuszcza się w wodzie. Jest to bezbarwna ciecz o kwaśnym smaku, którą znasz z napojów gazowanych. Właśnie ten kwas nadaje im charakterystyczny musujący smak.
Kwas węglowy jest bardzo nietrwały i łatwo rozpada się z powrotem na dwutlenek węgla i wodę. Występuje naturalnie w wodach mineralnych i leczniczych. Gdy otwierasz butelkę napoju gazowanego, obserwujesz jak kwas węglowy rozpada się, uwalniając dwutlenek węgla w postaci bąbelków.
Dysocjacja jonowa to proces rozpadu cząsteczek na jony pod wpływem wody. Dla kwasów można ją zapisać ogólnym równaniem: H₃R ⇌ mH⁺ + R^m-, gdzie H to atom wodoru, R to reszta kwasowa, a m to liczba atomów wodoru równa wartościowości reszty kwasowej.
Ten proces decyduje o tym, czy roztwór ma odczyn kwaśny. Im więcej jonów H⁺ w roztworze, tym kwas jest mocniejszy i ma niższe pH.
🧪 Eksperyment domowy: Możesz zaobserwować działanie kwasu węglowego, wrzucając tabletkę musującą do wody - bąbelki to uwalniający się CO₂!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dysocjacja jonowa to kluczowy proces zachodzący, gdy kwas rozpuszcza się w wodzie. Dzięki temu kwas może pełnić swoją funkcję chemiczną i wykazywać charakterystyczne właściwości.
Kwasy jednoprotonowe, jak kwas chlorowodorowy (HCl) czy kwas azotowy (HNO₃), dysocjują w jednym etapie, uwalniając jeden jon wodorowy: HCl ⇌ H⁺ + Cl⁻ HNO₃ ⇌ H⁺ + NO₃⁻
Kwasy wieloprotonowe dysocjują w kilku etapach. Na przykład kwas siarkowy (VI) (H₂SO₄) uwalnia dwa jony wodorowe: H₂SO₄ ⇌ 2H⁺ + SO₄²⁻, a kwas fosforowy (H₃PO₄) uwalnia aż trzy jony wodorowe: H₃PO₄ ⇌ 3H⁺ + PO₄³⁻.
Stopień dysocjacji kwasu określa jego moc - kwasy mocne (jak HCl, H₂SO₄) dysocjują prawie całkowicie, natomiast słabe (jak H₂S, H₂CO₃) dysocjują tylko częściowo.
💡 Wskazówka: Zapamiętaj, że liczba jonów H⁺ uwolnionych w dysocjacji odpowiada liczbie atomów wodoru w cząsteczce kwasu zdolnych do odłączenia się w postaci jonów.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kwaśne opady to jedno z poważniejszych zagrożeń dla środowiska. Powstają, gdy zanieczyszczenia powietrza w postaci tlenków niemetali (głównie SO₂ i NOₓ) reagują z wodą w atmosferze, tworząc roztwory kwasów.
Kwaśne deszcze, śniegi i mgły mają niszczący wpływ na przyrodę i infrastrukturę. Powodują korozję budynków i zabytków, zakwaszają gleby i zbiorniki wodne, prowadząc do wymierania roślin i zwierząt. W zakwaszonej glebie rośliny mają problemy z fotosyntezą i pobieraniem składników odżywczych.
Do określania kwasowości roztworów używamy skali pH, która przyjmuje wartości od 1 do 14. Roztwory o pH poniżej 7 mają odczyn kwaśny (więcej jonów H⁺ niż OH⁻), pH równe 7 oznacza odczyn obojętny (równowaga jonów H⁺ i OH⁻), a pH powyżej 7 wskazuje na odczyn zasadowy (więcej jonów OH⁻ niż H⁺).
Do otrzymywania kwasów stosujemy dwie metody: dla kwasów beztlenowych - reakcja wodoru z niemetalem, a dla kwasów tlenowych - reakcja tlenku niemetalu z wodą.
🌧️ Pamiętaj: Naturalne opady deszczu mają pH około 5,6 (lekko kwaśne) ze względu na rozpuszczony CO₂, ale kwaśne deszcze mogą mieć pH nawet poniżej 4, co jest szkodliwe dla środowiska!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
28
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
Zrozumienie kwasów tlenowych i beztlenowych, ich dysocjacji oraz wpływu na pH. Materiał obejmuje kluczowe informacje o kwasie siarkowym, azotowym i ich zastosowaniach w przemyśle oraz rolnictwie. Idealne dla studentów chemii.
Zgłębiaj temat kwasów beztlenowych, ich właściwości fizycznych i chemicznych oraz proces dysocjacji. Dowiedz się o kluczowych kwasach, takich jak HCl, HF, HBr, i ich zastosowaniach. Idealne dla studentów chemii, którzy chcą zrozumieć podstawowe zasady dotyczące kwasów i ich zachowań w reakcjach chemicznych.
Zbiór zadań z próbnej matury z chemii na poziomie rozszerzonym. Obejmuje zagadnienia takie jak: reakcje chemiczne, kinetyka, nazewnictwo związków organicznych i nieorganicznych, teoria kwasów i zasad, oraz funkcje kwasów. Idealne materiały do nauki i powtórek przed maturą.
Zrozumienie dysocjacji jonowej kwasów oraz ich nazewnictwa. Materiał omawia procesy elektrolityczne, różnice między kwasami tlenowymi a nietlenowymi oraz zasady ich nazywania. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Zrozumienie dysocjacji jonowej kwasów w roztworach wodnych. Ta notatka omawia mocne i słabe kwasy, ich kationy i aniony, oraz procesy dysocjacji. Idealna dla uczniów chemii, którzy chcą zgłębić temat kwasów i ich właściwości. Typ: podsumowanie.
Zrozumienie wskaźników pH i roztworów buforowych w chemii ogólnej. Notatki obejmują równania Hendersona-Hasselbalcha, zmiany barwy wskaźników oraz obliczenia pH roztworów. Idealne dla studentów biotechnologii i chemii.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS