Dysocjacja jonowa to kluczowy proces chemiczny, w którym substancje rozpuszczone... Pokaż więcej
Chemia roztworów wodnych - Notatka i zadania







Dysocjacja jonowa elektrolitów
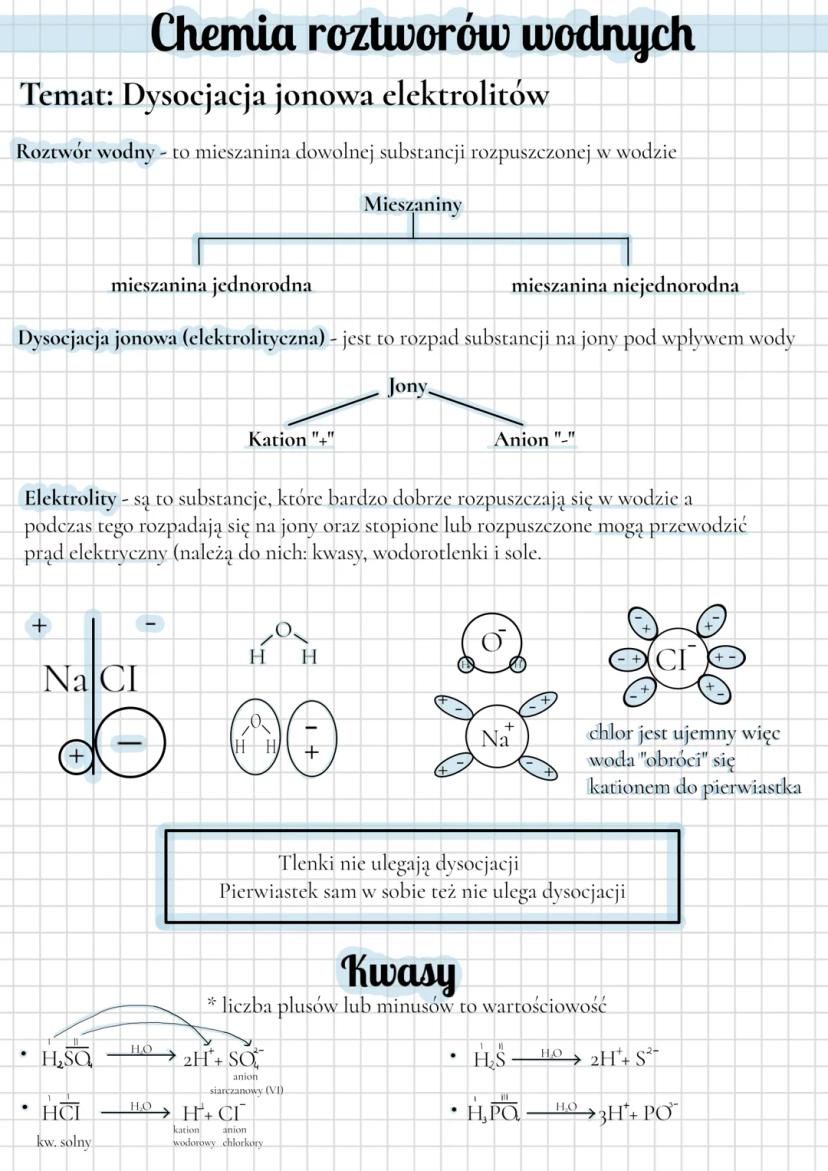
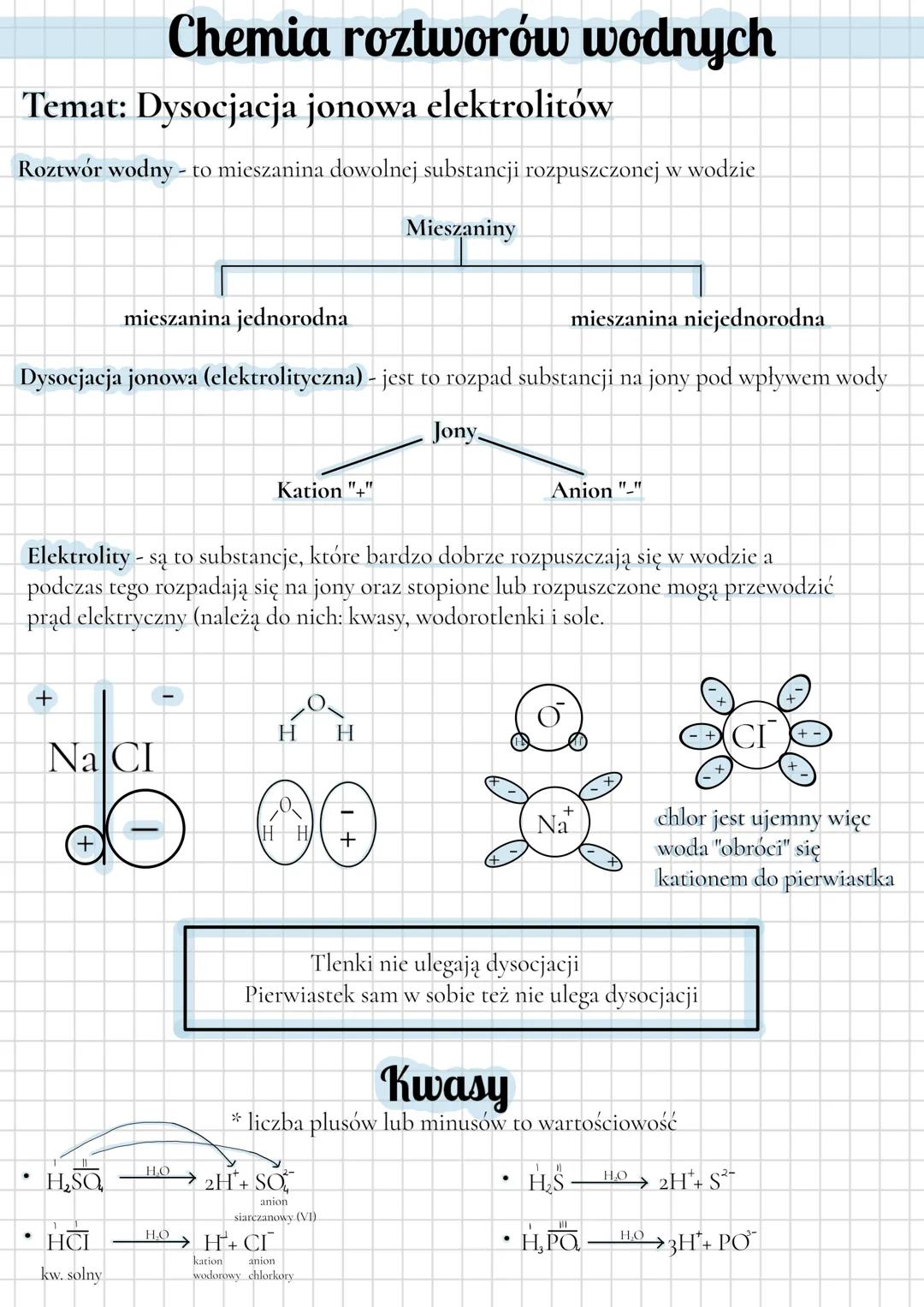
Dysocjacja jonowa to rozpad substancji na jony pod wpływem wody. Podczas tego procesu powstają kationy (jony dodatnie) i aniony (jony ujemne). Tylko niektóre substancje ulegają dysocjacji - nazywamy je elektrolitami.
Elektrolity to substancje, które dobrze rozpuszczają się w wodzie, rozpadając się na jony i mogą przewodzić prąd elektryczny. Do elektrolitów zaliczamy kwasy, wodorotlenki i sole. Pamiętaj, że tlenki i same pierwiastki nie ulegają dysocjacji!
Kiedy kwasy ulegają dysocjacji, zawsze tworzą kationy wodorowe H⁺. Na przykład:
- HCl → H⁺ + Cl⁻ (kwas solny)
- H₂SO₄ → 2H⁺ + SO₄²⁻ (kwas siarkowy)
- H₃PO₄ → 3H⁺ + PO₄³⁻ (kwas fosforowy)
Ciekawostka: Liczba plusów lub minusów przy jonach wskazuje na ich wartościowość, czyli ile ładunków elementarnych niesie dany jon. To ważna informacja przy zapisywaniu równań dysocjacji!

Dysocjacja wodorotlenków i soli
Wodorotlenki podczas dysocjacji zawsze tworzą aniony wodorotlenkowe OH⁻. Proces ten zapisujemy w formie równań, np.:
- KOH → K⁺ + OH⁻ (wodorotlenek potasu)
- Ca(OH)₂ → Ca²⁺ + 2OH⁻ (wodorotlenek wapnia)
- Fe(OH)₃ → Fe³⁺ + 3OH⁻ (wodorotlenek żelaza(III))
Sole to związki składające się z kationu metalu i anionu reszty kwasowej. Podczas dysocjacji rozpadają się na te jony, np.:
- NaCl → Na⁺ + Cl⁻ (chlorek sodu)
- BaCl₂ → Ba²⁺ + 2Cl⁻ (chlorek baru)
- K₂SO₄ → 2K⁺ + SO₄²⁻ (siarczan(VI) potasu)
Przy zapisywaniu równań dysocjacji pamiętaj o zachowaniu równowagi ładunków - suma ładunków po obu stronach równania musi być taka sama. Dzięki temu wiemy, ile jonów danego rodzaju powstaje.
Ważne: Aby prawidłowo zapisać równanie dysocjacji soli, musisz najpierw rozpoznać, z jakiego kwasu i z jakiego metalu powstała dana sól.

Dysocjacja stopniowa (etapowa)
Niektóre substancje ulegają dysocjacji stopniowej - oznacza to, że rozpad na jony zachodzi etapami. Dotyczy to głównie kwasów wieloprotonowych i wodorotlenków zawierających kilka grup OH.
W przypadku wodorotlenków proces przebiega etapowo, np. dla wodorotlenku glinu:
- Al(OH)₃ → OH⁻ + Al(OH)₂⁺
- Al(OH)₂⁺ → OH⁻ + AlOH²⁺
- AlOH²⁺ → OH⁻ + Al³⁺
Podobnie kwasy wieloprotonowe (zawierające dwa lub więcej atomów wodoru) dysocjują etapami:
- H₂CO₃ → H⁺ + HCO₃⁻, a następnie HCO₃⁻ → H⁺ + CO₃²⁻
- H₃PO₄ → H⁺ + H₂PO₄⁻ → H⁺ + HPO₄²⁻ → H⁺ + PO₄³⁻
Dysocjacja stopniowa jest ważna, ponieważ pozwala zrozumieć, dlaczego niektóre substancje mogą pełnić różne funkcje w zależności od tego, na jakim etapie dysocjacji się znajdują.
Spróbuj sam: Wybierz dowolny kwas wieloprotonowy i zapisz wszystkie etapy jego dysocjacji. Zwróć uwagę na zmianę ładunku anionu na każdym etapie!

Stopień dysocjacji jonowej
Nie wszystkie elektrolity dysocjują całkowicie. Elektrolit słaby to substancja, która tylko częściowo rozpada się na jony w roztworze wodnym. Właśnie dlatego wprowadzamy pojęcie stopnia dysocjacji.
Stopień dysocjacji (α) wyraża procent cząsteczek, które rozpadły się na jony. Obliczamy go ze wzoru:
α = (nz · 100%)/n0
gdzie:
- nz - liczba moli substancji zdysocjowanej
- n0 - liczba moli substancji wprowadzonej do roztworu
Stopień dysocjacji może przyjmować wartości od 0% do 100%. Im wyższy stopień dysocjacji, tym silniejszy elektrolit.
Znając stężenie molowe roztworu (C) i stopień dysocjacji, możemy obliczyć stężenie zdysocjowanych cząsteczek:
Cz = (α · C0)/100%
gdzie C0 to stężenie początkowe substancji.
Wskazówka: Przy rozwiązywaniu zadań pamiętaj, że stężenie początkowe to suma stężenia cząsteczek zdysocjowanych i niezdysocjowanych: C0 = Cz + CNz.

Zadania z obliczaniem stopnia dysocjacji
Rozwiązywanie zadań z dysocjacji jonowej wymaga systematycznego podejścia. Spójrz na przykłady:
-
Aby obliczyć stopień dysocjacji, gdy znamy stężenie zdysocjowane i początkowe:
α = (Cz · 100%)/C0Przykład: W roztworze o stężeniu 0,7 mol/dm³, stężenie zdysocjowane wynosi 0,2 mol/dm³: α = (0,2 · 100%)/0,7 = 28,57%
-
Gdy znamy liczbę moli substancji zdysocjowanej i początkowej:
α = (nz · 100%)/n0Przykład: Z 0,4 mola substancji zdysocjowało 0,05 mola: α = (0,05 · 100%)/0,4 = 12,5%
-
Aby obliczyć stężenie cząsteczek zdysocjowanych:
Cz = (α · C0)/100%Przykład: W roztworze o stężeniu 0,55 mol/dm³ i stopniu dysocjacji 5%: Cz = (5% · 0,55)/100% = 0,0275 mol/dm³
Pamiętaj: Stężenie cząsteczek niezdysocjowanych możesz obliczyć odejmując stężenie zdysocjowane od początkowego: CNz = C0 - Cz.
Sprawdź się: Oblicz stopień dysocjacji elektrolitu, jeśli w roztworze o stężeniu 0,3 mol/dm³ stężenie zdysocjowanych cząsteczek wynosi 0,09 mol/dm³.

Jony w roztworach i skala pH
W roztworach wodnych zawierających różne elektrolity trzeba pamiętać o bilansie ładunków - suma ładunków dodatnich musi równać się sumie ładunków ujemnych. Jest to kluczowe przy analizie składu jonowego mieszanin.
Skala pH pomaga określić odczyn roztworu. Wyróżniamy trzy podstawowe odczyny:
- Kwasowy: pH < 7, [H⁺] > [OH⁻]
- Obojętny: pH = 7, [H⁺] = [OH⁻]
- Zasadowy: pH > 7, [H⁺] < [OH⁻]
Odczyn możemy sprawdzić używając wskaźników, które zmieniają kolor w zależności od pH:
- Fenoloftaleina: bezbarwna w środowisku kwasowym i obojętnym, malinowa w zasadowym
- Oranż metylowy: czerwony w środowisku kwasowym, pomarańczowy w obojętnym, żółty w zasadowym
- Uniwersalny papierek wskaźnikowy: czerwony (kwasowy), pomarańczowy (obojętny), zielony/niebieski (zasadowy)
Do dokładnego pomiaru pH służy pehametr.
Ciekawostka: Skala pH jest skalą logarytmiczną - zmiana o 1 jednostkę oznacza 10-krotną zmianę stężenia jonów H⁺. Dlatego sok cytrynowy o pH 2 jest 100 razy bardziej kwasowy niż sok jabłkowy o pH 4!

Obliczanie pH roztworów
Wartość pH możemy obliczyć ze wzoru:
pH = -log[H⁺]
gdzie [H⁺] to stężenie jonów wodorowych w mol/dm³.
Podobnie dla jonów wodorotlenkowych mamy:
pOH = -log[OH⁻]
Pomiędzy pH i pOH istnieje zależność:
pH + pOH = 14
Przy obliczaniu pH roztworów kwasów mocnych pamiętaj, że:
- Dla kwasów jednoprotonowych: [H⁺] = stężenie kwasu
- Dla kwasów wieloprotonowych: [H⁺] = wartościowość kwasu × stężenie kwasu
Przykład: Dla roztworu HNO₃ o stężeniu 0,1 mol/dm³:
- [H⁺] = 0,1 mol/dm³
- pH = -log(0,1) = -log(10⁻¹) = 1
Dla zasad mocnych:
- [OH⁻] = stężenie zasady (dla zasad jednowodorotlenowych)
- [OH⁻] = liczba grup OH × stężenie zasady (dla zasad wielowodorotlenowych)
Następnie obliczamy pOH, a z niego pH.
Wskazówka: W obliczeniach często występują potęgi 10, np. 0,001 = 10⁻³. Używaj tej własności, aby uprościć liczenie logarytmów: -log(10⁻ᵏ) = k.

pH i reakcje jonowe
Przy obliczaniu pH roztworów wodorotlenków metali pamiętaj, że wodorotlenek rozpadając się daje tyle jonów OH⁻, ile grup wodorotlenkowych zawiera:
Przykład: Dla roztworu Ca(OH)₂ o stężeniu 0,00005 mol/dm³:
- [OH⁻] = 2 × 0,00005 = 0,0001 mol/dm³
- pOH = -log(0,0001) = 4
- pH = 14 - 4 = 10
Jedną z najważniejszych reakcji jonowych jest reakcja zobojętniania, w której kwas reaguje z zasadą, tworząc sól i wodę:
Kwas + Zasada → Sól + Woda
Odczyn roztworu po reakcji zależy od ilości reagentów:
- Jeśli ilości są równoważne, otrzymujemy roztwór obojętny (pH ≈ 7)
- Nadmiar kwasu daje odczyn kwasowy (pH < 7)
- Nadmiar zasady daje odczyn zasadowy (pH > 7)
W zapisie jonowym reakcji zobojętniania kluczowa jest reakcja:
H⁺ + OH⁻ → H₂O
Praktyczne zastosowanie: Reakcje zobojętniania są podstawą działania leków na zgagę, które neutralizują nadmiar kwasu w żołądku, oraz regulatorów pH w basenach czy akwariach.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Chemia kwasowo-zasadowa
9Wodorki i Wodorotlenki: Kluczowe Właściwości
Zgłębiaj właściwości, przygotowanie i reakcje wodorków oraz wodorotlenków. Dowiedz się o ich budowie, rozpuszczalności oraz zastosowaniach w chemii. Idealne dla uczniów i studentów chemii. Typ: Podsumowanie.
tlenki i wodorki
tlenki i wodorki, chemia, pierwsza liceum zakres podstawowy
Chemia Chromu: Właściwości i Reakcje
Zgłębiaj właściwości chemiczne chromu, jego stany utlenienia oraz reakcje w różnych środowiskach. Ta notatka zawiera szczegółowe obserwacje dotyczące kolorów związków chromu, ich zachowania w kwasach i zasadach oraz równania reakcji. Idealna dla studentów chemii na poziomie średnim i wyższym.
Skala pH i Odczyn Roztworu
Zrozumienie skali pH i odczynu roztworu jest kluczowe w chemii. Dowiedz się, jak pH wpływa na kwasowość i zasadowość roztworów oraz ich znaczenie w farmacji, ochronie środowiska, medycynie i rolnictwie. Materiał przeznaczony dla uczniów klasy 8.
Chemia Kwasy i Sole
Zrozumienie kwasów, wodorotlenków i soli w chemii nieorganicznej. Dowiedz się o ich strukturze, dysocjacji oraz zastosowaniach. Idealne dla uczniów przygotowujących się do egzaminów. Kluczowe pojęcia: kwasy, wodorotlenki, sole, dysocjacja, zastosowania.
pH Roztworu i Teoria Kwasów
Zrozumienie pH roztworu oraz klasyfikacja odczynów: kwasowy, obojętny i zasadowy. Dowiedz się o dysocjacji kwasów i zasad, ich stężeniu oraz wpływie na pH. Idealne dla studentów chemii. Typ: podsumowanie.
Chemia: Kwasy i Zasady
Zrozumienie kwasów, zasad i soli w kontekście chemii ogólnej. Notatki obejmują nazewnictwo kwasów, funkcje kwasów i zasad, a także reakcje z wodorotlenkami sodu i potasu. Idealne dla studentów biotechnologii oraz osób przygotowujących się do egzaminów z chemii.
Denaturacja i Wysalanie Białek
Zgłębiaj kluczowe procesy związane z białkami, takie jak denaturacja, wysalanie oraz reakcje biuretowa i ksantoproteinowa. Dowiedz się, jak czynniki chemiczne wpływają na strukturę białek i jak wykrywać ich obecność. Idealne dla studentów biologii i chemii.
Chemia Dział 1 kwasy klasa 8
Chemia dział 1
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Chemia roztworów wodnych - Notatka i zadania
Dysocjacja jonowa to kluczowy proces chemiczny, w którym substancje rozpuszczone w wodzie rozpadają się na jony. Ten proces jest podstawą dla zrozumienia działania kwasów, zasad i soli w roztworach wodnych. Poznanie mechanizmów dysocjacji pomaga zrozumieć odczyn pH oraz reakcje jonowe... Pokaż więcej

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Dysocjacja jonowa elektrolitów
Dysocjacja jonowa to rozpad substancji na jony pod wpływem wody. Podczas tego procesu powstają kationy (jony dodatnie) i aniony (jony ujemne). Tylko niektóre substancje ulegają dysocjacji - nazywamy je elektrolitami.
Elektrolity to substancje, które dobrze rozpuszczają się w wodzie, rozpadając się na jony i mogą przewodzić prąd elektryczny. Do elektrolitów zaliczamy kwasy, wodorotlenki i sole. Pamiętaj, że tlenki i same pierwiastki nie ulegają dysocjacji!
Kiedy kwasy ulegają dysocjacji, zawsze tworzą kationy wodorowe H⁺. Na przykład:
- HCl → H⁺ + Cl⁻ (kwas solny)
- H₂SO₄ → 2H⁺ + SO₄²⁻ (kwas siarkowy)
- H₃PO₄ → 3H⁺ + PO₄³⁻ (kwas fosforowy)
Ciekawostka: Liczba plusów lub minusów przy jonach wskazuje na ich wartościowość, czyli ile ładunków elementarnych niesie dany jon. To ważna informacja przy zapisywaniu równań dysocjacji!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Dysocjacja wodorotlenków i soli
Wodorotlenki podczas dysocjacji zawsze tworzą aniony wodorotlenkowe OH⁻. Proces ten zapisujemy w formie równań, np.:
- KOH → K⁺ + OH⁻ (wodorotlenek potasu)
- Ca(OH)₂ → Ca²⁺ + 2OH⁻ (wodorotlenek wapnia)
- Fe(OH)₃ → Fe³⁺ + 3OH⁻ (wodorotlenek żelaza(III))
Sole to związki składające się z kationu metalu i anionu reszty kwasowej. Podczas dysocjacji rozpadają się na te jony, np.:
- NaCl → Na⁺ + Cl⁻ (chlorek sodu)
- BaCl₂ → Ba²⁺ + 2Cl⁻ (chlorek baru)
- K₂SO₄ → 2K⁺ + SO₄²⁻ (siarczan(VI) potasu)
Przy zapisywaniu równań dysocjacji pamiętaj o zachowaniu równowagi ładunków - suma ładunków po obu stronach równania musi być taka sama. Dzięki temu wiemy, ile jonów danego rodzaju powstaje.
Ważne: Aby prawidłowo zapisać równanie dysocjacji soli, musisz najpierw rozpoznać, z jakiego kwasu i z jakiego metalu powstała dana sól.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Dysocjacja stopniowa (etapowa)
Niektóre substancje ulegają dysocjacji stopniowej - oznacza to, że rozpad na jony zachodzi etapami. Dotyczy to głównie kwasów wieloprotonowych i wodorotlenków zawierających kilka grup OH.
W przypadku wodorotlenków proces przebiega etapowo, np. dla wodorotlenku glinu:
- Al(OH)₃ → OH⁻ + Al(OH)₂⁺
- Al(OH)₂⁺ → OH⁻ + AlOH²⁺
- AlOH²⁺ → OH⁻ + Al³⁺
Podobnie kwasy wieloprotonowe (zawierające dwa lub więcej atomów wodoru) dysocjują etapami:
- H₂CO₃ → H⁺ + HCO₃⁻, a następnie HCO₃⁻ → H⁺ + CO₃²⁻
- H₃PO₄ → H⁺ + H₂PO₄⁻ → H⁺ + HPO₄²⁻ → H⁺ + PO₄³⁻
Dysocjacja stopniowa jest ważna, ponieważ pozwala zrozumieć, dlaczego niektóre substancje mogą pełnić różne funkcje w zależności od tego, na jakim etapie dysocjacji się znajdują.
Spróbuj sam: Wybierz dowolny kwas wieloprotonowy i zapisz wszystkie etapy jego dysocjacji. Zwróć uwagę na zmianę ładunku anionu na każdym etapie!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Stopień dysocjacji jonowej
Nie wszystkie elektrolity dysocjują całkowicie. Elektrolit słaby to substancja, która tylko częściowo rozpada się na jony w roztworze wodnym. Właśnie dlatego wprowadzamy pojęcie stopnia dysocjacji.
Stopień dysocjacji (α) wyraża procent cząsteczek, które rozpadły się na jony. Obliczamy go ze wzoru:
α = (nz · 100%)/n0
gdzie:
- nz - liczba moli substancji zdysocjowanej
- n0 - liczba moli substancji wprowadzonej do roztworu
Stopień dysocjacji może przyjmować wartości od 0% do 100%. Im wyższy stopień dysocjacji, tym silniejszy elektrolit.
Znając stężenie molowe roztworu (C) i stopień dysocjacji, możemy obliczyć stężenie zdysocjowanych cząsteczek:
Cz = (α · C0)/100%
gdzie C0 to stężenie początkowe substancji.
Wskazówka: Przy rozwiązywaniu zadań pamiętaj, że stężenie początkowe to suma stężenia cząsteczek zdysocjowanych i niezdysocjowanych: C0 = Cz + CNz.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zadania z obliczaniem stopnia dysocjacji
Rozwiązywanie zadań z dysocjacji jonowej wymaga systematycznego podejścia. Spójrz na przykłady:
-
Aby obliczyć stopień dysocjacji, gdy znamy stężenie zdysocjowane i początkowe:
α = (Cz · 100%)/C0Przykład: W roztworze o stężeniu 0,7 mol/dm³, stężenie zdysocjowane wynosi 0,2 mol/dm³: α = (0,2 · 100%)/0,7 = 28,57%
-
Gdy znamy liczbę moli substancji zdysocjowanej i początkowej:
α = (nz · 100%)/n0Przykład: Z 0,4 mola substancji zdysocjowało 0,05 mola: α = (0,05 · 100%)/0,4 = 12,5%
-
Aby obliczyć stężenie cząsteczek zdysocjowanych:
Cz = (α · C0)/100%Przykład: W roztworze o stężeniu 0,55 mol/dm³ i stopniu dysocjacji 5%: Cz = (5% · 0,55)/100% = 0,0275 mol/dm³
Pamiętaj: Stężenie cząsteczek niezdysocjowanych możesz obliczyć odejmując stężenie zdysocjowane od początkowego: CNz = C0 - Cz.
Sprawdź się: Oblicz stopień dysocjacji elektrolitu, jeśli w roztworze o stężeniu 0,3 mol/dm³ stężenie zdysocjowanych cząsteczek wynosi 0,09 mol/dm³.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Jony w roztworach i skala pH
W roztworach wodnych zawierających różne elektrolity trzeba pamiętać o bilansie ładunków - suma ładunków dodatnich musi równać się sumie ładunków ujemnych. Jest to kluczowe przy analizie składu jonowego mieszanin.
Skala pH pomaga określić odczyn roztworu. Wyróżniamy trzy podstawowe odczyny:
- Kwasowy: pH < 7, [H⁺] > [OH⁻]
- Obojętny: pH = 7, [H⁺] = [OH⁻]
- Zasadowy: pH > 7, [H⁺] < [OH⁻]
Odczyn możemy sprawdzić używając wskaźników, które zmieniają kolor w zależności od pH:
- Fenoloftaleina: bezbarwna w środowisku kwasowym i obojętnym, malinowa w zasadowym
- Oranż metylowy: czerwony w środowisku kwasowym, pomarańczowy w obojętnym, żółty w zasadowym
- Uniwersalny papierek wskaźnikowy: czerwony (kwasowy), pomarańczowy (obojętny), zielony/niebieski (zasadowy)
Do dokładnego pomiaru pH służy pehametr.
Ciekawostka: Skala pH jest skalą logarytmiczną - zmiana o 1 jednostkę oznacza 10-krotną zmianę stężenia jonów H⁺. Dlatego sok cytrynowy o pH 2 jest 100 razy bardziej kwasowy niż sok jabłkowy o pH 4!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczanie pH roztworów
Wartość pH możemy obliczyć ze wzoru:
pH = -log[H⁺]
gdzie [H⁺] to stężenie jonów wodorowych w mol/dm³.
Podobnie dla jonów wodorotlenkowych mamy:
pOH = -log[OH⁻]
Pomiędzy pH i pOH istnieje zależność:
pH + pOH = 14
Przy obliczaniu pH roztworów kwasów mocnych pamiętaj, że:
- Dla kwasów jednoprotonowych: [H⁺] = stężenie kwasu
- Dla kwasów wieloprotonowych: [H⁺] = wartościowość kwasu × stężenie kwasu
Przykład: Dla roztworu HNO₃ o stężeniu 0,1 mol/dm³:
- [H⁺] = 0,1 mol/dm³
- pH = -log(0,1) = -log(10⁻¹) = 1
Dla zasad mocnych:
- [OH⁻] = stężenie zasady (dla zasad jednowodorotlenowych)
- [OH⁻] = liczba grup OH × stężenie zasady (dla zasad wielowodorotlenowych)
Następnie obliczamy pOH, a z niego pH.
Wskazówka: W obliczeniach często występują potęgi 10, np. 0,001 = 10⁻³. Używaj tej własności, aby uprościć liczenie logarytmów: -log(10⁻ᵏ) = k.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
pH i reakcje jonowe
Przy obliczaniu pH roztworów wodorotlenków metali pamiętaj, że wodorotlenek rozpadając się daje tyle jonów OH⁻, ile grup wodorotlenkowych zawiera:
Przykład: Dla roztworu Ca(OH)₂ o stężeniu 0,00005 mol/dm³:
- [OH⁻] = 2 × 0,00005 = 0,0001 mol/dm³
- pOH = -log(0,0001) = 4
- pH = 14 - 4 = 10
Jedną z najważniejszych reakcji jonowych jest reakcja zobojętniania, w której kwas reaguje z zasadą, tworząc sól i wodę:
Kwas + Zasada → Sól + Woda
Odczyn roztworu po reakcji zależy od ilości reagentów:
- Jeśli ilości są równoważne, otrzymujemy roztwór obojętny (pH ≈ 7)
- Nadmiar kwasu daje odczyn kwasowy (pH < 7)
- Nadmiar zasady daje odczyn zasadowy (pH > 7)
W zapisie jonowym reakcji zobojętniania kluczowa jest reakcja:
H⁺ + OH⁻ → H₂O
Praktyczne zastosowanie: Reakcje zobojętniania są podstawą działania leków na zgagę, które neutralizują nadmiar kwasu w żołądku, oraz regulatorów pH w basenach czy akwariach.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Chemia kwasowo-zasadowa
9Wodorki i Wodorotlenki: Kluczowe Właściwości
Zgłębiaj właściwości, przygotowanie i reakcje wodorków oraz wodorotlenków. Dowiedz się o ich budowie, rozpuszczalności oraz zastosowaniach w chemii. Idealne dla uczniów i studentów chemii. Typ: Podsumowanie.
tlenki i wodorki
tlenki i wodorki, chemia, pierwsza liceum zakres podstawowy
Chemia Chromu: Właściwości i Reakcje
Zgłębiaj właściwości chemiczne chromu, jego stany utlenienia oraz reakcje w różnych środowiskach. Ta notatka zawiera szczegółowe obserwacje dotyczące kolorów związków chromu, ich zachowania w kwasach i zasadach oraz równania reakcji. Idealna dla studentów chemii na poziomie średnim i wyższym.
Skala pH i Odczyn Roztworu
Zrozumienie skali pH i odczynu roztworu jest kluczowe w chemii. Dowiedz się, jak pH wpływa na kwasowość i zasadowość roztworów oraz ich znaczenie w farmacji, ochronie środowiska, medycynie i rolnictwie. Materiał przeznaczony dla uczniów klasy 8.
Chemia Kwasy i Sole
Zrozumienie kwasów, wodorotlenków i soli w chemii nieorganicznej. Dowiedz się o ich strukturze, dysocjacji oraz zastosowaniach. Idealne dla uczniów przygotowujących się do egzaminów. Kluczowe pojęcia: kwasy, wodorotlenki, sole, dysocjacja, zastosowania.
pH Roztworu i Teoria Kwasów
Zrozumienie pH roztworu oraz klasyfikacja odczynów: kwasowy, obojętny i zasadowy. Dowiedz się o dysocjacji kwasów i zasad, ich stężeniu oraz wpływie na pH. Idealne dla studentów chemii. Typ: podsumowanie.
Chemia: Kwasy i Zasady
Zrozumienie kwasów, zasad i soli w kontekście chemii ogólnej. Notatki obejmują nazewnictwo kwasów, funkcje kwasów i zasad, a także reakcje z wodorotlenkami sodu i potasu. Idealne dla studentów biotechnologii oraz osób przygotowujących się do egzaminów z chemii.
Denaturacja i Wysalanie Białek
Zgłębiaj kluczowe procesy związane z białkami, takie jak denaturacja, wysalanie oraz reakcje biuretowa i ksantoproteinowa. Dowiedz się, jak czynniki chemiczne wpływają na strukturę białek i jak wykrywać ich obecność. Idealne dla studentów biologii i chemii.
Chemia Dział 1 kwasy klasa 8
Chemia dział 1
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Reakcje i Właściwości Soli
Zgłębiaj temat soli w chemii! Dowiedz się o reakcjach tlenków metali z kwasami, dysocjacji jonowej, oraz właściwościach i zastosowaniach soli. Obejmuje przykłady reakcji, nazewnictwo soli oraz ich zastosowania w codziennym życiu. Idealne dla uczniów i studentów chemii.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Wesele: Analiza Społeczeństwa
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego, który ukazuje podziały między inteligencją a chłopstwem w Polsce na początku XX wieku. Odkryj symbole, narodowe mity oraz kluczowe rozmowy, które ilustrują społeczne napięcia i brak zrozumienia. Idealne dla studentów literatury i kultury polskiej.
Mity Narodowe w 'Weselu'
Analiza symboliki i mitów narodowych w dramacie Stanisława Wyspiańskiego 'Wesele'. Odkryj, jak postacie i symbole odzwierciedlają społeczne napięcia i dążenia Polaków na początku XX wieku. Materiał zawiera omówienie głównych tematów, realistycznych bohaterów oraz kontekstu historycznego. Idealne dla studentów literatury i kultury polskiej.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.