Elektroliza to proces rozkładu substancji pod wpływem prądu elektrycznego -... Pokaż więcej
Podstawy Elektrolizy: Zasady, Zadania i Zastosowania





Elektroliza - podstawy i rodzaje
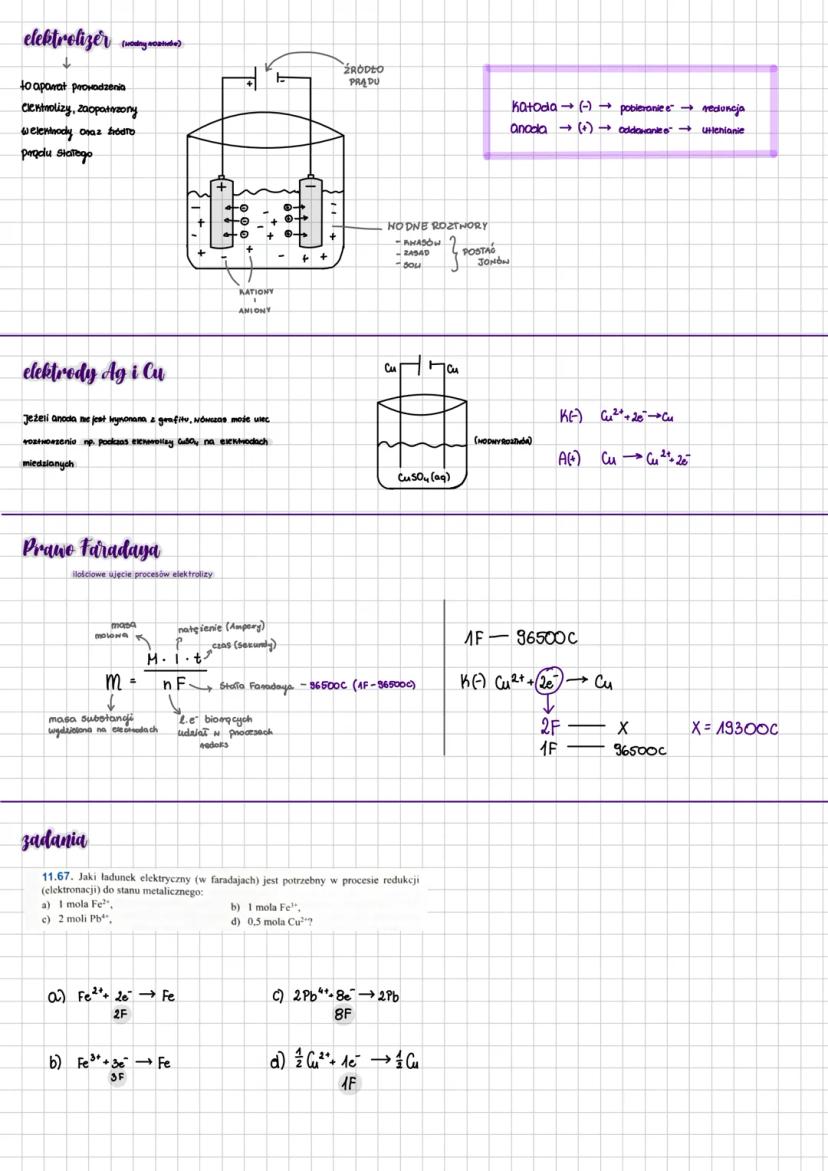
Elektroliza to wymuszony rozkład substancji pod wpływem pola elektrycznego. Proces zachodzi w specjalnym urządzeniu zwanym elektrolizerem, gdzie katoda (elektroda ujemna) pobiera elektrony, a anoda (elektroda dodatnia) je oddaje.
Wyróżniamy dwa główne typy elektrolizy. Elektroliza wodnych roztworów dotyczy substancji rozpuszczonych w wodzie - tu mamy różne scenariusze w zależności od rodzaju związku. Elektroliza substancji stopionych zachodzi przy wysokich temperaturach, gdy substancja jest w stanie płynnym.
W przypadku roztworów wodnych wszystko zależy od tego, z czym mamy do czynienia. Kwasy beztlenowe (jak HCl) zachowują się inaczej niż tlenowe (jak HNO₃), a sole różnych metali dają różne produkty na elektrodach.
Zapamiętaj: Na katodzie zawsze zachodzi redukcja (pobieranie elektronów), na anodzie utlenianie (oddawanie elektronów).

Elektrolizer i prawo Faradaya
Elektrolizer to aparat do prowadzenia elektrolizy, wyposażony w elektrody i źródło prądu stałego. Gdy elektrody są wykonane z miedzi czy srebra, mogą same uczestniczyć w reakcji i ulegać roztworzeniu.
Prawo Faradaya pozwala obliczyć dokładnie, ile substancji powstanie podczas elektrolizy. Kluczowy wzór to: m = (M × I × t)/(n × F), gdzie M to masa molowa, I to natężenie prądu, t to czas, n to liczba elektronów, a F to stała Faradaya (96500 C).
Stała Faradaya wynosi 96500 kulombów i określa ładunek potrzebny do przeniesienia 1 mola elektronów. To podstawa wszystkich obliczeń elektrochemicznych.
Wskazówka: Zawsze sprawdź, ile elektronów bierze udział w reakcji - to kluczowe dla poprawnych obliczeń!

Obliczenia - objętości gazów
Podczas elektrolizy często powstają gazy na elektrodach - wodór, tlen, chlor. Musisz umieć obliczyć ich objętości, korzystając z proporcji stechiometrycznych.
Przykład z elektrolizy wody: 2H₂O → 2H₂ + O₂. Jeśli na katodzie powstało 10 cm³ wodoru, to na anodzie powstanie 5 cm³ tlenu - proporcja 2:1. Stechiometria reakcji zawsze podpowiada, ile którego produktu powstanie.
Przy obliczeniach pamiętaj o warunkach normalnych (0°C, 1013 hPa). 1 mol gazu zajmuje 22,4 dm³ w tych warunkach. To podstawa do przeliczania między masą, liczbą moli i objętością.
Praktyczna rada: Zawsze zapisz równanie reakcji - to połowa sukcesu w rozwiązywaniu zadań!

Obliczenia - masa i czas elektrolizy
Wzór Faradaya pozwala obliczyć masę wydzielonej substancji, czas elektrolizy lub potrzebne natężenie prądu. Kluczowe jest określenie, ile elektronów bierze udział w procesie.
Dla reakcji Cu²⁺ + 2e⁻ → Cu potrzebujesz 2 elektronów na atom miedzi. Jeśli przepływa prąd 1A przez 1 godzinę, możesz obliczyć dokładnie, ile miedzi się wydzieli używając wzoru m = (M × I × t)/(n × F).
Pamiętaj o przeliczeniach jednostek: czas podawaj w sekundach, natężenie w amperach. Ładunek elektryczny to iloczyn natężenia i czasu .
Ważne: Sprawdź zawsze jednostki - to najczęstszy błąd w obliczeniach elektrochemicznych!

Zadania z gazami i atomami
Przy obliczaniu objętości gazów w elektrolizie używaj równania Clapeyrona: PV = nRT. Pozwala przeliczyć objętość gazu przy różnych warunkach temperatury i ciśnienia.
Elektroliza wody zawsze daje mieszaninę wodoru i tlenu w stosunku 2:1 objętościowo. Jeśli zmierzysz całkowitą objętość, możesz wyliczyć objętość każdego gazu osobno.
Liczba atomów wydzielonych na elektrodzie zależy od liczby moli i liczby Avogadro (6,02×10²³). Pamiętaj, że różne jony potrzebują różnej liczby elektronów do redukcji.
Ciekawostka: Przez przepuszczenie 1F (96500 C) możesz wydzielić 6,02×10²³ atomów jednowartościowego metalu!

Zadania wieloetapowe i mieszaniny
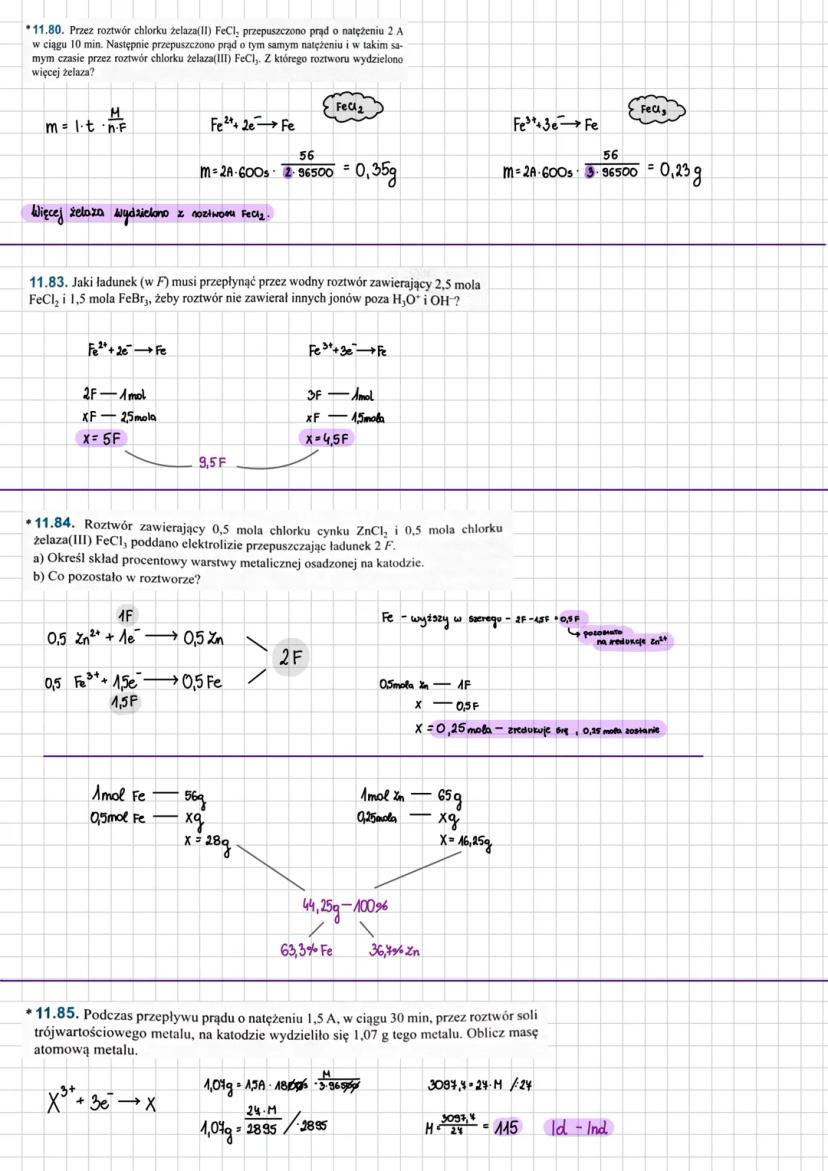
W mieszaninach soli różnych metali kolejność wydzielania zależy od szeregu aktywności. Metale szlachetniejsze (jak srebro) wydzielają się przed mniej szlachetnymi (jak cynkiem).
Obliczenia składu procentowego warstwy metalicznej wymagają znajomości mas poszczególnych metali i ich sum. Użyj wzoru Faradaya dla każdego metalu osobno.
Gdy ładunek jest ograniczony, nie wszystkie jony się zredukują. Musisz sprawdzić, który metal się wydzieli pierwszy i ile ładunku zostanie na pozostałe reakcje.
Strategia: W zadaniach z mieszaninami zawsze określ kolejność procesów i podziel obliczenia na etapy!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Prawo Faradaya elektrolizy
1Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Podstawy Elektrolizy: Zasady, Zadania i Zastosowania
Elektroliza to proces rozkładu substancji pod wpływem prądu elektrycznego - brzmi skomplikowanie, ale to naprawdę przydatna wiedza! Dowiesz się, jak działa ten proces w roztworach wodnych i stopionych substancjach, oraz nauczysz się obliczać, ile substancji powstanie podczas elektrolizy.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Elektroliza - podstawy i rodzaje
Elektroliza to wymuszony rozkład substancji pod wpływem pola elektrycznego. Proces zachodzi w specjalnym urządzeniu zwanym elektrolizerem, gdzie katoda (elektroda ujemna) pobiera elektrony, a anoda (elektroda dodatnia) je oddaje.
Wyróżniamy dwa główne typy elektrolizy. Elektroliza wodnych roztworów dotyczy substancji rozpuszczonych w wodzie - tu mamy różne scenariusze w zależności od rodzaju związku. Elektroliza substancji stopionych zachodzi przy wysokich temperaturach, gdy substancja jest w stanie płynnym.
W przypadku roztworów wodnych wszystko zależy od tego, z czym mamy do czynienia. Kwasy beztlenowe (jak HCl) zachowują się inaczej niż tlenowe (jak HNO₃), a sole różnych metali dają różne produkty na elektrodach.
Zapamiętaj: Na katodzie zawsze zachodzi redukcja (pobieranie elektronów), na anodzie utlenianie (oddawanie elektronów).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Elektrolizer i prawo Faradaya
Elektrolizer to aparat do prowadzenia elektrolizy, wyposażony w elektrody i źródło prądu stałego. Gdy elektrody są wykonane z miedzi czy srebra, mogą same uczestniczyć w reakcji i ulegać roztworzeniu.
Prawo Faradaya pozwala obliczyć dokładnie, ile substancji powstanie podczas elektrolizy. Kluczowy wzór to: m = (M × I × t)/(n × F), gdzie M to masa molowa, I to natężenie prądu, t to czas, n to liczba elektronów, a F to stała Faradaya (96500 C).
Stała Faradaya wynosi 96500 kulombów i określa ładunek potrzebny do przeniesienia 1 mola elektronów. To podstawa wszystkich obliczeń elektrochemicznych.
Wskazówka: Zawsze sprawdź, ile elektronów bierze udział w reakcji - to kluczowe dla poprawnych obliczeń!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczenia - objętości gazów
Podczas elektrolizy często powstają gazy na elektrodach - wodór, tlen, chlor. Musisz umieć obliczyć ich objętości, korzystając z proporcji stechiometrycznych.
Przykład z elektrolizy wody: 2H₂O → 2H₂ + O₂. Jeśli na katodzie powstało 10 cm³ wodoru, to na anodzie powstanie 5 cm³ tlenu - proporcja 2:1. Stechiometria reakcji zawsze podpowiada, ile którego produktu powstanie.
Przy obliczeniach pamiętaj o warunkach normalnych (0°C, 1013 hPa). 1 mol gazu zajmuje 22,4 dm³ w tych warunkach. To podstawa do przeliczania między masą, liczbą moli i objętością.
Praktyczna rada: Zawsze zapisz równanie reakcji - to połowa sukcesu w rozwiązywaniu zadań!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Obliczenia - masa i czas elektrolizy
Wzór Faradaya pozwala obliczyć masę wydzielonej substancji, czas elektrolizy lub potrzebne natężenie prądu. Kluczowe jest określenie, ile elektronów bierze udział w procesie.
Dla reakcji Cu²⁺ + 2e⁻ → Cu potrzebujesz 2 elektronów na atom miedzi. Jeśli przepływa prąd 1A przez 1 godzinę, możesz obliczyć dokładnie, ile miedzi się wydzieli używając wzoru m = (M × I × t)/(n × F).
Pamiętaj o przeliczeniach jednostek: czas podawaj w sekundach, natężenie w amperach. Ładunek elektryczny to iloczyn natężenia i czasu .
Ważne: Sprawdź zawsze jednostki - to najczęstszy błąd w obliczeniach elektrochemicznych!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zadania z gazami i atomami
Przy obliczaniu objętości gazów w elektrolizie używaj równania Clapeyrona: PV = nRT. Pozwala przeliczyć objętość gazu przy różnych warunkach temperatury i ciśnienia.
Elektroliza wody zawsze daje mieszaninę wodoru i tlenu w stosunku 2:1 objętościowo. Jeśli zmierzysz całkowitą objętość, możesz wyliczyć objętość każdego gazu osobno.
Liczba atomów wydzielonych na elektrodzie zależy od liczby moli i liczby Avogadro (6,02×10²³). Pamiętaj, że różne jony potrzebują różnej liczby elektronów do redukcji.
Ciekawostka: Przez przepuszczenie 1F (96500 C) możesz wydzielić 6,02×10²³ atomów jednowartościowego metalu!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Zadania wieloetapowe i mieszaniny
W mieszaninach soli różnych metali kolejność wydzielania zależy od szeregu aktywności. Metale szlachetniejsze (jak srebro) wydzielają się przed mniej szlachetnymi (jak cynkiem).
Obliczenia składu procentowego warstwy metalicznej wymagają znajomości mas poszczególnych metali i ich sum. Użyj wzoru Faradaya dla każdego metalu osobno.
Gdy ładunek jest ograniczony, nie wszystkie jony się zredukują. Musisz sprawdzić, który metal się wydzieli pierwszy i ile ładunku zostanie na pozostałe reakcje.
Strategia: W zadaniach z mieszaninami zawsze określ kolejność procesów i podziel obliczenia na etapy!
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: Prawo Faradaya elektrolizy
1Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.