Wodorotlenki to ważne związki chemiczne składające się z metalu i... Pokaż więcej
Wodorotlenki: Nauka nazw, właściwości i procesów chemicznych



Nazewnictwo i tworzenie wzorów wodorotlenków
Nazywanie wodorotlenków jest dość proste - zaczynamy od słowa "wodorotlenek" a następnie dodajemy nazwę metalu. Na przykład KOH to wodorotlenek potasu, a NaOH to wodorotlenek sodu. Gdy metal tworzy kilka różnych stopni utlenienia, musimy to zaznaczyć w nazwie, np. Cu(OH)₂ to wodorotlenek miedzi(II).
Tworzenie wzorów jest podobnie nieskomplikowane - najpierw zapisujemy symbol metalu, a następnie grupę OH z odpowiednim indeksem dolnym. Przykłady to Ca(OH)₂ (wodorotlenek wapnia) czy Fe(OH)₃ (wodorotlenek żelaza(III)).
Wodorotlenki ulegają dysocjacji elektrolitycznej w wodzie, która może być całkowita lub stopniowa. Przy dysocjacji całkowitej wodorotlenek rozpada się całkowicie na jony, np. NaOH ⇄ Na⁺ + OH⁻. Natomiast dysocjacja stopniowa zachodzi etapami, np. Al(OH)₃ najpierw tworzy Al(OH)₂⁺ i OH⁻, potem AlOH²⁺ i kolejny OH⁻, a na końcu Al³⁺ i trzeci OH⁻.
💡 Zapamiętaj! Wodorotlenki metali grupy I i II (z wyjątkiem berylu) dysocjują całkowicie, co sprawia, że są mocnymi zasadami, a ich roztwory dobrze przewodzą prąd elektryczny.
Otrzymywanie i właściwości wodorotlenków
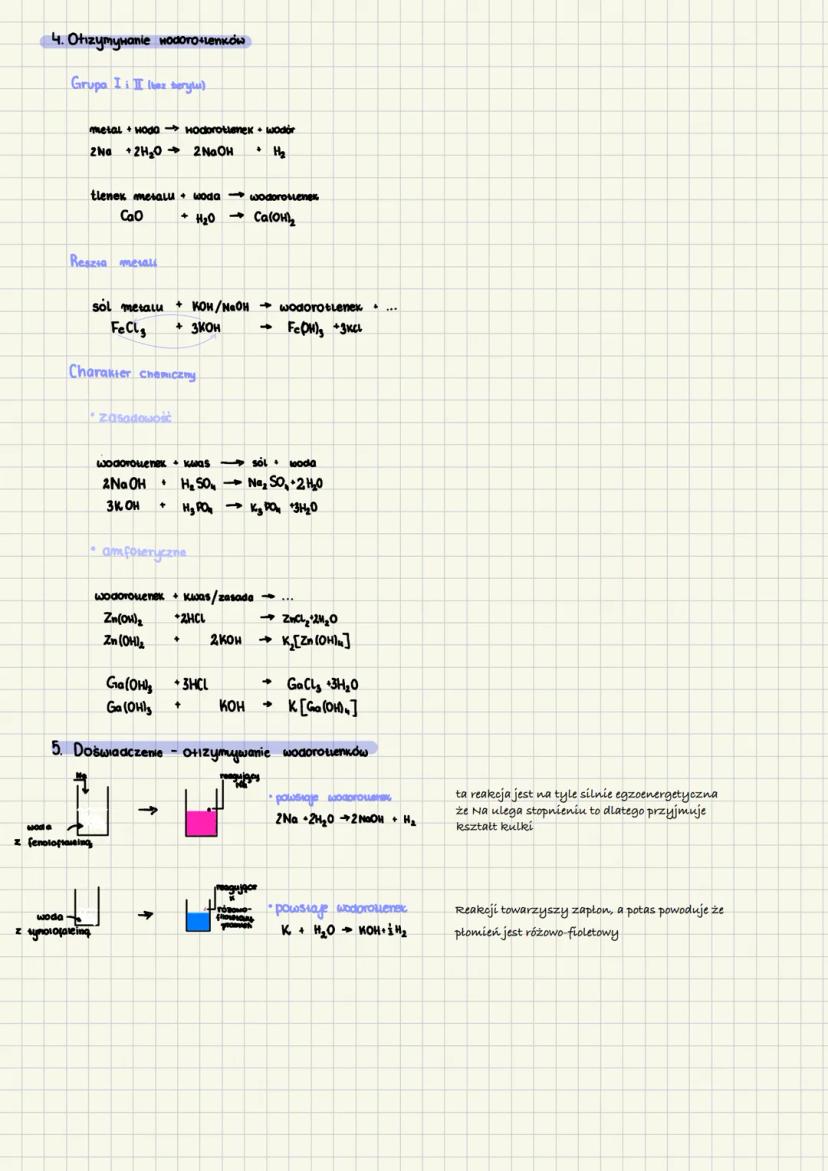
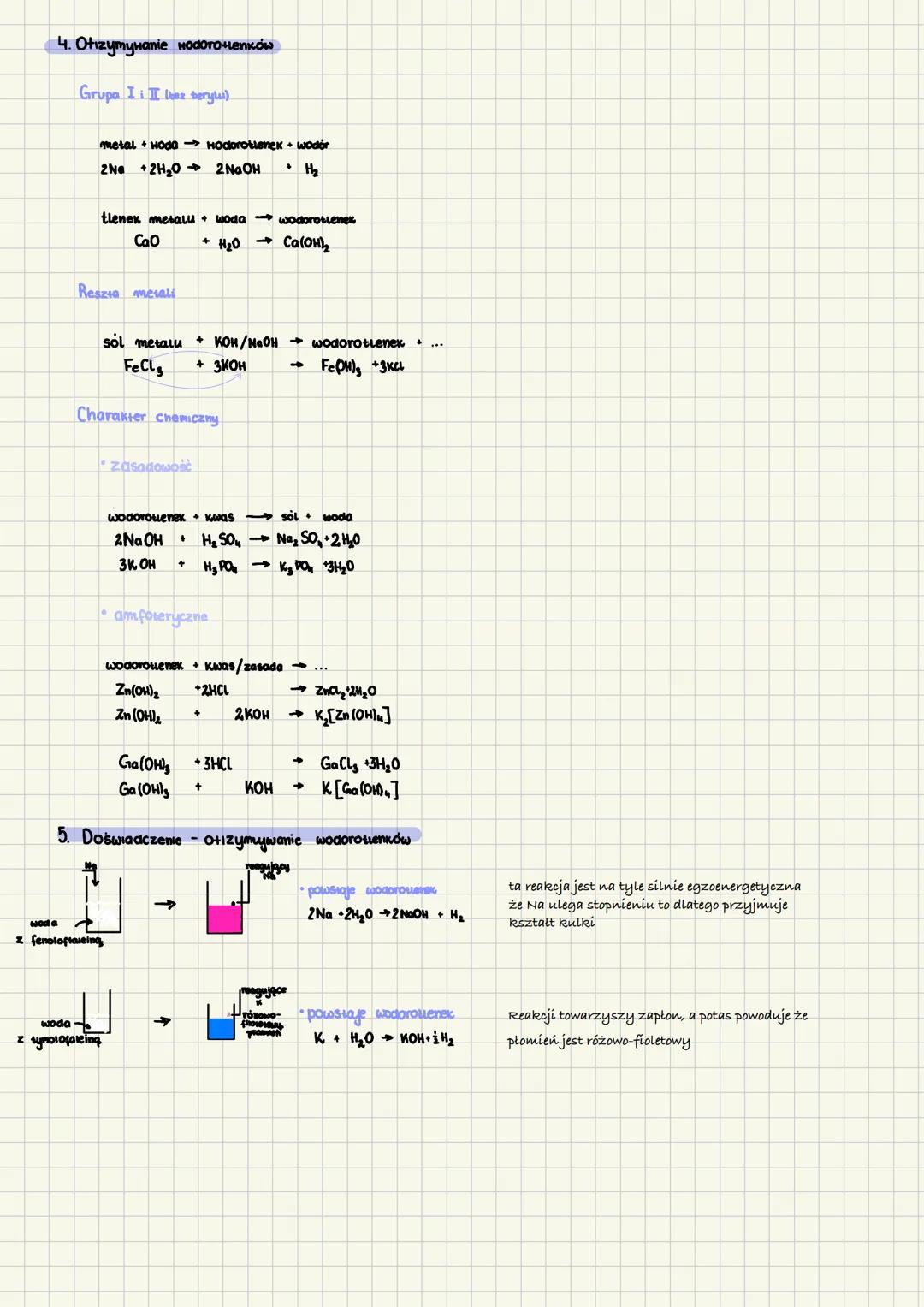
Wodorotlenki można otrzymać na kilka sposobów. Metale aktywne z grupy I i II (np. sód, potas, wapń) reagują bezpośrednio z wodą, tworząc wodorotlenki i uwalniając wodór. Reakcja 2Na + 2H₂O → 2NaOH + H₂ jest tak energetyczna (egzotermiczna), że sód topi się i formuje kulkę na powierzchni wody.
Inną metodą jest reakcja tlenku metalu z wodą, np. CaO + H₂O → Ca(OH)₂. Dla pozostałych metali stosuje się reakcję soli metalu z mocną zasadą, np. FeCl₃ + 3KOH → Fe(OH)₃ + 3KCl.
Ze względu na charakter chemiczny wodorotlenki dzielimy na zasadowe i amfoteryczne. Wodorotlenki zasadowe reagują z kwasami, tworząc sól i wodę, np. 2NaOH + H₂SO₄ → Na₂SO₄ + 2H₂O. Natomiast wodorotlenki amfoteryczne (np. Zn(OH)₂, Al(OH)₃) reagują zarówno z kwasami, jak i z mocnymi zasadami.
🔥 Uwaga! Reakcja potasu z wodą jest niezwykle gwałtowna i towarzyszy jej zapłon, a płomień ma charakterystyczną różowo-fioletową barwę. Nigdy nie przeprowadzaj tego eksperymentu samodzielnie!

Reakcje wodorotlenków amfoterycznych
Wodorotlenki amfoteryczne, jak Zn(OH)₂ czy Cr(OH)₃, wykazują unikalne właściwości - reagują zarówno z kwasami jak i z zasadami. Ta dwufunkcyjność czyni je wyjątkowo interesującymi w chemii.
Gdy wodorotlenek cynku reaguje z kwasem solnym, powstaje chlorek cynku i woda: Zn(OH)₂ + 2HCl → ZnCl₂ + 2H₂O. Jest to typowa reakcja zasady z kwasem. Jednak ten sam wodorotlenek może reagować z mocną zasadą, tworząc związki kompleksowe: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄].
Podobnie zachowują się inne wodorotlenki amfoteryczne, np. wodorotlenek chromu(III): Cr(SO₄)₃ + 6NaOH → 2Cr(OH)₃ + 3Na₂SO₄, a następnie Cr(OH)₃ może reagować z nadmiarem zasady.
📌 Warto zapamiętać! Możliwość reakcji zarówno z kwasami jak i zasadami jest kluczową cechą wodorotlenków amfoterycznych, co odróżnia je od typowych wodorotlenków zasadowych jak NaOH czy KOH.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: silna zasada
9Wodorotlenki: Właściwości i Reakcje
Zrozumienie wodorotlenków: ich właściwości, reakcje z kwasami i zasadami oraz metody przygotowania. Idealne materiały do nauki przed maturą. Kluczowe informacje o wodorotlenku sodu, potasu i wapnia oraz ich amfoteryczności.
Pierwiastki Bloku S
Zgłębiaj właściwości i reakcje pierwiastków bloku S, w tym metali alkalicznych i ziem alkalicznych. Dowiedz się o ich związkach, takich jak wodorotlenki, sole oraz reakcje z kwasami i wodą. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Wodorotlenki: Właściwości i Zastosowania
Poznaj wodorotlenki, ich wzory, metody otrzymywania oraz właściwości. Zawiera informacje o trudno rozpuszczalnych wodorotlenkach, zastosowaniach sodu i wapnia, dysocjacji, elektrolitach oraz wskaźnikach. Idealne dla uczniów chemii.
Właściwości i Zastosowania KOH i NaOH
Odkryj szczegółowe informacje na temat wodorotlenku potasu (KOH) i wodorotlenku sodu (NaOH). Dowiedz się, jak są one otrzymywane, ich właściwości fizyczne oraz zastosowania w różnych gałęziach przemysłu, takich jak przemysł spożywczy, chemiczny, kosmetyczny i farmaceutyczny. Idealne dla studentów chemii i technologii.
Wodorotlenki Metali
Zrozumienie wodorotlenków metali, ich przygotowania oraz właściwości. Obejmuje reakcje metali z wodą, dysocjację jonową oraz różnice między zasadami a wodorotlenkami. Idealne dla uczniów klasy 8. Typ: Podsumowanie.
Wodorotlenki i Zasady
Zgłębiaj wodorotlenki, ich właściwości oraz zastosowania w przemyśle. Dowiedz się, jak przygotować wodorotlenki, ich dysocjację jonową oraz różnice między zasadami. Idealne dla uczniów klasy 8. Materiał oparty na podręczniku 'Chemia Nowej Ery'.
Właściwości Wodorotlenków
Zgłębiaj właściwości i zastosowania wodorotlenków, w tym wodorotlenków sodu i potasu. Dowiedz się, jak przygotować wodorotlenki oraz ich rolę w różnych dziedzinach, takich jak rolnictwo i kosmetologia. Materiał oparty na vademecum maturalnym 'Teraz Matura' oraz wiedzy własnej.
Wodorotlenki i ich Reakcje
Zgłębiaj właściwości wodorotlenków, ich amfoteryczność oraz metody przygotowania. Dowiedz się, jak reagują z kwasami i zasadami, a także poznaj charakterystykę wodorotlenków sodu, potasu i wapnia. Idealne dla studentów chemii. Typ: Podsumowanie.
Litowce: Sód i Potas
Zgłębiaj właściwości litowców, w tym sodu i potasu. Dowiedz się o ich chemicznych charakterystykach, reakcjach oraz zastosowaniach. Notatka obejmuje kluczowe informacje o metalach alkalicznych, ich wodorotlenkach oraz barwieniu płomienia. Idealna dla uczniów przygotowujących się do egzaminów z chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Wodorotlenki: Nauka nazw, właściwości i procesów chemicznych
Wodorotlenki to ważne związki chemiczne składające się z metalu i grupy hydroksylowej (OH). Są one istotne zarówno w codziennym życiu, jak i w wielu procesach przemysłowych. Zrozumienie ich nazewnictwa, właściwości i reakcji chemicznych to podstawa chemii nieorganicznej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Nazewnictwo i tworzenie wzorów wodorotlenków
Nazywanie wodorotlenków jest dość proste - zaczynamy od słowa "wodorotlenek" a następnie dodajemy nazwę metalu. Na przykład KOH to wodorotlenek potasu, a NaOH to wodorotlenek sodu. Gdy metal tworzy kilka różnych stopni utlenienia, musimy to zaznaczyć w nazwie, np. Cu(OH)₂ to wodorotlenek miedzi(II).
Tworzenie wzorów jest podobnie nieskomplikowane - najpierw zapisujemy symbol metalu, a następnie grupę OH z odpowiednim indeksem dolnym. Przykłady to Ca(OH)₂ (wodorotlenek wapnia) czy Fe(OH)₃ (wodorotlenek żelaza(III)).
Wodorotlenki ulegają dysocjacji elektrolitycznej w wodzie, która może być całkowita lub stopniowa. Przy dysocjacji całkowitej wodorotlenek rozpada się całkowicie na jony, np. NaOH ⇄ Na⁺ + OH⁻. Natomiast dysocjacja stopniowa zachodzi etapami, np. Al(OH)₃ najpierw tworzy Al(OH)₂⁺ i OH⁻, potem AlOH²⁺ i kolejny OH⁻, a na końcu Al³⁺ i trzeci OH⁻.
💡 Zapamiętaj! Wodorotlenki metali grupy I i II (z wyjątkiem berylu) dysocjują całkowicie, co sprawia, że są mocnymi zasadami, a ich roztwory dobrze przewodzą prąd elektryczny.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Otrzymywanie i właściwości wodorotlenków
Wodorotlenki można otrzymać na kilka sposobów. Metale aktywne z grupy I i II (np. sód, potas, wapń) reagują bezpośrednio z wodą, tworząc wodorotlenki i uwalniając wodór. Reakcja 2Na + 2H₂O → 2NaOH + H₂ jest tak energetyczna (egzotermiczna), że sód topi się i formuje kulkę na powierzchni wody.
Inną metodą jest reakcja tlenku metalu z wodą, np. CaO + H₂O → Ca(OH)₂. Dla pozostałych metali stosuje się reakcję soli metalu z mocną zasadą, np. FeCl₃ + 3KOH → Fe(OH)₃ + 3KCl.
Ze względu na charakter chemiczny wodorotlenki dzielimy na zasadowe i amfoteryczne. Wodorotlenki zasadowe reagują z kwasami, tworząc sól i wodę, np. 2NaOH + H₂SO₄ → Na₂SO₄ + 2H₂O. Natomiast wodorotlenki amfoteryczne (np. Zn(OH)₂, Al(OH)₃) reagują zarówno z kwasami, jak i z mocnymi zasadami.
🔥 Uwaga! Reakcja potasu z wodą jest niezwykle gwałtowna i towarzyszy jej zapłon, a płomień ma charakterystyczną różowo-fioletową barwę. Nigdy nie przeprowadzaj tego eksperymentu samodzielnie!

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje wodorotlenków amfoterycznych
Wodorotlenki amfoteryczne, jak Zn(OH)₂ czy Cr(OH)₃, wykazują unikalne właściwości - reagują zarówno z kwasami jak i z zasadami. Ta dwufunkcyjność czyni je wyjątkowo interesującymi w chemii.
Gdy wodorotlenek cynku reaguje z kwasem solnym, powstaje chlorek cynku i woda: Zn(OH)₂ + 2HCl → ZnCl₂ + 2H₂O. Jest to typowa reakcja zasady z kwasem. Jednak ten sam wodorotlenek może reagować z mocną zasadą, tworząc związki kompleksowe: Zn(OH)₂ + 2NaOH → Na₂[Zn(OH)₄].
Podobnie zachowują się inne wodorotlenki amfoteryczne, np. wodorotlenek chromu(III): Cr(SO₄)₃ + 6NaOH → 2Cr(OH)₃ + 3Na₂SO₄, a następnie Cr(OH)₃ może reagować z nadmiarem zasady.
📌 Warto zapamiętać! Możliwość reakcji zarówno z kwasami jak i zasadami jest kluczową cechą wodorotlenków amfoterycznych, co odróżnia je od typowych wodorotlenków zasadowych jak NaOH czy KOH.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: silna zasada
9Wodorotlenki: Właściwości i Reakcje
Zrozumienie wodorotlenków: ich właściwości, reakcje z kwasami i zasadami oraz metody przygotowania. Idealne materiały do nauki przed maturą. Kluczowe informacje o wodorotlenku sodu, potasu i wapnia oraz ich amfoteryczności.
Pierwiastki Bloku S
Zgłębiaj właściwości i reakcje pierwiastków bloku S, w tym metali alkalicznych i ziem alkalicznych. Dowiedz się o ich związkach, takich jak wodorotlenki, sole oraz reakcje z kwasami i wodą. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Wodorotlenki: Właściwości i Zastosowania
Poznaj wodorotlenki, ich wzory, metody otrzymywania oraz właściwości. Zawiera informacje o trudno rozpuszczalnych wodorotlenkach, zastosowaniach sodu i wapnia, dysocjacji, elektrolitach oraz wskaźnikach. Idealne dla uczniów chemii.
Właściwości i Zastosowania KOH i NaOH
Odkryj szczegółowe informacje na temat wodorotlenku potasu (KOH) i wodorotlenku sodu (NaOH). Dowiedz się, jak są one otrzymywane, ich właściwości fizyczne oraz zastosowania w różnych gałęziach przemysłu, takich jak przemysł spożywczy, chemiczny, kosmetyczny i farmaceutyczny. Idealne dla studentów chemii i technologii.
Wodorotlenki Metali
Zrozumienie wodorotlenków metali, ich przygotowania oraz właściwości. Obejmuje reakcje metali z wodą, dysocjację jonową oraz różnice między zasadami a wodorotlenkami. Idealne dla uczniów klasy 8. Typ: Podsumowanie.
Wodorotlenki i Zasady
Zgłębiaj wodorotlenki, ich właściwości oraz zastosowania w przemyśle. Dowiedz się, jak przygotować wodorotlenki, ich dysocjację jonową oraz różnice między zasadami. Idealne dla uczniów klasy 8. Materiał oparty na podręczniku 'Chemia Nowej Ery'.
Właściwości Wodorotlenków
Zgłębiaj właściwości i zastosowania wodorotlenków, w tym wodorotlenków sodu i potasu. Dowiedz się, jak przygotować wodorotlenki oraz ich rolę w różnych dziedzinach, takich jak rolnictwo i kosmetologia. Materiał oparty na vademecum maturalnym 'Teraz Matura' oraz wiedzy własnej.
Wodorotlenki i ich Reakcje
Zgłębiaj właściwości wodorotlenków, ich amfoteryczność oraz metody przygotowania. Dowiedz się, jak reagują z kwasami i zasadami, a także poznaj charakterystykę wodorotlenków sodu, potasu i wapnia. Idealne dla studentów chemii. Typ: Podsumowanie.
Litowce: Sód i Potas
Zgłębiaj właściwości litowców, w tym sodu i potasu. Dowiedz się o ich chemicznych charakterystykach, reakcjach oraz zastosowaniach. Notatka obejmuje kluczowe informacje o metalach alkalicznych, ich wodorotlenkach oraz barwieniu płomienia. Idealna dla uczniów przygotowujących się do egzaminów z chemii.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.