Równowagi jonowe to kluczowy temat chemii, który wyjaśnia zachowanie elektrolitów... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
1,064
•
Zaktualizowano May 11, 2026
•
bartek
@bartek20_02
Równowagi jonowe to kluczowy temat chemii, który wyjaśnia zachowanie elektrolitów... Pokaż więcej
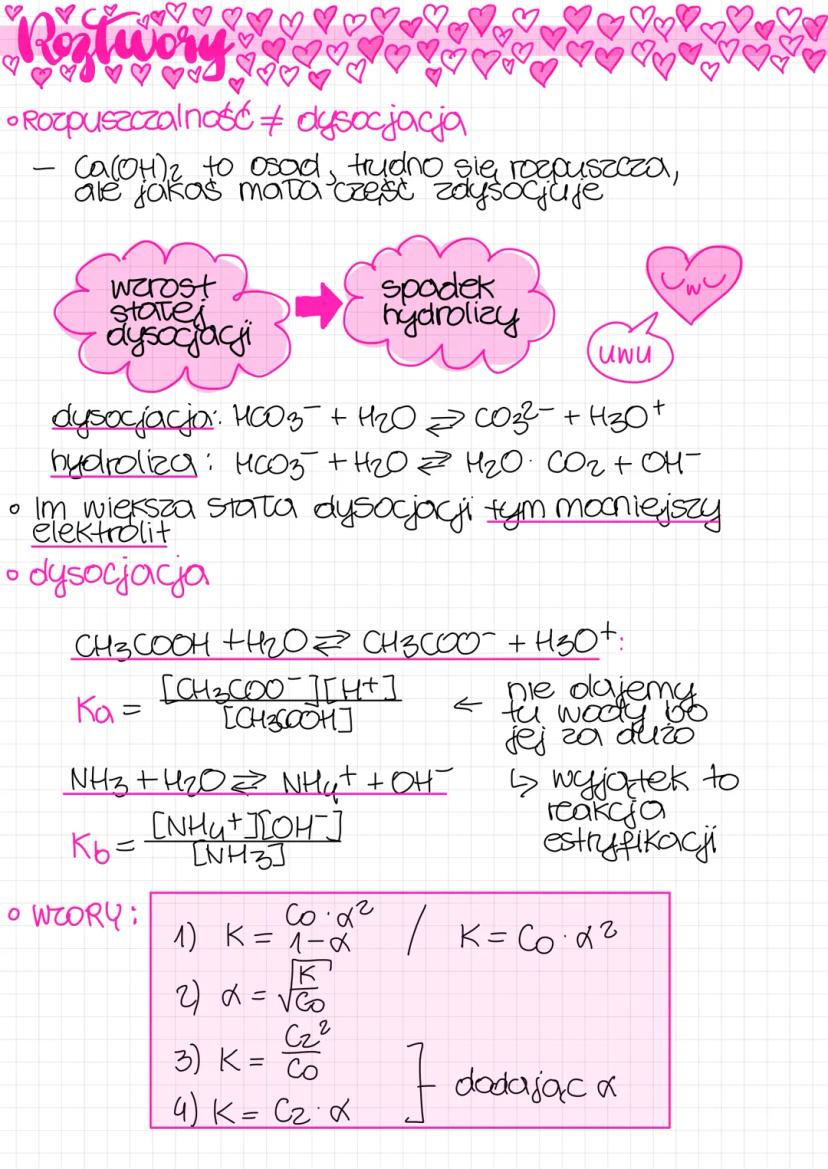

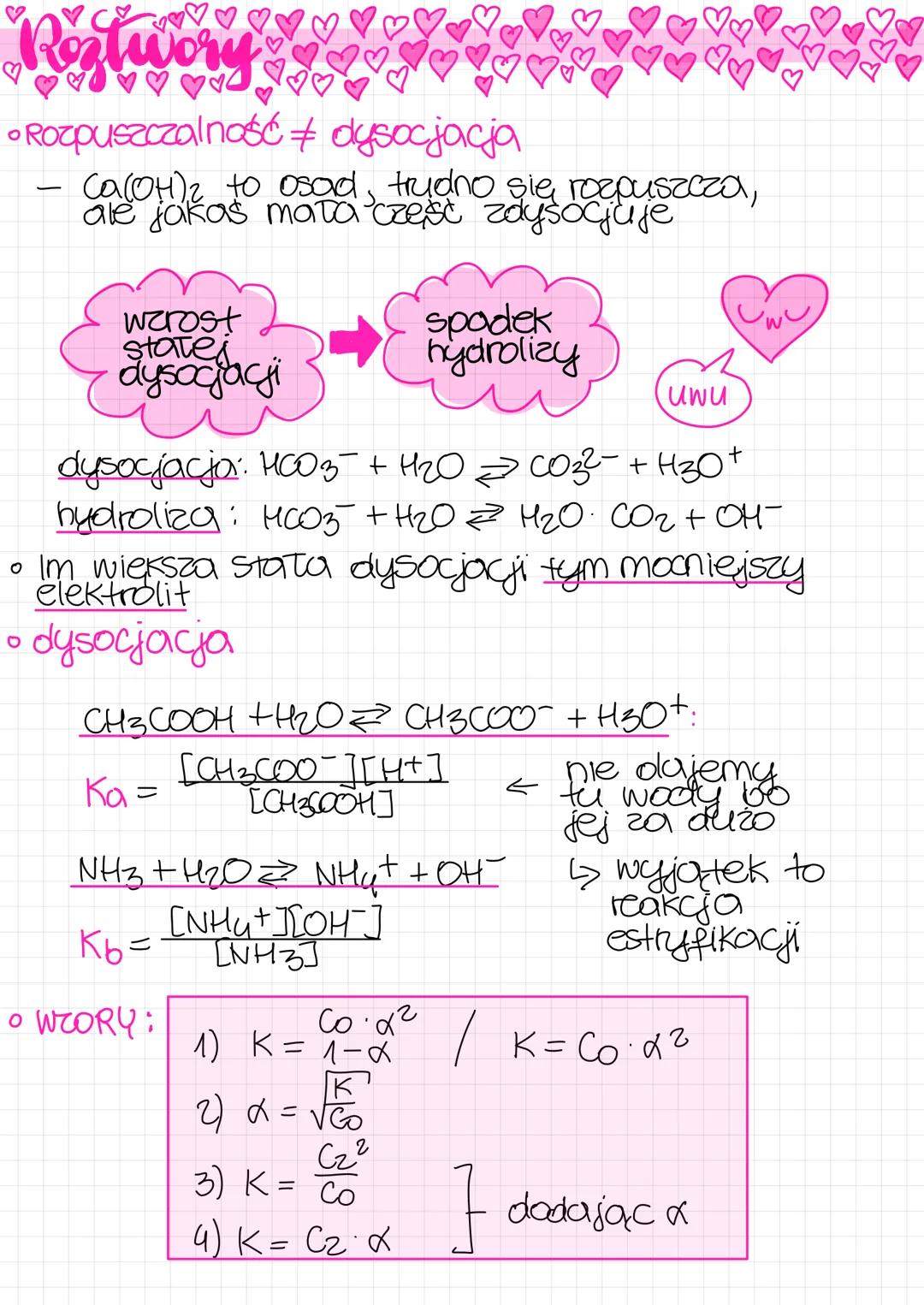
Dysocjacja i rozpuszczalność to różne procesy. Na przykład wodorotlenek wapnia Ca(OH)₂ jest trudno rozpuszczalny, ale ta niewielka ilość, która przechodzi do roztworu, ulega dysocjacji. Gdy mówimy o sile elektrolitu, pamiętaj: im większa stała dysocjacji, tym mocniejszy elektrolit.
Proces dysocjacji dla kwasu octowego zapisujemy jako: CH₃COOH + H₂O ⇄ CH₃COO⁻ + H₃O⁺, gdzie stała dysocjacji wynosi: Ka = [CH₃COO⁻][H⁺]/[CH₃COOH]. Z kolei dla amoniaku: NH₃ + H₂O ⇄ NH₄⁺ + OH⁻, a stała dysocjacji Kb = [NH₄⁺][OH⁻]/[NH₃].
W obliczeniach związanych z dysocjacją przydatne są wzory łączące stałą dysocjacji (K), stężenie początkowe elektrolitu (C₀), stężenie zdysocjowane (C₂) i stopień dysocjacji (α):
Na sprawdzianie! Pamiętaj, że proces dysocjacji wzmacnia się przy rozcieńczaniu roztworu, natomiast hydroliza zachodzi intensywniej w roztworach bardziej stężonych.
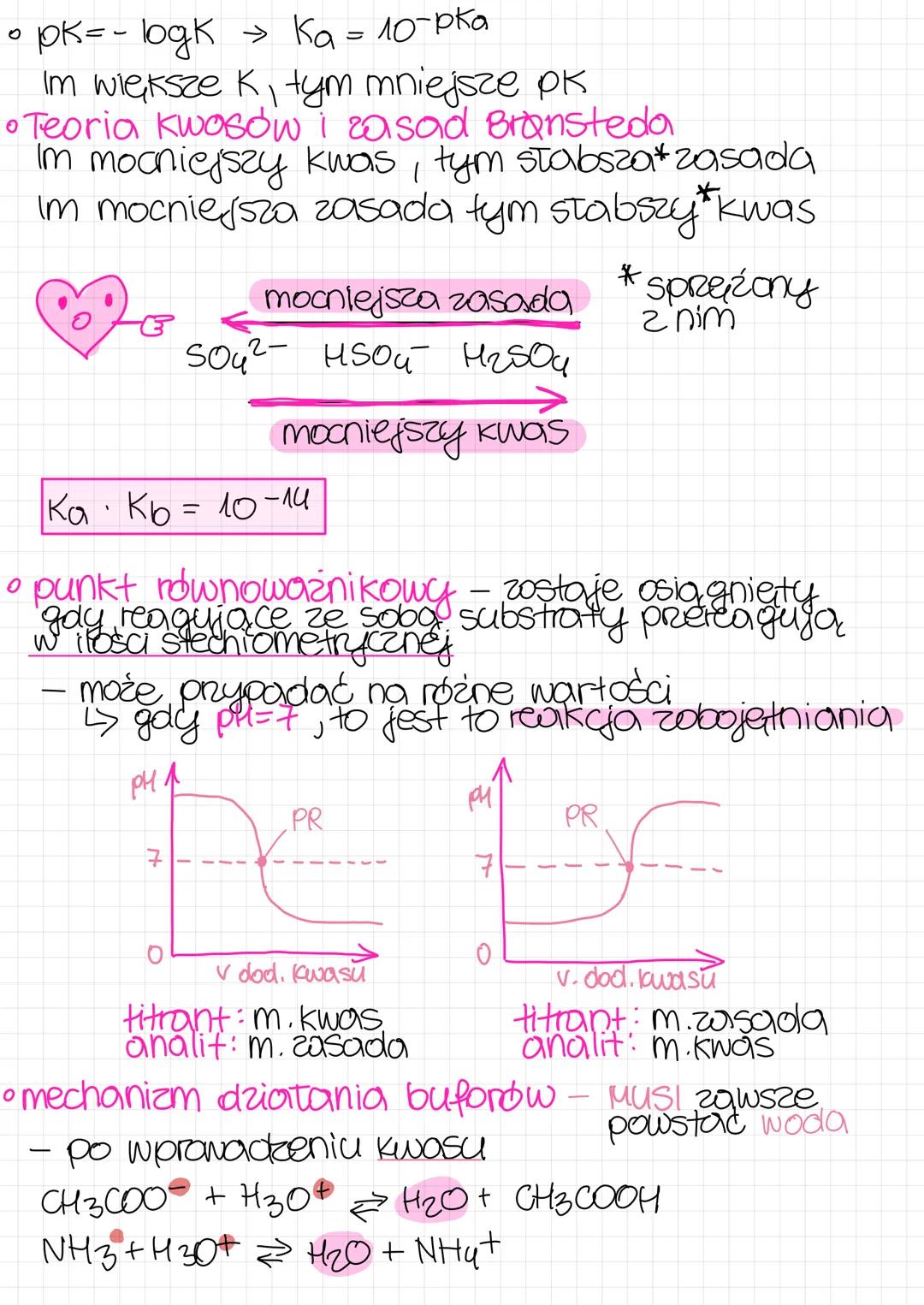
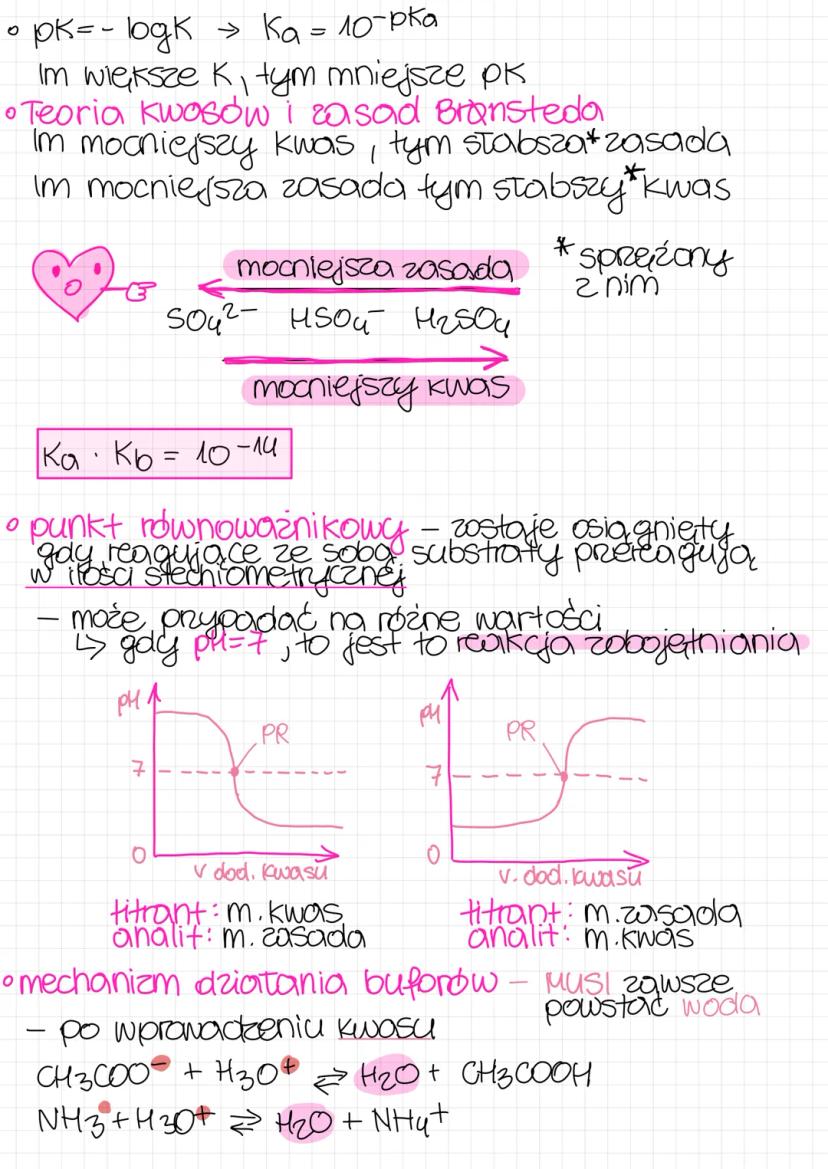
Stałą dysocjacji (K) można wyrażać jako pK, gdzie pK = -log K. Im większa wartość K, tym mniejsza wartość pK. Jeśli znasz pKa, możesz łatwo obliczyć Ka korzystając ze wzoru: Ka = 10^.
Według teorii Brønsteda, istnieje zależność między siłą kwasów i zasad: im mocniejszy kwas, tym słabsza sprzężona z nim zasada. Odwrotnie też - im mocniejsza zasada, tym słabszy sprzężony z nią kwas. Przykładowo w szeregu SO₄²⁻ → HSO₄⁻ → H₂SO₄ siła zasady maleje, a siła kwasu rośnie.
Ważne dla buforów: iloczyn stałych dysocjacji kwasu i sprzężonej z nim zasady wynosi 10⁻¹⁴ . Punkt równoważnikowy to moment, gdy reagujące substancje przereagują w stosunku stechiometrycznym. Nie zawsze oznacza to pH = 7 - zależy od siły kwasu i zasady!
Wskazówka maturalna: Analizując wykresy miareczkowania, zwróć uwagę na kształt krzywej - dla miareczkowania mocnego kwasu mocną zasadą (lub odwrotnie) przejście w punkcie równoważnikowym jest bardzo strome.

Bufory to roztwory utrzymujące stałe pH. Ich działanie opiera się na prostym mechanizmie: po dodaniu kwasu, anion buforowy reaguje z jonami H₃O⁺ tworząc wodę . Po dodaniu zasady, składnik kwasowy reaguje z jonami OH⁻ również tworząc wodę .
Wodorosole powstają w wyniku niedoboru zasady lub nadmiaru kwasu w reakcji. Pochodzą od kwasów wieloprotonowych, gdzie tylko część atomów wodoru zostaje zastąpiona przez metal lub kation amonowy. Ich zachowanie w roztworach wodnych może być różne:
Większość wodorosoli tworzy roztwory kwasowe, np.:
Uwaga na maturę! Wodorowęglany (np. KHCO₃) są wyjątkiem - tworzą roztwory zasadowe: HCO₃⁻ + H₂O → H₂O + CO₂ + OH⁻. To częsty temat na egzaminie!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
bartek
@bartek20_02
Równowagi jonowe to kluczowy temat chemii, który wyjaśnia zachowanie elektrolitów w roztworach wodnych. Zrozumienie dysocjacji, hydrolizy i działania buforów jest niezbędne zarówno do rozwiązywania zadań maturalnych, jak i wyjaśnienia wielu zjawisk chemicznych.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Dysocjacja i rozpuszczalność to różne procesy. Na przykład wodorotlenek wapnia Ca(OH)₂ jest trudno rozpuszczalny, ale ta niewielka ilość, która przechodzi do roztworu, ulega dysocjacji. Gdy mówimy o sile elektrolitu, pamiętaj: im większa stała dysocjacji, tym mocniejszy elektrolit.
Proces dysocjacji dla kwasu octowego zapisujemy jako: CH₃COOH + H₂O ⇄ CH₃COO⁻ + H₃O⁺, gdzie stała dysocjacji wynosi: Ka = [CH₃COO⁻][H⁺]/[CH₃COOH]. Z kolei dla amoniaku: NH₃ + H₂O ⇄ NH₄⁺ + OH⁻, a stała dysocjacji Kb = [NH₄⁺][OH⁻]/[NH₃].
W obliczeniach związanych z dysocjacją przydatne są wzory łączące stałą dysocjacji (K), stężenie początkowe elektrolitu (C₀), stężenie zdysocjowane (C₂) i stopień dysocjacji (α):
Na sprawdzianie! Pamiętaj, że proces dysocjacji wzmacnia się przy rozcieńczaniu roztworu, natomiast hydroliza zachodzi intensywniej w roztworach bardziej stężonych.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Stałą dysocjacji (K) można wyrażać jako pK, gdzie pK = -log K. Im większa wartość K, tym mniejsza wartość pK. Jeśli znasz pKa, możesz łatwo obliczyć Ka korzystając ze wzoru: Ka = 10^.
Według teorii Brønsteda, istnieje zależność między siłą kwasów i zasad: im mocniejszy kwas, tym słabsza sprzężona z nim zasada. Odwrotnie też - im mocniejsza zasada, tym słabszy sprzężony z nią kwas. Przykładowo w szeregu SO₄²⁻ → HSO₄⁻ → H₂SO₄ siła zasady maleje, a siła kwasu rośnie.
Ważne dla buforów: iloczyn stałych dysocjacji kwasu i sprzężonej z nim zasady wynosi 10⁻¹⁴ . Punkt równoważnikowy to moment, gdy reagujące substancje przereagują w stosunku stechiometrycznym. Nie zawsze oznacza to pH = 7 - zależy od siły kwasu i zasady!
Wskazówka maturalna: Analizując wykresy miareczkowania, zwróć uwagę na kształt krzywej - dla miareczkowania mocnego kwasu mocną zasadą (lub odwrotnie) przejście w punkcie równoważnikowym jest bardzo strome.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Bufory to roztwory utrzymujące stałe pH. Ich działanie opiera się na prostym mechanizmie: po dodaniu kwasu, anion buforowy reaguje z jonami H₃O⁺ tworząc wodę . Po dodaniu zasady, składnik kwasowy reaguje z jonami OH⁻ również tworząc wodę .
Wodorosole powstają w wyniku niedoboru zasady lub nadmiaru kwasu w reakcji. Pochodzą od kwasów wieloprotonowych, gdzie tylko część atomów wodoru zostaje zastąpiona przez metal lub kation amonowy. Ich zachowanie w roztworach wodnych może być różne:
Większość wodorosoli tworzy roztwory kwasowe, np.:
Uwaga na maturę! Wodorowęglany (np. KHCO₃) są wyjątkiem - tworzą roztwory zasadowe: HCO₃⁻ + H₂O → H₂O + CO₂ + OH⁻. To częsty temat na egzaminie!
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
25
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
Zrozumienie kwasów: ich otrzymywanie, dysocjacja elektrolityczna oraz nazewnictwo. Dowiedz się o kwasach beztlenowych i tlenowych, ich reakcjach oraz właściwościach chemicznych. Idealne materiały do nauki przed maturą.
Zrozumienie toksyczności benzenu, jego źródeł w materiałach budowlanych oraz objawów zatrucia. Dowiedz się, dlaczego benzen jest niebezpieczny dla zdrowia, jakie ma zastosowania w przemyśle oraz jak chronić się przed jego szkodliwym działaniem. Typ: prezentacja.
Zgłębiaj kluczowe procesy związane z białkami, takie jak denaturacja, wysalanie oraz reakcje biuretowa i ksantoproteinowa. Dowiedz się, jak czynniki chemiczne wpływają na strukturę białek i jak wykrywać ich obecność. Idealne dla studentów biologii i chemii.
Zgłębiaj właściwości wyższych kwasów karboksylowych oraz ich zastosowanie w produkcji mydeł. Dowiedz się o reakcjach chemicznych, dysocjacji oraz zastosowaniach w medycynie i przemyśle. Idealne dla uczniów chemii na poziomie średnim.
Zgłębiaj właściwości amin i amidów w chemii organicznej. Ta notatka zawiera szczegółowe informacje o strukturze, reakcjach, izomerach oraz metodach otrzymywania tych związków. Idealna dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje związane z grupami funkcyjnymi i ich zastosowaniami.
Zrozumienie dysocjacji jonowej kwasów, zasad i soli. Przykłady reakcji chemicznych, w tym dysocjacja kwasu fosforowego i wodorotlenku wapnia. Kluczowe pojęcia: jony, stężenia, reakcje chemiczne. Idealne dla studentów chemii.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS