Termochemia to dziedzina, która bada efekty energetyczne towarzyszące reakcjom chemicznym.... Pokaż więcej
Zarejestruj się, aby zobaczyć notatkęTo nic nie kosztuje!
Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Knowunity AI
Przedmioty
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Pokaż wszystkie tematy
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Pokaż wszystkie tematy
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Pokaż wszystkie tematy
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Pokaż wszystkie tematy
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Pokaż wszystkie tematy
995
•
Zaktualizowano Apr 24, 2026
•
notes_marta
@notes_marta
Termochemia to dziedzina, która bada efekty energetyczne towarzyszące reakcjom chemicznym.... Pokaż więcej
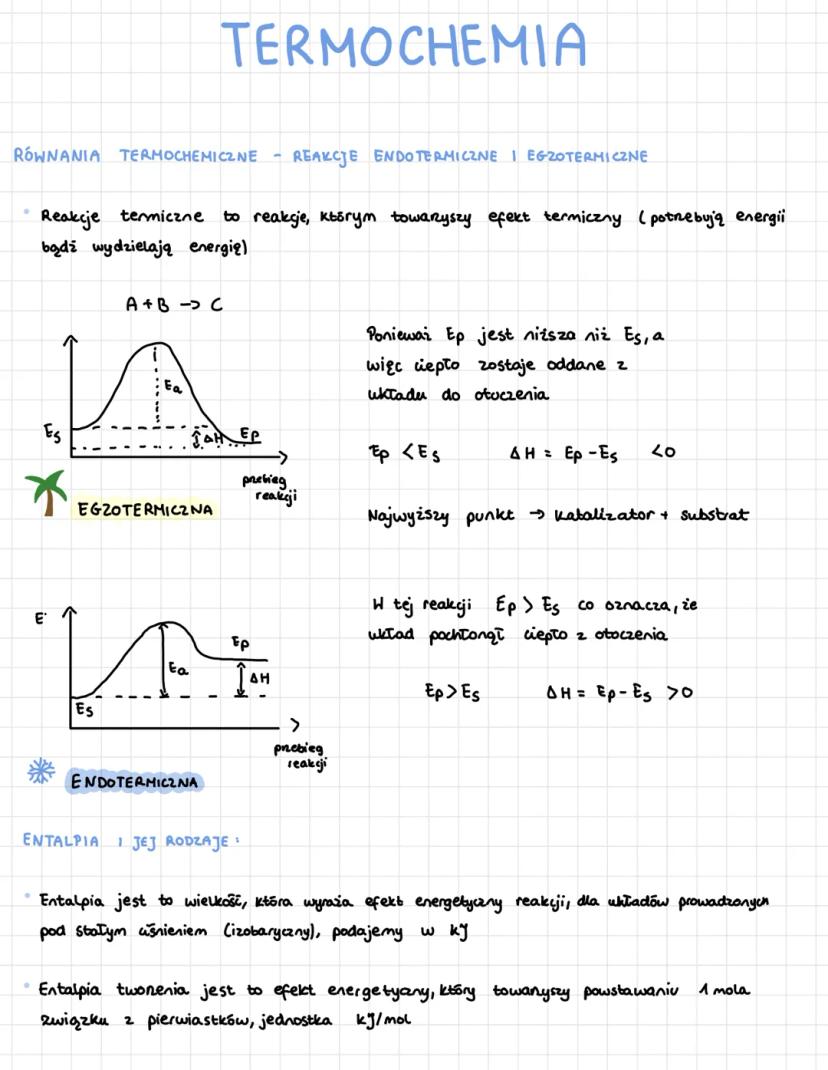









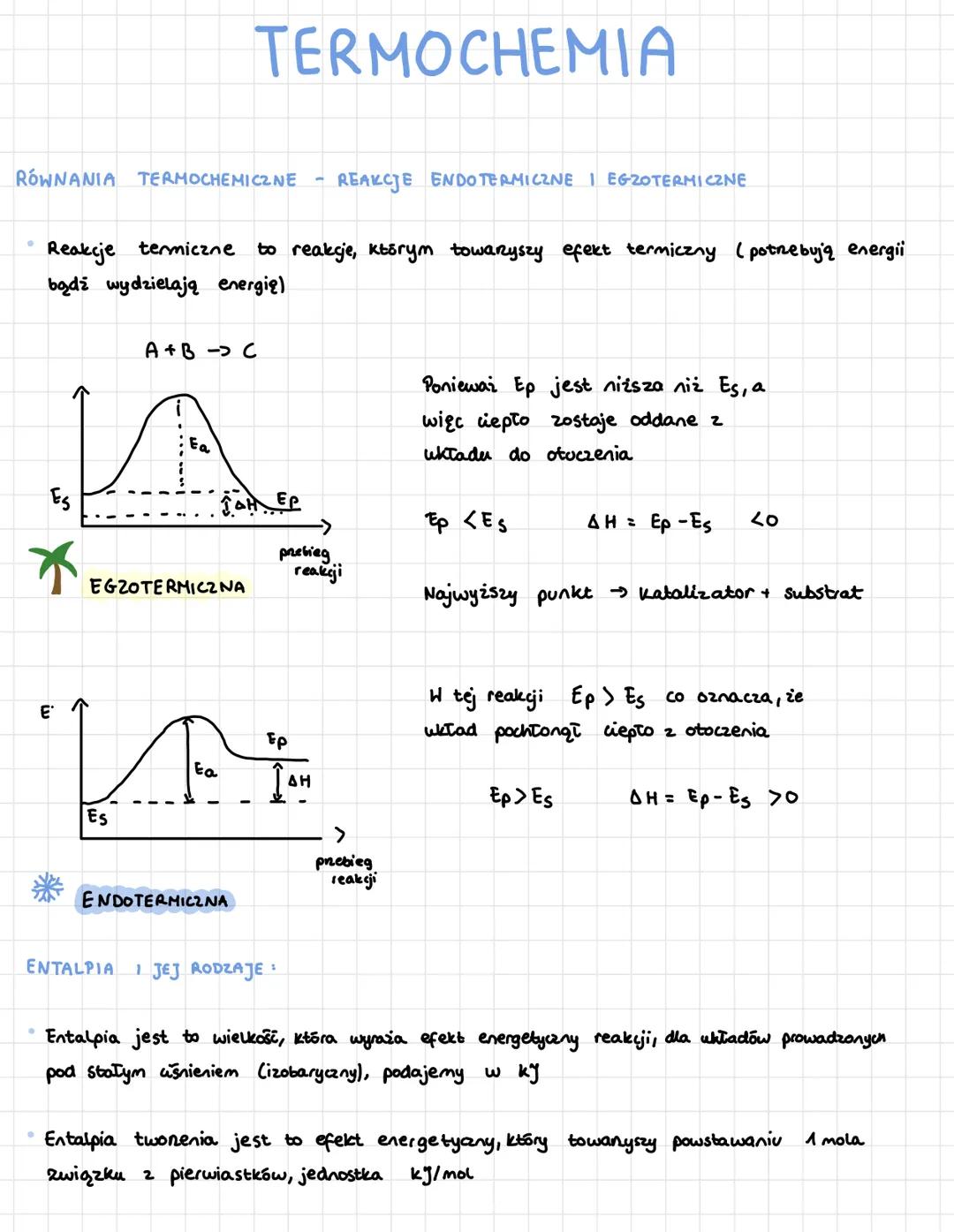
Reakcje egzotermiczne to te, które oddają ciepło do otoczenia - energia produktów (Ep) jest niższa niż energia substratów (Es). W reakcjach endotermicznych układ pochłania ciepło z otoczenia, więc Ep > Es.
Entalpia to wielkość wyrażająca efekt energetyczny reakcji prowadzonej pod stałym ciśnieniem, podawana w kJ/mol. Entalpia tworzenia to energia potrzebna do utworzenia 1 mola związku z pierwiastków - dla pierwiastków wynosi zawsze 0.
Entalpia spalania to efekt energetyczny spalania 1 mola związku do produktów trwałych (np. CO₂ i H₂O).
💡 Zapamiętaj: Reakcje egzotermiczne mają ujemny ΔH (oddają ciepło), a endotermiczne dodatni ΔH (pochłaniają ciepło).

Prawo Lavoisiera-Laplacea mówi, że reakcje odwrotne mają taką samą wartość efektu energetycznego, ale z przeciwnym znakiem. Prawo Hessa głosi, że zmiana entalpii nie zależy od drogi przemiany, tylko od stanu początkowego i końcowego.
Podstawowe wzory do obliczeń:
Zawsze uwzględniaj liczbę moli każdego reagenta w obliczeniach!
💡 Wskazówka: W zadaniach z prawem Hessa układaj równania tak, żeby po zsumowaniu otrzymać pożądaną reakcję.

W zadaniach praktycznych często obliczasz entalpię tworzenia na podstawie danych doświadczalnych. Przykład: jeśli 0,05 mola ZnS wydziela 10,15 kJ energii, to entalpia tworzenia wynosi -203 kJ/mol.
Przy reakcjach spalania pamiętaj o stechiometrii - 1 mol CH₄ wymaga 2 moli O₂ i daje 1 mol CO₂ oraz 2 mole H₂O. Jeśli wydziela się 881 kJ energii, możesz obliczyć objętość potrzebnego tlenu.
Ważne jest też uwzględnianie wydajności reakcji - jeśli reakcja przebiega w 90%, musisz to uwzględnić w obliczeniach końcowej entalpii.
💡 Praktyczna rada: Zawsze sprawdzaj jednostki - czy wynik ma być w kJ, czy kJ/mol, i czy uwzględniłeś wszystkie mole reagentów.

Prawo Hessa pozwala obliczać entalpię reakcji, których nie można zmierzyć bezpośrednio. Przykład: dla reakcji Fe₂O₃ + 3Mg → 2Fe + 3MgO używasz danych dla spalania żelaza i magnezu.
Metoda polega na "budowaniu" pożądanej reakcji z reakcji o znanych entalpiach. Możesz odwracać równania (zmieniając znak ΔH) i mnożyć przez współczynniki stechiometryczne.
Drugi sposób to używanie entalpii tworzenia: ΔH = Σ ΔHtworzenia produktów - Σ ΔHtworzenia substratów. Dla powyższego przykładu: ΔH = [3×(-602) + 0] - [(-822) + 0] = -984 kJ.
💡 Zapamiętaj: Oba sposoby (prawo Hessa i entalpia tworzenia) muszą dać ten sam wynik - to świetny sposób na sprawdzenie obliczeń!

Energia wiązania to energia potrzebna do zerwania 1 mola wiązań w fazie gazowej. W reakcjach chemicznych niektóre wiązania się zrywają (Es), a inne powstają (Ep).
Wzór: ΔH = Es - Ep, gdzie Es to suma energii zrywanych wiązań, a Ep to suma energii tworzonych wiązań. Przykład dla spalania metanu: Es = 4×413 + 2×499 = 2650 kJ, Ep = 2×799 + 4×465 = 3458 kJ, więc ΔH = -808 kJ.
Ta metoda jest szczególnie przydatna dla reakcji w fazie gazowej, gdzie wszystkie cząsteczki są w postaci pojedynczych molekuł.
💡 Uwaga: Energia wiązania jest zawsze dodatnia (trzeba energii, żeby zerwać wiązanie), ale w obliczeniach odejmujemy ją, gdy wiązanie powstaje.

Przy obliczaniu entalpii spalania na podstawie energii wiązań pamiętaj o dokładnym policzeniu wszystkich wiązań. Dla 2H₂ + O₂ → 2H₂O: zrywasz 2 wiązania H-H i 1 wiązanie O=O, a tworzysz 4 wiązania O-H.
W przypadku tworzenia amoniaku zrywasz 3 wiązania H-H i 1 bardzo mocne wiązanie N≡N , tworząc 6 wiązań N-H. Wynik ΔH = -85 kJ pokazuje, że reakcja jest egzotermiczna, ale słabo.
Rozkład związków wymaga zerwania wiązań w cząsteczce wyjściowej i utworzenia nowych w produktach. Dodatni ΔH oznacza reakcję endotermiczną.
💡 Strategia: Zawsze rysuj wzory strukturalne - łatwiej policzyć wiązania, gdy je widzisz!

Kombinowanie równań według prawa Hessa pozwala rozwiązać skomplikowane problemy. Dla reakcji N₂ + ½O₂ → N₂O używasz danych z innych reakcji, manipulując równaniami tak, żeby otrzymać pożądaną reakcję.
Przykład: jeśli masz dane dla C + 2N₂O → CO₂ + 2N₂ oraz C + O₂ → CO₂, możesz obliczyć entalpię tworzenia N₂O. Kluczowe jest prawidłowe odwrócenie i przeskalowanie równań.
Praktyczne zastosowania obejmują obliczanie entalpii dla reakcji metalurgicznych, jak redukcja tlenków miedzi czy reakcje z udziałem wodoru.
💡 Wskazówka: Zawsze zapisuj target-equation na początku i systematycznie "budujesz" ją z dostępnych danych.

Przemiany fazowe (np. H₂O(g) → H₂O(c)) też mają swoją entalpię, którą musisz uwzględnić w obliczeniach. Parowanie/skraplanie dodaje dodatkowy człon do równań termochemicznych.
Analiza trwałości cząsteczek na podstawie energii wiązań wyjaśnia, dlaczego azot tworzy N₂ , a fosfor występuje jako P₄ z wiązaniami pojedynczymi.
Praktyczne zastosowania przemysłowe: obliczenia dla pieca wapiennego pokazują, jaki stosunek molowy wapienia do koksu zapewni proces bez dodatkowego ogrzewania (reakcja endotermiczną równoważy egzotermiczna).
💡 Ciekawostka: Im mocniejsze wiązania w produktach, tym więcej energii się wydziela i tym bardziej egzotermiczna jest reakcja.

Entalpia izomeryzacji (np. propen → cyklopropen) obliczana jest z różnicy entalpii spalania izomerów. Skoro oba izomery spalają się do tych samych produktów, różnica pokazuje różnicę stabilności.
Spalanie węglowodorów wymaga precyzyjnego liczenia atomów - propen C₃H₆ + 4,5O₂ → 3CO₂ + 3H₂O. Pamiętaj o ułamkowych współczynnikach dla tlenu lub podwój całe równanie.
Energia wiązań w węglowodorach: wiązania C-H , C-C , C=C . Produkty spalania mają bardzo mocne wiązania C=O i O-H , dlatego spalanie jest tak egzotermiczne.
💡 Zapamiętaj: Izomery mają tę samą formułę molekularną, ale różną strukturę - stąd różne entalpie spalania!

Spalanie propanu wymaga policzenia wszystkich wiązań: 8 wiązań C-H, 2 wiązania C-C w substratach oraz wiązań w produktach. Systematyczne podejście zapobiega błędom.
Porównywanie entalpii spalania różnych węglowodorów pokazuje, że większe cząsteczki mają większe entalpie spalania w wartościach bezwzględnych, ale w przeliczeniu na gram często są podobne.
Kontrola wyników: entalpia spalania węglowodorów jest zawsze ujemna (reakcje egzotermiczne) i zazwyczaj wynosi około -40 do -50 kJ/g dla większości węglowodorów.
💡 Praktyczna rada: W złożonych cząsteczek rysuj struktury i systematycznie oznaczaj każde wiązanie - to zapobiega pomyłkom w liczeniu.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
notes_marta
@notes_marta
Termochemia to dziedzina, która bada efekty energetyczne towarzyszące reakcjom chemicznym. Poznasz różnice między reakcjami endotermicznymi i egzotermicznymi oraz nauczysz się obliczać entalpię różnymi sposobami.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Reakcje egzotermiczne to te, które oddają ciepło do otoczenia - energia produktów (Ep) jest niższa niż energia substratów (Es). W reakcjach endotermicznych układ pochłania ciepło z otoczenia, więc Ep > Es.
Entalpia to wielkość wyrażająca efekt energetyczny reakcji prowadzonej pod stałym ciśnieniem, podawana w kJ/mol. Entalpia tworzenia to energia potrzebna do utworzenia 1 mola związku z pierwiastków - dla pierwiastków wynosi zawsze 0.
Entalpia spalania to efekt energetyczny spalania 1 mola związku do produktów trwałych (np. CO₂ i H₂O).
💡 Zapamiętaj: Reakcje egzotermiczne mają ujemny ΔH (oddają ciepło), a endotermiczne dodatni ΔH (pochłaniają ciepło).

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Prawo Lavoisiera-Laplacea mówi, że reakcje odwrotne mają taką samą wartość efektu energetycznego, ale z przeciwnym znakiem. Prawo Hessa głosi, że zmiana entalpii nie zależy od drogi przemiany, tylko od stanu początkowego i końcowego.
Podstawowe wzory do obliczeń:
Zawsze uwzględniaj liczbę moli każdego reagenta w obliczeniach!
💡 Wskazówka: W zadaniach z prawem Hessa układaj równania tak, żeby po zsumowaniu otrzymać pożądaną reakcję.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
W zadaniach praktycznych często obliczasz entalpię tworzenia na podstawie danych doświadczalnych. Przykład: jeśli 0,05 mola ZnS wydziela 10,15 kJ energii, to entalpia tworzenia wynosi -203 kJ/mol.
Przy reakcjach spalania pamiętaj o stechiometrii - 1 mol CH₄ wymaga 2 moli O₂ i daje 1 mol CO₂ oraz 2 mole H₂O. Jeśli wydziela się 881 kJ energii, możesz obliczyć objętość potrzebnego tlenu.
Ważne jest też uwzględnianie wydajności reakcji - jeśli reakcja przebiega w 90%, musisz to uwzględnić w obliczeniach końcowej entalpii.
💡 Praktyczna rada: Zawsze sprawdzaj jednostki - czy wynik ma być w kJ, czy kJ/mol, i czy uwzględniłeś wszystkie mole reagentów.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Prawo Hessa pozwala obliczać entalpię reakcji, których nie można zmierzyć bezpośrednio. Przykład: dla reakcji Fe₂O₃ + 3Mg → 2Fe + 3MgO używasz danych dla spalania żelaza i magnezu.
Metoda polega na "budowaniu" pożądanej reakcji z reakcji o znanych entalpiach. Możesz odwracać równania (zmieniając znak ΔH) i mnożyć przez współczynniki stechiometryczne.
Drugi sposób to używanie entalpii tworzenia: ΔH = Σ ΔHtworzenia produktów - Σ ΔHtworzenia substratów. Dla powyższego przykładu: ΔH = [3×(-602) + 0] - [(-822) + 0] = -984 kJ.
💡 Zapamiętaj: Oba sposoby (prawo Hessa i entalpia tworzenia) muszą dać ten sam wynik - to świetny sposób na sprawdzenie obliczeń!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Energia wiązania to energia potrzebna do zerwania 1 mola wiązań w fazie gazowej. W reakcjach chemicznych niektóre wiązania się zrywają (Es), a inne powstają (Ep).
Wzór: ΔH = Es - Ep, gdzie Es to suma energii zrywanych wiązań, a Ep to suma energii tworzonych wiązań. Przykład dla spalania metanu: Es = 4×413 + 2×499 = 2650 kJ, Ep = 2×799 + 4×465 = 3458 kJ, więc ΔH = -808 kJ.
Ta metoda jest szczególnie przydatna dla reakcji w fazie gazowej, gdzie wszystkie cząsteczki są w postaci pojedynczych molekuł.
💡 Uwaga: Energia wiązania jest zawsze dodatnia (trzeba energii, żeby zerwać wiązanie), ale w obliczeniach odejmujemy ją, gdy wiązanie powstaje.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Przy obliczaniu entalpii spalania na podstawie energii wiązań pamiętaj o dokładnym policzeniu wszystkich wiązań. Dla 2H₂ + O₂ → 2H₂O: zrywasz 2 wiązania H-H i 1 wiązanie O=O, a tworzysz 4 wiązania O-H.
W przypadku tworzenia amoniaku zrywasz 3 wiązania H-H i 1 bardzo mocne wiązanie N≡N , tworząc 6 wiązań N-H. Wynik ΔH = -85 kJ pokazuje, że reakcja jest egzotermiczna, ale słabo.
Rozkład związków wymaga zerwania wiązań w cząsteczce wyjściowej i utworzenia nowych w produktach. Dodatni ΔH oznacza reakcję endotermiczną.
💡 Strategia: Zawsze rysuj wzory strukturalne - łatwiej policzyć wiązania, gdy je widzisz!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Kombinowanie równań według prawa Hessa pozwala rozwiązać skomplikowane problemy. Dla reakcji N₂ + ½O₂ → N₂O używasz danych z innych reakcji, manipulując równaniami tak, żeby otrzymać pożądaną reakcję.
Przykład: jeśli masz dane dla C + 2N₂O → CO₂ + 2N₂ oraz C + O₂ → CO₂, możesz obliczyć entalpię tworzenia N₂O. Kluczowe jest prawidłowe odwrócenie i przeskalowanie równań.
Praktyczne zastosowania obejmują obliczanie entalpii dla reakcji metalurgicznych, jak redukcja tlenków miedzi czy reakcje z udziałem wodoru.
💡 Wskazówka: Zawsze zapisuj target-equation na początku i systematycznie "budujesz" ją z dostępnych danych.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Przemiany fazowe (np. H₂O(g) → H₂O(c)) też mają swoją entalpię, którą musisz uwzględnić w obliczeniach. Parowanie/skraplanie dodaje dodatkowy człon do równań termochemicznych.
Analiza trwałości cząsteczek na podstawie energii wiązań wyjaśnia, dlaczego azot tworzy N₂ , a fosfor występuje jako P₄ z wiązaniami pojedynczymi.
Praktyczne zastosowania przemysłowe: obliczenia dla pieca wapiennego pokazują, jaki stosunek molowy wapienia do koksu zapewni proces bez dodatkowego ogrzewania (reakcja endotermiczną równoważy egzotermiczna).
💡 Ciekawostka: Im mocniejsze wiązania w produktach, tym więcej energii się wydziela i tym bardziej egzotermiczna jest reakcja.

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Entalpia izomeryzacji (np. propen → cyklopropen) obliczana jest z różnicy entalpii spalania izomerów. Skoro oba izomery spalają się do tych samych produktów, różnica pokazuje różnicę stabilności.
Spalanie węglowodorów wymaga precyzyjnego liczenia atomów - propen C₃H₆ + 4,5O₂ → 3CO₂ + 3H₂O. Pamiętaj o ułamkowych współczynnikach dla tlenu lub podwój całe równanie.
Energia wiązań w węglowodorach: wiązania C-H , C-C , C=C . Produkty spalania mają bardzo mocne wiązania C=O i O-H , dlatego spalanie jest tak egzotermiczne.
💡 Zapamiętaj: Izomery mają tę samą formułę molekularną, ale różną strukturę - stąd różne entalpie spalania!

Dostęp do wszystkich materiałów
Popraw swoje oceny
Dołącz do milionów studentów
Spalanie propanu wymaga policzenia wszystkich wiązań: 8 wiązań C-H, 2 wiązania C-C w substratach oraz wiązań w produktach. Systematyczne podejście zapobiega błędom.
Porównywanie entalpii spalania różnych węglowodorów pokazuje, że większe cząsteczki mają większe entalpie spalania w wartościach bezwzględnych, ale w przeliczeniu na gram często są podobne.
Kontrola wyników: entalpia spalania węglowodorów jest zawsze ujemna (reakcje egzotermiczne) i zazwyczaj wynosi około -40 do -50 kJ/g dla większości węglowodorów.
💡 Praktyczna rada: W złożonych cząsteczek rysuj struktury i systematycznie oznaczaj każde wiązanie - to zapobiega pomyłkom w liczeniu.
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Aplikację możesz pobrać z Google Play i Apple Store.
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
19
Inteligentne Narzędzia NOWE
Przekształć te notatki w: ✓ 50+ Pytań Testowych ✓ Interaktywne Fiszki ✓ Pełny egzamin próbny ✓ Plany Eseju
Zgłębiaj kluczowe zasady termochemii, w tym Prawo Hessa oraz pojęcia entalpii i efektów energetycznych reakcji chemicznych. Dowiedz się, jak obliczać zmiany entalpii (ΔH) dla reakcji egzo- i endoenergetycznych oraz zrozum, jak stan skupienia reagentów wpływa na ciepło reakcji. Idealne dla studentów chemii poszukujących zrozumienia podstawowych koncepcji termodynamicznych.
Zrozumienie entalpii H oraz jej roli w reakcjach chemicznych. Omówienie szybkości reakcji, energii aktywacji, entalpii tworzenia i spalania, a także prawa Hessa i równania termochemicznego. Materiał obejmuje również różnice między reakcjami endoenergetycznymi i egzoenergetycznymi oraz regułę Lavoisiera-Laplace’a. Idealne dla studentów chemii.
Zrozumienie szybkości reakcji chemicznych, w tym wpływu katalizatorów i inhibitorów. Obejmuje wzory na szybkość reakcji oraz czynniki wpływające na tempo reakcji, takie jak temperatura i stężenie substratu. Idealne dla studentów chemii na poziomie podstawowym.
Zrozumienie entalpii reakcji chemicznych, w tym entalpii tworzenia i spalania. Dowiedz się, jak obliczać zmiany entalpii zgodnie z prawem Hessa oraz różnice między procesami egzoenergetycznymi i endoenergetycznymi. Materiał zawiera przykłady obliczeń entalpii oraz zastosowanie wzorów termochemicznych. Typ: Podsumowanie.
Zrozumienie szybkości reakcji chemicznych oraz wpływu energii na procesy chemiczne. Dowiedz się o czynnikach wpływających na szybkość reakcji, roli katalizatorów, rodzajach układów oraz procesach endo- i egzoenergetycznych. Idealne dla studentów chemii, którzy chcą zgłębić temat chemicznych kinetyk i energetyki reakcji.
Zrozumienie efektów energetycznych i szybkości reakcji chemicznych. Ta notatka omawia kluczowe pojęcia, takie jak entalpia, energia aktywacji, czynniki wpływające na szybkość reakcji oraz rolę katalizatorów i inhibitorów. Idealna dla studentów chemii, którzy chcą zgłębić temat reakcji egzotermicznych i endotermicznych oraz ich praktyczne przykłady.
App Store
Google Play
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Stefan S
użytkownik iOS
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Samantha Klich
użytkownik Androida
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Anna
użytkownik iOS
Kocham tę aplikację! Pomaga mi w zadaniach domowych, motywuje mnie i polepsza mi dzień. Dzięki tej aplikacji moje oceny się poprawiły. Lepszej aplikacji nie znajdę!🩷
Patrycja
użytkowniczka iOS
Super aplikacja! Ma odpowiedzi na wszystkie zadania. Testuję ją od paru miesięcy i jest po prostu perfekcyjna.
Szymon
użytkownik Android
Super aplikacja do nauki i sprawdzania wiedzy. Można znaleźć notatki z WSZYSTKICH przedmiotów. Polecam tym, którzy celują w oceny 5 i 6 😄
Szymon
użytkownik iOS
Aplikacja jest po prostu świetna! Wystarczy, że wpiszę w pasku wyszukiwania swój temat i od razu mam wyniki. Nie muszę oglądać 10 filmów na YouTube, żeby coś zrozumieć, więc oszczędzam swój czas. Po prostu polecam!
Kuba T
użytkownik Androida
W szkole byłem bardzo kiepski z matematyki, ale dzięki tej aplikacji radzę sobie teraz lepiej. Jestem bardzo wdzięczny, że ją stworzyliście.
Kriss
użytkownik Androida
Korzystam z Knowunity od ponad roku i jest mega! Najlepsze opcje z tej apki: ⭐️ Gotowe notatki ⭐️ Spersonalizowane treści ⭐️ Dostęp do chatu GPT W WERSJI SZKOLNEJ ⭐️ Konwersacje z innymi uczniami 🤍 NAUKA WRESZCIE NIE JEST NUDNA 🤍
Gosia
użytkowniczka Android
Bardzo lubię aplikację Knowunity, ponieważ pomaga mi w nauce. Odkąd ją mam moje oceny się poprawiają :)
Sara
użytkowniczka iOS
QUIZY I FISZKI SĄ SUPER PRZYDATNE I UWIELBIAM Knowunity AI. TO JEST DOSŁOWNIE JAK CHATGPT ALE MĄDRZEJSZY!! POMÓGŁ MI NAWET Z PROBLEMAMI Z TUSZEM DO RZĘS!! A TAKŻE Z PRAWDZIWYMI PRZEDMIOTAMI! OCZYWIŚCIE 😍😁😲🤑💗✨🎀😮
Krzysztof
użytkownik Android
Bardzo fajna aplikacja. Pomaga przygotować się do sprawdzianu, kartkówki lub odpowiedzi ustnej.
Oliwia
użytkowniczka iOS