Chemia jądrowa i struktura atomu to fascynujące podstawy, które wyjaśniają... Pokaż więcej
Kompendium chemii nieorganicznej dla maturzystów






Budowa atomu i promieniotwórczość
Atom składa się z jądra zawierającego nukleony (protony i neutrony) oraz elektronów krążących wokół jądra. Liczba atomowa (Z) określa liczbę protonów, a liczba masowa (A) sumę protonów i neutronów. Liczba elektronów w neutralnym atomie zawsze równa się liczbie protonów.
Izotopy to odmiany tego samego pierwiastka różniące się liczbą neutronów. Niektóre izotopy ulegają rozpadowi promieniotwórczemu, emitując promieniowanie:
- Promieniowanie α (jądra helu)
- Promieniowanie β (elektrony)
- Promieniowanie γ (energia)
Przemiany promieniotwórcze mogą być naturalne lub sztuczne. Każdą charakteryzuje czas połowicznego rozpadu - okres, w którym rozpada się połowa atomów danego izotopu.
💡 Promieniowanie ma różną zdolność przenikania: promieniowanie γ przenika nawet przez beton, β przez aluminium, a α zatrzymuje zwykły papier!
Model atomu według Bohra zakłada, że elektrony krążą po ściśle określonych orbitach. Elektrony w atomie opisują liczby kwantowe, które określają ich położenie i właściwości:
- Główna (n) - określa numer powłoki
- Poboczna (l) - określa podpowłokę
- Magnetyczna (m)
- Spinowa (ms)

Układ okresowy i wiązania chemiczne
Układ okresowy pierwiastków zawiera mnóstwo informacji o właściwościach pierwiastków. Warto zapamiętać kluczowe tendencje:
Aktywność chemiczna pierwiastków zmienia się regularnie - u metali rośnie w dół grupy i na lewo okresu, a u niemetali odwrotnie. Pierwiastek bardziej aktywny zawsze wypiera mniej aktywny z roztworu soli.
Elektroujemność to zdolność atomu do przyciągania elektronów. Wzrasta wraz z liczbą atomową w okresie i maleje w grupie. Im wyższa elektroujemność, tym łatwiej atom przyciąga elektrony.
💡 Różnica elektroujemności decyduje o typie wiązania: poniżej 0,4 - kowalencyjne, 0,4-1,7 - kowalencyjne spolaryzowane, powyżej 1,7 - jonowe!
Rodzaje wiązań chemicznych różnią się właściwościami:
- Wiązanie jonowe - tworzy sieć krystaliczną, ma wysoką temperaturę topnienia i dobrze przewodzi prąd w stanie ciekłym
- Wiązanie kowalencyjne - tworzy kryształy, które nie przewodzą prądu, słabo rozpuszczają się w wodzie
- Wiązanie wodorowe - powoduje anormalne temperatury wrzenia i świetną rozpuszczalność w wodzie
- Wiązanie metaliczne - tworzy "chmurę elektronów", zapewnia dobre przewodnictwo prądu i ciepła

Hybrydyzacja i substancje chemiczne
Hybrydyzacja orbitali to nakładanie się orbitali atomowych, co prowadzi do powstawania nowych orbitali o innym kształcie przestrzennym. Poboczna liczba kwantowa decyduje o kształcie orbitali, a magnetyczna o ich orientacji w przestrzeni.
Wodór tworzy kwasy i wodorki. Kwasy są substancjami, które w wodzie uwalniają jony wodorowe. Możemy je otrzymać na kilka sposobów, na przykład przez reakcję metalu z wodą. Kwas mocny zawsze wypiera z roztworu soli kwas słabszy.
Zasady to głównie wodorotlenki metali 1 i 2 grupy (z wyjątkiem berylu). Są to substancje stałe, dobrze rozpuszczalne w wodzie. Do ich wykrywania używa się wskaźników, np. fenoloftaleiny, która w środowisku zasadowym przybiera malinowy kolor.
💡 Amfotery to związki wykazujące właściwości zarówno kwasowe jak i zasadowe, np. wodorotlenki glinu, chromu, cynku czy miedzi!
Sole powstają z metali i reszt kwasowych. Każda sól podczas rozpuszczania dysocjuje na kation metalu i anion reszty kwasowej. Ciekawym typem soli są wodorosole (np. NaHCO₃), które zawierają jeszcze wodór i są bardzo dobrze rozpuszczalne w wodzie, co ma wpływ na proces krasowienia skał wapiennych.
Podstawy obliczeń chemicznych
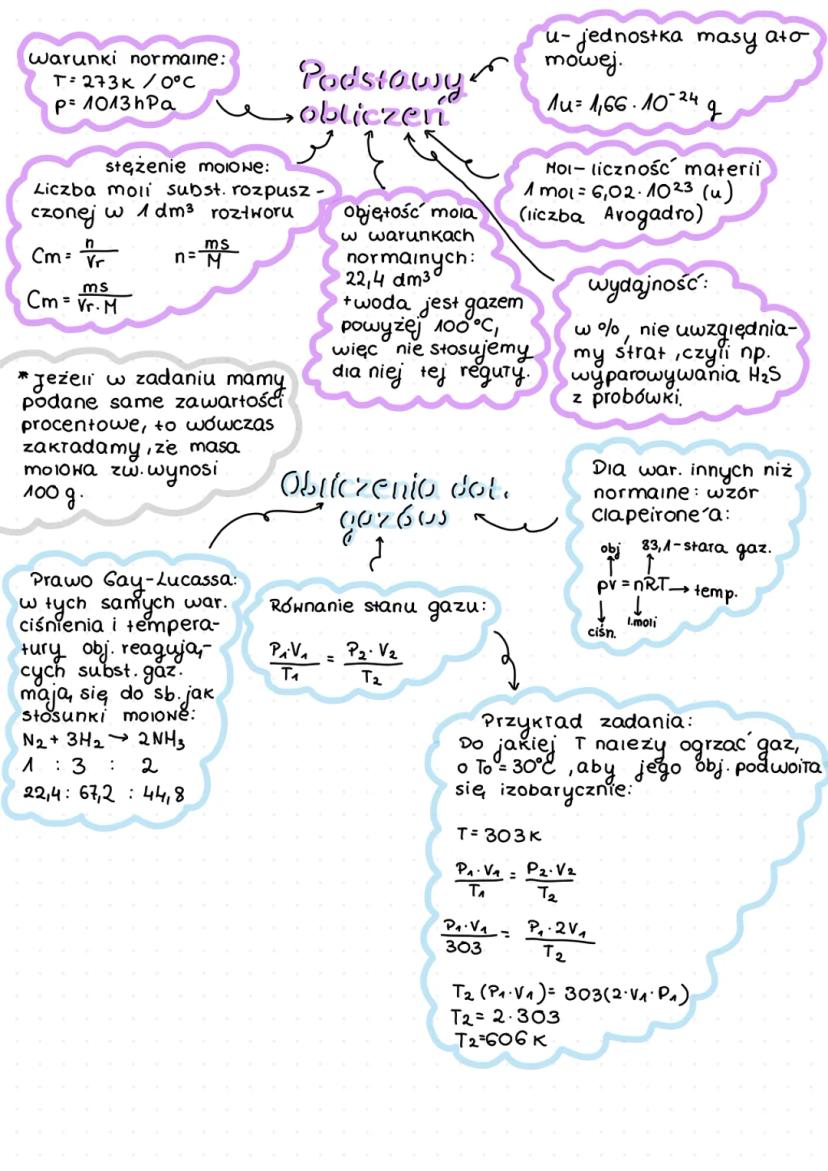
Obliczenia w chemii wymagają znajomości kilku kluczowych pojęć i wzorów. Mol to podstawowa jednostka ilości materii zawierająca liczbę Avogadra (6,02·10²³) cząsteczek. Masa jednego mola substancji wyrażona w gramach równa się jej masie molowej.
Stężenie molowe to liczba moli substancji rozpuszczonej w 1 dm³ roztworu:
- Cm = n/Vr (gdzie n to liczba moli, a Vr to objętość roztworu)
- n = m/Ms (gdzie m to masa substancji, a Ms to masa molowa)
W warunkach normalnych jeden mol gazu zajmuje objętość 22,4 dm³. Korzystając z tego, możemy stosować prawo Gay-Lussaca, według którego objętości reagujących substancji gazowych mają się do siebie jak stosunki molowe.
💡 Pamiętaj, że objętość mola dotyczy tylko gazów! Woda jest gazem dopiero powyżej 100°C, więc dla niej tej reguły nie stosujemy w normalnych warunkach.
Dla gazów w różnych warunkach stosujemy równanie stanu gazu (równanie Clapeyrona):
- pV = nRT
- P₁V₁/T₁ = P₂V₂/T₂
Obliczając wydajność reakcji uwzględniamy straty, np. wyparowywanie substancji z probówki, i wyrażamy ją w procentach.
Roztwory i kinetyka reakcji chemicznych
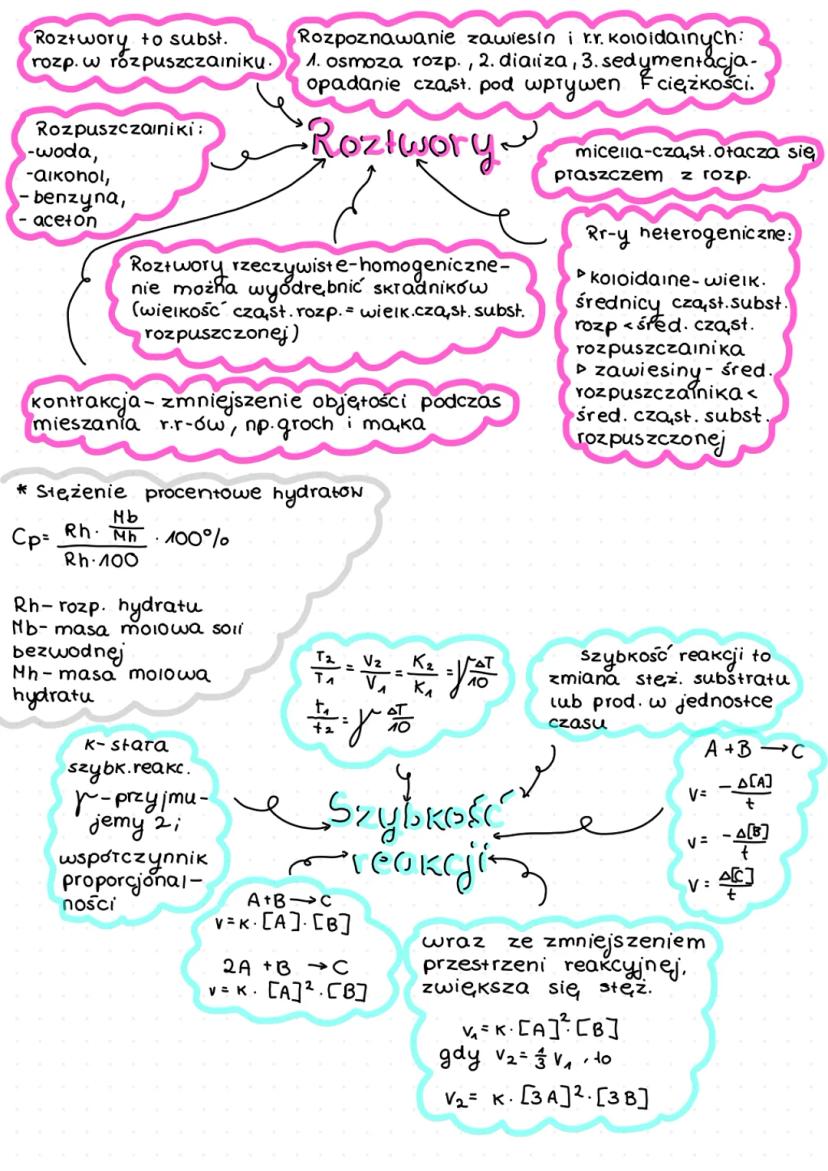
Roztwory to mieszaniny substancji rozpuszczonych w rozpuszczalnikach (np. woda, alkohol, benzyna). Dzielimy je na:
- Roztwory rzeczywiste - homogeniczne, nie można wyodrębnić składników
- Roztwory koloidalne - cząstki substancji rozpuszczonej są większe niż cząstki rozpuszczalnika, tworząc micelle
- Zawiesiny - heterogeniczne, z cząstkami większymi od cząstek rozpuszczalnika
Podczas mieszania roztworów może nastąpić kontrakcja - zmniejszenie całkowitej objętości mieszaniny (podobnie jak gdy mieszamy groch z mąką).
💡 Zawiesiny i roztwory koloidalne można rozpoznać przez: osmozę, dializę lub sedymentację (opadanie cząstek pod wpływem siły ciężkości)!
Szybkość reakcji to zmiana stężenia substratów lub produktów w jednostce czasu. Dla reakcji A + B → C wyrażamy ją wzorem:
- v = -Δ[A]/t = -Δ[B]/t = Δ[C]/t = k[A][B]
Szybkość reakcji zależy od:
- Stężenia substratów
- Temperatury
- Przestrzeni reakcyjnej
Dla zależności temperaturowej stosujemy wzór: T₂/T₁ = V₂/V₁ = K₂/K₁ = γ^, gdzie γ to współczynnik proporcjonalności (zwykle przyjmujemy wartość 2).
Równowaga chemiczna
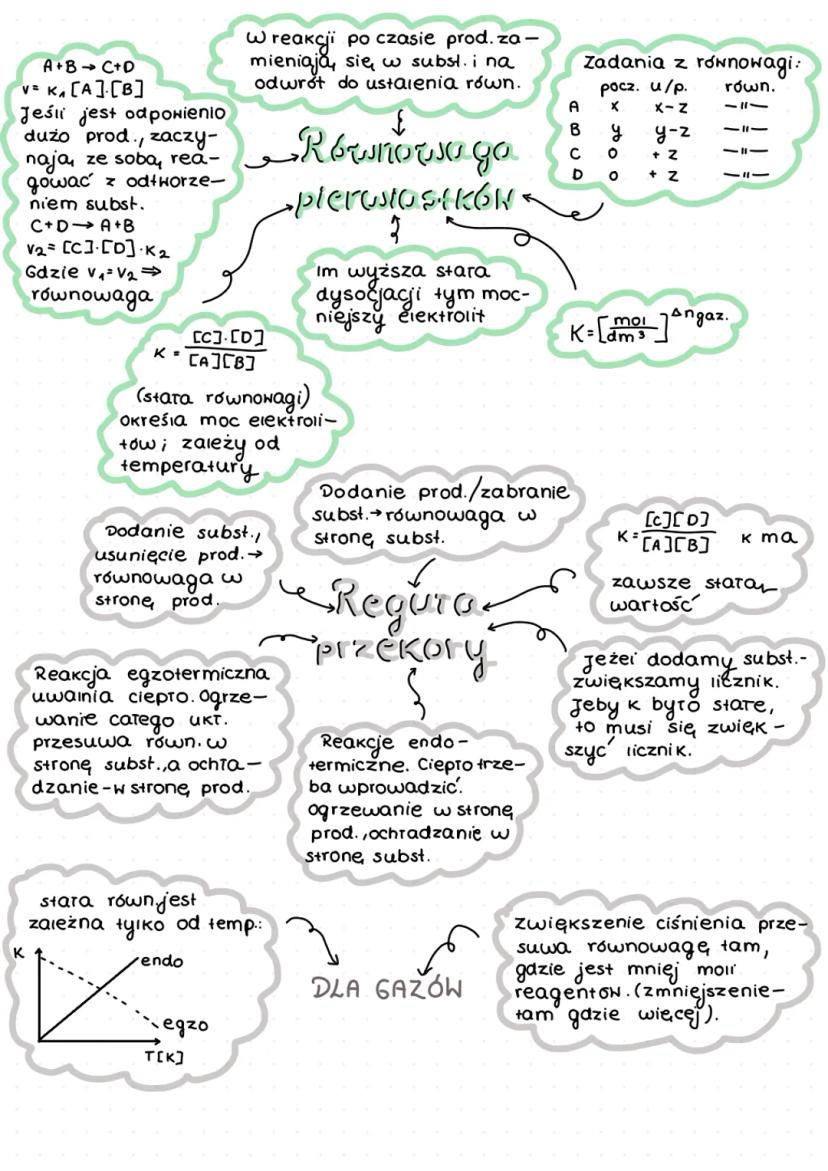
W wielu reakcjach po pewnym czasie produkty zaczynają reagować ze sobą, odtwarzając substraty. Gdy szybkość reakcji w obu kierunkach zrównuje się, mówimy o równowadze chemicznej.
Dla reakcji A + B ⇄ C + D:
- Szybkość reakcji w prawo: v₁ = k₁[A][B]
- Szybkość reakcji w lewo: v₂ = k₂[C][D]
- W stanie równowagi: v₁ = v₂
Stała równowagi K = [C][D]/[A][B] określa stosunek stężeń produktów do substratów w stanie równowagi. Jest ona zależna tylko od temperatury i określa moc elektrolitów.
💡 Stała równowagi zawsze ma stałą wartość w danej temperaturze! To kluczowa informacja przy rozwiązywaniu zadań z równowagą chemiczną.
Na równowagę chemiczną możemy wpływać zgodnie z regułą przekory :
- Dodanie substratów/usunięcie produktów → równowaga przesuwa się w stronę produktów
- Dodanie produktów/usunięcie substratów → równowaga przesuwa się w stronę substratów
W przypadku reakcji egzotermicznych (uwalniających ciepło):
- Ogrzewanie → równowaga przesuwa się w stronę substratów
- Ochładzanie → równowaga przesuwa się w stronę produktów
Dla reakcji endotermicznych (pochłaniających ciepło) jest odwrotnie.
W przypadku gazów, zwiększenie ciśnienia przesuwa równowagę w stronę, gdzie jest mniej moli reagentów.

Kataliza i termochemia
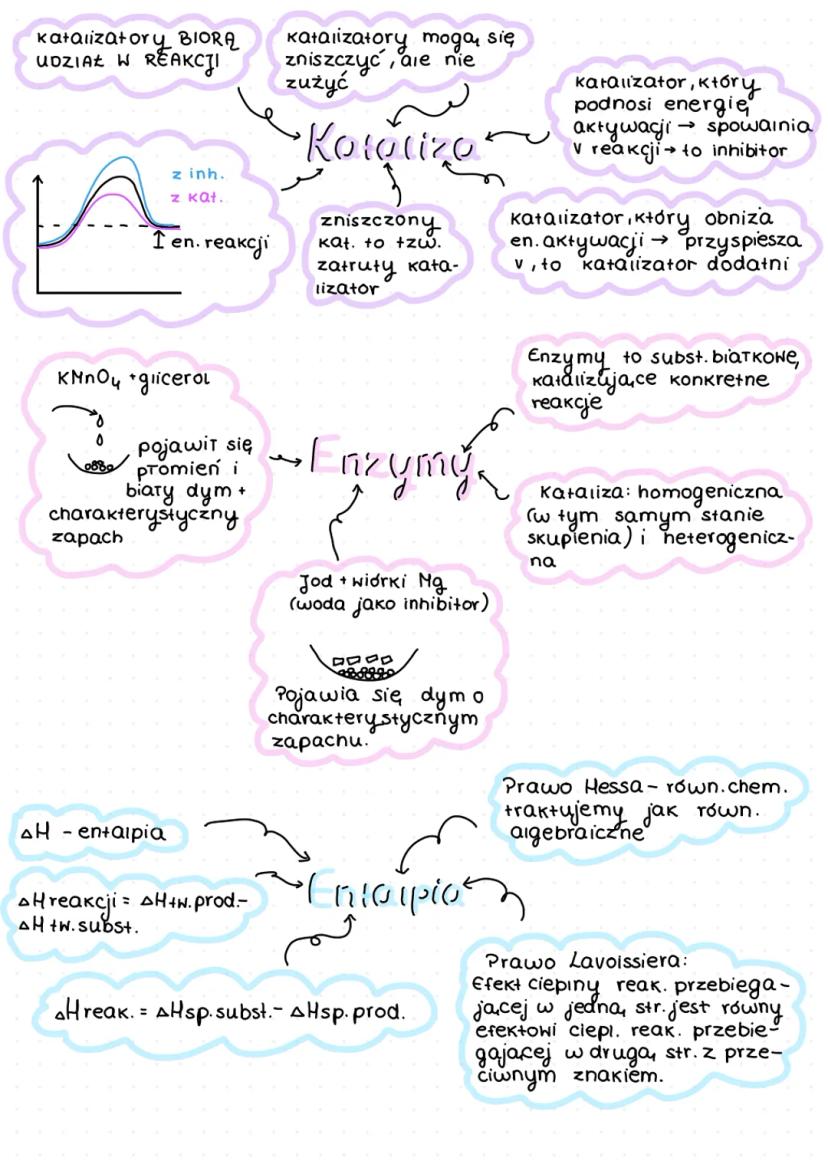
Katalizatory to substancje, które biorą udział w reakcji, ale się nie zużywają (mogą jednak ulec zniszczeniu, co nazywamy "zatruciem katalizatora"). Katalizatory przyspieszają reakcje przez obniżenie energii aktywacji.
Rozróżniamy:
- Katalizatory dodatnie - obniżają energię aktywacji i przyspieszają reakcję
- Inhibitory - podnoszą energię aktywacji i spowalniają reakcję
- Enzymy - substancje białkowe katalizujące konkretne reakcje
💡 Kataliza może być homogeniczna (katalizator i reagenty w tym samym stanie skupienia) lub heterogeniczna (w różnych stanach skupienia).
Efekty cieplne reakcji opisujemy przez entalpię (ΔH):
- Entalpia reakcji = entalpia tworzenia produktów - entalpia tworzenia substratów
- Lub: entalpia spalania substratów - entalpia spalania produktów
Prawo Hessa mówi, że równania chemiczne możemy traktować jak równania algebraiczne. Natomiast prawo Lavoisiera stwierdza, że efekt cieplny reakcji przebiegającej w jedną stronę jest równy efektowi cieplnemu reakcji przebiegającej w drugą stronę, ale z przeciwnym znakiem.
Ciekawe przykłady katalizy:
- KMnO₄ + glicerol - pojawia się płomień i biały dym
- Jod + wiórki magnezu (woda jako inhibitor) - powstaje dym o charakterystycznym zapachu
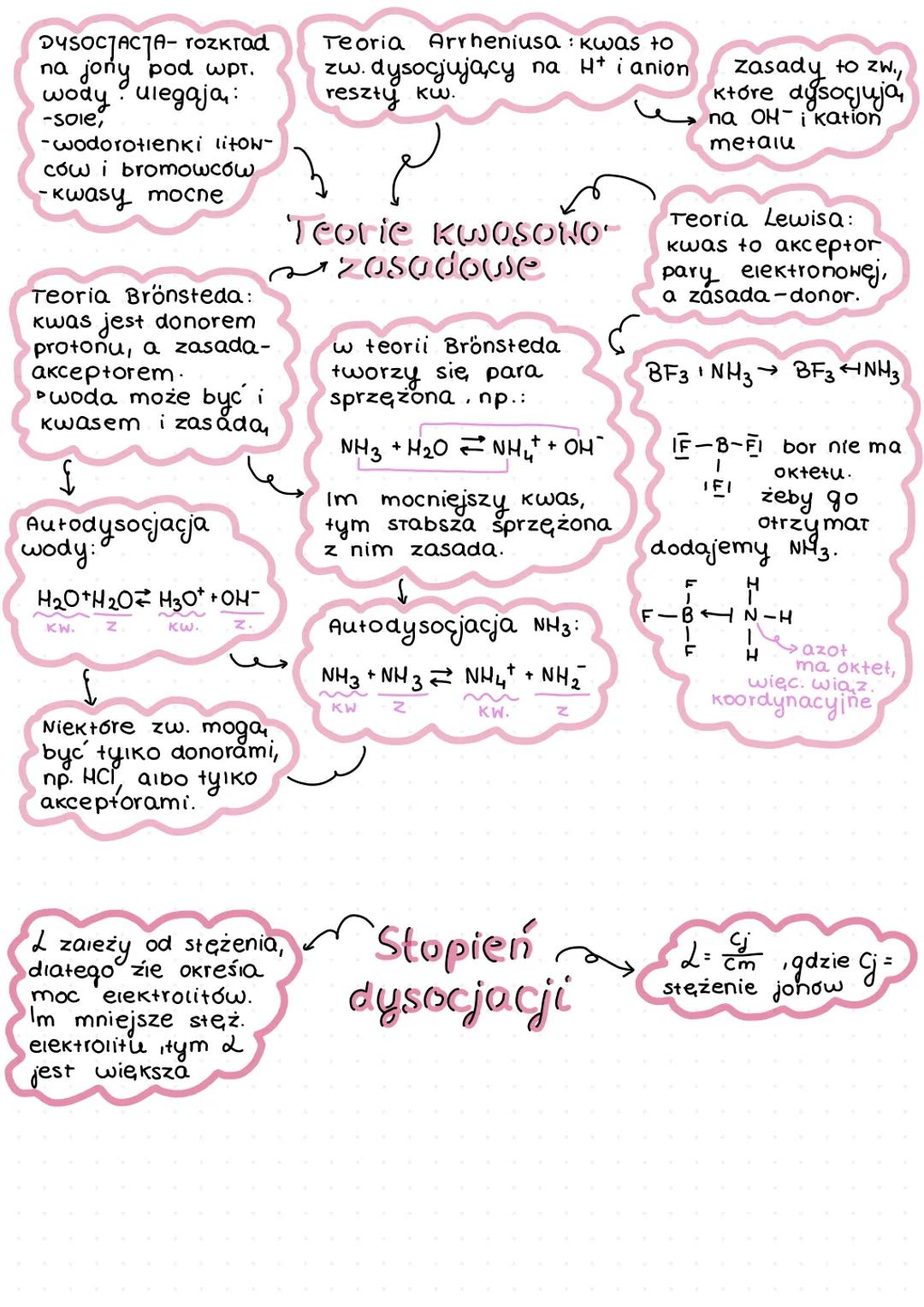
Teorie kwasowo-zasadowe i dysocjacja
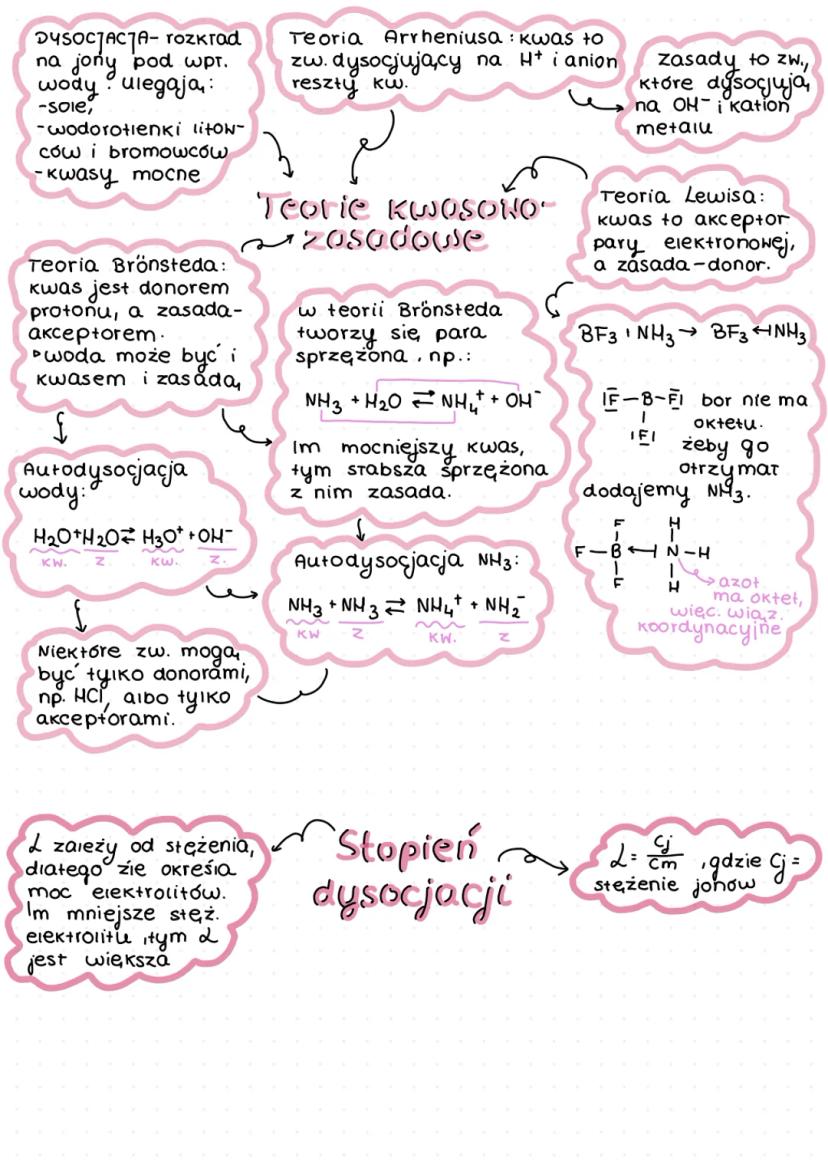
Dysocjacja to rozkład związku chemicznego na jony pod wpływem wody. Dysocjacji ulegają sole, wodorotlenki litowców i berylowców oraz mocne kwasy.
Istnieją różne teorie kwasowo-zasadowe:
-
Teoria Arrheniusa:
- Kwasy to związki dysocjujące na H⁺ i anion reszty kwasowej
- Zasady to związki dysocjujące na OH⁻ i kation metalu
-
Teoria Brönsteda:
- Kwas jest donorem protonu
- Zasada jest akceptorem protonu
- Woda może pełnić rolę zarówno kwasu jak i zasady (autodysocjacja)
💡 W teorii Brönsteda tworzy się para sprzężona kwas-zasada. Im mocniejszy kwas, tym słabsza sprzężona z nim zasada!
- Teoria Lewisa:
- Kwas to akceptor pary elektronowej
- Zasada to donor pary elektronowej
- Przykład: BF₃ + NH₃ → BF₃←NH₃ (wiązanie koordynacyjne)
Stopień dysocjacji (α) łączy stężenie jonów (cᵢ) ze stężeniem molowym elektrolitu (cₘ): α = cᵢ/cₘ Im wyższa stała dysocjacji (K), tym mocniejszy elektrolit. Stała dysocjacji zależy od temperatury.
Dla słabych elektrolitów, gdy α ≤ 5% lub cₘ ≥ 400, możemy stosować uproszczony wzór: K = α² · cₘ

pH roztworów i iloczyn rozpuszczalności
pH to ujemny logarytm dziesiętny ze stężenia jonów H⁺. Skala pH obejmuje wartości od 0 do 14, gdzie:
- pH < 7 - roztwór kwasowy
- pH = 7 - roztwór obojętny
- pH > 7 - roztwór zasadowy
Zawsze zachodzi zależność: pH + pOH = 14
Przykładowo, jeśli [H⁺] = 10⁻² mol/dm³, to pH = 2, a [OH⁻] = 10⁻¹² mol/dm³ i pOH = 12.
💡 Zmiana pH o jedną jednostkę oznacza 10-krotną zmianę stężenia jonów wodorowych! To dlatego skala pH jest logarytmiczna.
Iloczyn rozpuszczalności (Kₛₒ) to stała równowagi dla reakcji rozpuszczania osadu. Dotyczy wyłącznie słabo rozpuszczalnych soli i wodorotlenków. Np. dla AgCl:
- AgCl ⇄ Ag⁺ + Cl⁻
- Kₛₒ = [Ag⁺][Cl⁻] = x²
- Rozpuszczalność molowa x = √Kₛₒ
Im mniejszy iloczyn rozpuszczalności, tym trudniej rozpuszczalny osad. Osad wytrąci się, gdy iloczyn stężeń jonów przekroczy wartość Kₛₒ, a rozpuści się, gdy przesuniemy równowagę w stronę produktów.
W praktyce za nierozpuszczalne w wodzie uważa się związki takie jak: Cu(OH)₂, Mg(OH)₂, PbSO₄, FeS, Zn₃(PO₄)₂, które mogą stanowić produkty reakcji jonowej.

Reakcje jonowe i struktura przestrzenna cząsteczek
Reakcje jonowe to reakcje przebiegające w roztworach wodnych między jonami. Produktami reakcji jonowej mogą być:
- Osad
- Słaby elektrolit
- Gaz
Przykład: AgNO₃ + NaBr → AgBr↓ + NaNO₃ Zapis jonowy: Ag⁺ + NO₃⁻ + Na⁺ + Br⁻ → AgBr↓ + Na⁺ + NO₃⁻
Aby przewidzieć, czy utworzy się osad, należy sprawdzić w tablicach rozpuszczalność potencjalnego produktu.
Metoda VSEPR (odpychania par elektronów walencyjnych) pozwala określić kształt przestrzenny cząsteczek:
- Określamy liczbę elektronów walencyjnych w całym związku
- Obliczamy liczbę wolnych par elektronów: lwpe = lew - 4m - n (gdzie m to liczba atomów przyłączonych do atomu centralnego, n to liczba wiązań wielokrotnych)
- Ustalamy liczbę przestrzenną: lp = lwpe + m + n
💡 Cząsteczka nie jest dipolem, gdy liczba przestrzenna równa się liczbie atomów przyłączonych do atomu centralnego. Na przykład SO₃²⁻ jest dipolem, bo lp = 4, a m = 3.
Struktura przestrzenna cząsteczek wpływa na ich właściwości, w tym polarność, rozpuszczalność i reaktywność.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: chemia nieorganiczna
2Charakterystyka Fluorowców
Zgłębiaj właściwości chemiczne fluorowców (grupa 17) w tym fluor, brom, jod i chlor. Dowiedz się o ich reakcjach, zastosowaniach oraz strukturze chemicznej. Idealne dla uczniów chemii na poziomie rozszerzonym. Materiał zawiera kluczowe informacje o tlenkach, kwasach i związkach tych pierwiastków.
Właściwości Żelaza i Związków
Zgłębiaj właściwości chemiczne żelaza, jego stany utlenienia oraz reakcje z kwasami. Dowiedz się o kolorach soli żelaza, amfoteryczności wodorotlenków oraz stabilności jonów Fe^{2+} i Fe^{3+}. Materiał przeznaczony dla uczniów na poziomie rozszerzonym chemii nieorganicznej.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.
Kompendium chemii nieorganicznej dla maturzystów
Chemia jądrowa i struktura atomu to fascynujące podstawy, które wyjaśniają naturę materii i jej przemiany. Poznamy budowę atomu, promieniotwórczość, wiązania chemiczne i inne kluczowe zagadnienia, które pozwolą Ci zrozumieć, jak działają pierwiastki i związki chemiczne.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Budowa atomu i promieniotwórczość
Atom składa się z jądra zawierającego nukleony (protony i neutrony) oraz elektronów krążących wokół jądra. Liczba atomowa (Z) określa liczbę protonów, a liczba masowa (A) sumę protonów i neutronów. Liczba elektronów w neutralnym atomie zawsze równa się liczbie protonów.
Izotopy to odmiany tego samego pierwiastka różniące się liczbą neutronów. Niektóre izotopy ulegają rozpadowi promieniotwórczemu, emitując promieniowanie:
- Promieniowanie α (jądra helu)
- Promieniowanie β (elektrony)
- Promieniowanie γ (energia)
Przemiany promieniotwórcze mogą być naturalne lub sztuczne. Każdą charakteryzuje czas połowicznego rozpadu - okres, w którym rozpada się połowa atomów danego izotopu.
💡 Promieniowanie ma różną zdolność przenikania: promieniowanie γ przenika nawet przez beton, β przez aluminium, a α zatrzymuje zwykły papier!
Model atomu według Bohra zakłada, że elektrony krążą po ściśle określonych orbitach. Elektrony w atomie opisują liczby kwantowe, które określają ich położenie i właściwości:
- Główna (n) - określa numer powłoki
- Poboczna (l) - określa podpowłokę
- Magnetyczna (m)
- Spinowa (ms)

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Układ okresowy i wiązania chemiczne
Układ okresowy pierwiastków zawiera mnóstwo informacji o właściwościach pierwiastków. Warto zapamiętać kluczowe tendencje:
Aktywność chemiczna pierwiastków zmienia się regularnie - u metali rośnie w dół grupy i na lewo okresu, a u niemetali odwrotnie. Pierwiastek bardziej aktywny zawsze wypiera mniej aktywny z roztworu soli.
Elektroujemność to zdolność atomu do przyciągania elektronów. Wzrasta wraz z liczbą atomową w okresie i maleje w grupie. Im wyższa elektroujemność, tym łatwiej atom przyciąga elektrony.
💡 Różnica elektroujemności decyduje o typie wiązania: poniżej 0,4 - kowalencyjne, 0,4-1,7 - kowalencyjne spolaryzowane, powyżej 1,7 - jonowe!
Rodzaje wiązań chemicznych różnią się właściwościami:
- Wiązanie jonowe - tworzy sieć krystaliczną, ma wysoką temperaturę topnienia i dobrze przewodzi prąd w stanie ciekłym
- Wiązanie kowalencyjne - tworzy kryształy, które nie przewodzą prądu, słabo rozpuszczają się w wodzie
- Wiązanie wodorowe - powoduje anormalne temperatury wrzenia i świetną rozpuszczalność w wodzie
- Wiązanie metaliczne - tworzy "chmurę elektronów", zapewnia dobre przewodnictwo prądu i ciepła

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Hybrydyzacja i substancje chemiczne
Hybrydyzacja orbitali to nakładanie się orbitali atomowych, co prowadzi do powstawania nowych orbitali o innym kształcie przestrzennym. Poboczna liczba kwantowa decyduje o kształcie orbitali, a magnetyczna o ich orientacji w przestrzeni.
Wodór tworzy kwasy i wodorki. Kwasy są substancjami, które w wodzie uwalniają jony wodorowe. Możemy je otrzymać na kilka sposobów, na przykład przez reakcję metalu z wodą. Kwas mocny zawsze wypiera z roztworu soli kwas słabszy.
Zasady to głównie wodorotlenki metali 1 i 2 grupy (z wyjątkiem berylu). Są to substancje stałe, dobrze rozpuszczalne w wodzie. Do ich wykrywania używa się wskaźników, np. fenoloftaleiny, która w środowisku zasadowym przybiera malinowy kolor.
💡 Amfotery to związki wykazujące właściwości zarówno kwasowe jak i zasadowe, np. wodorotlenki glinu, chromu, cynku czy miedzi!
Sole powstają z metali i reszt kwasowych. Każda sól podczas rozpuszczania dysocjuje na kation metalu i anion reszty kwasowej. Ciekawym typem soli są wodorosole (np. NaHCO₃), które zawierają jeszcze wodór i są bardzo dobrze rozpuszczalne w wodzie, co ma wpływ na proces krasowienia skał wapiennych.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Podstawy obliczeń chemicznych
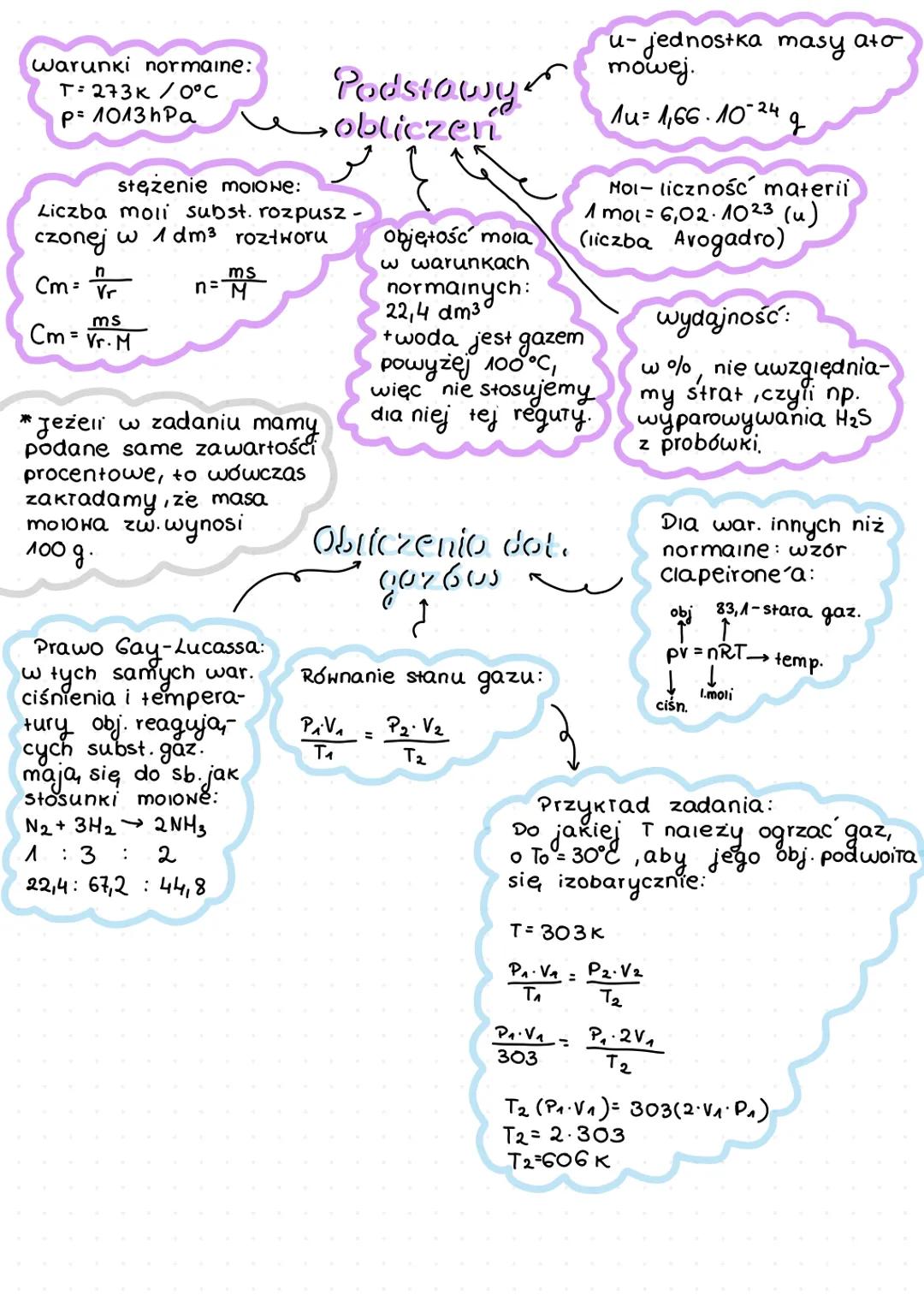
Obliczenia w chemii wymagają znajomości kilku kluczowych pojęć i wzorów. Mol to podstawowa jednostka ilości materii zawierająca liczbę Avogadra (6,02·10²³) cząsteczek. Masa jednego mola substancji wyrażona w gramach równa się jej masie molowej.
Stężenie molowe to liczba moli substancji rozpuszczonej w 1 dm³ roztworu:
- Cm = n/Vr (gdzie n to liczba moli, a Vr to objętość roztworu)
- n = m/Ms (gdzie m to masa substancji, a Ms to masa molowa)
W warunkach normalnych jeden mol gazu zajmuje objętość 22,4 dm³. Korzystając z tego, możemy stosować prawo Gay-Lussaca, według którego objętości reagujących substancji gazowych mają się do siebie jak stosunki molowe.
💡 Pamiętaj, że objętość mola dotyczy tylko gazów! Woda jest gazem dopiero powyżej 100°C, więc dla niej tej reguły nie stosujemy w normalnych warunkach.
Dla gazów w różnych warunkach stosujemy równanie stanu gazu (równanie Clapeyrona):
- pV = nRT
- P₁V₁/T₁ = P₂V₂/T₂
Obliczając wydajność reakcji uwzględniamy straty, np. wyparowywanie substancji z probówki, i wyrażamy ją w procentach.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Roztwory i kinetyka reakcji chemicznych
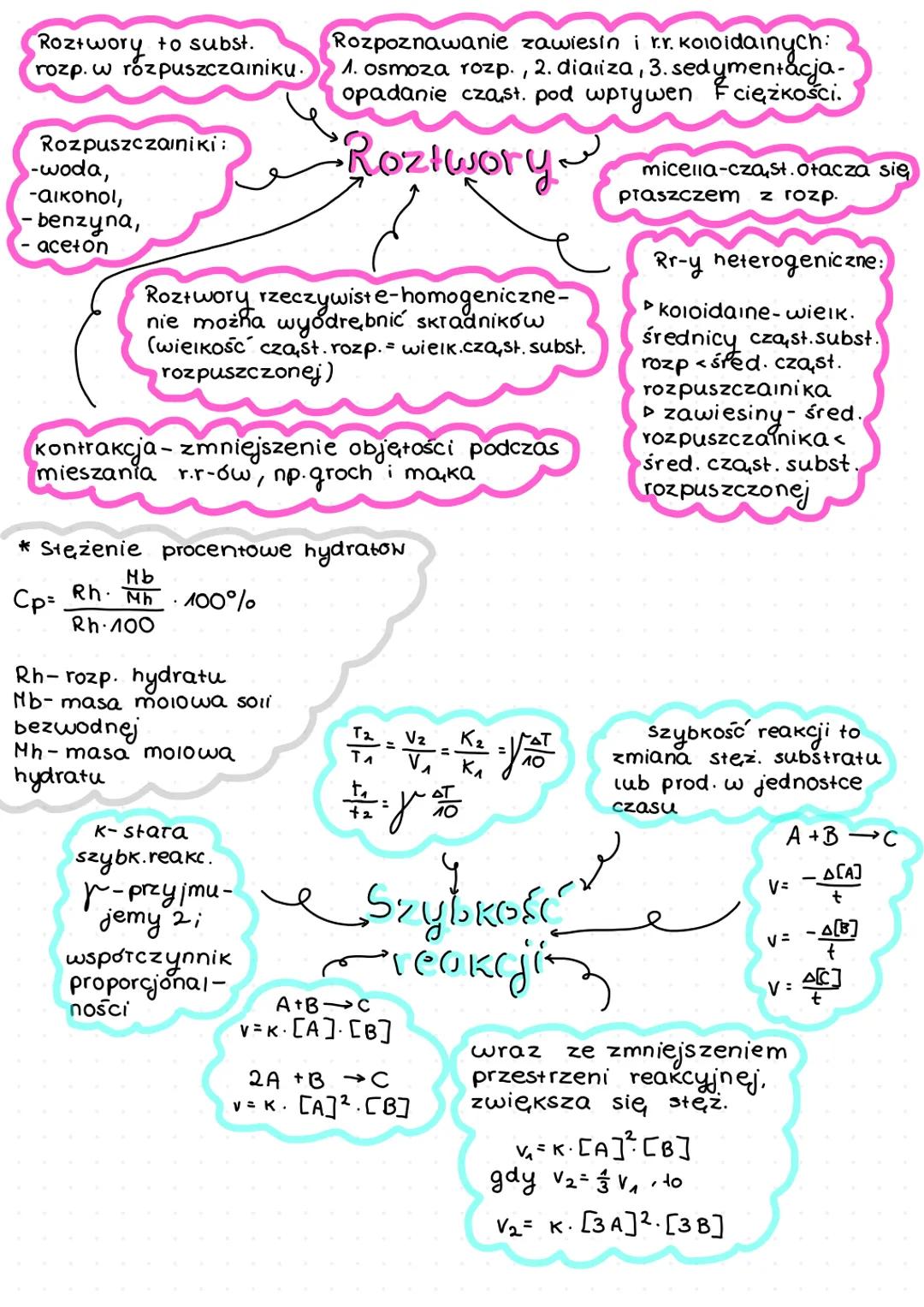
Roztwory to mieszaniny substancji rozpuszczonych w rozpuszczalnikach (np. woda, alkohol, benzyna). Dzielimy je na:
- Roztwory rzeczywiste - homogeniczne, nie można wyodrębnić składników
- Roztwory koloidalne - cząstki substancji rozpuszczonej są większe niż cząstki rozpuszczalnika, tworząc micelle
- Zawiesiny - heterogeniczne, z cząstkami większymi od cząstek rozpuszczalnika
Podczas mieszania roztworów może nastąpić kontrakcja - zmniejszenie całkowitej objętości mieszaniny (podobnie jak gdy mieszamy groch z mąką).
💡 Zawiesiny i roztwory koloidalne można rozpoznać przez: osmozę, dializę lub sedymentację (opadanie cząstek pod wpływem siły ciężkości)!
Szybkość reakcji to zmiana stężenia substratów lub produktów w jednostce czasu. Dla reakcji A + B → C wyrażamy ją wzorem:
- v = -Δ[A]/t = -Δ[B]/t = Δ[C]/t = k[A][B]
Szybkość reakcji zależy od:
- Stężenia substratów
- Temperatury
- Przestrzeni reakcyjnej
Dla zależności temperaturowej stosujemy wzór: T₂/T₁ = V₂/V₁ = K₂/K₁ = γ^, gdzie γ to współczynnik proporcjonalności (zwykle przyjmujemy wartość 2).

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Równowaga chemiczna
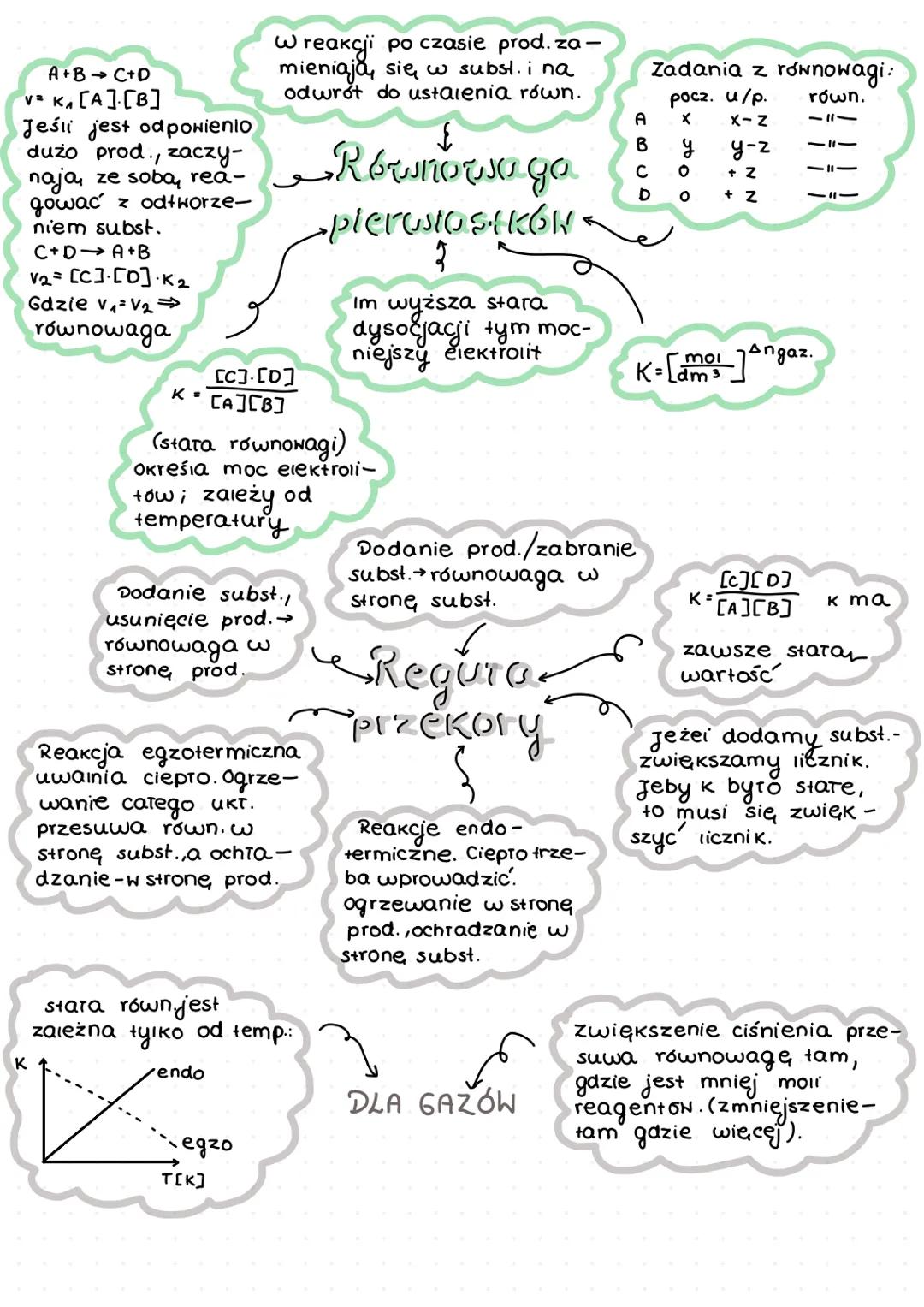
W wielu reakcjach po pewnym czasie produkty zaczynają reagować ze sobą, odtwarzając substraty. Gdy szybkość reakcji w obu kierunkach zrównuje się, mówimy o równowadze chemicznej.
Dla reakcji A + B ⇄ C + D:
- Szybkość reakcji w prawo: v₁ = k₁[A][B]
- Szybkość reakcji w lewo: v₂ = k₂[C][D]
- W stanie równowagi: v₁ = v₂
Stała równowagi K = [C][D]/[A][B] określa stosunek stężeń produktów do substratów w stanie równowagi. Jest ona zależna tylko od temperatury i określa moc elektrolitów.
💡 Stała równowagi zawsze ma stałą wartość w danej temperaturze! To kluczowa informacja przy rozwiązywaniu zadań z równowagą chemiczną.
Na równowagę chemiczną możemy wpływać zgodnie z regułą przekory :
- Dodanie substratów/usunięcie produktów → równowaga przesuwa się w stronę produktów
- Dodanie produktów/usunięcie substratów → równowaga przesuwa się w stronę substratów
W przypadku reakcji egzotermicznych (uwalniających ciepło):
- Ogrzewanie → równowaga przesuwa się w stronę substratów
- Ochładzanie → równowaga przesuwa się w stronę produktów
Dla reakcji endotermicznych (pochłaniających ciepło) jest odwrotnie.
W przypadku gazów, zwiększenie ciśnienia przesuwa równowagę w stronę, gdzie jest mniej moli reagentów.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Kataliza i termochemia
Katalizatory to substancje, które biorą udział w reakcji, ale się nie zużywają (mogą jednak ulec zniszczeniu, co nazywamy "zatruciem katalizatora"). Katalizatory przyspieszają reakcje przez obniżenie energii aktywacji.
Rozróżniamy:
- Katalizatory dodatnie - obniżają energię aktywacji i przyspieszają reakcję
- Inhibitory - podnoszą energię aktywacji i spowalniają reakcję
- Enzymy - substancje białkowe katalizujące konkretne reakcje
💡 Kataliza może być homogeniczna (katalizator i reagenty w tym samym stanie skupienia) lub heterogeniczna (w różnych stanach skupienia).
Efekty cieplne reakcji opisujemy przez entalpię (ΔH):
- Entalpia reakcji = entalpia tworzenia produktów - entalpia tworzenia substratów
- Lub: entalpia spalania substratów - entalpia spalania produktów
Prawo Hessa mówi, że równania chemiczne możemy traktować jak równania algebraiczne. Natomiast prawo Lavoisiera stwierdza, że efekt cieplny reakcji przebiegającej w jedną stronę jest równy efektowi cieplnemu reakcji przebiegającej w drugą stronę, ale z przeciwnym znakiem.
Ciekawe przykłady katalizy:
- KMnO₄ + glicerol - pojawia się płomień i biały dym
- Jod + wiórki magnezu (woda jako inhibitor) - powstaje dym o charakterystycznym zapachu

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Teorie kwasowo-zasadowe i dysocjacja
Dysocjacja to rozkład związku chemicznego na jony pod wpływem wody. Dysocjacji ulegają sole, wodorotlenki litowców i berylowców oraz mocne kwasy.
Istnieją różne teorie kwasowo-zasadowe:
-
Teoria Arrheniusa:
- Kwasy to związki dysocjujące na H⁺ i anion reszty kwasowej
- Zasady to związki dysocjujące na OH⁻ i kation metalu
-
Teoria Brönsteda:
- Kwas jest donorem protonu
- Zasada jest akceptorem protonu
- Woda może pełnić rolę zarówno kwasu jak i zasady (autodysocjacja)
💡 W teorii Brönsteda tworzy się para sprzężona kwas-zasada. Im mocniejszy kwas, tym słabsza sprzężona z nim zasada!
- Teoria Lewisa:
- Kwas to akceptor pary elektronowej
- Zasada to donor pary elektronowej
- Przykład: BF₃ + NH₃ → BF₃←NH₃ (wiązanie koordynacyjne)
Stopień dysocjacji (α) łączy stężenie jonów (cᵢ) ze stężeniem molowym elektrolitu (cₘ): α = cᵢ/cₘ Im wyższa stała dysocjacji (K), tym mocniejszy elektrolit. Stała dysocjacji zależy od temperatury.
Dla słabych elektrolitów, gdy α ≤ 5% lub cₘ ≥ 400, możemy stosować uproszczony wzór: K = α² · cₘ

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
pH roztworów i iloczyn rozpuszczalności
pH to ujemny logarytm dziesiętny ze stężenia jonów H⁺. Skala pH obejmuje wartości od 0 do 14, gdzie:
- pH < 7 - roztwór kwasowy
- pH = 7 - roztwór obojętny
- pH > 7 - roztwór zasadowy
Zawsze zachodzi zależność: pH + pOH = 14
Przykładowo, jeśli [H⁺] = 10⁻² mol/dm³, to pH = 2, a [OH⁻] = 10⁻¹² mol/dm³ i pOH = 12.
💡 Zmiana pH o jedną jednostkę oznacza 10-krotną zmianę stężenia jonów wodorowych! To dlatego skala pH jest logarytmiczna.
Iloczyn rozpuszczalności (Kₛₒ) to stała równowagi dla reakcji rozpuszczania osadu. Dotyczy wyłącznie słabo rozpuszczalnych soli i wodorotlenków. Np. dla AgCl:
- AgCl ⇄ Ag⁺ + Cl⁻
- Kₛₒ = [Ag⁺][Cl⁻] = x²
- Rozpuszczalność molowa x = √Kₛₒ
Im mniejszy iloczyn rozpuszczalności, tym trudniej rozpuszczalny osad. Osad wytrąci się, gdy iloczyn stężeń jonów przekroczy wartość Kₛₒ, a rozpuści się, gdy przesuniemy równowagę w stronę produktów.
W praktyce za nierozpuszczalne w wodzie uważa się związki takie jak: Cu(OH)₂, Mg(OH)₂, PbSO₄, FeS, Zn₃(PO₄)₂, które mogą stanowić produkty reakcji jonowej.

Zarejestruj się, aby zobaczyć notatkę. To nic nie kosztuje!
- Dostęp do wszystkich materiałów
- Popraw swoje oceny
- Dołącz do milionów studentów
Reakcje jonowe i struktura przestrzenna cząsteczek
Reakcje jonowe to reakcje przebiegające w roztworach wodnych między jonami. Produktami reakcji jonowej mogą być:
- Osad
- Słaby elektrolit
- Gaz
Przykład: AgNO₃ + NaBr → AgBr↓ + NaNO₃ Zapis jonowy: Ag⁺ + NO₃⁻ + Na⁺ + Br⁻ → AgBr↓ + Na⁺ + NO₃⁻
Aby przewidzieć, czy utworzy się osad, należy sprawdzić w tablicach rozpuszczalność potencjalnego produktu.
Metoda VSEPR (odpychania par elektronów walencyjnych) pozwala określić kształt przestrzenny cząsteczek:
- Określamy liczbę elektronów walencyjnych w całym związku
- Obliczamy liczbę wolnych par elektronów: lwpe = lew - 4m - n (gdzie m to liczba atomów przyłączonych do atomu centralnego, n to liczba wiązań wielokrotnych)
- Ustalamy liczbę przestrzenną: lp = lwpe + m + n
💡 Cząsteczka nie jest dipolem, gdy liczba przestrzenna równa się liczbie atomów przyłączonych do atomu centralnego. Na przykład SO₃²⁻ jest dipolem, bo lp = 4, a m = 3.
Struktura przestrzenna cząsteczek wpływa na ich właściwości, w tym polarność, rozpuszczalność i reaktywność.
Myśleliśmy, że nigdy nie zapytasz...
Czym jest Towarzysz AI z Knowunity?
Nasz asystent AI jest specjalnie dostosowany do potrzeb uczniów. W oparciu o miliony treści, które mamy na platformie, możemy udzielać uczniom naprawdę znaczących i trafnych odpowiedzi. Ale nie chodzi tylko o odpowiedzi, towarzysz prowadzi również uczniów przez codzienne wyzwania związane z nauką, ze spersonalizowanymi planami nauki, quizami lub treściami na czacie i 100% personalizacją opartą na umiejętnościach i rozwoju uczniów.
Gdzie mogę pobrać aplikację Knowunity?
Aplikację możesz pobrać z Google Play i Apple Store.
Czy aplikacja Knowunity naprawdę jest darmowa?
Tak, masz całkowicie darmowy dostęp do wszystkich notatek w aplikacji, możesz w każdej chwili rozmawiać z Ekspertami lub ich obserwować. Możesz użyć punktów, aby odblokować pewne funkcje w aplikacji, które również możesz otrzymać za darmo. Dodatkowo oferujemy usługę Knowunity Premium, która pozwala na odblokowanie większej liczby funkcji.
Podobne notatki
Najpopularniejsze notatki: chemia nieorganiczna
2Charakterystyka Fluorowców
Zgłębiaj właściwości chemiczne fluorowców (grupa 17) w tym fluor, brom, jod i chlor. Dowiedz się o ich reakcjach, zastosowaniach oraz strukturze chemicznej. Idealne dla uczniów chemii na poziomie rozszerzonym. Materiał zawiera kluczowe informacje o tlenkach, kwasach i związkach tych pierwiastków.
Właściwości Żelaza i Związków
Zgłębiaj właściwości chemiczne żelaza, jego stany utlenienia oraz reakcje z kwasami. Dowiedz się o kolorach soli żelaza, amfoteryczności wodorotlenków oraz stabilności jonów Fe^{2+} i Fe^{3+}. Materiał przeznaczony dla uczniów na poziomie rozszerzonym chemii nieorganicznej.
Najpopularniejsze notatki z Chemia
9Właściwości i Reakcje Węglowodorów
Odkryj kluczowe informacje na temat alkanów, alkenów i alkinów, w tym ich właściwości fizyczne i chemiczne, reakcje substytucji oraz zastosowania w przemyśle. Zrozumienie szeregów homologicznych i wzorów ogólnych pomoże w nauce chemii organicznej. Typ: Podsumowanie.
Rodzaje Tlenków i Reakcje
Zrozumienie tlenków: ich klasyfikacja (zasadowe, kwasowe, amfoteryczne), właściwości oraz reakcje chemiczne. Dowiedz się, jak tlenki reagują z kwasami i zasadami oraz jak je otrzymywać. Idealne dla studentów chemii, którzy chcą zgłębić temat tlenków i ich zastosowań.
Pochodne Węglowodorów: Alkohole i Kwasy
Zgłębiaj temat pochodnych węglowodorów, w tym alkoholi, kwasów karboksylowych oraz ich właściwości. Dowiedz się o grupach funkcyjnych, szeregach homologicznych oraz reakcjach chemicznych. Idealne dla studentów chemii, którzy chcą zrozumieć kluczowe koncepcje organicznej chemii. Typ: Podsumowanie.
Rodzaje i Właściwości Kwasów
Zgłębiaj różnorodność kwasów chemicznych, ich klasyfikację na tlenowe i beztlenowe, metody otrzymywania oraz reakcje chemiczne. Dowiedz się o dysocjacji kwasów i ich mocy. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Rodzaje Wiązań Chemicznych
Zrozumienie rodzajów wiązań chemicznych: kowalencyjnych (spolaryzowanych i niespolaryzowanych), jonowych oraz koordynacyjnych. Dowiedz się, jak różnice elektroujemności wpływają na typ wiązania oraz poznaj przykłady i wzory chemiczne. Idealne dla uczniów przygotowujących się do egzaminów z chemii.
Metabolizm i Energetyka
Zgłębiaj kluczowe procesy metaboliczne, w tym oddychanie tlenowe, fotosyntezę, fermentację oraz regulację aktywności enzymów. Dowiedz się, jak energia jest pozyskiwana i wykorzystywana w komórkach. Idealne dla studentów biologii i nauk przyrodniczych.
Systematyka Związków Nieorganicznych
Zrozumienie systematyki związków nieorganicznych, w tym kwasów, zasad, soli oraz ich właściwości. Materiał obejmuje przygotowanie wodorotlenków, tlenków, hydratów oraz zastosowanie soli. Idealne dla uczniów liceum, poziom podstawowy. Typ: Podsumowanie.
Węglowodory kl8
Węglowodory
Właściwości Węglowodorów
Zgłębiaj właściwości węglowodorów, w tym alkanów, alkenów i alkinów. Dowiedz się o procesie polimeryzacji, izomerii oraz chemicznych i fizycznych właściwościach tych związków. Idealne dla uczniów chemii przygotowujących się do egzaminów.
Najpopularniejsze notatki
9Przedwiośnie: Analiza Tematów
Zanurz się w analizę powieści 'Przedwiośnie' Stefana Żeromskiego. Odkryj kluczowe motywy, takie jak dojrzewanie, rewolucja i podróż, oraz ich znaczenie w kontekście niepodległej Polski. Notatka zawiera szczegółowe omówienie bohaterów, narracji oraz symboliki, co czyni ją idealnym materiałem do nauki i przygotowania do egzaminów.
Analiza Lalki Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca kompozycję, problematykę, głównych bohaterów oraz kontekst społeczny Warszawy lat 70. i 80. XIX wieku. Zawiera omówienie miłości Wokulskiego do Izabeli Łęckiej, różnorodności narracji oraz otwartości zakończenia. Idealna dla studentów literatury i miłośników polskiej prozy.
Analiza 'Lalki' Prusa
Szczegółowa analiza powieści 'Lalka' Bolesława Prusa, obejmująca gatunek, czas i miejsce akcji, kluczowych bohaterów, oraz motywy literackie. Zawiera omówienie postaci Stanisława Wokulskiego jako romantyka i pozytywisty oraz realistyczny obraz Warszawy i Paryża. Idealne dla studentów literatury polskiej.
Makbet: Analiza Tragedii Szekspira
Odkryj kluczowe cechy dramatu 'Makbet' Williama Szekspira, w tym złamanie zasady decorum, psychologię postaci oraz tematykę zbrodni i ambicji. Zrozum, jak Szekspir przekształca klasyczną tragedię, wprowadzając elementy fantastyki i psychologii. Idealne dla uczniów i studentów literatury. Typ: analiza literacka.
Wesele: Analiza Symboli
Zanurz się w głęboką analizę dramatu 'Wesele' Stanisława Wyspiańskiego. Odkryj kluczowe symbole, takie jak chochoł i złoty róg, oraz ich znaczenie w kontekście polskiego społeczeństwa przełomu XIX i XX wieku. Notatka zawiera omówienie genezy, kompozycji, tematów oraz portretu społecznego, co czyni ją idealnym materiałem do nauki i przygotowań do egzaminów.
Młoda Polska: Kluczowe Tematy
Odkryj istotne cechy i motywy epoki Młodej Polski, w tym dekadentyzm, sztukę dla sztuki oraz wpływ filozofii Nietzschego i Schopenhauera. Analiza najważniejszych twórców, ich dzieł oraz typów bohaterów. Idealne dla studentów literatury i kultury polskiej.
Przedwiośnie: Kluczowe Motywy
Analiza powieści 'Przedwiośnie' Stefana Żeromskiego, obejmująca gatunek, czas i miejsce akcji, głównych bohaterów oraz szczegółowy plan wydarzeń. Zawiera omówienie kluczowych motywów literackich, takich jak patriotyzm, rewolucja, miłość i przemiana Cezarego Baryki. Idealne dla studentów przygotowujących się do egzaminów.
Wprowadzenie do lektury Zemsta
Sprawdź znajomość czasu i miejsca akcji oraz głównych wątków komedii Aleksandra Fredry.
Części Mowy w Języku Polskim
Zrozumienie części mowy w języku polskim: rzeczownik, czasownik, przymiotnik, liczebnik, zaimek, przysłówek, spójnik, przyimek, partykuła i wykrzyknik. Przykłady i zastosowanie każdego z typów, aby ułatwić naukę i poprawić umiejętności językowe. Idealne dla uczniów i studentów.
Nie ma nic odpowiedniego? Sprawdź inne przedmioty.
Zobacz, co mówią o nas nasi użytkownicy. Pokochali nas — pokochasz też i Ty.
Aplikacja jest bardzo prosta i dobrze przemyślana. Do tej pory znalazłem wszystko, czego szukałem i mogłem się wiele nauczyć z innych notatek! Na pewno wykorzystam aplikację do pomocy przy robieniu prac domowych! No i oczywiście bardzo pomaga też jako inspiracja do robienia swoich notatek.
Ta aplikacja jest naprawdę świetna. Jest tak wiele notatek i pomocnych informacji [...]. Moim problematycznym przedmiotem jest język niemiecki, a w aplikacji jest w czym wybierać. Dzięki tej aplikacji poprawiłam swój niemiecki. Polecam ją każdemu.
Wow, jestem w szoku. Właśnie wypróbowałam aplikację, ponieważ widziałam ją kilka razy reklamowaną na TikToku jestem absolutnie w szoku. Ta aplikacja jest POMOCĄ, której potrzebujesz w szkole i przede wszystkim oferuje tak wiele rzeczy jak notatki czy streszczenia, które są BARDZO pomocne w moim przypadku.